INTRODUCCIÓN
El trasplante de precursores hematopoyéticos (TPH) es un procedimiento que consiste en una mieloablación, seguida de la infusión intravenosa de células madre hematopoyéticas para restablecer la función de la médula ósea. En la actualidad, se utiliza como una estrategia terapéutica para enfermedades hematológicas y algunos tumores sólidos (1,2).
Los tipos más comunes de TPH corresponden al alogénico (TAL) y al autólogo (TAU). En el TAL se transfieren células progenitoras hematopoyéticas de un donante a un receptor. El receptor recibe acondicionamiento mieloablativo que combina altas dosis de quimioterapia con irradiación total del cuerpo y, luego del trasplante, la administración de inmunosupresores y corticoides. En el TAU se usan las propias células progenitoras hematopoyéticas extraídas del paciente, después de administrarse solo altas dosis de quimioterapia (1-3).
Los pacientes sometidos a TPH son considerados en riesgo de malnutrición debido a varios factores como su enfermedad de base, los regímenes de acondicionamiento mieloablativos y la administración de fármacos inmunosupresores. Por lo general, estos pacientes presentan una disminución de la ingesta, un aumento de la demanda metabólica y alteraciones digestivas como náuseas, vómitos, odinofagia y diarrea (1,4,5).
El estado nutricional es un factor importante en la restauración inmunitaria y la regeneración de la médula ósea después del TPH. Por lo tanto, evaluar correctamente el estado nutricional de los pacientes y mantenerlo durante el periodo postrasplante son elementos esenciales para una reconstitución inmunitaria exitosa, reducir complicaciones infecciosas y mejorar la calidad de vida de los pacientes (6,7).
Para evaluar los cambios en el estado nutricional de pacientes sometidos a TPH, algunos estudios han utilizado la Valoración Global Subjetiva (VGS) o el Nutritional Risk Screening 2002 (NRS-2002). Sin embargo, este último es una herramienta más bien de cribado nutricional que puede presentar una alta variabilidad interobservador (2,6). Otros indicadores propuestos para evaluar el estado nutricional han sido el peso corporal y el índice de masa corporal (IMC). Sin embargo, una limitación importante de estos es su baja sensibilidad, ya que pueden subestimar el diagnóstico de sarcopenia en pacientes con sobrepeso u obesidad, debido a que no evalúan los cambios en la composición corporal como la pérdida de masa magra, cuya medición, por otra parte, puede estar enmascarada por la retención de líquido relacionada con la quimioterapia durante el periodo de acondicionamiento asociado al uso de corticoides, junto con la hidratación profusa durante el tratamiento postrasplante (4,8,9).
Algunos estudios han utilizado la bioimpedancia (BIA) para evaluar la composición corporal de pacientes con TPH. Este es un método no invasivo basado en la capacidad de los tejidos para conducir la corriente eléctrica. Las mediciones que realiza la bioimpedancia son la resistencia (R), que corresponde a la oposición de un tejido biológico al flujo de una corriente alterna, y la reactancia (Xc), que se refiere a la capacidad del tejido de almacenar la carga eléctrica como un condensador. El análisis de ambas variables permite estimar el agua corporal total (ACT) e, indirectamente, la masa libre de grasa (MLG) y la masa grasa (10).
Otro parámetro utilizado para evaluar la composición corporal y que puede ser cuantificado mediante BIA es el ángulo de fase (AF), que corresponde al arco tangente entre la resistencia y la reactancia. Este parámetro refleja la integridad de las membranas celulares y muestra la distribución de agua entre el espacio intracelular y el extracelular. Por este motivo, los cambios en la celularidad, el tamaño de la célula, la permeabilidad de la membrana celular o la hidratación de los tejidos generan variaciones en los valores del AF. Un AF bajo sugiere muerte celular y/o disminución de la integridad celular y se puede asociar a un aumento de la morbimortalidad en los pacientes hospitalizados (11).
Los cambios en la composición corporal y la dinamometría durante el periodo de acondicionamiento mieloablativo y postrasplante no han sido estudiados y se desconoce si los posibles cambios observables pueden ser factores que se asocian al desarrollo de complicaciones postrasplante.
El objetivo de este estudio es comparar los cambios en la antropometría, dinamometría e indicadores de la BIA de pacientes sometidos a TAU y TAL luego del periodo de acondicionamiento y una semana postrasplante, así como evaluar si estos cambios precoces se asocian con el desarrollo de complicaciones como mucositis y enfermedad de injerto versus huésped (EICH), además de la longitud de la estadía hospitalaria y la mortalidad durante la hospitalización.
PACIENTES Y MÉTODOS
POBLACIÓN EN ESTUDIO
Este estudio incluyó pacientes adultos mayores de 18 años admitidos en la Clínica de la Universidad Católica para TAL o TAU entre mayo de 2017 y noviembre de 2018. El protocolo del estudio fue aprobado por el comité de ética local. Los criterios de exclusión fueron pacientes adultos mayores de 70 años y usuarios de marcapaso cardiaco.
DISEÑO DEL ESTUDIO Y RECOLECCIÓN DE DATOS
Este es un estudio prospectivo de cohorte. Las mediciones del estado nutricional y la composición corporal fueron efectuadas en tres tiempos distintos: tiempo 1 (T1), que corresponde a 24-36 horas luego del ingreso; tiempo 2 (T2), que corresponde día +1 postrasplante de precursores hematopoyéticos; y tiempo 3 (T3), que corresponde al día +8 post-TPH.
EVALUACIÓN DEL ESTADO NUTRICIONAL
La medición del peso corporal se realizó con una mínima cantidad de ropa, sin calzado, en ayuno y después de haber evacuado la vejiga. Se utilizó una la balanza marca Seca® 769 con precisión de 100 g y con tallímetro incorporado. La circunferencia braquial se midió en el punto medio entre el acromion y el olécranon del brazo derecho, con una cinta métrica inextensible de 1 mm de exactitud. En este mismo nivel, se midió el pliegue tricipital utilizando un plicómetro marca Harpenden® (12). La dinamometría se evaluó en el brazo no dominante utilizando el dinamómetro de mano digital Jamar®. Para esta medición, el paciente empuñó el dinamómetro con el brazo en abducción, el codo extendido y la muñeca neutra, y luego realizó la fuerza máxima. Se realizaron tres mediciones con un intervalo de un minuto entre cada una y se registró el valor promedio entre las tres mediciones. Se compararon los datos con la referencia nacional (13). El análisis de la BIA se realizó con un bioimpedanciómetro tetrapolar monofrecuencia de 50 Hz AKERN BIA 101 Anniversary®. Los pacientes fueron evaluados en decúbito supino, con piernas y brazos separados, en ayunas durante al menos ocho horas, con la vejiga vacía y con los electrodos en partes específicas del tobillo, pie, muñeca y mano.
ANÁLISIS ESTADÍSTICO
El análisis de datos se realizó con el programa Minitab 18.0. Las variables continuas se presentan como medianas, máximas y mínimas (rango) y las variables categóricas, como porcentajes. Las diferencias de las medianas entre las variables continuas independientes se analizaron mediante el test no paramétrico Mann-Whitney. Se consideraron valores de p < 0,05 como estadísticamente significativos.
RESULTADOS
Un total de 40 pacientes fueron evaluados, 17 recibieron TAU y 23 recibieron TAL. El promedio de edad fue de 41 ± 15,4 años en el grupo de pacientes con TPH autólogo y 42,5 ± 12,5 en el grupo de pacientes con TPH alogénico. Otras características generales de los pacientes se muestran en la tabla I.
Tabla I. Características de los pacientes.

IMC: índice de masa corporal; EICH: enfermedad injerto contra huésped; DE: desviación estándar. NS: no significativo.
Al momento del ingreso (T1), no se observan diferencias significativas en la composición corporal, antropometría y dinamometría evaluada en los pacientes sometidos a TAU y TAL (Tabla II). Asimismo, los pacientes sometidos a TAU y TAL recibieron alimentación por vía oral, al momento del ingreso y durante el periodo de acondicionamiento mieloablativo. Solo tres pacientes, que se encontraban bajo peso, recibieron suplemento nutricional oral previo al TPH para logar cubrir sus requerimientos nutricionales.
Tabla II. Evaluación de la antropometría y BIA al momento del ingreso hospitalario.
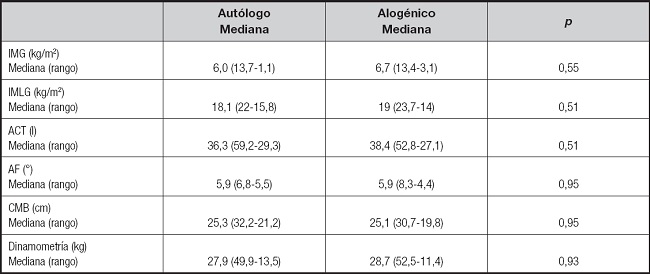
IMG: índice de masa grasa; IMLG: índice de masa libre de grasa; ACT: agua corporal total; AF: ángulo de fase; CMB: circunferencia muscular braquial.
En cuanto a los cambios del estado nutricional que se observan en T2, fue significativa la modificación del AF, con una disminución significativamente mayor en pacientes con TAL (Fig. 1). En T2, también se observan cambios significativos en el IMLG y el ACT. Los pacientes con TAU disminuyen su IMLG mientras que los pacientes con TAL aumentan su IMLG (TAU -0,6 kg/m2, TAL +0,2 kg/m2, p = 0,03), y se observa lo mismo con el ACT. Los pacientes con TAU disminuyen su ACT y los pacientes con TAL aumentan su ACT (TAU -2,4 l, TAL +0,7 l, p = 0,02). Luego del TPH, siete pacientes con TAU y 12 con TAL recibieron nutrición parenteral central (41,2 % vs. 52,2 %, respectivamente; p = 0,538) debido a que cursaron con mucositis o a la disminución de la ingesta alimentaria por náuseas o vómitos.
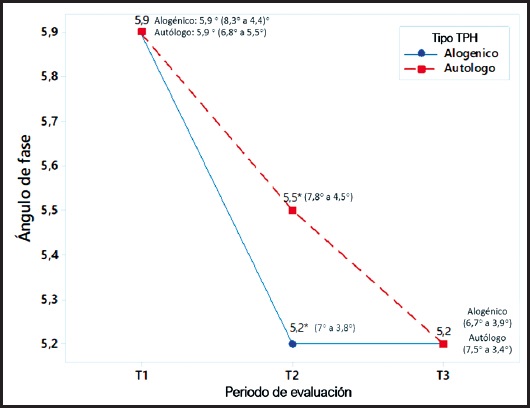
Figura 1. Evolución del ángulo de fase, como mediana (rango), de los pacientes con TPH autólogo (TAU) y TPH alogénico (TAL), en los tres tiempos de medición. T1: ángulo de fase basal de los pacientes al momento del ingreso; T2: cambio del ángulo de fase después del periodo de acondicionamiento mieloablativo; T3: cambio del ángulo de fase desde el ingreso al postrasplante inmediato (día + 8 TMO). T2: *diferencia significativa (p < 0,05).
Al estudiar el estado nutricional en T3, se observa una diferencia significativa entre estos grupos al evaluar la fuerza prensil de la mano con dinamometría. Los pacientes sometidos a TAU aumentan su fuerza prensil en 0,6 kg, mientras que los pacientes sometidos a TAL la disminuyen en 1,9 kg (p = 0,01). Además, se observan diferencias significativas en el peso y el IMC al comparar ambos grupos. Los pacientes con TPH autólogo disminuyen su peso e IMC y los pacientes con TPH alogénico aumentan su peso e IMC durante este periodo de tiempo (peso TAU -1,8 kg, peso TAL +0,5 kg, p = 0,025, e IMC TAU -0,7 kg/m2, IMC TAL +0,1 kg/m2, p = 0,021, respectivamente). No se observaron diferencias significativas entre los pacientes con TPH autólogo y alogénico en el índice de masa grasa (IMG), el peso seco y la circunferencia muscular braquial (CMB) durante ninguno de los periodos analizados. Además, es importante destacar que durante el periodo de seguimiento post-TPH (+8 días), los pacientes no presentaron complicaciones infecciosas.
En cuanto a la evaluación de la composición corporal y el ACT mediante BIA, se observan cambios significativos en T3, así como una correlación significativa entre los cambios del IMLG y el ACT de todos los pacientes evaluados (TAU y TAL) (Fig. 2).

Figura 2. Correlación de los cambios del IMLG y del agua corporal total en el periodo total de observación, de todos los pacientes estudiados. IMLG: índice de masa libre de grasa. Coeficiente de correlación: r = 0,90, p ≤ 0,001.
Es posible que la mayor acumulación de agua en TAL también pudiese explicar el mayor peso e IMC de este grupo.
En la figura 3, se muestra la evolución del AF de los pacientes con TAL. Los pacientes que desarrollaron EICH presentaban un menor AF que aquellos que no desarrollaron esta complicación. Esta diferencia es significativa.
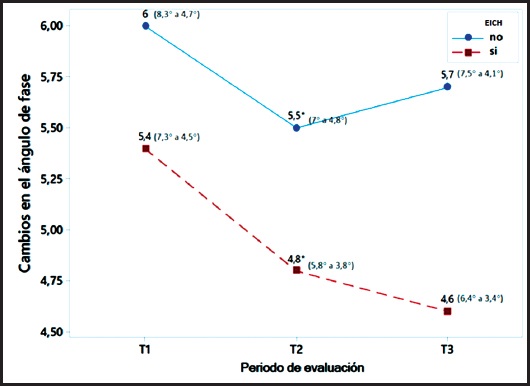
Figura 3. Evolución del ángulo de fase (mediana y rango) de pacientes con TPH alogénico con EICH (n = 8) y sin EICH (n = 15). EICH: enfermedad injerto contra huésped; T1: ángulo de fase basal; T2: cambio del ángulo de fase después del periodo de acondicionamiento mieloablativo; T3: cambio del ángulo de fase desde el ingreso al postrasplante inmediato (día + 8 TMO). T2: *diferencia significativa del ángulo de fase después del periodo de acondicionamiento mieloablativo de los pacientes con y sin EICH p = 0,007.
Por otra parte, se observa una diferencia significativa en la estadía hospitalaria. Los pacientes con TAU presentan una mediana de hospitalización de 21 días, mientras que en los pacientes con TAL fue de 30 días (p < 0,000) (Tabla I). La estadía hospitalaria no se correlacionó significativamente con ninguno de los parámetros utilizados para evaluar el estado nutricional.
Otro resultado relevante es la mortalidad durante la hospitalización. Ninguno de los pacientes sometidos a TAU falleció durante la hospitalización, mientras que un 13 % de los pacientes sometidos a TAL murieron en este periodo. En total, fallecieron tres pacientes con TAL; todos desarrollaron EICH y presentaron AF inferior a 5° en T3 (AF = 4,8°, 4,4° y 4,1°, respectivamente).
DISCUSIÓN Y CONCLUSIÓN
El TPH es una condición que requiere un alto nivel de energía, ya que se produce un estado hipermetabólico, en el que se combinan el aumento del catabolismo como consecuencia de la terapia citorreductora y el anabolismo necesario para la reconstitución de la médula ósea luego del trasplante (9). Para garantizar una óptima consolidación del injerto y evitar complicaciones en el periodo postrasplante, es importante que los pacientes presenten un buen estado nutricional. Por esta razón, evaluar los cambios que se producen evolutivamente en los parámetros nutricionales es fundamental para entregar un soporte nutricional óptimo e individualizado (9,14).
Nuestro estudio describe cambios precoces en indicadores del estado nutricional de pacientes con TPH alogénico y autólogo antes y después del trasplante. En nuestra muestra, la mayoría de los pacientes presentan un buen estado nutricional al ingreso hospitalario, un 35 % de los pacientes presentaba un IMC normal y un 45 %, sobrepeso. Esta situación también ha sido descrita en estudios anteriores (1,15). Se requiere de una buena condición clínica de los pacientes previo al TPH y, por lo general, en esta etapa los pacientes presentan una alimentación adecuada y un peso estable al momento del ingreso hospitalario (1).
La evidencia actual confirma que cuando se utiliza el IMC para determinar el estado nutricional, los resultados son contradictorios (15-17). En este aspecto es importante destacar que los cambios en el IMC no siempre informan sobre cambios en la composición corporal del paciente. Lo anterior es importante, pues los cambios de la masa muscular podrían ser un factor involucrado en el desarrollo de complicaciones y el riesgo de mortalidad (15,16). Por este motivo, el IMC no parece un parámetro adecuado para evaluar el estado nutricional de los pacientes con TPH. Por otra parte, la MLG se puede medir mediante análisis de BIA, lo que es más relevante que el IMC por sí solo, ya que entrega información sobre la cantidad de masa muscular (18). El IMLG, que corresponde a la MLG/talla2, se ha postulado como un indicador válido para el diagnóstico de desnutrición intrahospitalaria (19). En nuestro estudio, se observó una correlación directa entre el ACT y el IMLG al analizar las mediciones de todos los pacientes evaluados. Este resultado tiene relación con el hecho de que la MLG incluye preferentemente el agua corporal, por lo tanto, sus variaciones dependen en gran parte del estado de hidratación de los pacientes. Este hallazgo explicaría también por qué los pacientes con TAL aumentan su IMLG y su peso corporal durante el periodo de acondicionamiento y luego de la primera semana de trasplante, ya que su tratamiento de acondicionamiento previo al TPH considera altas dosis de quimioterapia junto con hidratación profusa, para luego combinarse con el uso de corticoides, lo que favorece la retención hídrica. Lo previo no se observa en el grupo de pacientes sometidos a TAU (19).
El AF, obtenido a partir del análisis de impedancia bioeléctrica (BIA), se ha utilizado en la práctica clínica para detectar modificaciones celulares que puedan reflejar la salud de estas, por lo que se ha considerado como un posible indicador pronóstico en varios tipos de enfermedades (19). Nuestros resultados muestran una diferencia significativa del AF de los pacientes sometidos a TAU con los pacientes sometidos a TAL luego del periodo de acondicionamiento (T2), observándose una disminución mayor en aquellos pacientes con TAL. Esta diferencia podría ser explicada por el tipo de acondicionamiento mieloablativo que se realiza a los pacientes con TAL, en el cual el tratamiento dura más tiempo y se basa en quimioterapias en altas dosis y radiación de cuerpo entero, provocando muerte celular y cambios en el potencial eléctrico de las membranas celulares (19). El AF reducido puede ser el resultado o la combinación de pérdida de masa celular corporal, debilidad de la membrana celular y aumento del desplazamiento de agua corporal hacia el espacio extracelular (20). Estos mismos resultados fueron descritos previamente, con una rápida disminución del AF inmediatamente después del inicio del tratamiento de acondicionamiento en pacientes con TAL. En este caso, el AF bajo se atribuye a un cambio en la fisiología de las células, que se traduce en modificaciones en las características eléctricas y las propiedades de los tejidos que cambian la conducción iónica (19).
Un resultado relevante de nuestro estudio corresponde al hallazgo de un menor AF en los pacientes sometidos a TAL que desarrollaron EICH después del periodo de acondicionamiento mieloablativo. Se ha descrito que el AF pretrasplante y posacondicionamiento es un parámetro independiente para predecir sobrevida y mortalidad sin recaídas de la enfermedad (2). En nuestro estudio, se observa una mortalidad del 13 % en los pacientes sometidos a TAL (tres pacientes) y los pacientes que fallecieron presentaban bajos ángulos de fase en T3 (día + 8 post-TPH alogénico). Si bien en nuestro estudio los pacientes sometidos a TAL presentan una caída importante del AF luego del acondicionamiento mieloablativo, al analizar el subgrupo que desarrolla EICH, se puede observar que luego del TPH alogénico continúa disminuyendo su AF, mientras que los pacientes que no desarrollan EICH suben su AF después del trasplante. Por lo tanto, luego del TPH, algunos pacientes no son capaces de recuperar la masa celular corporal y su integridad de membrana, lo que podría explicar por qué la mortalidad en este estudio se observa en pacientes con muy bajo AF en el día + 8 post-TPH alogénico (19,20).
Debido a que el AF disminuye luego del acondicionamiento mieloablativo en pacientes con TAL, parecería interesante tratar de incrementar este parámetro antes de la admisión hospitalaria, combinando un apoyo nutricional adecuado y un entrenamiento físico, ya que, de esta forma, podrían mejorar los resultados clínicos postrasplante (20).
Otro parámetro nutricional evaluado en este estudio es la dinamometría, una prueba de función muscular que se utiliza cada vez más en el ámbito clínico debido a que es un marcador simple, no invasivo y adecuado como indicador de la función muscular. Se ha descrito que una dinamometría deteriorada se relaciona con el aumento de las complicaciones postoperatorias, una mayor duración de hospitalización, mayor tasa de rehospitalización y disminución de la condición física (21). En nuestro estudio observamos diferencias significativas al comparar los dos tipos de TPH. Los pacientes con TAU presentan un aumento discreto de la dinamometría durante la primera semana postrasplante, mientras que los pacientes con TAL disminuyen su dinamometría en este mismo periodo. Esta diferencia puede estar asociada a la fatiga producto de la irradiación del cuerpo entero que se realiza durante el periodo de acondicionamiento de los pacientes con TAL (20). Por otra parte, la disminución de la contractilidad muscular debido a la quimioterapia en altas dosis podría afectar las funciones de la membrana celular y los canales de calcio celulares (21). En el caso de los pacientes con TAU, su quimioterapia mieloablativa es más corta y no se someten a irradiación de cuerpo entero, por lo que la funcionalidad muscular se podría ver menos afectada en comparación con los pacientes con TPH alogénico.
En conclusión, los pacientes sometidos a trasplante de precursores hematopoyéticos, especialmente el alogénico, presentan un deterioro precoz de su estado nutricional. Por este motivo, la evaluación de parámetros nutricionales como AF y dinamometría debe realizarse durante las primeras etapas del tratamiento y posterior al trasplante (22). Los parámetros clásicos de evaluación nutricional, como peso corporal e IMC, pueden subestimar cambios corporales tempranos, retrasando el inicio de la terapia nutricional (19,23). Este estudio empleó varios métodos de evaluación nutricional para determinar las diferencias entre los pacientes con TAU y TAL. Los pacientes sometidos a TAL tienen un mayor riesgo de malnutrición y deterioro de su estado nutricional desde el periodo de acondicionamiento mieloablativo, debido a que su terapia pretrasplante combina altas dosis de quimioterapia, radiación de cuerpo entero y uso de corticoides, lo que provoca modificaciones en el ángulo de fase y complicaciones que afectan el estado nutricional como EICH y mucositis (20,22,23).
Al estudiar los distintos parámetros de evaluación nutricional, se evidencia que el agua corporal se relacionó directamente con el IMLG, por lo que este no sería un indicador válido, en especial para los pacientes con TAL ya que su tratamiento de acondicionamiento favorece el aumento del agua corporal, lo que afecta la medición del IMLG (19). Sin embargo, los cambios en el AF y la dinamometría parecen prometedores en la evaluación nutricional precoz de estos pacientes, puesto que no se ven alterados por la retención de agua y se pueden evaluar antes de que los cambios antropométricos sucedan.














