INTRODUCCIÓN
PharmaMar es una compañía española dedicada a la búsqueda de fármacos de origen marino provenientes de organismos sésiles adheridos al sustrato marino, sin defensas mecánicas, por lo que su supervivencia a lo largo de la historia probablemente se deba a compuestos químicos que son capaces de producir. En base a la experiencia acumulada por esta compañía en la investigación, el desarrollo y posterior proceso de aprobación de los fármacos, se pueden extraer algunas ideas de interés.
UN PROCESO COMPLEJO… Y LARGO
Durante el desarrollo de un fármaco, en los ensayos clínicos, hay distintas etapas (1):
- Fase 1: estudiar la seguridad.
- Fase 2: observar la eficacia y seguridad en un grupo mayor de pacientes.
- Fase 3: se estudian los efectos del fármaco en una cohorte de hasta 3000 pacientes antes de su aprobación.
- Revisión: la Agencia Americana del Medicamento (FDA), así como la Agencia Europea del Medicamento (EMA) hacen un seguimiento del fármaco para confirmar seguridad y eficacia.
- Fase 4: se analiza el comportamiento del fármaco en la población tras su aprobación.
De cada 10 000 compuestos estudiados, se estima que solo 1 logra ser comercializado, suponiendo todo este proceso un coste aproximado de unos 2500 millones de euros. Desde que una compañía farmacéutica española solicita a la EMA la aprobación de un fármaco hasta que este llega a los pacientes españoles pasan aproximadamente 1 050 días, es decir, 3 años (2). Además, para que un medicamento obtenga financiación pública y sea incluido en la prestación farmacéutica del SNS en España, debe superar varios requisitos rigurosos y procesos regulatorios.
El proceso de autorización se inicia una vez que el CHMP (Comité de Productos Medicinales para Uso Humano) da el visto bueno y la Comisión Europea aprueba el fármaco. En este momento pasa a las agencias reguladoras, como la Agencia Española del Medicamento. De forma paralela se le da un código a nivel nacional y se desarrolla un informe de posicionamiento terapéutico.
En cuanto a financiación, precio y reembolso, hay varios aspectos a considerar. Por ejemplo, es importante saber que la esperanza de vida de España es la más elevada de la Unión Europea, lo que explicaría la alta tasa de comorbilidades existentes en la población española, que suponen un gasto elevado en medicamentos y en cuidados. A pesar de esto, el gasto español en sanidad se situaba un 0,3 % por debajo de la media europea.
Para que un fármaco obtenga financiación pública debe estar aprobado y tiene que incluirse en la prestación farmacéutica del Sistema Nacional de Salud (SNS). Los criterios para la financiación de medicamentos son:
- Gravedad, duración y secuelas de las distintas patologías para las que resulten indicados.
- Necesidades específicas de ciertos colectivos.
- Valor terapéutico y social del medicamento, y beneficio clínico incremental del mismo teniendo en cuenta su relación coste-efectividad.
- Racionalización del gasto público destinado a prestación farmacéutica e impacto presupuestario en el SNS.
- Existencia de medicamentos u otras alternativas terapéuticas para las mismas afecciones a menor precio o inferior coste de tratamiento.
- Grado de innovación del medicamento. Criterio de innovación ("avances terapéuticos indiscutibles por modificar el curso de la enfermedad o mejorar el curso de la misma, el pronóstico y el resultado terapéutico de la intervención").
En el proceso de inclusión de un medicamento en la prestación farmacéutica del SNS en España, se consideran varios aspectos adicionales que van más allá de la eficacia clínica y la seguridad del medicamento.
Uno de los criterios fundamentales es el impacto presupuestario del medicamento en la sociedad española y su contribución a la sostenibilidad del SNS. Esto implica evaluar si, para obtener el mismo resultado en salud, el medicamento puede generar beneficios económicos adicionales, como un aumento del producto interior bruto (PIB), lo cual es crucial para la sostenibilidad a largo plazo del sistema de salud.
Además, se tienen en cuenta los mecanismos de retorno que permiten al Estado recuperar los fondos invertidos en medicamentos innovadores, asegurando así una gestión eficiente de los recursos públicos (Fig. 1).
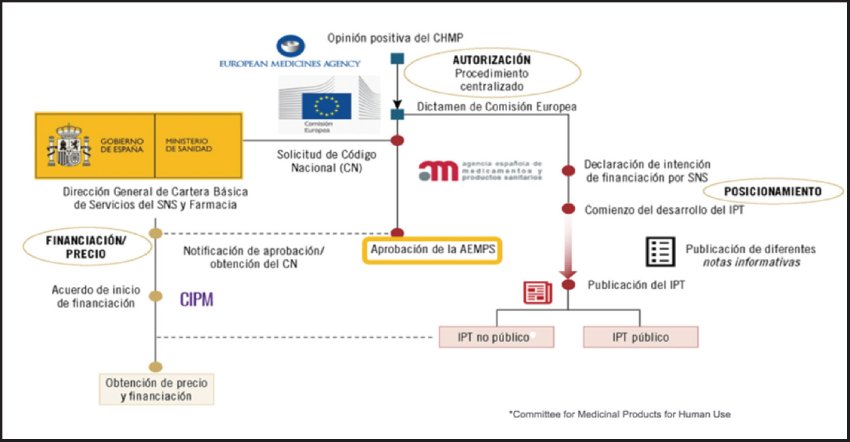
Figura 1. Procedimiento para la autorización de la comercialización, y precio/reembolso, de un medicamento en España (CHPM: Committee for Medicinal Products for Human Use; SNS: Sistema Nacional de Salud; CN: código nacional; CIPM: Comisión Interministerial de Precios de Medicamentos; AEMPS: Agencia Española de Medicamentos y Productos Sanitarios; IPT: Informe de Posicionamiento Terapéutico) (3).
La determinación del precio de los fármacos está a cargo de la Comisión Interministerial de Precios de Medicamentos (CIPM), que incluye miembros del Ministerio de Sanidad y también de áreas como Hacienda, Economía e Industria. Esta comisión se encarga de establecer precios que sean justos y razonables, considerando tanto los costos de desarrollo y producción como los beneficios para los pacientes y el sistema de salud.
El Informe de Posicionamiento Terapéutico (IPT) juega un papel crucial al delimitar la utilidad clínica y los usos específicos del medicamento, indicando en qué casos debe ser utilizado (3). Este informe es elaborado inicialmente por expertos clínicos y finalizado por las CC. AA., quienes añaden consideraciones adicionales y consensuan un informe final. Este documento se remite luego a asociaciones de pacientes, industria y sociedades científicas para su revisión y comentarios. Entre los aspectos evaluados se encuentra la estimación de los "años ganados con calidad de vida", un parámetro utilizado para comparar diferentes fármacos en términos de beneficios adicionales para los pacientes.
Una vez establecido el precio del medicamento, este es analizado por los comités de evaluación de cada comunidad autónoma, lo que puede resultar en variaciones en el acceso al medicamento en diferentes regiones de España.
A lo largo de los años se han implementado diversos reales decretos con medidas para controlar el gasto farmacéutico y garantizar la sostenibilidad del sistema de salud (4).
DIFERENCIAS NUTRICIÓN VS. FARMACIA
En términos regulatorios, existen diferencias significativas entre los productos de nutrición y los generados por la industria farmacéutica. Por ejemplo, la Agencia Española de Seguridad Alimentaria y Nutrición (AESAN) no pertenece al Ministerio de Sanidad, sino al Ministerio de Consumo, lo que implica regulaciones y procedimientos diferentes para los productos de nutrición en comparación con los medicamentos.
Los AUME son productos especialmente formulados y destinados al manejo dietético de pacientes (incluidos lactantes) bajo supervisión médica. Están diseñados para satisfacer total o parcialmente las necesidades alimenticias de pacientes cuya capacidad para consumir, digerir, absorber, metabolizar o excretar alimentos normales o nutrientes específicos esté limitada, deficiente o alterada, y que no puedan manejar estas necesidades únicamente modificando su dieta normal.
Cuando una empresa presenta un potencial AUME, el proceso de aprobación suele ser ágil en las CC. AA. de España. La aprobación inicial puede ocurrir en menos de 2 meses, tras lo cual el producto es derivado a la AESAN. La AESAN se encarga de evaluar y decidir si el AUME cumple con los criterios para su financiación, lo cual completa el proceso en aproximadamente 6 meses en total.
Este procedimiento es considerablemente más rápido en comparación con el proceso de aprobación de fármacos mencionado anteriormente. Además, los requisitos de evidencia necesarios para la aprobación de AUME también son diferentes y menos rigurosos, adaptándose a las necesidades específicas de los pacientes para quienes están destinados estos productos dietéticos especiales.














