INTRODUCCIÓN
Los edulcorantes son sustancias que proveen sabor dulce a los alimentos o a las preparaciones. Existen edulcorantes naturales (como el azúcar de mesa) o artificiales, que son elaborados químicamente. Estos últimos también son conocidos como edulcorantes no nutritivos, edulcorantes artificiales o sustitutos del azúcar. La guía de la Organización Mundial de la Salud (OMS) utiliza el término edulcorantes sin azúcar (ESA), y los define como edulcorantes sintéticos, naturales o modificados, no nutritivos y no clasificados como azúcares, excluyendo los alcoholes de azúcar y los azúcares bajos en calorías (1).
El uso de ESA ha venido cobrando relevancia como una alternativa para reducir el consumo de azúcares libres, especialmente ante el alarmante aumento de la prevalencia de enfermedades no transmisibles (ENT) vinculadas con la alimentación. Estas enfermedades contribuyen al 74 % de las muertes a nivel mundial, principalmente en países de ingresos bajos y medios según la OMS (2). Una de estas enfermedades es la obesidad, cuya prevalencia a nivel mundial es de 37 % (IC 95 % 33 a 42 %) (3) y contribuye al desarrollo de otras ENT, mediante cambios patológicos y mecánicos relacionados con el exceso de adiposidad e incremento en el peso corporal. Entre ellas se encuentran la apnea obstructiva del sueño, la enfermedad cardiovascular, la osteoartritis, algunos tipos de cáncer, la diabetes tipo 2 y el síndrome metabólico. Además, la obesidad aumenta el riesgo de mortalidad asociada a estas condiciones en más de 2,5 veces (4).
Un estilo de vida sedentario y la adopción de patrones de alimentación poco saludables, han contribuido al aumento en la prevalencia de las ENT, creando una carga significativa para los sistemas de salud en términos de atención y de costos. La relación entre la alimentación y las enfermedades crónicas es crucial para comprender la magnitud de este problema. Un patrón de alimentación que incluya frutas, verduras, granos enteros, y que sea bajo en sodio, grasas saturadas y trans, así como azúcares libres, ha demostrado ser efectivo para reducir el riesgo de incidencia de este grupo de enfermedades (5). En respuesta a esta necesidad, la industria de alimentos ha implementado el uso de ingredientes que cumplen funciones tecnológicas al ser incorporados en los alimentos, como asegurar su inocuidad, extender su vida útil y mantener su calidad sensorial (sabor, olor, color y textura). La incorporación de este tipo de ingredientes ha contribuido a la reducción del contenido de algunos nutrientes críticos relacionados con efectos adversos sobre la salud como el sodio, las grasas saturadas y los azúcares libres. Con respecto a estos últimos, la disminución en su consumo es una medida fundamental para combatir la creciente incidencia de las ENT, por lo cual se han implementado diversas estrategias, una de ellas es el uso de los ESA como una opción para mantener el sabor dulce en los alimentos y bebidas sin aportar energía. Sin embargo, su impacto sobre la salud a largo plazo sigue siendo un tema de debate en la comunidad científica.
La OMS ha sido una de las principales entidades que ha intervenido en este debate, con la publicación de su guía en 2023 sobre el uso de los ESA (1). Este documento ofrece una recomendación sobre el uso de los ESA en el contexto de la prevención del aumento de peso y la reducción del riesgo de ENT. A pesar de que los ESA son comúnmente promovidos como una herramienta para controlar el peso y mejorar la salud metabólica, la evidencia científica que respalda estos beneficios no es concluyente. La guía de la OMS se basa en el análisis de estudios clínicos y ensayos observacionales, cuyos resultados han sido variados y no conclusivos, salvo por la única recomendación reportada por esta guía. Esto ha derivado en interpretaciones erróneas de la información y hasta en la posibilidad equivoca de eliminar el consumo de los ESA y remplazarlo por el azúcar. Este artículo tiene como objetivo proporcionar una visión crítica y reflexiva de la guía de la OMS sobre el uso de los ESA, como aporte a la discusión sobre su uso en la población general, incluyendo pacientes con ENT.
GENERALIDADES SOBRE LOS EDULCORANTES SIN AZÚCAR
DEFINICIÓN
Los ESA son aditivos alimentarios que confieren sabor dulce a un alimento (6). Su principal objetivo de uso es remplazar el azúcar libre y contribuir a la reducción del contenido energético de los alimentos. Son considerados alimentos seguros o Generally Recognized as Safe (GRAS). No aportan energía y son sintetizados de manera artificial, a excepción de los glucósidos de esteviol. Los ESA son 20 a 20 000 veces más potentes en su dulzor que la sacarosa, y cuando son utilizados en combinación este dulzor presenta una mayor potencia, razón por la cual tienden a ser ampliamente utilizados de esta manera (7). Los ESA tienen diferentes funciones tecnológicas en la industria de alimentos como acentuadores de sabor, humectantes, estabilizadores y espesantes, entre otras (8), su característica principal es incrementar la intensidad de dulzura, persistencia del sabor dulce y efecto en el retrogusto (9). Los ESA se utilizan ampliamente debido a su bajo contenido energético y su capacidad de no afectar el apetito y la respuesta glucémica posterior a la ingesta de alimentos. Esto es particularmente beneficioso para las personas con diabetes, sobrepeso u obesidad que buscan sustitutos del azúcar (10). En este sentido, en los Estados Unidos se ha observado un aumento en el uso de los ESA, de aproximadamente 200 % entre los niños y 54 % entre los adultos, en una posible respuesta a las campañas para hacer menor uso de azúcares libres como una alternativa para hacer frente a la elevada prevalencia de esta enfermedad (11).
DIGESTIÓN Y METABOLISMO DE ALGUNOS EDULCORANTES SIN AZÚCAR
Los ESA tienen una composición química diferencial y de esto depende su grado de digestión y absorción a nivel intestinal:
- El aspartamo se compone de un éster metílico de dipéptido que contiene dos aminoácidos: el ácido L-aspártico y L-fenilalanina. Tras su consumo, las peptidasas y esterasas gastrointestinales descomponen casi por completo el aspartamo, lo que da como resultado que cantidades insignificantes del compuesto entren en el torrente sanguíneo (12).
- El acesulfame K es derivado de un ácido orgánico hidrofílico que se absorbe casi en su totalidad a nivel del intestino delgado y se distribuye por la sangre a diferentes tejidos. Sin sufrir ningún metabolismo, más del 99 % del acesulfame K ingerido se excreta por vía urinaria en las primeras 24 horas y el restante en las heces.
- La sucralosa es un disacárido compuesto por 1,6-dicloro-1,6-didesoxifructosa y 4-cloro-4-desoxigalactosa, tiene un nivel de absorción muy bajo (menos del 15 %) y prácticamente no se metaboliza, siendo su eliminación por vía urinaria (13).
- Los glucósidos de esteviol, sólo 18 de las 150 a 300 especies del género Stevia exhiben propiedades edulcorantes, y los dos edulcorantes principales son el esteviósido (~9,1 %) y el rebaudiósido A (~3,8 %). Estos no presentan afectación por la presencia de ácido gástrico y no es digerido por las enzimas intestinales, por tanto, no se absorbe a nivel de intestino delgado debido a su alto peso molecular. El esteviósido puede ser degradado por la flora intestinal bacteriana, transformándolo en esteviol libre, un aglicón de los glicósidos de esteviol (14).
- El ciclamato es un edulcorante artificial cuya composición química es N-ciclohexilsulfamato, y se caracteriza por la presencia de un anión sulfamato unido a un anillo de ciclohexilo. Se absorbe en el intestino delgado y se excreta principalmente sin cambios en la orina, aunque una fracción puede ser metabolizada a ciclohexilamina por la microbiota intestinal, con una considerable variabilidad interindividual en esta capacidad metabólica (15).
LíMITES EN SU CONSUMO
El consumo de los ESA debe estar en concordancia con los límites permitidos para su uso. La ingesta diaria admisible (IDA) es una estimación efectuada por el Comité Mixto FAO/OMS de Expertos en Aditivos Alimentarios (JECFA, por su sigla en inglés) de la cantidad de aditivo alimentario (en este caso ESA), expresada en relación con el peso corporal, que una persona puede ingerir diariamente durante toda la vida sin riesgo apreciable para su salud (8). Actualmente existen diferencias en la IDA de cada ESA según la región. A noviembre de 2024, en Estados Unidos, existen seis ESA aprobados para el consumo por parte de la Administración de Alimentos y Medicamentos (FDA, por su sigla en inglés) (16), mientras que en la Unión Europea, la gama de ESA aceptados por la Autoridad Europea de Seguridad Alimentaria (EFSA, por su sigla en inglés) y el Comité Científico de Alimentos (SCF, por su sigla en inglés) es más amplia e incluye el ciclamato (Tabla I).
Tabla I. Edulcorantes sin azúcar disponibles en los EE. UU. y la Unión Europea, y sus niveles de ingesta diaria admisible, según lo definen los organismos reguladores
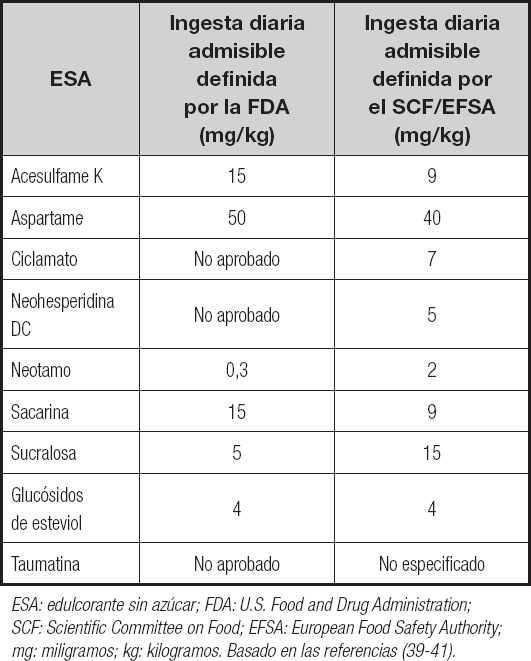
ESA: edulcorante sin azúcar; FDA: U.S. Food and Drug Administration; SCF: Scientific Committee on Food; EFSA: European Food Safety Authority; mg: miligramos; kg: kilogramos. Basado en las referencias (39-41).
Una de las preocupaciones es que, al sustituir el consumo de azúcar libre por ESA, se superen las IDA y pueda generar efectos no deseados para la salud. En 2018, Martyn et al. (17) publicaron una revisión exhaustiva que caracteriza las estimaciones de exposición a nivel mundial basado en el análisis de diferentes cohortes nacionales para siete ESA (acesulfame K, aspartamo, ciclamato, sacarina, glucósidos de esteviol, sucralosa y taumatina). Los hallazgos identificaron que los niveles de exposición se encuentran por debajo de los límites de la IDA definida para cada ESA (Tabla II).
Tabla II. Consumo promedio del ADI por cada ESA según región
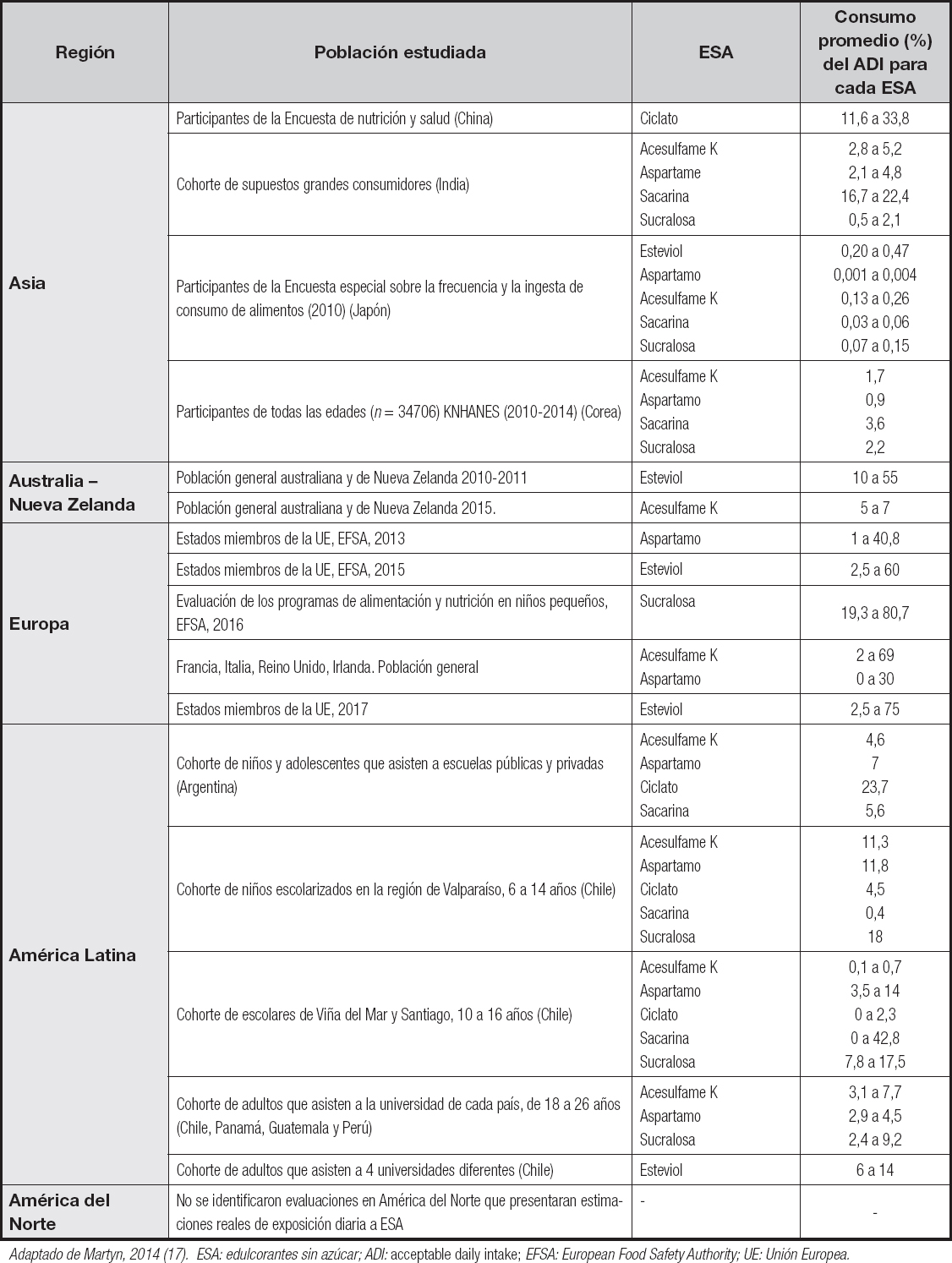
Adaptado de Martyn, 2014 (17). ESA: edulcorantes sin azúcar; ADI: acceptable daily intake; EFSA: European Food Safety Authority; UE: Unión Europea.
USO DE EDULCORANTES SIN AZÚCAR: GUÍA DE LA OMS
En 2023, la OMS publicó el informe titulado “Uso de edulcorantes sin azúcar”, cuyo objetivo era proporcionar recomendaciones basadas en la evidencia sobre el consumo de ESA en adultos, mujeres gestantes y niños aparentemente sanos, incluyendo a personas con un índice de masa corporal (IMC) alto. Estas recomendaciones están dirigidas a tomadores de decisiones en distintos ámbitos de atención y a profesionales de la salud, entre otros (1). La guía se desarrolló mediante la búsqueda y selección sistemática de literatura científica, mientras que la certeza de la evidencia fue evaluada utilizando la metodología GRADE (Grading of Recommendations, Assessment, Development, and Evaluations) (18).
Después de la revisión y análisis de toda la evidencia científica, la guía de la OMS elaboró una única recomendación: “La OMS propone que no se utilicen edulcorantes sin azúcar como medio para controlar el peso o reducir el riesgo de enfermedades no transmisibles (recomendación condicional)”. Esta recomendación está dirigida exclusivamente a la población para la cual se obtuvo la evidencia, es decir, niños, adultos y mujeres gestantes aparentemente sanos, así como personas con un IMC alto. Por esta razón, no es adecuado aplicar esta recomendación a otras poblaciones, especialmente aquellas que presentan enfermedades asociadas. Del mismo modo, se debe evitar formular conclusiones en forma de recomendaciones a partir de la información de la guía, ya que su construcción requiere la implementación de un análisis metodológico que evalúe el conjunto de la evidencia, su grado de certeza y otras implicaciones para la práctica.
El carácter condicional de la recomendación se debe a que la certeza global de la evidencia fue clasificada como baja, lo que redujo la confianza del grupo desarrollador de la guía para emitir una recomendación definitiva en la que los efectos indeseables superen a los deseables.
En cuanto a la evidencia científica, la guía incluyó el análisis de 50 ensayos clínicos controlados aleatorizados, 97 estudios de cohortes prospectivas y 47 estudios de casos y controles. En general, la evidencia de ensayos clínicos en adultos indicó una reducción en el peso (diferencia de medias -0,71 kg IC 95 % -1,13 a -0,28 kg), una disminución en la ingesta de energía (diferencia de medias -569 kj/d IC 95 % -859 a -278 kj/d) y una reducción en el consumo de azúcares libres (diferencia de medias -38,4 g/d IC 95 % -57,8 a -19,1 g/d) asociada al uso de ESA, aunque con una baja certeza de la evidencia.
Los hallazgos de los ensayos clínicos difieren de los resultados identificados por los estudios observacionales (casos y controles, y cohortes). La certeza de este tipo de estudios fue calificada de baja a muy baja. Los estudios observacionales detectaron asociaciones entre el uso de los ESA y el incremento del IMC (diferencia de medias +0,14 kg/m2 IC 95 % 0,03 a 0,25 kg/m2), aumento en la incidencia de obesidad (HR 1,76 IC 95 % 1,25 a 2,49), incremento en la incidencia de diabetes tipo 2 (HR - bebidas 1,23 IC 95 % 1,14 a 1,32; HR - disponibles en mesa 1,34 IC 95 % 1,21 a 1,48), elevación de la mortalidad por cualquier causa (HR 1,12 IC 95 % 1,05 a 1,19) y por causas cardiovasculares (HR 1,19 IC 95 % 1,07 a 1,32). Además, aumento en la incidencia de la enfermedad coronaria (HR 1,32 IC 95 % 1,17 a 1,50), el accidente cerebrovascular (HR 1,19 IC 95 % 1,09 a 1,29), la hipertensión (HR 1,13 IC 95 % 1,09 a 1,17) y el cáncer de vejiga (HR 1,31 IC 95 % 1,06 a 1,62).
Al contrario del volumen de evidencia identificada en adultos, la información sobre el uso de ESA en niños es muy limitada. Por ejemplo, las asociaciones a favor del uso de los ESA, derivan de un único ensayo clínico que mostró una reducción del perímetro abdominal (diferencia de medias -0,66 cm IC 95 % -1,23 a -0,09 cm), así como para la disminución de la masa grasa corporal (diferencia de medias -0,57 kg IC 95 % -1,02 a -0,12 kg), ambos con una certeza moderada de la evidencia. No se identificaron asociaciones entre el consumo de los ESA y la incidencia de sobrepeso, diabetes tipo 2, enfermedades cardiovasculares, cáncer cerebral y caries, así como alteraciones negativas con la neurocognición, ni aumento en la ingesta de energía y azúcares libres (1).
En el caso de las gestantes, la evidencia también fue escasa. El análisis conjunto de los estudios observacionales identificó una asociación entre un alto consumo de ESA y un mayor riesgo de parto pretérmino (OR 1,25 IC 95 % 1,07 a 1,46), con certeza de evidencia muy baja. Ante la ausencia de evidencia, no fue posible elaborar un metaanálisis para identificar un efecto consolidado de las asociaciones entre el uso de los ESA y la grasa corporal, el asma, las alergias y la neurocognición en hijos de mujeres que consumieron ESA durante la gestación. Sin embargo, una cohorte prospectiva (19) identificó una asociación en contra de los ESA y el riesgo de desarrollar asma a los 18 meses o a los 7 años (OR ajustado 1,14 IC 95 % 1,00 a 1,28 y OR ajustado 1,2 IC 95 % 1,07 a 1,35; respectivamente) con una certeza de evidencia muy baja. Los autores de este estudio reportan limitaciones en torno a la clasificación de consumo de los ESA, lo cual pudo modificar el efecto estimado. Por otro lado, en el desenlace de neurocognición, una cohorte prospectiva elaborada por Cohen y colaboradores (20) encontró cambios únicamente relacionados con la capacidad verbal de la escala KBIT-II para niños con una mediana de edad de 7,7 años (-3,2 IC 95 % -5,0 a -1,5), pero esta diferencia, a pesar de ser estadísticamente significativa, no se considera clínicamente importante debido a que el puntaje total de la escala es 100 puntos. Los resultados de este estudio fueron considerados con muy baja certeza.
Desde una perspectiva de salud pública, la guía de la OMS busca no solo proporcionar directrices sobre el uso de ESA, sino también motivar una reflexión más amplia sobre los patrones dietéticos y el consumo de productos alimenticios ultraprocesados. La OMS advierte que remplazar el azúcar libre con edulcorantes en productos alimenticios ultraprocesados no mejora sustancialmente la calidad de la alimentación. De igual manera, es muy importante mantener los esfuerzos para reducir el consumo de productos alimenticios con azúcares libres dentro de una estrategia más amplia que promueva la ingesta de alimentos sin procesar y mínimamente procesados.
POSIBLES LIMITACIONES DE LA GUÍA DE LA OMS
La guía de la OMS representa un paso importante hacia una mejor comprensión del papel de los ESA en la alimentación humana, pero también señala que quedan muchas preguntas sin responder. En particular, la incertidumbre sobre los efectos a largo plazo de los ESA subraya la necesidad de más investigaciones rigurosas y de largo plazo que puedan ofrecer respuestas más concluyentes sobre su seguridad y efectividad.
Al revisar la guía de la OMS, un aspecto relevante es el tipo de estudios incluidos. Estos fueron ensayos clínicos, estudios de cohortes prospectivos y estudios de casos y controles. En cuanto a los ensayos clínicos, son los únicos estudios a los que se les puede atribuir un efecto de causalidad debido a su diseño experimental y prospectivo. Generalmente, estos estudios asignan aleatoriamente una intervención y un placebo a una población definida y, mediante un control riguroso de las variables, evalúan y analizan su efecto tras un periodo determinado de tiempo. Además, los ensayos clínicos se consideran el estándar más alto para decidir sobre la implementación de una intervención (por ejemplo, vacunas) debido a las fortalezas inherentes a su metodología.
Por otro lado, los estudios de cohortes prospectivos y los estudios de casos y controles tienen una naturaleza observacional, lo que significa que no se realiza ninguna intervención. En este caso, se evalúa la relación o asociación entre una exposición y la presencia de una condición o enfermedad, lo que implica que no se puede determinar causalidad. Por esta razón, identificar una asociación en un estudio observacional no equivale a establecer una causa entre la exposición y el evento. Además, estos tipos de estudios son más propensos a sesgos propios de su diseño, incluso cuando se controlan múltiples variables de confusión (21).
Un aspecto importante para considerar dentro del análisis de los estudios observacionales es la posibilidad de presentar causalidad inversa. Esta se puede explicar de siguiente manera: en la actualidad un individuo con alto riesgo de diabetes tipo 2 comienza a hacer uso de los ESA, pero al cabo de un tiempo desarrolla la enfermedad, por lo cual se desconoce si la causa de la enfermedad es debida específicamente al uso de los ESA, o a otras situaciones que actúan como factores de confusión como los antecedentes familiares de patologías crónicas, la carga genética o el patrón global de la alimentación. Para reducir el efecto de la causalidad inversa, se debe realizar el control de las variables de confusión, para lo cual existen diferentes alternativas durante el análisis de la información como la estratificación, la regresión multivariada, el uso de los puntajes de propensión y los análisis de sensibilidad. En esta línea, los autores de la guía de la OMS concluyeron que “la causalidad inversa y los factores de confusión residuales pueden contribuir a las asociaciones encontradas en los estudios observacionales entre el consumo de ESA y los resultados de salud, pero que no hay evidencias que permitan descartarlas por ser atribuibles exclusivamente a la causalidad inversa o a la confusión residual” (1). Por este motivo la certeza de la evidencia de los estudios observacionales tiende a ser menor que la que incorpora los ensayos clínicos, lo cual puede modificar los desenlaces evaluados.
En relación con lo anterior, los estudios observacionales en comparación con los ensayos clínicos pueden sobre o subestimar la dirección del efecto y su magnitud. Por esta razón una buena parte de los estudios observacionales concluyen que es necesario el diseño y ejecución de ensayos clínicos para confirmar los hallazgos identificados, cuando estos son éticamente posibles. En este sentido, los datos agrupados de los ensayos clínicos de la guía de la OMS tienen un efecto significativo en la disminución del peso corporal en adultos, por el contrario, el metaanálisis de los estudios observacionales no identifica un efecto significativo a favor o en contra. En el caso del IMC, el conjunto de los datos de los estudios observacionales concluye que existe un efecto sobre la ganancia de peso, mientras que los ensayos clínicos no lo hacen (22,23).
En cuanto a la certeza de la información o el grado de confianza en la magnitud del efecto, según la metodología GRADE, los ensayos clínicos inician con una certeza alta en su evaluación, mientras que los estudios de cohortes prospectivos tienen mayor riesgo de sesgo, lo que los sitúa en un nivel de baja certeza cuando se utiliza esta metodología. Cuando la evidencia proviene tanto de ensayos clínicos como de estudios de cohortes, se da mayor peso a los ensayos clínicos en términos de confiabilidad. Ante la ausencia de estudios clínicos para la mayoría de los desenlaces evaluados en la guía de la OMS, el grupo desarrollador utilizó la información derivada de estudios observacionales (24).
Otro de los aspectos relevantes de la guía, es la ausencia en la incorporación de metodologías de análisis secuenciales y modelamiento de sustitución de los azúcares libres por ESA en estudios de cohorte prospectivos. El uso de estas metodologías dentro de estudios de cohorte prospectivos de larga duración permitiría reducir el sesgo inherente en los estudios observacionales retrospectivos y de caso control, así como pueden proveer un mejor estimador del riesgo asociado. El uso de este tipo de análisis fue realizado por Khan y colaboradores (25) estima de manera agrupada los desenlaces cardiometabólicos y el uso de ESA, según el tipo de análisis de la cohorte (análisis prevalente, por cambio o por sustitución). En síntesis, se identifica que los estudios de cohorte prevalentes tienden a sobreestimar el efecto e identificar asociaciones adversas, mientras que las cohortes con análisis por cambio o sustitución reportan efectos favorables en el consumo de ESA sobre los desenlaces cardiometabólicos.
Adicional a todo lo anterior, durante 2023 y 2024 se ha publicado nueva evidencia basada en revisiones sistemáticas y metaanálisis que resultan contradictorios a los hallazgos presentados en la guía de la OMS. Un ejemplo de los resultados en contra de los ESA es el metaanálisis de Chen Z y colaboradores (26) quien identificó que un elevado consumo de ellos se asociaba con mortalidad por cualquier causa o específica, sin embargo, los propios autores indican que existen varias limitaciones en los hallazgos por lo cual las conclusiones deben ser interpretadas con cautela. No obstante, otros autores han encontrado asociaciones a favor para el cáncer colorrectal, pero negativas para la incidencia de leucemia (27) y la enfermedad cardiovascular (28). Mientras tanto, otros autores han identificado resultados a favor del uso de los ESA para la reducción del peso corporal en niños y adultos (29,30) y ningún riesgo de desarrollar cáncer de endometrio (31), de vejiga (32) o de seno (33).
Otro aspecto que aborda la guía es la diversidad de los efectos de los diferentes tipos de edulcorantes. Aunque todos los ESA se agrupan bajo una misma categoría, existen diferencias en la estructura química, el metabolismo y el impacto fisiológico de cada uno de ellos. Por ejemplo, edulcorantes como la sucralosa, el aspartame o la estevia entre otros, pueden tener efectos distintos sobre el metabolismo de la glucosa y la microbiota intestinal, tales como una reducción en las bacterias benéficas y aumento de bacterias patógenas, aumento del pH intestinal y efectos no conclusivos al respecto de la alteración en la producción de ácidos grasos de cadena corta y expresión de genes involucrados en el metabolismo microbiano (9). Conz et al. (10) reportan que la principal limitación de los estudios asociados al consumo de ESA y el impacto en la microbiota intestinal es la diferencia en el número de participantes, los hábitos dietéticos y los estilos de vida que influyen directamente en la composición inicial de la microbiota y su respuesta con los ESA. Por otro lado, la ingesta de ESA es sólo uno de los múltiples factores que pueden impactar la composición y variedad de la microbiota, por lo que se hace necesario formular investigaciones para dar respuesta a estas inquietudes. Esta heterogeneidad ha complicado la interpretación de los resultados de los estudios, y la OMS ha señalado que se necesita más investigación para comprender completamente cómo afectan estas sustancias a largo plazo.
EDULCORANTES Y ENFERMEDADES CRÓNICAS
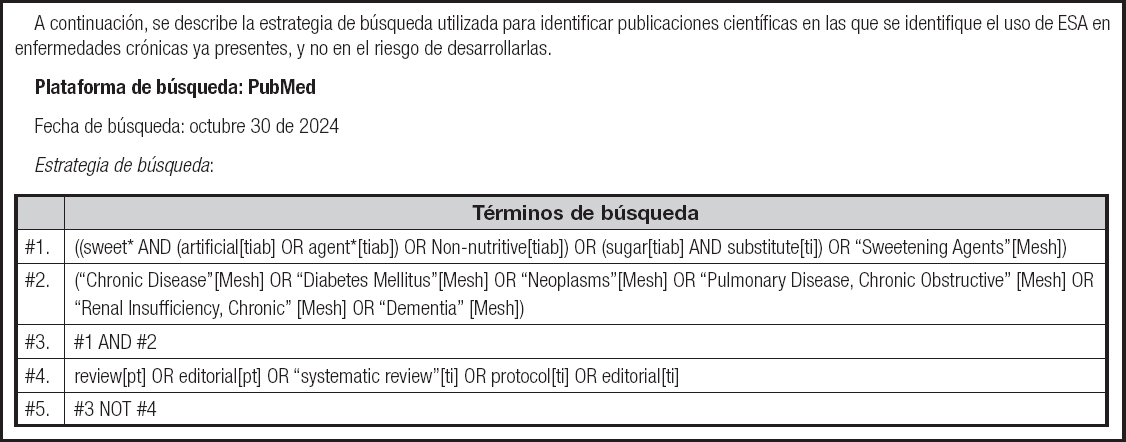
Como se mencionó anteriormente, la población objetivo de la guía de la OMS incluye adultos, niños, mujeres gestantes aparentemente sanas y personas con un IMC alto. La recomendación principal de la guía es proporcionar directrices para la prevención del aumento de peso no saludable y reducir la incidencia de enfermedades no transmisibles relacionadas con la alimentación. Cabe destacar que la guía no tiene como objetivo ofrecer pautas para el manejo de la diabetes tipo 2 o la prediabetes (1). Además, la evidencia disponible sobre la relación entre los ESA y el manejo de otras condiciones clínicas, como la desnutrición, el cáncer, enfermedades infecciosas, pulmonares o renales, es escasa o inexistente. En una búsqueda sistemática de la literatura realizada durante la elaboración de este artículo (Anexo 1), solo se identificaron estudios en humanos que relacionan el consumo de ESA con la incidencia de recidivas de cáncer y mortalidad por esta enfermedad (34) así como efectos sobre marcadores bioquímicos y resultados en salud en pacientes con diabetes (35). Sin embargo, el estudio relacionado con cáncer es de tipo observacional, lo que introduce un alto riesgo de sesgo debido a la presencia de variables de confusión, como la medición de la ingesta de bebidas con adición de ESA a partir de una frecuencia de consumo de los tres últimos meses, por lo cual no es posible cuantificar la cantidad y tipo de ESA que se asoció con el desenlace. Por otro lado, la publicación sobre diabetes es una revisión sistemática de la colaboración Cochrane, que busca evaluar los efectos de los ESA sobre esta enfermedad, concluye que la evidencia disponible es inconclusa y de muy baja certeza (35).
A partir de lo anterior, es evidente la necesidad de realizar investigaciones sobre el efecto o las posibles asociaciones del uso de ESA en pacientes con comorbilidades ya existentes distintas al exceso de peso (9). Adicionalmente, los profesionales de la salud, especialmente nutricionistas dietistas, deben evaluar el uso seguro de los ESA sin exceder la IDA definida para cada tipo de edulcorante, en el contexto del tratamiento nutricional indicado para los pacientes.
OTRAS CONSIDERACIONES
MUJERES GESTANTES, MADRES LACTANTES Y NIÑOS
La gestación, la lactancia y los primeros 1000 días de vida son periodos críticos para un apropiado crecimiento y desarrollo de los niños, en donde el aspecto nutricional juega un papel de vital importancia. En cuanto al uso de los ESA en los niños menores de 2 años, el consenso de la Academia Americana de Pediatría (2019) (36) indica que no se aconseja su uso ante la ausencia de evidencia científica en este grupo de edad. Por otro lado, el consenso mexicano sobre el uso de ESA en la mujer en edad reproductiva (publicado en 2019) (37) concluyó que no hay suficiente evidencia para establecer una relación de causa-efecto para los partos prematuros, la incidencia de alergias, presencia de ESA en la leche materna y manejo del peso corporal durante la gestación. Se debe anotar que la evidencia evaluada por este consenso se consideró de baja y muy baja certeza. Sin embargo, evidencia de un metaanálisis reciente (2024) demuestra una relación entre el consumo de ESA en mujeres gestantes y el parto pretérmino, mientras que no encontró asociaciones con otros desenlaces (38). Aunque la evidencia sobre el uso de los ESA en estos grupos poblacionales es limitada o nula, la guía de la OMS subraya la necesidad de tener precaución en su uso en mujeres gestantes, madres lactantes y niños, sin embargo, esta guía no proporcionó ninguna recomendación específica sobre este tema.
EDUCACIÓN NUTRICIONAL
Los ESA siguen siendo una opción común en muchos productos alimenticios, especialmente en bebidas y alimentos procesados, que pueden contribuir a reducir la ingesta de azúcar libre a corto plazo, pero no son una solución definitiva para mejorar el perfil y calidad de la alimentación. Es así como la OMS recomienda que las políticas de salud pública se centren en promover patrones de alimentación basados en alimentos naturales, ricos en nutrientes y con fuentes de dulzor natural, como las frutas, en lugar de depender exclusivamente de los ESA para reducir el consumo de azúcares libres. Sin embargo, el acceso a una alimentación saludable varía considerablemente, especialmente en las comunidades más vulnerables y en países de América Latina, donde las políticas alimentarias y las condiciones socioeconómicas pueden limitar el acceso a una alimentación y nutrición adecuada. Esto subraya la necesidad de intervenciones integrales, entre ellas la educación alimentaria y nutricional a la población general y a los profesionales de la salud, que promuevan no solo cambios en el comportamiento individual, sino también políticas públicas que garanticen entornos alimentarios más saludables. La educación alimentaria y nutricional debe basarse en metodologías adaptadas a las diferentes poblaciones, con mensajes claros y comprensibles que le permitan tomar decisiones acertadas sobre los alimentos que adquieren y consumen.
En el caso del exceso de peso o la obesidad, la inclusión de los ESA no debe considerarse como una solución aislada al problema, pueden ser una alternativa complementaria, pero es necesario que se integre a un enfoque más amplio que considere la educación alimentaria, la actividad física y la modificación de hábitos no saludables. La educación juega un papel importante para fomentar la adopción de cambios significativos y duraderos en el comportamiento. Los ESA pueden ser aliados en el control del consumo de azúcar, pero su uso debe alinearse con un plan integral diseñado por profesionales de la salud, orientado a prevenir y manejar problemas metabólicos de manera sostenible.
CONCLUSIÓN
Los ESA son ingredientes que se utilizan ampliamente en la industria de alimentos con diferentes funciones tecnológicas. Estos son utilizados como una alternativa para sustituir el azúcar de mesa o los azúcares libres, con el fin de reducir al aporte energético. La guía de la OMS indica que no deben recomendarse como herramienta principal para el control del peso o la prevención de enfermedades crónicas, aunque existen datos que sugieren posibles beneficios en la reducción de peso y consumo de energía en adultos, también se han encontrado asociaciones potenciales entre el uso de ESA y ciertos riesgos de salud. Sin embargo, estas asociaciones han sido detectadas principalmente en estudios observacionales, limitados en su capacidad para establecer causalidad debido a la posibilidad de sesgos y factores de confusión.
A pesar de los numerosos estudios evaluados, incluyendo ensayos clínicos y estudios observacionales, la evidencia se considera de baja a muy baja certeza, especialmente para desenlaces clave como el riesgo de obesidad, diabetes tipo 2 y mortalidad, entre otros. Esta incertidumbre subraya la necesidad de realizar investigaciones adicionales, particularmente en poblaciones específicas como los niños y las mujeres gestantes, donde la evidencia es limitada. Los ESA requieren una comprensión más profunda sobre cómo interactúan a largo plazo con la salud humana. Además, los resultados contradictorios de estudios recientes refuerzan la necesidad de desarrollar métodos de análisis más robustos y específicos que permitan a los tomadores de decisiones y profesionales de la salud establecer directrices basadas en evidencia sólida y confiable.