INTRODUCCIÓN
La implantología oral ha revolucionado la práctica clínica odontológica demostrando que la rehabilitación oral de los pacientes con pérdidas dentales unitarias, múltiples o totales con implantes dentales es un tratamiento predecible y con una elevada tasa de éxito. En este sentido, los resultados favorables a largo plazo de los tratamientos implantológicos orales está relacionado con el desarrollo del fenómeno de la oseointegración y de una buena reacción de los tejidos periimplantarios 1 .
La investigación experimental y la experiencia clínica en implantología oral ha originado el desarrollo de diferentes superficies de implantes que mejoran los fenómenos biológicos de la oseointegración y favorecen los resultados clínicos de los implantes en el tratamiento de los pacientes con diversos grados de pérdidas dentales 1 .
Desde la introducción de la superficie mecanizada por la escuela sueca de Branemark, posteriormente las superficies por aposición de plasma de titanio (escuela suiza de Schroeder) o hidroxiapatita, hasta las más recientes con sustracción de material, con chorreado de arena y/o grabado ácido existe una intensa y prolongada trayectoria investigadora con estudios de laboratorio (in vitro), con animales de experimentación (in vivo) y con pacientes en su incorporación a la clínica que constituye en la actualidad uno de los campos más importantes de la implantología oral 2-3.
El material más frecuentemente utilizado en la realización de los implantes dentales ha sido el titanio comercialmente puro, debido a que presenta una gran biocompatibilidad y constituye el material ideal para conseguir la oseointegración con éxito a largo plazo tras la carga funcional 4 . La biocompatibilidad del titanio está relacionada con las propiedades de su óxido de superficie. En contacto con el aire o el agua, el titanio rápidamente forma un espesor de óxido de 3-5 nm a la temperatura ambiente. El óxido más frecuente es el dióxido de titanio (Ti O 2 ). Este óxido es muy resistente al ataque químico lo que hace que el titanio sea uno de los metales más resistentes a la corrosión y que contribuye a su biocompatibilidad. Además el titanio es un material de una resistencia más que suficiente para su aplicación clínica 5 .
IMPLANTES CON SUPERFICIE MECANIZADA
El prototipo de los implantes con esta superficie fué el desarrollado por el grupo sueco de Branemark 5 . Aunque su superficie se consideraba lisa, sin embargo el proceso de fresado y pulido creaba algunas irregularidades mínimas que le daban cierto carácter de rugosidad, por lo que se aceptaba más el término de mecanizada 6 . La superficie mecanizada es la que más ha sido estudiada en el laboratorio ya que los estudios pioneros de Branemark fueron realizados con este tipo de superficie, concluyendo en el concepto de oseointegración que definía la naturaleza de la unión del titanio al hueso de una forma estable y predecible, como el “contacto directo entre el hueso vivo y la superficie del implante cargado funcionalmente sin interposición de tejido blando a nivel del microscopio óptico” 7 - 8 . La experiencia clínica acumulada en los últimos 40 años con esta superficie mecanizada, ha demostrado que la inserción de varios implantes pueden soportar una rehabilitación fija con un éxito superior al 90%. Además, las rehabilitaciones orales fijas sobre implantes oseointegrados pueden satisfacer globalmente al paciente edéntulo al proporcionar una gran estabilidad prostodóncica lo que mejora la función oral, con una estética aceptable muy favorable 9 - 10 .
IMPLANTES CON SUPERFICIE RUGOSA
La superficie de los implantes o más precisamente, la topografía superficial de los implantes, es decir su grado de rugosidad y la orientación de estas irregularidades superficiales constituye desde hace más de 15 años, un reto de investigación e interés en la implantología oral. No hay que olvidar que el tratamiento de la superficie de los implantes orales incrementado la rugosidad o desarrollando microcavidades, fisuras o grietas mediante diversas tecnologías puede favorecer la unión entre las macromoléculas de la superficie del implante y del hueso, incrementando la integración del implante con una mejor respuesta tisular osteoblástica y resultando en una mayor resistencia a la compresión, tensión y estrés. Esta respuesta biológica y física se ha correspondido con los resultados clínicos de muchos estudios que demuestran que la utilización de implantes con superficie rugosa mejora la oseointegración y el éxito del tratamiento con los pacientes 11 - 12 .
Inicialmente, la posibilidad de incrementar la rugosidad de la superficie de los implantes mediante la aposición de material como el plasma de titanio o la hidroxiapatita fué desarrollado por algunas empresas de implantes con el objetivo de favorecer la superficie de contacto hueso-implante 13 . La superficie recubierta con plasma de titanio incrementa la superficie de contacto hueso-implante y puede estimular la osteogénesis por mecanismos de adhesión celular, además aumentan la resistencia a las cargas funcionales convencionales, a la tracción y cizallamiento 14 . La hidroxiapatita ha sido utilizada para incrementar la rugosidad de la superficie de los implantes de forma similar a la de TPS. La unión entre esta superficie y el hueso es mayor que la del titanio. De hecho se ha demostrado histológicamente que la superficie recubierta de hidroxiapatita provoca una mayor adhesión osteoblástica y proliferación de la matriz extracelular que mejora la unión hueso-implante 15 .
Posteriormente, la investigación experimental ha desarrollado por nuevas superficies que presentan la característica común de que su rugosidad ha sido conseguida por sustracción de material. Es decir, las diferentes superficies de los implantes han sido tratadas con diversas substancias (arenado de alúmina, etc) y/o ácidos (clorhídrico, nítrico, sulfúrico) que han provocado en su superficie diversos grados de rugosidad, manifestadas por grietas, cavidades o hendiduras con el objetivo de lograr una superficie más biocompatible y que mejore su unión con el hueso del paciente 2 - 3 , 11 - 13 .
Estos tipos de superficies presentan la evidencia experimental de un incremento en la adherencia celular (estudios in vitro), y una mayor y más rápida unión hueso-implante (estudios in vivo) 16 - 17 . Los estudios in vitro demuestran que estas superficies rugosas incrementan la actividad de los osteoblastos con una mayor producción de proteínas morfogenéticas que acelera la respuesta biológica celular 16 .
Los estudios in vivo en animales de experimentación demuestran que la unión de estas superficies rugosas mejora la unión del implante al tejido óseo. En este sentido, los estudios histomorfométricos confirman un mayor diferencia en el porcentaje de unión hueso-implante entre estas superficies y las mecanizadas; y así mismo los valores de la fuerza de torque necesarias para la remoción de los implantes insertados son mayores en los implantes con superficies rugosas por sustracción 17 .
Los implantes con superficie arenada han demostrado que incrementan la adhesión, proliferación y diferenciación osteoblástica 16 . En este sentido, la rugosidad y las características topográficas son de los aspectos más relevantes de la superficie de implantes para el éxito de la oseointegración. La topografía afecta a la interacción celular, que influye en la orientación, migración, crecimiento y diferenciación de las células que se adhieren a la superficie. Las investigaciones in vitro e in vivo han demostrado que la rugosidad de la superficie arenada estimula la oseointegración de los implantes dentales 16 .
El grado de rugosidad de la superficie arenada de los implantes, su química, su topografía, y su humectabilidad pueden afectar a la función celular, la adhesión y la viabilidad. El desarrollo de la interfase hueso-implante depende de las directas interacciones de los osteoblastos y la posterior deposición de matriz ósea que son esenciales para la oseointegración. Las células humanas cultivadas sobre las superficies de los implantes tratadas (ej. arenadas, grabadas) muestran más signos de diferenciación celular que las cultivadas sobre superficies mecanizadas 16 .
El grabado de la superficie de los implantes con diferentes combinaciones de ácidos (ácido nítrico, clorhídrico, sulfúrico, etc) ha sido introducido para incrementar su rugosidad y mejorar su respuesta biológica 18 . La adherencia celular es estimulada, y la actividad de la fosfatasa alcalina y la osteocalcina se incrementan significativamente. Estos hallazgos implican que las características químicas de las superficies tratadas con ácidos, juegan un importante papel en su respuesta celular pudiendo mejorar la oseointegración 18 .
Los estudios in vivo demuestran que los implantes con superficie grabada con ácidos mejoran su oseointegración 18 . En este sentido, se ha demostrado que el grabado ácido de la superficie de los implantes incrementa varias veces la fuerza de la oseointegración determinada por la resistencia a la rotación inversa del torque en comparación con implantes de titanio de superficie pulida 19 .
La superficie SLA incluye en la misma superficie dos técnicas de tratamiento, el arenado y posteriormente el grabado ácido. Esta superficie presenta una gran evidencia científica de estudios experimentales en laboratorio (in vitro), y con animales (in vivo), que demuestran su eficacia 20 - 23 .
Estudios in vitro demuestra que la superficie tratada con arenado y grabado ácido, incrementa la rugosidad del implante, y puede mejorar la adhesión de células de estirpe osteoblástica y tener un efecto sobre la configuración y conformación de pseudópodos celulares lo que aumentaría la proliferación celular en la superficie del implante 20 . La topografía de la superficie de los implantes parece modular el crecimiento celular y la diferenciación en osteoblastos que afecta al proceso de cicatrización ósea, mostrando que la topografía de la superficie puede influir en la expresión fenotípica de los osteoblastos. Particularmente, la superficie SLA induce un significativa deposición de esta expresión cuando se le compara con la superficie mecanizada, lo que origina una tendencia de las células hacia su maduración osteoblástica durante la fase de cicatrización ósea 21 .
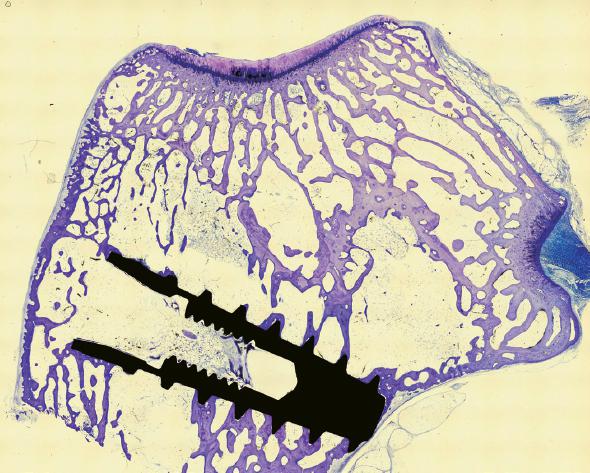
Diversos estudios in vivo realizados en animales de experimentación han demostrado que la oseointegración puede facilitarse por el incremento de la rugosidad de la superficie de los implantes promovida por la acción del arenado y el grabado ácido (ej. superficie Nanoblast Plus, Galimplant ® ) Figuras 1 - 3 ) 22 - 23 . Un estudio compara la oseointegración de dos superficies, SLA y mecanizada en conejos. A los 3 días, una nueva formación de tejido osteoide se originó rapidamente en la superficie tratada SLA, comparada con la superficie mecanizada. Los osteoblastos comenzaron a depositar un nuevo tejido osteoide en estos primeros días de la cicatrización ósea 22 . Un estudio similar investigó los efectos de las modificaciones de las superficies en respuestas óseas in vivo para comparar superficies arenadas hidrofílicas, arenadas, arenadas+grabadas, SLA y anodizadas 23 . Los resultados sugieren que la superficie SLA hidrofílica presentaba una mayor afinidad por el tejido óseo que la anodizada durante el proceso temprano de cicatrización. De hecho, el estudio describió un mayor contacto de coágulos sanguíneos con la superficie SLA 23 .
LA OSEOINTEGRACION DE LAS SUPERFICIES DE IMPLANTES EN ANIMALES DE EXPERIMENTACIÓN
La superficie de los implantes dentales constituye el puente de unión con el tejido óseo del huésped y hace posible el fenómeno biológico de la oseointegración. La oseointegración es una compleja secuencia de sucesos biológicos, como la proliferación celular, la inducción de los genes relacionados con la maduración y organización del hueso y finalmente con la fase de mineralización de la matriz 24 - 26 .
Diferentes tratamientos de la superficie de titanio pueden modificar las propiedades de la microestructura del implante y favorecer la afinidad por el proceso de formación ósea. Las propiedades de la morfología de la superficie juegan un papel crítico en la absorción de moléculas, la adhesión celular y la maduración de las células osteoblásticas 27 - 28 .
La morfología del implante tiene un papel crucial en el contacto hueso-implante y puede favorecer el proceso de la oseointegración. Para mejorar la estabilidad del implante se han realizado diferentes modificaciones que pretenden mejorar las propiedades de los implantes de titanio. Estas modificaciones de la superficie de los implantes pueden mejorar la interacción hueso-implante, sin embargo, no está claro la explicación de los mecanismos de mejora 29 .
La imposibilidad por razones éticas de realizar la mayoría de los estudios sobre los mecanismos biológicos de la oseointegración en los seres humanos, impulsó la experimentación animal. Desde los estudios clásicos de la escuela sueca con implantes de superficie mecanizada y técnica sumergida y suiza con superficie con plasma de titanio y técnica no sumergida, la contribución de los ensayos realizados en animales ha sido fundamental para el desarrollo de la implantología actual 30 .
Son muchos los trabajos que evalúan la oseointegración mediante estudios histológicos e histomorfométricos en experimentación animal. De esta forma, se ha podido determinar la cuantificación y el nivel de calidad del contacto que consigue la superficie del implante con el hueso receptor a través del tiempo, mediante el uso de diferentes técnicas de tratamiento de las imágenes de los cortes y escalonando el sacrificio de los animales de experimentación (Figuras 1 - 3 ) 30 .
Los métodos de cuantificación utilizados normalmente son el análisis histomorfométrico y el porcentaje de contacto hueso-implante (BIC) ya sea a partir de observaciones hechas en el microscopio óptico como en el microscopio electrónico de barrido (el procesado de las muestras es distinto según el método utilizado para observarlas) 30 . Dentro del análisis histomorfométrico, se han ido desarrollando parámetros como la cuantificación del número de osteoblastos/osteocitos, la distribución de otros tipos de células (fibroblastos, osteoclastos y macrófagos), la distribución y orientación de las fibras colágenas, así como el grado de madurez y calcificación, para de esta forma cualificar la oseointegración en función del tiempo y comparar diferentes implantes con un mayor grado de precisión biológica 30 .
La oseointegración de los implantes dentales de titanio depende de un número importante de variables, que son resultados de varios parámetros que no están estandarizados en los sistemas actuales de evaluación. De esta forma, muchas variables determinan la frecuencia y extensión de la oseointegración en diferentes tiempos en varias especies. Estos factores necesitan ser identificados y clarificados por su significación en la velocidad y extensión de la oseointegración. Se reconoce que los mecanismos tempranos de la oseointegración son el doble de efectivo que en los seres humanos. Sin embargo, no está aceptado de forma unánime la metodología para valorar la oseointegración y comparar los diversos estudios 30 .
El éxito de la oseointegración depende de una serie de factores biológicos que se integran de forma simultánea y secuencial y que definen la complejidad de la respuesta ósea a los implantes dentales. Entre estos factores críticos más importantes se encuentran los relacionados con la macroestructura y superficie de los implantes 24 - 30 .
Muchos estudios han mostrado que la superficie rugosa comparada con la mecanizada presenta una mejor absorción molecular, incrementa la producción de matriz extracelular y estimula la diferenciación de las células mesenquimales hacia un fenotipo osteoblástico. Las células detectan las variaciones en la superficie geométrica a través de mecanismos de contacto que regulan su expresión fenotípica. Una diferencia de 1 µm puede producir diferentes respuestas relacionadas con su fenotipo específico 21 , 31 .
La superficie de los implantes dentales es uno de los factores que afectan al ratio y la extensión de la oseointegración. El proceso de oseointegración es ahora conocido por la descripción histológica y celular. La adhesión de un coágulo de fibrina y la población en la superficie del implante de células sanguíneas y mesenquimatosas, conducen a la organización del osteoide y posteriormente la mineralización. La progresión de los cambios de la población celular y la elaboración y modificación de la interfase tejido/implante resulta en hueso formado en contacto directo con la superficie del implante. Precisamente la cantidad de superficie que contacta con el hueso, la velocidad del hueso y la conexión mecánica natural del hueso/implante es influenciada por la naturaleza del implante 32 - 33 .
La investigación experimental in vivo ha utilizado a diversos animales de experimentación (ej. perros, cerdos, conejos, ratas) para la evaluación de los materiales relacionados con los implantes dentales. Los conejos presentan algunas ventajas para ser utilizados como modelo animal para testar las superficies de implantes 34 - 39 . Un estudio ha demostrado la importancia de las propiedades físicas y químicas de la superficie de implantes para su integración en el tejido óseo vivo de los conejos Nueva Zelanda 34 . En este trabajo se compararon tres tipos de superficies (mecanizada, anodizada y SLA) que fueron preparadas para su implantación en el fémur de los animales. Todas las superficies se oseointegraron, aunque no hubo diferencias significativas entre ellas con respecto al grado de oseointegración 34 .
Un estudio analiza la influencia de la superficie de implante en 4 tipos de superficies, (arenada, grabada con ácidos recubierta de hidroxiapatita, grabada con ácidos y arenada+grabada) en tibia de conejos 35 . Los investigadores encuentran una clara tendencia a mejores resultados en la arenada+grabada y en la recubierta por hidroxiapatita, aunque sin diferencias significativas. Los implantes estaban en contacto predominantemente con el hueso cortical a lo largo de las estrías cervicales, y con la médula ósea en el resto del cuerpo de los implantes. Se describió una demacración entre el hueso neoformado y el hueso primitivo 35 .
Diversos estudios experimentales realizados en conejos han valorado el grado de oseointegración de superficies arenadas y grabadas tipo SLA, aunque también con ciertas modificaciones (el grado humectabilidad, introducción en soluciones salinas, nanoporosidad), con el objetivo de identificar aquellas características físicas y/o químicas en la superficie de los implantes que puedan mejorar el grado de oseointegración 36 - 39 .
Los implantes con superficie SLA fueron comparados con implantes con superficie arenada con hidroxiapatita del mismo tamaño y diseño en la tibia de conejos. 4 semanas después de la inserción se midió la oseointegración de los implantes mediante un torque digital de remoción. La rugosidad de los implantes fué evaluado mediante un microscopio electrónico de barrido. Ambos grupos de implantes presentaron una porosidad regular sin diferencias significativas en el nivel del torque lo que indica un mismo nivel de oseointegración 37 .
CONCLUSIONES
La superficie de los implantes influye de forma significativa en la oseointegración. En este sentido, las superficies rugosas o tratadas, especialmente con procesos de arenado y/o grabado han demostrado una favorable respuesta biológica con una unión directa entre la superficie de los implantes y el hueso, en estudios realizados en animales de experimentación, sobre todo en conejos Nueva Zelanda.