INTRODUCCIÓN
La colocación de implantes dentales es una solución eficaz para la pérdida de dientes, pero su éxito a largo plazo depende de varios factores críticos como la curación del sitio quirúrgico, la osteointegración y la estabilidad del tejido óseo, entre otros. Estos aspectos son fundamentales para evitar enfermedades periimplantarias y garantizar la salud duradera del implante(1). Si bien lograr la osteointegración exitosa y la posterior rehabilitación protésica es significativo, garantizar la salud a largo plazo y la estabilidad de la restauración apoyada por implantes sigue siendo una gran preocupación. El tejido óseo exhibe una remodelación dinámica y está sujeto a resorción y remodelación bajo la influencia de varios factores, intrínsecos y extrínsecos, incluidas las particularidades específicas del paciente y posibles condiciones patológicas. La pérdida de hueso alrededor del implante es denominada pérdida ósea marginal(2). Los factores que comprometen las enfermedades periimplantarias y las reacciones inflamatorias asociadas representan los desafíos más frecuentes y clínicamente significativos. Al igual que el impacto de la enfermedad periodontal en los dientes naturales, la periimplantitis plantea obstáculos para la salud de los implantes dentales(3).
La osteoinmunología se define como una disciplina científica que estudia la interacción entre el sistema óseo y el sistema inmunológico. Esta área de investigación se centra en comprender cómo las células y moléculas del sistema inmunitario influyen en la formación, mantenimiento y degradación del hueso en la regulación de las respuestas inmunitarias(4).
Según sus aportes, la pérdida ósea marginal alrededor de los implantes dentales no es causada únicamente por bacterias patógenas asociadas a enfermedades periimplantarias, sino también por la respuesta inflamatoria del sistema inmunitario, influida por el estado general del paciente, destacando su importancia en la implantología dental(5). Los dentistas enfrentan numerosos desafíos tras la cirugía de implantes, y es fundamental que tanto los profesionales como los pacientes mantengan un cuidado y seguimiento constante para asegurar el éxito a largo plazo de los implantes2. Además, como otro factor influyente en la salud periimplantaria, se ha visto que la inflamación crónica como consecuencia de la enfermedad periodontal influye en enfermedades sistémicas como la diabetes, enfermedades cardiovasculares, respiratorias, entre muchas otras(6,7).
Para el tratamiento de la periimplantitis, se pueden emplear dos enfoques terapéuticos principales: terapias no quirúrgicas y terapias quirúrgicas. Las terapias no quirúrgicas incluyen el desbridamiento mecánico, que consiste en la limpieza de la superficie del implante; la irrigación y desinfección, utilizando soluciones antisépticas; el uso de antibióticos sistémicos y locales para controlar la infección; y otras terapias adyuvantes como el tratamiento con láser, la fototerapia, agentes antimicrobianos y el uso de probióticos(8). En casos más severos, o cuando las terapias no quirúrgicas no son efectivas, se recurre a terapias quirúrgicas. Estas incluyen la cirugía de acceso, que permite la limpieza directa de la superficie del implante mediante la elevación de un colgajo gingival; la cirugía resectiva, donde se elimina el hueso afectado; la regeneración ósea guiada, utilizando injertos óseos o membranas para promover la regeneración del hueso perdido; y en situaciones extremas donde la periimplantitis no puede ser controlada, la extracción del implante. La combinación de estas terapias se adapta según las necesidades específicas de cada paciente para lograr un tratamiento óptimo(3,9). Con el objetivo de mejorar el resultado de la terapia no quirúrgica, se ha evaluado el uso coadyuvante de antibióticos o probióticos sistémicos/locales, mostrando resultados prometedores en un número importante de casos. Sin embargo, al reunir todos los estudios, la eficacia de estas y otras medidas complementarias, tanto del tratamiento quirúrgico, como el del no quirúrgico aún no está claro(10,11).
Los probióticos, que son microorganismos beneficiosos, pueden jugar un papel clave en este proceso. Actúan inhibiendo patógenos, promoviendo la homeostasis del tejido óseo y facilitando la regeneración de los tejidos a través de la modulación de la respuesta inmunitaria e inflamatoria. Hasta ahora se han utilizado para tratar alteraciones gastrointestinales entre otras afectaciones sistémicas, pero, la investigación sugiere que los probióticos podrían ser útiles para superar los desafíos asociados con la implantación dental, aunque se requiere más investigación para confirmar su efectividad y aplicaciones clínicas(1).
La cavidad oral, como parte del sistema digestivo, es susceptible a los beneficios potenciales de los probiótico, que se utilizan comúnmente para influir en las enfermedades orales(12). Se ha descubierto que estos antagonizan a los patógenos e inhiben su virulencia, desempeñando así un papel positivo en el mantenimiento de la salud bucal y la prevención de enfermedades. Numerosos estudios han aplicado probióticos en el tratamiento de enfermedades de la mucosa oral, enfermedad periodontal, caries dental, enfermedades periimplantantes e incluso cáncer oral, con recomendaciones de administración específicas, observándose mejoras a nivel clínico, microbiológico e inflamatorio(7,12,13,14,15).
Así pues, el cuidado posterior a la implantación dental no solo depende de factores locales, sino también de la preparación sistémica del paciente. La salud de los implantes requiere una adecuada curación de los tejidos blandos, regeneración ósea, control de bacterias y modulación de las respuestas inmunitarias. Aprovechar el potencial de los microorganismos probióticos, como estrategia para promover la salud de los implantes orales, parece ser un enfoque viable. Esta scoping review tiene como objetivo resumir los posibles roles de los probióticos en la salud de los implantes dentales, sobre todo en la regeneración/osteointegración ósea, intentando proporcionar direcciones factibles para la investigación futura.
Enfermedad periodontal / periimplantitis
La enfermedad periodontal es una de las enfermedades más prevalentes a nivel oral, con un curso crónico, produciendo destrucción ósea y pérdidas dentales. Esta enfermedad puede originarse cuando hay un desequilibrio en el microbioma oral(6).
La periimplantitis se define como una condición patológica que afecta los tejidos periimplantarios y asociado con la acumulación de biopelícula dental. Se caracteriza por la inflamación de la mucosa periimplantaria y la posterior pérdida progresiva de hueso. En última instancia, esto puede resultar en el aflojamiento y el fallo del implante(16). Se considera una infección polimicrobiana asociada con Staphylococcus epidermidis y periodontopatógenos gramnegativos específicos, como Porphyromonas gingivalis, Tannerella forsythia, Fusobacterium nucleatum y Porphyromona intermedia, las cuales exhiben gran abundancia en enfermedades periimplantarias(17).
A pesar de una supervivencia superior al 90% de los implantes a largo plazo, la prevalencia de enfermedades periimplantarias es elevada. La falta de consenso en los estándares de tratamiento se debe a la heterogeneidad de enfoques terapéuticos, con resultados moderados. El tratamiento no quirúrgico es eficaz para la mucositis periimplantaria, pero presenta eficacia limitada en la periimplantitis avanzada y en casos con defectos complejos(11).
Etiología y factores de riesgo de la periodontitis/periimplantitis
La placa bacteriana o biofilm es el principal factor etiológico en la enfermedad periodontal y la respuesta del huésped determinará la progresión de esta. En el desarrollo de esta enfermedad hay tres factores a considerar: la susceptibilidad del huésped, la presencia de especies periodontopatógenas y la presencia de bacterias beneficiosas(6,18).
Los microorganismos que residen en la cavidad oral, cuando se mantienen en equilibrio (simbiosis) se habla de estado saludable, ya que estas tienen actividades pro y antiinflamatorias cruciales para mantener la homeostasis en la cavidad oral. Por el contrario, la ruptura de dicho equilibrio (disbiosis) se asocia con enfermedad y alteración de las proporciones de especies de la microbiota, predominando pocas especies y aumentando el riesgo asociado de enfermedad(6,19).
La alteración del microbioma se ha vinculado a: 1) exposición a moléculas perturbadoras (como azúcar, antibióticos, entre otros), 2) escasez de nutrientes que fomenten colonias saludables de bacterias (dietas deficientes en vegetales o con excesivas grasas saturadas) y 3) situaciones que provoquen estrés(6).
Por otro lado, se han descrito factores de riesgo locales y sistémicos que pueden hacer al huésped más susceptible a desarrollar enfermedad periodontal y pueden influir en el mantenimiento a corto y a largo plazo de los tratamientos periodontales. Entre ellos se destaca el mal control de placa, el tabaco, la diabetes mellitus no controlada, la susceptibilidad genética, el consumo de alcohol, la dieta y el estrés, factores ambientales, entre otros(20,21,22,23,24,25). Además, en un nivel de evidencia medio y medio-alto, el tabaquismo, la diabetes mellitus, la falta de profilaxis y la historia o la presencia de periodontitis se identificaron como factores de riesgo de la periimplantitis. Hay evidencia media-alta de que la edad del paciente, el sexo, la osteoporosis y los implantes zigomáticos no están relacionados con la periimplantitis(26).
Regeneración ósea en odontología
La regeneración ósea en odontología es un campo esencial para restaurar el tejido óseo maxilofacial perdido por patologías como enfermedades periodontales, traumatismos o infecciones, especialmente relevante para la estabilidad de implantes dentales. En las últimas décadas, se han perfeccionado técnicas como el uso de injertos óseos (autólogos, alogénicos, xenogénicos y aloplásticos) y biomoléculas como factores de crecimiento y proteínas morfogenéticas óseas. Además, enfoques innovadores como la ingeniería de tejidos y la terapia celular han mostrado potencial para optimizar resultados clínicos. Los retos actuales incluyen mejorar la biocompatibilidad, osteoconductividad y seguridad de los materiales, además de perfeccionar los protocolos terapéuticos (27,28,29).
Probióticos
La palabra "probióticos" se acuñó inicialmente como un antónimo para "antibióticos". Las especies bacterianas ahora reconocidas como probióticos se han utilizado desde la antigüedad para su uso en la fabricación del queso y para la fermentación de productos. A lo largo de los años, la definición de probióticos se ha refinado y ahora, de acuerdo con la Food and Agriculture Organization of the United Nations/World Health Organization (FAO/WHO) en 2001, los probióticos son definidos como microorganismos vivos cuyo consumo en adecuadas cantidades puede aportar beneficios para la salud(13,30).
El concepto que las bacterias de los probióticos podrían influir en la salud fue establecido en Rusia por el bacteriólogo Elie Metchnikoff, que reportó que la esperanza de vida de Bulgaria era mayor supuestamente por su consumo de leche fermentada que contenía Lactobacillus bulgaricus30. Las especies de probióticos más usados y que, por lo tanto, llevan más seguimiento serían: Lactobacillus, Bifidobacterium, Lactococus, Streptococcus, Enterococcus(31).
Los beneficios de los probióticos han sido ampliamente estudiados a nivel sistémico y se ha demostrado su efecto positivo en diferentes patologías, tales como determinadas enfermedades gastrointestinales, infecciones urogenitales, etc(32,33). También se han observado efectos favorables a nivel oral, en la prevención y tratamiento de la enfermedad periodontal(34,35) y periimplantaria(10), la caries(36,37) y la candidiasis oral(14,38).
El probiótico más utilizado en estudios periodontales, es L. Reuteri, ya que, se ha visto en estudios in vitro que produce un compuesto antimicrobiano llamado Reuterina, que tiene un efecto inhibitorio contra los principales patógenos periodontales. Existen muchos subtipos: L. plantarum, L. paracasei, L. acidophilus, L. casei, L. rhamnosus, L. crispatus, L. gasseri, L. reuteri, L. bulgaricus(39).
Por definición los probióticos tendrían que ser seguros en animales, resistentes a los ácidos biliares, y con posibilidad de adherirse y colonizar el intestino. En Europa, se introdujo el término de QPS (Qualified Presumption of Safety) que incluye criterios adicionales de seguridad, incluyendo la historia de uso seguro y la ausencia de riesgo de resistencia a los antibióticos(31,40).
Efectos orales
Diversos estudios clínicos demuestran que el consumo regular de probióticos de Lactobacillus paracasei SD1 disminuye el nombre de Estreptococos cariogénicos en la placa salival y dental, y por lo tanto reduce el riesgo de caries(36,37). Sin embargo, un estudio realizado con L. reuteri reporta que no hay diferencias significativas en la reducción de Estreptococos cariogénicos(41). Asimismo, hay algunos estudios que revelan que el probiótico Lactobacillus puede reducir la inflamación gingival, mejorando la salud periodontal y disminuyendo la concentración de P. gingivalis en la saliva y en la placa subgingival(42,43,44). Aunque también hay estudios que revelan que los probióticos no mejoran los parámetros clínicos de la gingivitis(43,45,46).
Se ha visto en estudios clínicos que el tratamiento periodontal convencional unido a probióticos puede mejorar la disbiosis y produce mejoras clínicas significativas de la enfermedad. Por otro lado, se ha demostrado que los probióticos disminuyen la secreción de citoquinas proinflamatorias como TNF, IL-1, IL-8, IL-17, mejorando así la actividad inflamatoria de esta enfermedad y mejorando el curso de esta(15). De la misma forma, en diversos ensayos sobre periimplantitis tratados con Lactobacillus reuteri muestran una mejora significativa de todos los parámetros clínicos de esta enfermedad, con reducción de los niveles de citoquinas proinflamatorias(10,47,48).
En los casos de halitosis, estudios que han utilizado Lactobacillus salivarius indican tener un efecto positivo en la disminución de esta y en la mejoría de la percepción del propio paciente(49,50). Asimismo, se ha reportado que como tratamiento de la candidiasis las especies Lactobacillus y Bifidobacterium, reducen significativamente los niveles de cándidas, como en un ensayo que se obtuvo una reducción de niveles de cándidas del 16,7% respecto al 92,0% del grupo placebo. Por lo tanto, puede ser usado para prevenir las candidiasis, aunque no existe una clara mejoría de la clínica de las estomatitis en todos los estudios(14,38,51,52). No obstante, todos estos efectos mencionados anteriormente, no se mantienen a lo largo del tiempo en el huésped después de su uso.
Tratamiento de enfermedades periimplantares con probióticos
Las enfermedades periimplantarias se clasifican en "mucositis periimplantar" (que involucra solo tejidos blandos) y "periimplantitis" (que involucra tanto tejidos blandos como duros)(16). En general, la mucositis periimplantar, si no se trata, puede progresar a periimplantitis. Las enfermedades periimplantarias pueden causar daños a los tejidos blandos y duros periimplantarios y conducir directamente a un fracaso del implante(53).
Durante mucho tiempo se ha demostrado que los probióticos son un tratamiento para las infecciones, incluida la disbiosis y las enfermedades infecciosas dentro de la cavidad oral(54). Estos microorganismos beneficiosos pueden inhibir la colonización de bacterias patógenas alrededor de los implantes dentales, lo que ayuda a equilibrar la microbiota oral y ejerce un efecto antiinfeccioso, beneficiando específicamente en el manejo de enfermedades periimplantarias(55).
Microscópicamente, los probióticos ejercen sus efectos de la Manera especificada en la Figura 1. Por lo tanto, los probióticos muestran un efecto inhibidor directo sobre los patógenos, es decir, dificultan directamente el crecimiento y la proliferación de microorganismos patógenos en el cuerpo humano. Se ha demostrado que las cepas probióticas como Weissella cibaria, Limosilactobacillus reuteri y Lactobacillus salivarius inhiben significativamente el crecimiento de patógenos de la periimplantitis como Porphyromonas gingivalis, Fusobacterium nucleatum, Prevotella intermedia, Tannerella forsythia y Staphylococcus aureus in vitro(56, 57). También afectan a la colonización de estas bacterias en las superficies de titanio(57).

Figura 1. Mecanismo local de los probióticos en la lucha contra las enfermedades periimplantarias. Basada en: Xu J y cols.(1).
Streptococcus salivarius ha demostrado capacidad para inhibir biopelículas patógenas en implantes in vitro, sugiriendo su potencial en la prevención de enfermedades periimplantarias (58). Bifidobacterium y Lactobacillaceae, como Limosilactobacillus fermentum y Lactobacillus acidophilus, también inhiben patógenos como Porphyromonas gingivalis mediante la producción de peróxido de hidrógeno, bacteriocinas y ácidos orgánicos(59, 60).
En estudios anteriores, se encontró que Limosilactobacillus reuteri ejerce efectos antibacterianos mediante la utilización de reuterina para oxidar patógenos de la periimplantitis 61. Algunos autores descubrieron que Lactococcus lactis que produce nisina (una bacteriocina) exhibía efectos inhibitorios contra varios patógenos de la periimplantitis como Fusobacterium nucleatum, Porphyromonas gingivalis y Treponema denticola. Este Lactococcus lactis en particular puede interrumpir la formación de biopelícula de bacterias patógenas en la superficie de los materiales de implantes(62).
Los probióticos compiten con otra microbiota oral, particularmente por los nutrientes y los sitios de unión. Debido a su propia ventaja competitiva en términos de nutrientes y factores de crecimiento, Bifidobacterium puede inhibir competitivamente los patógenos de la enfermedad periimplantaria como Porphyromonas gingivalis(63). La bifidobacteria puede tener implicaciones potenciales para la agregación bacteriana y la formación de biopelículas de patógenos, ya que puede competir por los sitios de unión y, en consecuencia, afectar la coagregación de patógenos(64).
Además, otros autores, realizaron una revisión sistemática del efecto del Lactobacillus reuteri en el tratamiento de la periimplantitis, concluyendo que, el uso de probióticos, ya sea como tratamiento básico o complementario de las enfermedades periimplantarias, mostró una tendencia hacia la significación(65).
Así pues, los probióticos, especialmente Lactobacillus y Bifidobacterium, parecen tener un gran potencial para prevenir enfermedades periimplantarias al inhibir el crecimiento de patógenos y afectar la formación de biopelículas en la cavidad oral. Aunque los estudios clínicos a gran escala sobre su uso en la prevención de estas enfermedades son escasos, la literatura existente sugiere que podrían convertirse en herramientas clave para el manejo y prevención de enfermedades periimplantarias.
Probióticos en regeneración ósea y homeostasis ósea
La restauración exitosa de implantes dentales se basa en la estabilidad. Una vez el cirujano ha colocado los implantes, a relación hueso-implante se vuelve interdependiente, con su éxito-fracaso entrelazados. La teoría de la osteointegración propuesta inicialmente por el profesor Brånemark, sigue siendo ampliamente aceptada y utilizada hoy en día(66).
La osteointegración es el contacto directo y la unión cercana entre el implante y el tejido óseo, sin ningún otro componente tisular intermedio y algunos autores lo definen como reacción de cuerpo extraño, donde la interfaz genera un hueso compacto como una respuesta defensiva, y los implantes orales utilizan este tipo de reacción(67). Requiere la capacidad de diferenciación osteogénica y regeneración ósea y depende del sistema inmunitario y de la capacidad del paciente para la regeneración ósea. Este proceso, similar a la curación de fracturas, incluye osteogénesis, inflamación y angiogénesis. En casos de volumen óseo insuficiente, se emplean técnicas de aumento óseo, siendo crucial la estabilidad y prevención de la pérdida ósea marginal para la longevidad del implante(68).
Investigaciones recientes han demostrado que los probióticos ejercen efectos beneficiosos sobre el tejido óseo sistémico incluso sin contacto directo(69). Aunque el hueso se considera tradicionalmente un entorno estéril, se ha reconocido la influencia significativa de la microbiota intestinal en la salud ósea a través del denominado eje intestino-hueso, donde los probióticos actúan como moduladores clave de la homeostasis y metabolismo óseo(70).
La evidencia de los efectos beneficiosos de los probióticos vino inicialmente de estudios sobre la curación de fracturas y el tratamiento de la osteoporosis, lo que indica sus efectos sistémicos. Numerosos estudios en animales y en humanos han encontrado que la administración de varias cepas probióticas, como las especies de Lactobacillaceae y Bifidobacterium, puede acelerar la curación de fracturas, promover la diferenciación osteogénica y mejorar los parámetros trabeculares óseos(71,72,73). La suplementación con cepas específicas de Bifidobacterium, particularmente en la población anciana, puede acelerar la reparación de la fractura(73).
En modelos de osteoporosis inducida por varios factores, se ha demostrado que la administración de probióticos como Lactobacillaceae y Bifidobacterium aumenta la densidad ósea, atenúa la pérdida ósea y mantiene la homeostasis ósea(74,75). En el modelo animal del pez cebra, los probióticos como Lactococcus lactis y Bacillus subtilis también pueden promover la diferenciación osteogénica y la formación ósea(76).
Para la salud de la mandíbula, el papel de los probióticos también es importante77. También ha habido estudios que exploran el papel de la aplicación local de probióticos en la promoción de la osteointegración de implantes, lo que ha mostrado resultados prometedores. Se encontró que la biopelícula de Lacticaseibacillus casei inactivada localmente en la superficie del implante puede acelerar la osteointegración y mejorar su eficacia(78).
Actualmente, el impacto de los probióticos en el tejido óseo se origina principalmente en el intestino. Las cepas probióticas del intestino desempeñan un papel positivo en la promoción de la salud y la estabilidad de los huesos de la mandíbula. Se cree que los mecanismos por los cuales los probióticos ejercen sus efectos sobre el tejido óseo implican varios aspectos interconectados.
Probióticos y regulación de niveles de inflamación
Los probióticos ejercen un mecanismo adicional significativo para promover la cicatrización de heridas, que implica reducir la regulación de las citocinas proinflamatorias mientras se reducen a la regulación de los factores antiinflamatorios(61,79).
Cepas de Lactobacillus, pueden reducir eficazmente la expresión de IL-1β y TNF-α, que son citoquinas proinflamatorias, en el tejido epitelial gingival dañado(80). En heridas diabéticas: Lactobacillus bulgaricus y Lactiplantibacillus plantarum reduce significativamente los niveles de IL-1β y TNF-α. En particular Lacticaseibacillus casei inhibe modestamente la expresión de varias citocinas proinflamatorias, como IL-1β, IL-2, IL-6, IL-12, IL-17α, IFN-γ y TNF-α(81).
Los probióticos regulan los factores antiinflamatorios locales. Lactiplantibacillus plantarum mejora la expresión de IL-10 en los tejidos de la mucosa postoperatoria, contribuyendo a un entorno de curación favorable(82). La administración de Limosilactobacillus reuteri induce la regulación ascendente de la citocina antiinflamatoria IL-10, minimizando así el daño tisular en el borde de la herida y regulando aún más el mediador antiinflamatorio IL-17ª(83).
Resumiendo, después del tratamiento con sobrenadantes probióticos o probióticos, hay una disminución significativa en los niveles locales de inflamación81. Numerosos estudios sugieren que los efectos beneficiosos de los probióticos en la cicatrización de heridas están estrechamente asociados con su capacidad para modular la inflamación(61).
Probióticos y promoción de angiogénesis
En implantología oral, la angiogénesis es indispensable. Estudios limitados han indicado que ciertos probióticos pueden estimular la angiogénesis local al inducir la producción de VEGF, lo que promueve el crecimiento y migración de células endoteliales(61). En un modelo de fractura en ratones, Akkermansia muciniphila ha demostrado inducir la formación de vasos tipo H en el callo óseo, favoreciendo la regeneración ósea. Sin embargo, se necesitan más investigaciones para confirmar estos efectos en la regeneración de tejido óseo periimplantario(84).
Probióticos y curación de heridas
La velocidad y la calidad de la cicatrización de heridas después de la cirugía de implantes son factores cruciales y fácilmente observables. Una buena cicatrización de heridas es uno de los requisitos previos para la oseointegración posterior del implante y el control de la infección(85).
Después de la aparición de una herida de la mucosa oral, el proceso de curación se desarrolla a través de distintas etapas: hemostasia, respuesta inflamatoria, proliferación y remodelación. A los pocos minutos del inicio de la herida, se desencadena una cascada de reacciones hemostáticas. Posteriormente, se produce una respuesta inflamatoria en el transcurso de varios días(86). Es una realidad el papel de los probióticos en la curación de heridas. Inicialmente se descubrió en la piel, pero más adelante, se vio que la aplicación local o sistémica de probióticos en pacientes después de quemaduras o cirugía puede acelerar la cicatrización de heridas y reducir las complicaciones relacionadas con las heridas(87). Concretamente, en pacientes con trastornos de cicatrización como la diabetes, los probióticos pueden tener un buen efecto en la cicatrización de heridas(88).
Numerosos estudios que se centran en la importancia de los probióticos en la cicatrización de heridas orales. Se demostró que la aplicación local de limosilactobacillus reuteri lysate mejoró significativamente la cicatrización de heridas en un modelo de herida gingival de ratón y en heridas de la zona del paladar del ratón(55,89). En la Figura 2 se hace un resumen de los diferentes beneficios(1).
Probióticos y absorción de nutrientes
Los probióticos pueden contribuir a la salud del esqueleto, ya que se ha demostrado que varios probióticos, como Lactobacillus acidophilus, Lacticaseibacillus casei, Limosilactobacillus reuteri y Bifidobacterium longum, mejoran la absorción de calcio, vitamina D y vitamina K, satisfaciendo las demandas esquléticas de los tratamientos con implantes(74,90). Estos nutrientes se consideran cruciales para la osteointegración del implante y la estabilidad del tejido óseo circundante(91,92).
Justificación
La periimplantitis o enfermedad periimplantaria, como enfermedad de gran prevalencia a nivel mundial, con tantas implicaciones locales y sistémicas, así como la necesidad de tratamientos quirúrgicos que precisan regeneraciones y consecuentemente suelen provocar inflamación, exige buscar alternativas terapéuticas más eficaces y con menos efectos secundarios.
Las limitaciones de los tratamientos actuales, como sería el riesgo a complicaciones quirúrgicas, el creciente desarrollo de resistencias bacterianas debidas al uso inadecuado de antibióticos, provocan necesidades de buscar otras estrategias terapéuticas.
Los resultados encontrados con los probióticos como medida de intervención, parecen tener un valor intrínseco debido a sus beneficios, incluido un riesgo de seguridad relativamente bajo y un modo de intervención no invasivo. Son considerados coadyuvantes al tratamiento de colocación de implantes, enfermedad periimplantaria, enfermedad periodontal y patología de mucosa oral, entre muchos otros beneficios para la salud en general, cosa que nos permite establecer un nuevo enfoque terapéutico con resultados prometedores.
Es por los motivos descritos y teniendo en cuenta que los probióticos podrían ser dignos de un uso generalizado, con este estudio se pretende evaluar si fuera posible el uso de los probióticos también en procedimientos quirúrgicos de regeneración ósea.
En base a todo lo anterior nuestro objetivo fue evaluar el posible uso de los probióticos en los procedimientos quirúrgicos de regeneración ósea. Para ello realizamos una "scoping review", para intentar identificar y sintetizar la información disponible en la literatura.
MATERIAL Y MÉTODOS
Desarrollo de protocolo y pregunta
El protocolo de esta "scoping review" siguió la declaración PRISMA-ScR (Preferred Reporting Items for Systematic Review and Meta-Analyses, for Scoping Reviews). Este protocolo, tiene como objetivo encontrar la máxima evidencia posible para responder la siguiente pregunta específica (PCC): "¿El uso de probióticos como coadyuvantes en procedimientos quirúrgicos de regeneración ósea podría mejorar significativamente la formación y calidad del nuevo tejido óseo en comparación con los métodos sin probióticos?"
Inclusión (PCC)
-Población: población humana, animal o in vitro sometida a procedimientos quirúrgicos de regeneración ósea. -Concepto: uso de probióticos como coadyuvantes para mejorar la formación y calidad del tejido óseo. -Contexto: procedimientos quirúrgicos de regeneración ósea comparados con métodos tradicionales sin el uso de probióticos.
Exclusión
Que no cumplan con los criterios anteriores, que no estén en inglés, duplicados y anteriores al año 2014.
Tipos de intervención y comparación
Se seleccionaron los estudios que pudieran valorar el posible el uso de los probióticos a nivel de regeneración oral.
Fuentes de información y búsqueda
Se realiza una búsqueda electrónica y para ello se utilizaron tres bases de datos electrónicas como fuentes en la búsqueda de estudios que cumplieron los criterios de inclusión: (1) PubMed; (2) Biblioteca Cochrane (incluida la base de datos Cochrane para revisiones sistemáticas y el registro Cochrane CENTRAL para ensayos clínicos). Se buscaron en estas bases de datos estudios publicados durante los últimos 10 años, en inglés, y a texto completo. La búsqueda se limitó a sujetos tanto humanos como animales y a estudios informados en inglés. No se consideraron más idiomas. Los términos buscados fueron: (("Probiotics" [MeshTerms]) AND ("Oral bone regeneration"[MeshTerms])); (("Probiotics" [MeshTerms]) AND ("Oral bone augmentation"[MeshTerms]); (("Probiotics" [MeshTerms]) AND ("Zebra Fish" [MeshTerms]) "[MeshTerms]) AND ("Oral bone regeneration"[MeshTerms])) - Pubmed i Cochrane.
Luego se realiza una búsqueda manual y para ello se verificaron todas las listas de referencias de los estudios incluidos y las revisiones sistemáticas publicadas previamente. También se realizaron búsquedas manuales en revistas como Journal of Clinical Periodontology, Journal of Periodontology, entre otras, durante los años 2014 y 2024.
Métodos de detección
Dos revisores (R.P.R. y C.O.C.) examinaron de forma independiente los títulos y resúmenes. Los dos revisores seleccionaron los manuscritos completos de los estudios que cumplían con los criterios de inclusión, así como aquellos cuyos títulos y resúmenes no proporcionaban datos suficientes para tomar una decisión clara. Cuando hubo discrepancias se consultó con S.E.M y J.L.L.
RESULTADOS
Selección y descripción de los estudios
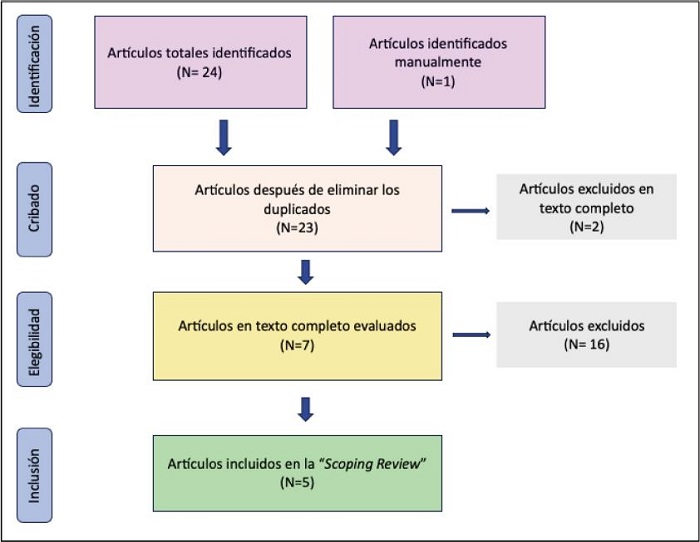
Se encontraron 26 artículos en la búsqueda. Después de leer los títulos y los resúmenes, se excluyeron 17 porque no cumplían con el objetivo, el texto completo no estaba disponible o trataban otras enfermedades o tipo de tratamiento que no fuese la regeneración ósea con probióticos. Fueron evaluados 7 artículos en texto completo y se eliminaron 2 ensayos por no cumplir los criterios de inclusión y exclusión, ni adecuarse a responder la hipótesis planteada, ya que uno se centra inhibición de la diferenciación de osteoclastos y la reducción de la resorción ósea, particularmente en el contexto de la periodontitis, sin abordar la regeneración del tejido óseo(93); y otro fue excluido por no examinar directamente el efecto de la administración de probióticos específicos, si no los cambios en la microbiota(94). Un total de 5 ensayos clínicos fueron incluidos en esta revisión. En la figura 3 se presenta el diagrama de flujo.
Características generales de los estudios incluidos
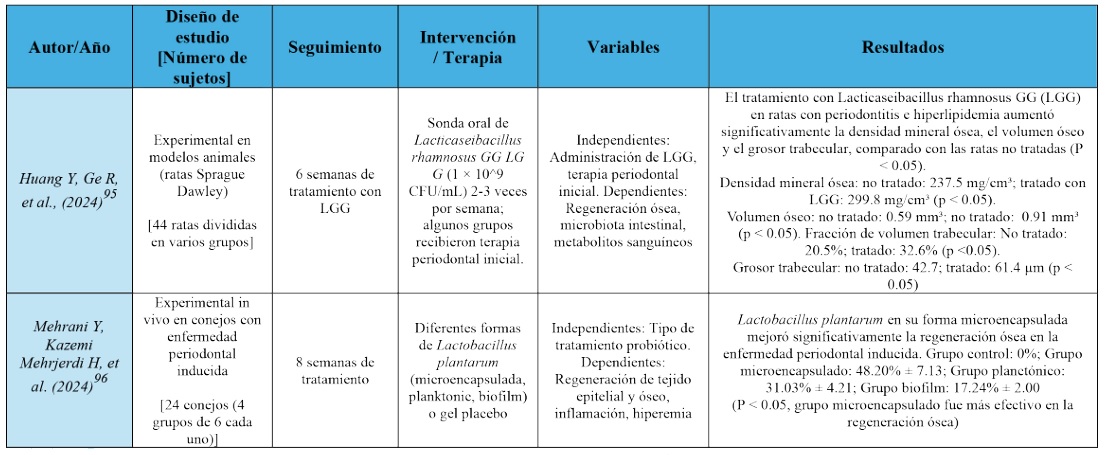
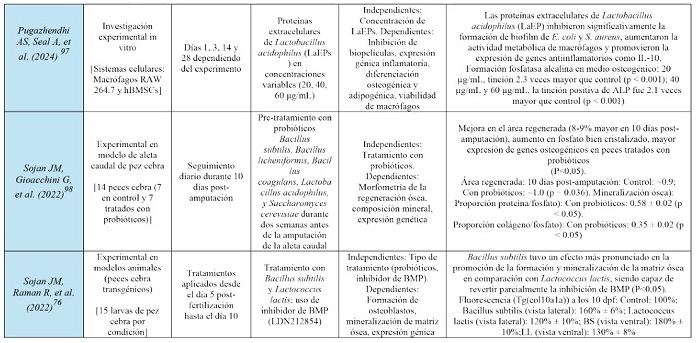
Las características generales presentadas, se reflejan en la Tabla 1. Se analizaron diversos estudios experimentales que investigan el uso de probióticos y sus derivados en la regeneración ósea, tanto en modelos animales como en estudios in vitro. Todos compararon el efecto de tratamientos con probióticos frente a controles, evaluando la regeneración ósea, la modulación de la inflamación y la prevención de infecciones.
Cuatro estudios utilizaron modelos animales para investigar la regeneración ósea: ratas con periodontitis e hiperlipidemia inducidas(93), conejos con enfermedad periodontal inducida(94), peces cebra (incluyendo líneas transgénicas) para estudiar el efecto de probióticos en la formación ósea(76,95,98). Un estudio empleó cultivos celulares de macrófagos RAW 264.7 y células madre mesenquimales derivadas de la médula ósea humana (hBMSCs) para evaluar la acción de proteínas extracelulares aisladas de Lactobacillus acidophilus(97).
Los estudios en animales, concretamente en ratas, conejos y peces cebra incluyeron entre 14 y 44 sujetos, con tratamientos que duraron de 6 a 8 semanas(95,96). En peces cebra, se realizó un seguimiento diario durante 10 días post-amputación, en peces zebra con "Bactosafe H" (Bacillus subtilis, Bacillus licheniformis, Bacillus coagulans, Lactobacillus acidophilus, y Saccharomyces cerevisiae)(98,76). En los estudios in vitro, en cambio, los cultivos celulares fueron tratados y evaluados en periodos que varían desde 1 día hasta 28 días, según el experimento(97).
Los estudios emplearon diferentes especies de probióticos, como Lacticaseibacillus rhamnosus GG(95) y Lactobacillus plantarum(96), administrados en formas variadas (microencapsulada, biofilm) y dosis (1 × 10^9 CFU/mL). En peces cebra, se usaron Bacillus subtilis y Lactococcus lactis76, además de un pre-tratamiento con probióticos antes de la amputación de la aleta caudal(98).
Además, algunos autores combinaron la administración de probióticos con terapias adicionales (en este caso periodontales iniciales), como enjuagues y desbridamiento de bolsillos gingivales antes de la aplicación del probiótico(96).
Todos los estudios observaron una mejora en la regeneración ósea con el uso de probióticos, evaluada mediante densidad mineral ósea, volumen óseo, grosor trabecular, y formación de osteoblastos. Se demostró un incremento significativo en la densidad mineral ósea y volumen óseo en ratas tratadas con L. rhamnosus GG(95), mayor regeneración ósea en conejos tratados con L. plantarum en forma microencapsulada(96), mejora en la morfometría y la composición mineral en peces cebra tratados con probióticos(98) y aumento de la formación de osteoblastos y mineralización de la matriz ósea con Bacillus subtilis(76).
Por otro lado, se observó una regulación positiva de la inflamación crónica mediante la promoción de un fenotipo de macrófagos M2, con un aumento en la expresión de genes antiinflamatorios (IL-10, TGF-β) y una reducción de marcadores proinflamatorios (RANKL, CTSK)(97). Además de valorar la prevención de infecciones, evaluando la formación de biopelículas, las proteínas derivadas de probióticos inhibieron la formación de biopelículas patógenas, como las de S. aureus, MRSA, y E. coli(97).
Resultados de los estudios
La investigación reciente ha puesto de relieve el potencial de diversos probióticos en la mejora de la regeneración ósea, especialmente en contextos de enfermedades periodontales y otras condiciones que afectan la salud ósea. Los estudios revisados revelan que probióticos como Lacticaseibacillus rhamnosus GG, Lactobacillus plantarum, Bacillus subtilis, Bacillus licheniformis, Bacillus coagulans, Lactobacillus acidophilus, y Saccharomyces cerevisiae, y proteínas extracelulares de Lactobacillus acidophilus han mostrado efectos positivos en la promoción de la osteogénesis, la regulación de la inflamación y la inhibición de la formación de biopelículas patógenas. Todos los resultados concluyeron que los probióticos o sus componentes derivados tienen un efecto positivo significativo en la regeneración ósea(76,95,96,98,97).
En modelos con animales, concretamente en ratas con periodontitis e hiperlipidemia inducidas, Lacticaseibacillus rhamnosus GG (LGG) mejoró la densidad mineral ósea, el volumen óseo, y el grosor trabecular, además de modular favorablemente la microbiota intestinal y los metabolitos sanguíneos que contribuyen a la osteogénesis(95). En conejos con enfermedad periodontal inducida, Lactobacillus plantarum en su forma microencapsulada mostró la mayor regeneración ósea en comparación con otras formas del probiótico y con el grupo control(96). Y en modelos de pez cebra, el tratamiento con probióticos aceleró la regeneración ósea y mejoró la calidad del hueso regenerado, incrementando la mineralización y la expresión de genes osteogénicos, revertiendo la inhibición de BMP, un importante regulador de la osteogénesis(76,98). En estudios in vitro en cambio, las proteínas extracelulares de Lactobacillus acidophilus (LaEPs) aumentaron significativamente la diferenciación osteogénica y la deposición de minerales en células madre mesenquimales humanas, mientras que redujeron la adipogénesis, sugiriendo un efecto positivo en la formación ósea(97).
Por otro lado, varios estudios demostraron que los probióticos y sus derivados modulan eficazmente la respuesta inflamatoria, favoreciendo un entorno que promueve el procedimiento de regeneración ósea(76,95,96,97,98). Se reveló que las proteínas extracelulares de Lactobacillus acidophilus inhiben la formación de biopelículas patógenas y promueven la diferenciación osteogénica mientras regulan la inflamación crónica. Las LaEPs promovieron un cambio hacia un fenotipo de macrófagos M2, que es antiinflamatorio y reparador. Este cambio se reflejó en un aumento de la expresión de genes antiinflamatorios (IL-10, TGF-β) y una reducción de marcadores proinflamatorios (RANKL, CTSK)(97). En el estudio con ratas, LGG moduló la inflamación sistémica al alterar los metabolitos sanguíneos y enriquecer la microbiota intestinal con géneros bacterianos beneficiosos que se correlacionaron positivamente con la regeneración ósea. Así pues, pudiendo ser especialmente favorable en pacientes con factores de riesgo sistémicos como la hiperlipidemia(95).
Los estudios que investigaron la capacidad de los probióticos para prevenir infecciones demostraron su eficacia en la inhibición de la formación de biopelículas patógenas. Las LaEPs mostraron un efecto inhibidor significativo sobre la formación de biopelículas de Staphylococcus aureus, MRSA, y Escherichia coli. Este efecto fue dependiente de la dosis y se caracterizó por un efecto bacteriostático, que impidió la proliferación y la formación de biopelículas(97).
En conjunto, Lacticaseibacillus rhamnosus GG, Lactobacillus plantarum, Bacillus subtilis, y Lactobacillus acidophilusemergen como los probióticos más destacados en la investigación actual sobre regeneración ósea(76,95,96,97,98). Concretamente el probiótico Lactobacillus plantarum podría ser particularmente útil en terapias periodontales, sugiriendo su potencial aplicabilidad en tratamientos de regeneración ósea en la cavidad oral(96). Los estudios revisados sugieren que estos probióticos tienen gran potencial como coadyuvantes de la regeneración ósea, la modulación favorable de la inflamación y prevención de infecciones en diferentes modelos experimentales. podrían ser aplicables en tratamientos de regeneración ósea oral, mejorando la formación y calidad del nuevo tejido óseo y controlando la inflamación, lo cual es esencial para el éxito de intervenciones como los implantes dentales y la terapia periodontal(76, 95,96,97,98). Estos hallazgos son prometedores para su futuro uso en entornos clínicos, especialmente en tratamientos que requieren la regeneración ósea y control de infecciones, como en implantes dentales y otras intervenciones orales, ofreciendo una nueva perspectiva para su uso clínico en medicina regenerativa.
DISCUSIÓN
La presente "Scoping Review", pudo identificar 5 estudios publicados que evalúan medidas complementarias con potencial para el tratamiento de regeneración ósea. Los resultados obtenidos a partir de los estudios experimentales revisados proporcionan un marco sólido para explorar el uso de probióticos y sus derivados en la regeneración ósea, destacando su potencial no solo en la osteogénesis, sino también en la modulación de la inflamación y la prevención de infecciones. La evidencia apunta de manera consistente a que probióticos como Lacticaseibacillus rhamnosus GG(95), Lactobacillus plantarum(96), Bacillus subtilis(76), Bacillus licheniformis, Bacillus coagulans, Lactobacillus acidophilus, y Saccharomyces cerevisiae(96) y proteínas extracelulares de Lactobacillus acidophilus(97) juegan un papel significativo en la mejora de la regeneración ósea, tanto en modelos animales como en estudios in vitro.
En particular, los estudios realizados en modelos animales con ratas, conejos y peces cebra demostraron mejoras notables en la regeneración ósea tras el tratamiento con probióticos(98). Estos resultados destacan la capacidad de los probióticos para influir en parámetros clave de la salud ósea, como la densidad mineral ósea, el volumen óseo y la formación de osteoblastos. Estos hallazgos son consistentes en distintos modelos experimentales, lo que sugiere un efecto generalizado de los probióticos en la regeneración ósea, independientemente de las especies o condiciones específicas de estudio.
Un aspecto crucial que emerge de los estudios es la capacidad de los probióticos para modular la respuesta inflamatoria, particularmente a través de la promoción de un fenotipo de macrófagos M2 antiinflamatorio, como se evidenció en los estudios in vitro con proteínas extracelulares de Lactobacillus acidophilus. Este cambio en la inflamación, junto con la reducción de marcadores proinflamatorios como RANKL y CTSK, sugiere que los probióticos no solo promueven la regeneración ósea directamente, sino que también crean un entorno biológico más propicio para dicho proceso. Este aspecto es especialmente relevante en condiciones inflamatorias crónicas, como la periodontitis, donde el control de la inflamación es fundamental para la reparación ósea efectiva(97).
Asimismo, el efecto antimicrobiano observado en varios estudios es otro punto clave a considerar. La capacidad de las proteínas derivadas de probióticos, como las LaEPs, para inhibir la formación de biopelículas patógenas, incluyendo especies como Staphylococcus aureus y MRSA, presenta una ventaja significativa en el contexto de la regeneración ósea, especialmente en entornos clínicos donde las infecciones pueden comprometer la cicatrización ósea y la integración de implantes dentales. Este efecto bacteriostático, junto con la modulación inflamatoria y la promoción de la osteogénesis, refuerza la idea de que los probióticos pueden ser herramientas multifuncionales en el tratamiento de patologías óseas y periodontales.
Limitaciones
No obstante, a pesar de los resultados prometedores, es importante señalar algunas limitaciones de los estudios revisados. En primer lugar, una de las limitaciones es que los estudios revisados utilizan modelos animales (ratas, conejos, peces cebra) o sistemas celulares in vitro. Aunque estos modelos proporcionan información valiosa sobre los mecanismos biológicos, los resultados no siempre son directamente transferibles a humanos.
El tamaño de muestra es pequeño, esto puede afectar la potencia estadística y la generalización de los resultados, ya que aumenta la variabilidad de los resultados y puede no reflejar la respuesta en una población más amplia o diversa.
En muchos de los artículos, falta seguimiento a largo plazo, en muchos casos, el tiempo de observación es relativamente corto (de días a semanas). La regeneración ósea y la respuesta a los tratamientos probióticos pueden requerir un seguimiento a más largo plazo para evaluar plenamente la calidad y la sostenibilidad del nuevo tejido óseo.
En cuanto a la variabilidad en los protocolos de administración, los estudios emplearon diferentes especies de probióticos, dosis y formas de administración, lo que introduce cierta heterogeneidad en los resultados. Sin embargo, este aspecto también abre la puerta a futuras investigaciones para optimizar las dosis y las combinaciones de probióticos que puedan ofrecer los mejores resultados en entornos clínicos.
Finalmente, aunque los estudios muestran beneficios potenciales de los probióticos, no comparan directamente estos enfoques con los métodos clínicos estándar utilizados en la regeneración ósea oral, como los injertos óseos, el uso de membranas o elevaciones de seno, por ejemplo. Esto limita la capacidad de evaluar si los probióticos ofrecen una ventaja significativa en un entorno clínico real.
Implicaciones clínicas y futuras investigaciones
Los hallazgos de esta "Scoping review" sugieren que los probióticos tienen un gran potencial como coadyuvantes en la regeneración ósea, particularmente en el contexto de la odontología y la medicina regenerativa. Específicamente, la mejora de la formación ósea y el control de la inflamación proporcionan una base sólida para considerar el uso de probióticos en tratamientos como los implantes dentales y la terapia periodontal, donde la calidad del tejido óseo y la prevención de infecciones son factores cruciales para el éxito del tratamiento.
En futuras investigaciones, sería recomendable explorar la sinergia entre probióticos y otras terapias regenerativas, como la ingeniería tisular o el uso de biomateriales, para mejorar aún más los resultados clínicos. Además, estudios clínicos bien diseñados en pacientes humanos serán esenciales para validar los efectos observados en modelos experimentales y para determinar la seguridad, efectividad y dosificación óptima de probióticos en escenarios clínicos.
En resumen, los resultados de esta revisión resaltan el potencial clínico de los probióticos en la regeneración ósea, ofreciendo una vía prometedora para futuras aplicaciones en la odontología regenerativa y otras áreas de la medicina que requieren la regeneración ósea.
CONCLUSIONES
Los probióticos ofrecen una serie de beneficios notables en el cuerpo humano, particularmente en el contexto de la implantología oral, ya que tienen la capacidad de influir tanto en los tejidos duros como en los blandos, mejorando el pronóstico de los implantes a través de la promoción de la regeneración tisular, la exhibición de propiedades antimicrobianas y la reducción de la inflamación local. Además, a nivel sistémico, los probióticos pueden regular las respuestas inmunoinflamatorias y mejorar la absorción de nutrientes.
De acuerdo los resultados obtenidos con los estudios, se confirma que la administración de probióticos muestra un gran potencial como coadyuvantes en la regeneración ósea oral, ya que puede ofrecer beneficios mejorando la densidad y calidad del tejido óseo. También puede reducir la inflamación y la inhibición de biopelículas patógenas, factores cruciales para el éxito de la regeneración ósea en la cavidad oral.
Es crucial seleccionar cepas probióticas específicas que ofrezcan beneficios óptimos, dado que diferentes cepas pueden tener efectos variados en la osteogénesis, la curación de heridas y la lucha contra los patógenos periimplantarios.
En conclusión, aunque los probióticos muestran un gran potencial para mejorar la salud del implante y la regeneración ósea, es necesario un enfoque cuidadoso y basado en la evidencia con protocoles clínicos para confirmar su eficacia y seguridad en el campo de la cirugía oral regenerativa, por lo que se hacen necesarias futuras investigaciones en este campo.