Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos de la Sociedad Española de Oftalmología
versión impresa ISSN 0365-6691
Arch Soc Esp Oftalmol vol.87 no.2 feb. 2012
Resultados a medio plazo de dispositivos de drenaje para glaucoma en pacientes pediátricos
Intermediate results on the use of drainage devices for paediatric glaucoma
T. Colás-Tomás, E. Gutiérrez-Díaz, P. Tejada-Palacios, A. Barceló-Mendiguchía y E. Mencía-Gutiérrez
Servicio de Oftalmología, Hospital 12 de Octubre, Universidad Complutense, Madrid, España
Dirección para correspondencia
RESUMEN
Propósito: Evaluar los resultados y complicaciones a largo plazo de los dispositivos de drenaje para glaucoma (DDG) en pacientes pediátricos (0-15 años).
Material y métodos: Estudio retrospectivo de cohortes de 17 DDG implantadas desde julio de 1994 hasta abril del año 2007 en 14 pacientes (17 ojos). En dos pacientes (3 ojos) se implantó un DDG de Molteno (DDGM) y en 12 pacientes (14 ojos) un DDG de Ahmed (DDGA). Se han recogido datos demográficos y relacionados con la afección glaucomatosa de cada paciente. Se ha estudiado el porcentaje de éxito de la cirugía, así como el tiempo durante el cual se ha mantenido controlada la tensión desde el implante del dispositivo y las complicaciones derivadas de este.
Resultados: De los 14 pacientes, nueve (64,28%) presentaban glaucoma congénito, y cinco (35,71%) glaucoma afáquico secundario a cirugía de catarata. La media de la presión intraocular (PIO) preoperatoria fue de 29,82mmHg (DS: 6,98). La media de la PIO posquirúrgica fue de 14,05mmHg (DS: 7,57). La media del seguimiento ha sido de 3,14 años (3 meses-8,3 años). Se ha considerado como éxito mantener, en las dos últimas revisiones, la PIO igual o por debajo de 21mmHg sin signos de progresión de glaucoma con o sin uso de fármacos hipotensores tópicos, sin necesidad de cirugías de glaucoma adicionales y sin la aparición de complicaciones devastadoras para la visión. La probabilidad acumulada de éxito según el análisis de Kaplan Meier ha sido de 76, 63 y 55% a los 6 meses, 1-3 años y 4-8 años respectivamente. El 41,17% de los DDG fracasaron (7/17).
Conclusiones: Los DDG son una buena opción quirúrgica para los glaucomas refractarios pediátricos cuando otros procedimientos quirúrgicos han fracasado o tienen un mal pronóstico.
Palabras clave: Glaucoma pediátrico. Válvula de Ahmed. Implante de Molteno.
ABSTRACT
Purpose: To evaluate the results and long-term complications of glaucoma drainage devices (GDD) in paediatric patients (0-15 years).
Methods: Retrospective cohort study was conducted on 17 implanted glaucoma drainage devices from July 1994 to April 2007 in 14 patients (17 eyes). In two patients (3 eyes) a Molteno GDD (MGDD) was implanted, and in 12 patients (14 eyes) an Ahmed GDD (AGDD) was used. We studied the demographic and glaucoma related patient data, as well as the probability of surgical success. The time which intraocular pressure (IOP) was controlled and the postoperative complications were also studied.
Results: Of the fourteen patients, 9 (64.28%) showed congenital glaucoma, and 5 (35.71%) aphakic glaucoma. The pre-aqueous drainage device median IOP was 29.82mmHg (SD: 6.98), and 14.05mmHg (SD: 7.57) postoperative. The median follow-up was 3.14 years (3 months-8.3 years). Success of aqueous drainage device was defined as an IOP less than 21mmHg with or without medication on the last two follow-up visits, and without severe complications or further glaucoma surgery. Using a Kaplan Meier analysis there was success in 76%, 63% and 55% at the six months, 1-3 years and 4-8 years respectively. The GDD was a failure in 41.17%.
Conclusions: GDDs are a good surgery option for refractory paediatric glaucoma when other surgery procedures have failed or have bad prognosti.
Key words: Paediatric glaucoma. Ahmed glaucoma valve. Molteno device.
Introducción
Además de la goniotomía y la trabeculotomía, de primera elección en el tratamiento del glaucoma congénito, las opciones quirúrgicas que existen para los glaucomas pediátricos son la trabeculectomía, con o sin terapia antifibrótica coadyuvante, los dispositivos de drenaje para glaucoma (DDG) o los procedimientos de cicloablación. La elección de cada técnica depende de las características individuales del paciente y de las preferencias del cirujano1.
En la población pediátrica, la trabeculectomía presenta un porcentaje de éxito menor que en los adultos si esta se realiza durante el primer año de vida. El uso adicional de agentes antifibróticos, como la mitomicina C o el 5-fluouracilo (5-FU), mejora la tasa de éxito, pero el desconocimiento que aún existe de las complicaciones derivadas de su uso en la población pediátrica, así como la tasa de blebitis y endoftalmitis descrita (7-17%) han suscitado un rechazo hacia esta técnica2-5. Los procedimientos de ciclodestrucción, como la ciclocrioterapia, se han asociado a una alta tasa de complicaciones. La ciclofotocoagulación con diodo, aunque presenta una tasa menor de efectos adversos severos que las modalidades quirúrgicas, se asocia a una disminución menor y temporal de la presión intraocular6. De ahí que siga siendo considerada como tratamiento coadyuvante a la cirugía, y quede relegada a pacientes donde esta no es recomendada, o como tratamiento paliativo en casos de glaucoma absoluto con dolor.
El uso de los DDG en población pediátrica ha ido incrementándose desde 1969, cuando fue descrito por primera vez por Molteno7, hasta la actualidad. La tasa de éxito descrita varía desde un 54 hasta un 95%, dependiendo del periodo de seguimiento, el tipo de glaucoma estudiado y los distintos criterios de éxito considerados8.
En ojos buftálmicos con adelgazamiento escleral los DDG son una buena opción, aunque en la mayoría de los casos su implante se decide tras el fracaso de otras opciones quirúrgicas.
El DDG de Ahmed (DDGA), que comenzó a utilizarse en 19929, presenta un mecanismo valvulado. Se trata de un sistema unidireccional restrictivo del flujo que, a diferencia del implante de Molteno (DDGM), permite prevenir la hipotonía postoperatoria, al mantener la PIO por encima de 8mmHg7.
En este estudio presentamos nuestra experiencia clínica con los DDG (DDGA y DDGM) a medio y largo plazo en pacientes pediátricos.
Sujetos, material y métodos
Se ha realizado un estudio retrospectivo de los DDG implantados en pacientes pediátricos en el Servicio de Oftalmología Infantil del Hospital 12 de Octubre de Madrid desde julio de 1994 hasta abril de 2007. Se incluyeron solo aquellos que tuvieran más de 1 año de seguimiento y en el único caso donde se implantó más de un DDG en un mismo ojo, solo se consideró el primero ya que el segundo no cumplía más de un año de seguimiento. Se seleccionaron, por tanto, un total de 17 dispositivos, implantados en 17 ojos de 14 pacientes. En tres pacientes con glaucoma bilateral se implantó un dispositivo en cada ojo, realizándose en el mismo acto quirúrgico en 2 de los casos.
Se han estudiado dos tipos de implante: el DDGA modelos S-2, S-3 y FP8 (New World Medical Inc., Rancho Cucamonga, California, EE.UU.) utilizado en 12 pacientes (10 implantes modelo S-2, 1 implante modelo S-3 y tres implantes FP8) y el DDGM (Ophthalmic Limited, Dunedin, Nueva Zelanda) utilizado en los dos primeros pacientes de la serie (tres dispositivos). La intervención ha sido realizada por los dos mismos cirujanos en todos los casos. La técnica quirúrgica empleada fue la misma en todos los casos, realizándose disección conjuntival con base fórnix y aislamiento de los músculos rectos del cuadrante correspondiente al lugar de implantación del reservorio, que se suturó a 8-10mm de limbo, anclándose a esclera con dos puntos de poliéster 5-0 y con nylon de 9-0 en los operados desde el año 2000. De los 17 DDG implantados el 88,23% se situaron en el cuadrante temporal superior, 11,76% en el nasal superior y 5,88% en el temporal inferior. La tunelización para el tubo se hizo con una aguja de 23 G, situándose la entrada aproximadamente a 2mm de limbo en los tubos situados en cámara anterior y a 5mm en los situados en cavidad vítrea. Para el recubrimiento del trayecto extraocular del tubo se utilizó un parche de fascia lata (Pacific Coast Tissue Bank, Los Ángeles, CA, EE.UU.) en la mayoría de los casos9, aunque en cinco casos se usaron otros materiales: colgajo escleral autólogo (2, 1994), y parches de duramadre (2, 1995-1996), o de esclera conservada (1, 2001). El cierre conjuntival se hizo mediante sutura continua con poliglicano 910 de 7-0. El tratamiento postoperatorio consistió en antibióticos y corticoides tópicos. En el caso del DDGA, previamente se irrigó el tubo con solución salina para abrir el mecanismo de la válvula. En los DDGM se colocó dentro del tubo un hilo de prolene 4-0 para bloquear parcialmente su luz y reducir la hipotonía postoperatoria.
Se han recogido datos demográficos y preoperatorios, incluyendo la edad en el momento de la cirugía, procedimientos quirúrgicos previos, número de fármacos hipotensores, PIO y agudeza visual (AV). La PIO fue medida con tonómetro de aplanación de Goldmann o con tonómetro de Perkins, en el momento previo a la cirugía y en las dos últimas revisiones. La AV fue medida con el optotipo de Pigassou o con el optotipo de Snellen siempre y cuando la edad y la colaboración del niño lo hicieron posible. En cada revisión se realizó examen en lámpara de hendidura y oftalmoscopia indirecta. Los datos posquirúrgicos recogidos han sido la PIO en las dos últimas revisiones, la AV y la aparición de complicaciones.
Se ha considerado como éxito completo una PIO igual o por debajo de 21mmHg sin signos de progresión de glaucoma en las dos últimas visitas (aumento del tamaño corneal, del diámetro antero-posterior del globo ocular o de la excavación papilar), con o sin uso de fármacos hipotensores y sin cirugía de glaucoma adicional (exceptuando recolocación o acortamiento del tubo o cirugías de revisión del DDG como la cistitomía o la capsulectomía) ni aparición de complicaciones devastadoras para la visión (endoftalmitis, desprendimiento de retina, hemorragia supracoroidea).
Todos loa análisis se llevaron a cabo con el paquete estadístico SPSS v.15.0 para Windows (SPSS Inc., Chicago, Illinois, EE.UU.).
Resultados
Desde julio de 1994 hasta abril de 2007 se han incluido 14 pacientes menores de 15 años. El estudio comprende un total de 17 dispositivos: 3 DDGM implantados entre 1994-1995 y 14 DDGA implantados entre 1997- 2007.
Datos demográficos
En la Tabla 1 se muestran los datos demográficos de los pacientes, recogidos antes de la cirugía. La mediana de la edad en el momento de la cirugía era de 3 años (15 días -15 años). El tipo de glaucoma era congénito en nueve pacientes (nueve ojos), y afáquico secundario a cirugía de catarata en cinco pacientes (ocho ojos).
En el 64,70% de los casos (11/17 ojos) se habían realizado previamente otros procedimientos de glaucoma, siendo la trabeculectomía la técnica más frecuente (Tabla 2). Dentro de este grupo, en el 90,9% (10/11 ojos) se había realizado también cirugía de catarata. En el 17,64% de los casos (3/17 ojos) solo se había realizado previamente cirugía de catarata. En el 23,52% restante (4/17 ojos/3 pacientes) el implante del DDG fue la primera cirugía efectuada; este grupo estaba compuesto por pacientes con edades entre 0,5 y 16 meses con ojos buftálmicos con edema corneal, PIO preoperatoria entre 34 y 41mmHg y síndromes malformativos asociados en dos de los casos (síndrome de Dandy-Walker y neurofibromatosis tipo 1).
Presión intraocular
La media de la PIO preoperatoria fue de 29,82mmHg (DS: 6,98) con una media de 1,94 fármacos hipotensores (0-3). La media de la PIO posquirúrgica (considerando la PIO de las dos últimas medidas en los DDG con progresión favorable y la PIO de la última medida en los que han fracasado) fue de 14,05mmHg (DS: 7,57) con una media de 1,05 fármacos hipotensores (0-3). La media de la PIO posquirúrgica considerando solo los DDG con evolución favorable fue de 11,90mmHg (9-20) con una media de 0,90 fármacos hipotensores (0-3).
Agudeza visual
Muchos de los niños eran demasiado pequeños o presentaban patología asociada que impedía una colaboración suficiente para poder objetivar su AV, por lo que solo se pudo explorar en seis pacientes preoperatoriamente (42,85%) (siete ojos) y en 7 pacientes postoperatoriamente (50%) (nueve ojos). La media de la AV preoperatorio fue de 0,75 logMar (logaritmo del mínimo ángulo de resolución) (1,30-0,30) y la media de AV postoperatoria fue de 0,71 logMar (0-1). En todos los casos se mantuvo estable excepto en un paciente afáquico con glaucoma bilateral que presentó un desprendimiento de retina bilateral a los 3 y 10 meses de la cirugía de glaucoma.
Complicaciones y probabilidad acumulada de éxito
El 50% de los casos (siete pacientes) requirieron intervenciones posteriores: en tres pacientes (21,42%) fue necesaria una sutura conjuntival por dehiscencia precoz en dos casos y sutura de membrana amniótica por extrusión del reservorio en el tercero, en dos pacientes (14,28%) capsulectomía asociada a inyecciones de 5-FU por encapsulación precoz, en un paciente (7,14%) recolocación del tubo por retracción del mismo, en un paciente vitrectomía y cerclaje por desprendimiento de retina y en el paciente restante fotocoagulación transescleral con láser diodo por mal control tensional.
Las complicaciones que han surgido a lo largo del seguimiento en relación con el tubo o con el reservorio, pero que no han supuesto el fracaso del DDG son: 1) un caso de encapsulación precoz (al mes de la cirugía) con buena respuesta tras cistitomía y administración de 5-FU, 2) un caso de exposición precoz del tubo, con buena evolución tras sutura de fascia lata, 3) dos casos de alteraciones de la motilidad por formación de ampolla gigante alrededor del reservorio a partir del primer año de la cirugía. En uno de los pacientes con neurofibromatosis tipo 1, esta restricción podía deberse también a la presencia de tejido neurofibromatoso a nivel orbitario.
Siete cirugías de cinco pacientes (41,17%) se han considerado fracaso por complicaciones o insuficiente control tensional. Las complicaciones que han surgido en relación con el tubo o con el reservorio y que han supuesto el fracaso del DDG han sido: 1) retracción del tubo de drenaje a los 4 años de su colocación en un paciente con microesferofaquia congénita, en el que se realizó un alargamiento y recolocación del tubo sin obtenerse control tensional. En este caso se implantó un segundo DDGA que ha evolucionado favorablemente tras 2,58 años de seguimiento; 2) extrusión del reservorio al mes de la cirugía con necrosis escleral posterior en un paciente con un síndrome malformativo (síndrome de Dandy-Walker), buftalmos y descematocele central, en el cual fue preciso eviscerar el globo ocular a los 4 meses del implante de la válvula; y 3) dehiscencia conjuntival recurrente con dos episodios de endoftalmitis secundarios a los 5 meses y al año de la cirugía. Otra complicación que ha supuesto el fracaso del DDG pero sin relación directa con la presencia del tubo o reservorio fue un desprendimiento de retina bilateral en un paciente a los 6 meses y al año de la cirugía. En uno de los ojos (OI) se había producido una encapsulación precoz de la ampolla que se había resuelto tras cistitomía y cinco inyecciones de 5- FU. Por último, otro caso se consideró fracaso por insuficiente control tensional, siendo necesaria la aplicación de ciclodiodo bilateral al año de la cirugía.
El análisis de Kaplan Meier mostró un probabilidad acumulada de éxito del 76% a los 6 meses, del 63% del primer año hasta el tercero y del 55% del cuarto año hasta el octavo Fig. 1).
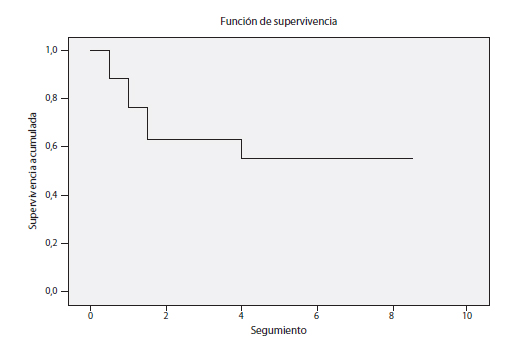
Fig. 1. Curva de Kaplan Meier de probabilidad acumulada de éxito.
Discusión
La tasa de éxito de los DDG descrita en población pediátrica es de un 54-95%, dependiendo de la edad del paciente, los criterios de éxito considerados, el tiempo de seguimiento, y otros factores8. El uso adicional de fármacos hipotensores u otras cirugías no filtrantes como la revisión de la ampolla, son necesarios en la mayoría de los pacientes para el control de la PIO después de la cirugía, por lo que generalmente suelen ser considerados como criterio de éxito relativo.
La mayoría de los estudios de revisiones de DDG en población pediátrica presentan un periodo de seguimiento a corto plazo. Se ha demostrado que la tasa de éxito disminuye a medida que este periodo aumenta8. El estudio de Cunliffe y Molteno es el que mayor periodo de seguimiento presenta solo con DDGM, con una media de 11,2 años y una tasa de éxito del 85%, a pesar de que el 71% requirió una cirugía posterior10. Chen et al. publican el mayor periodo de seguimiento solo con DDGA, con una media de 2,2± 1,8 años (3 meses-7,5 años), una tasa de éxito del 85,1% en el primer año y del 41,8% a los cuatro11. Prácticamente no hay estudios donde se incluyan varios tipos de implante. O'Malley et al. presentan el seguimiento de DDGA y DDGM, pero distinguiendo dos grupos según el tipo de glaucoma (afáquico o congénito), con una media de 3,5 y 5,5 años respectivamente y una tasa de éxito de 90-92% en el primer año y del 55-42% a los diez12. Autrata et al. presentan un estudio sobre DDGM y dispositivos de Baerveldt (DDGB) con una media de seguimiento de 7,1±6,5 años y una tasa de éxito del 91% en el primer año y del 65% a los seis13. En nuestro estudio también hemos considerado 2 tipos de implante (DDGA y DDGM) con un seguimiento medio de 3,14 años y una tasa de éxito del 63% en el primer año y del 55% a los 8 años.
Es difícil comparar las probabilidades de éxito de los diferentes DDG en la población pediátrica debido a la falta de uniformidad de criterio a la hora de elegir el implante. Beck et al.18 realizaron el único estudio comparando DDGA y DDGB en población pediátrica, no encontrando diferencias significativas entre ellos. Aun así, la elección del implante no fue aleatorizada.
Se ha considerado como factor de peor pronóstico la menor edad del paciente en el momento de la cirugía13. La mayoría de los estudios se refieren a niños menores de 18 años en el momento de la cirugía. O´Malley et al. y Coleman et al.9,12 recogen pacientes menores de 15 años (medias de 0,75, 4,3 y 2,4 años respectivamente). Nosotros también hemos incluido solo pacientes menores de 15 años, con una mediana de 3 años.
Algunos estudios han encontrado una tasa de éxito similar entre los dos tipos de glaucoma pediátrico más frecuente, afáquico y congénito12-14, y otros describen un peor pronóstico en el de tipo congénito11,15, aunque esta diferencia solo ha sido estadísticamente significativa en el estudio publicado por Djodeyre et al.16. En nuestro trabajo hemos encontrado un 50% de fracaso en el grupo del glaucoma afáquico y un 33% en el congénito, aunque dada la pequeña muestra de casos los valores no resultan significativos.
La realización de cirugías filtrantes de glaucoma previas (no así de cataratas) ha sido considerada por Souza et al.17 como factor de riesgo para el fracaso del DDG, aunque debemos tener en cuenta que el estudio de estos autores también recoge implantes en adultos. Sin embargo otros autores como Autrata et al. y Djodyre et al., no consideran que lo sea13,16. En nuestro estudio el 71,14% de los DDG que fracasaron se habían implantado en ojos con cirugía de glaucoma previa.
En nuestra serie el 52,94% de los casos necesitó fármacos hipotensores para el control tensional tras el implante del DDG. Este dato es similar al resto de las series publicadas donde la tasa oscila entre un 54-55,6%11,14.
Respecto a la visión, en otras series se describe entre un 60 y un 93,3% de mejora de la AV de al menos una línea en la escala de Snellen14. En nuestro estudio el 83,34% de los pacientes no presentaron alteraciones en su AV, aunque debemos considerar que la muestra de la que disponemos es pequeña, ya que solo en seis pacientes pudo ser valorada pre- y postoperatoriamete.
Entre las complicaciones, una de las más comunes después del implante de un DDG en población pediátrica es el mal control tensional por obstrucción del tubo o por encapsulación de la ampolla. La obstrucción puede producirse por sangre, fibrina, iris o vítreo. El aumento de la PIO por esta complicación presenta una tasa de incidencia en las distintas series de entre un 6 y un 20%8. La reparación quirúrgica de la obstrucción suele tener buenos resultados. En caso de encapsulación de la ampolla se emplea terapia antifibrótica coadyuvante (5- FU), asociada o no a técnicas de revisión de la ampolla o capsulotomías. Si estas no disminuyen la PIO se considerarían otros procedimientos como la ciclofotocoagulación o el implante de otro DDG en otro cuadrante. En nuestra serie hemos encontrado cuatro casos, el 23,52% (4/17 ojos), de encapsulación de la ampolla. Dos de ellos (2 pacientes) se resolvieron con cistitomías y terapia antifibrótica (5-FU). Los otros dos ojos (un paciente) necesitaron otro procedimiento adicional del glaucoma (ciclodiodo) por el mal control tensional.
Otra de la complicaciones postoperatorias más frecuente en población pediátrica es la migración del tubo de drenaje, que muchas veces puede ocasionar el contacto de este con el endotelio. Es más frecuente en ojos buftálmicos. En las series publicadas, y considerando distintos tipos de DDG, se describe una tasa entre el 5,7 y el 26,2%8. En nuestro estudio solo hemos encontrado un caso (5,8%) de retracción del tubo en un ojo con buftalmos, que no llegó a contactar con el endotelio.
La incidencia de erosión o extrusión del tubo o del reservorio se ha descrito entre un 0 y un 13%, asociándose a endoftalmitis secundaria en un 0-5% de los casos8. En nuestra serie hemos encontrado tres casos de extrusión (21,14%). En uno de ellos se produjo extrusión del reservorio al mes de la cirugía, con necrosis de la esclera subyacente. En los otros dos se produjo una exposición del tubo por dehiscencia conjuntival precoz, que asoció una endoftalmitis por Propionibacterim acnes en uno de ellos15.
En nuestra revisión no hemos registrado ningún episodio de hipotonía postoperatoria o hemorragia supracoroidea, sin embargo se ha descrito en las distintas series una incidencia de 0-25 y 0-22% de las mismas8.
Por último, también pueden producirse alteraciones persistentes de la motilidad extraocular, estando descrita en la literatura una tasa entre el 0 y el 11%8, aunque en el último articulo publicado por O´Malley et al. asciende a un 37%19. Estas alteraciones pueden deberse al efecto masa producido por la ampolla de filtración o por el plato del implante, por adhesión o cicatrización de los músculos extrínsecos (efecto Faden) o por un síndrome de adherencias. En nuestra serie encontramos dos casos (14,28%) con endotropia y restricción de la motilidad secundaria a la formación de una ampolla gigante en el cuadrante supero- temporal.
En nuestra serie, aunque la tasa de fracaso global es del 41,17%, similar o incluso superior a otras referidas en la literatura, la mayoría de los fracasos se produjo durante el primer año, y a partir de ese momento la evolución ha sido muy favorable, con muy baja tasa de fracaso a medio y largo plazo. Por otra parte, la mayoría se debieron a complicaciones, algunas de ellas no relacionadas con el DDG, como el desprendimiento de retina. Tan solo un caso ha fracasado por mal control tensional, precisando una nueva cirugía de glaucoma, por lo que en nuestra experiencia los DDG han resultado un procedimiento efectivo y duradero para el control de la PIO.
Los DDG se han convertido en una buena opción quirúrgica para los glaucomas refractarios pediátricos. Cuando otros procedimientos quirúrgicos han fracasado o tienen mal pronóstico, o cuando se trata de ojos buftálmicos o con conjuntivas cicatriciales por cirugías filtrantes previas, debemos considerarlos como una buena opción para el control de la PIO. Aunque las complicaciones derivadas de su uso son numerosas, la mayoría son reversibles y no son lo suficientemente graves como para provocar pérdida de visión. Sin embargo aún son necesarios estudios prospectivos aleatorizados que aporten más información acerca de sus resultados a largo plazo.
Conflicto de intereses
Los autores declaran que no tienen ningún conflicto de intereses.
Bibliografía
1. Tanimoto SA, Brandt JD. Options in pediatric glaucoma after angle surgery has failed. Curr Opin Ophthalmol. 2006; 17:132-7. [ Links ]
2. Mandal AK, Walton DS, John T, Jayaqandan A. Mitomycin C-augmented trabeculectomy in refractory congenital glaucoma. Ophthalmology. 1997; 104:996-1001. [ Links ]
3. Freedman SF, McCormick K, Cox TA. Mitomycin C-augmented trabeculectomy with postoperative wound modulation in pediatric glaucoma. J AAPOS. 1999; 3:117-24. [ Links ]
4. Beck AD, Wilson WR, Lynch MG, Lynn MJ, Noe R. Trabeculectomy with adjunctive mitomycin C in pediatric glaucoma. Am J Ophthalmol. 1998; 126:648-57. [ Links ]
5. Waheed S, Ritterband DC, Greenfield DS, Liebmann JM, Sidoti PA, Ritch R. Bleb related ocular infection in children after trabeculectomy with mitomycin C. Ophthalmolgy. 1997; 104:2117-20. [ Links ]
6. Kirwan JF, Shah P, Khaw PT. Diode Laser Cyclophotocoagulation. Ophthalmology. 2002; 109:316-23. [ Links ]
7. Molteno AC. New implant for drainage glaucoma. Clinical trial. Br J Ophthalmol. 1969; 53:606-15. [ Links ]
8. Ishida K, Mandal AK, Netland PA. Glaucoma drainage implants in pediatric patients. Ophthalmol Clin North Am. 2005; 18:431-42. vii. [ Links ]
9. Coleman AL, Smyth RJ, Wilson MR, Tam M. Initial clinical experience with the Ahmed Glaucoma Valve implant in pediatric patients. Arch Ophthalmol. 1997; 115:186-91. [ Links ]
10. Cunliffe IA, Molteno AC. Long- term follow- up of Molteno drains used in the treatment of glaucoma presenting in chidhood. Eye. 1998; 12(Pt 3a):379-85. [ Links ]
11. Chen TC, Bhatia LS, Walton DS. Ahmed valve surgery for refractory pediatric glaucoma: a report of 52 eyes. J Pediatr Ophthalmol Strabismus. 2005; 42:274-83. [ Links ]
12. O´Malley Schotthoefer E, Yanovitch TL, Freedman SF. Aqueous drainage device surgery in refractory pediatric glaucomas: I. Long term outcomes. J AAPOS. 2008; 12:33-9. [ Links ]
13. Autrata R, Helmanova I, Oslejkova H, Vondracek P, Rehurek J. Glaucoma drainage implants in the treatment of refractory glaucoma in pediatric patients. Eur J Ophthalmol. 2007; 17:928-37. [ Links ]
14. Englert JA, Freedman SF, Cox TA. The Ahmed Valve in refractory pediatric glaucoma. Am J Ophthalmol. 1999; 127:34-42. [ Links ]
15. Gutiérrez-Díaz E, Montero-Rodríguez M, Mencía-Gutiérrez E, Fernández-González MC, Pérez-Blázquez E. Propionibacterium acnes endophthalmitis in Ahmed glaucoma valve. Eur J Ophthalmol. 2001; 11:383-5. [ Links ]
16. Djodeyre MR, Peralta Calvo J, Abelairas Gómez J. Clinical evaluation and risk factors of time to failure of Ahmed Glaucoma Valve implant in pediatric patients. Ophthalmology. 2001; 108:614-20. [ Links ]
17. Souza C, Tran DH, Loman J, Law SK, Coleman AL, Caprioli J. Long- term outcomes of Ahmed glaucoma valve implantation in refractory glaucomas. Am J Ophthalmol. 2007; 144:893-900. [ Links ]
18. Beck AD, Freedman S, Kammer J, Jin J. Aqueous shunt devices compared with trabeculectomy with Mitomycin-C for children in the first two years of life. Am J Ophthalmol. 2003; 136:994-1000. [ Links ]
19. O´Malley Schotthoefer E, Yanovitch TL, Freedman SF. Aqueous drainage device surgery in refractory pediatric glaucomas: II. Ocular motility consequences. J AAPOS. 2008; 12:40-5. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico: teresacolas@hotmail.com
(T. Colás-Tomás)
Recibido el 3 de marzo de 2011
Aceptado el 19 de julio de 2011
















