Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Cirugía Plástica Ibero-Latinoamericana
versión On-line ISSN 1989-2055versión impresa ISSN 0376-7892
Cir. plást. iberolatinoam. vol.42 no.1 Madrid ene./mar. 2016
PEDIÁTRICA
ORIGINAL / Series Clínicas
Dermatofibrosarcoma protuberans en pacientes pediátricos
Dermatofribosarcoma protuberans in pediatric patients
Ana Domènech*; Trinidad Delgado-Ruíz**; Eva María López-Blanco***; Patricia Gutiérrez-Ontalvilla**** y Juan-José Vila-Carbó*****
* Médico Interno Residente del Servicio de Cirugía Pediátrica
** Médico Interno Residente del Servicio de Cirugía Plástica
*** Facultativo Adjunto y Coordinadora del Servicio de Cirugía Plástica Infantil
**** Facultativo Adjunto del Servicio de Cirugía Plástica Infantil
***** Jefe Clínico del Servicio de Cirugía Pediátrica
Hospital Universitari i Politècnic La Fe, Valencia, España.
Conflicto de intereses: los autores declaran no tener ningún interés financiero relacionado con el contenido de este artículo.
Dirección para correspondencia
RESUMEN
Antecedentes y Objetivos. Presentamos 3 casos de dermatofibrosarcomaprotuberans (DFSP) en pacientes pediátricos para documentar la presentación clínica poco frecuente de esta patología.
Pacientes y Método. Realizamos un análisis descriptivo retrospectivo de los 3 últimos casos de DFSP en nuestro centro durante los años 2010-2013.
Resultados. Una niña de 12 años remitida desde otra institución por DFSP en parte distal del muslo, en la que ampliamos bordes quirúrgicos de resección en 3 cm y practicamos cobertura con dermis artificial e injerto autólogo; tras 1 año de observación sin recidiva, realizamos reconstrucción del defecto mediante injertos autólogos de grasa.
Otra niña de 12 años diagnosticada de Síndrome de Hamartomatosis Múltiple asociado al gen PTEN, que presentó DFSP en labio mayor derecho y en mama derecha, recidivante en esta última localización.
Por último, un DFSP congénito en una paciente remitida a los 3 meses de vida con tumoración gigante de pared abdominal. El diagnóstico orientativo inicial con resonancia magnética con gadolino, solo se confirmó finalmente por los hallazgos histopatológicos de la pieza de resección; ni la punción aspiración ni la biopsia cutánea lograron confirmar el diagnóstico.
Conclusiones. El DFSP es un tipo de sarcoma raro de la piel del niño y del adulto, localmente agresivo y con una alta tasa de recidiva. La escisión local amplia puede provocar mutilaciones y desfigurar al paciente; por ello la cirugía micrográfica de Mohs permite reducir los márgenes quirúrgicos.
Palabras clave: Dermatofibrosarcoma, Dermatofibrosarcoma protuberans, Cirugía micrográfica de Mohs, Pacientes pediátricos.
Nivel de evidencia científica: 4 Diagnóstico.
ABSTRACT
Background and Objectives. We present 3 cases of dermato fibro sarcoma protuberans (DFSP) to document the unusual clinical presentation of this condition in pediatric patients.
Patients and Methods. We conduct a retrospective descriptive analysis of the last 3 cases of DFSP treated in our institution during years 2010-2013.
Results. A 12-year-old girl referred from another institution for DFSP in distal thigh; we practised surgical margins extended 3 cm resection and cover with artificial dermis and autologous graft; after 1 year follow up without recurrence, reconstruction of the defect was performed using autologous fat grafts.
Another 12-year-old girl diagnosed of Multiple Hamartoma Syndrome associated with PTEN gene, who presented DFSP at the right labia major and at the right breast, being recurrent in this last location.
Finally, a congenital DFSP in a patient referred at 3 months with giant tumour of abdominal wall. The initial diagnosis was made by MRI with gadolinium. The final diagnosis of DFSP was made based on histopathological findings of the piece following surgical resection, because percutaneous biopsy or skin biopsy couldn't confirm the diagnostic.
Conclusions. DFSP is a rare type of sarcoma of the skin in children and adults, locally aggressive, with a high rate of recurrence. Wide local excision may cause maiming and disfiguring to the patient, thereby Mohs micrographic surgery (CMM) enables to reduce surgical margins.
Key words: Dermatofibrosarcoma, Dermatofibrosarcoma protuberans, Mohs' micrographic surgery, Pediatric patients.
Level of evidence: 4 Diagnostic.
Introducción
El Dermatofibrosarcoma Protuberans (DFSP) es un sarcoma de bajo grado derivado de una célula de origen incierto en la dermis reticular (1). Se trata de una tumoración de bajo grado de malignad y baja tasa de metástasis, aunque localmente agresiva. En la literatura, existen pocos estudios sobre esta patología que hagan referencia a la población pediátrica, ya que sobre todo afecta a adultos jóvenes y de mediana edad. Excepcionalmente, también puede aparecer en la infancia y en la niñez, y tan solo un 6% de estos tumores se diagnostican en edad pediátrica (2). Sin embargo, una proporción importante de los DFSP diagnosticados en adultos comienzan en la infancia o incluso, están presentes en el nacimiento, y la falta de sospecha clínica de esta entidad conduce a importantes retrasos en su diagnóstico. Por este motivo, la prevalencia del DFSP infantil está probablemente infraestimada; Gooskens y col., en una revisión publicada en el año 2010, recogen 166 casos de DFSP de los que aproximadamente 38 eran formas congénitas (3). Hasta donde hemos podido conocer, están recogidos en la literatura de 38 a 61 casos de DFSP congénitos en niños, en diferentes series publicadas (3).
El DFSP en la edad pediátrica se describe sin predisposición alguna por sexo o con una incidencia levemente superior en niñas, siendo más frecuente en la raza negra. En series largas de pacientes se establece una incidencia de 0.8-5 casos anuales por millón de habitantes. Con mayor frecuencia se localiza en el tronco y en las extremidades proximales, y es raro encontrarlo en la cabeza y en el cuello (4).
Debido a la rareza del tumor y a su aspecto abigarrado, el diagnóstico de DFSP en los niños es muy difícil. Además presenta una alta tasa de recidiva. El diagnóstico clínico en los estadios iniciales es muy complejo. Tanto la presentación clínica como la histopatología y las anomalías moleculares en los niños son similares a las de los adultos. En los niños, el aspecto clínico puede ser heterogéneo y se necesita un alto índice de sospecha para evitar demoras en el diagnóstico final, lo que puede conducir a una mayor morbilidad. Se necesita examen histológico junto con el uso de técnicas inmunohistoquímicas para lograr su diagnóstico.
Los avances en la compresion de la genetica molecular de DFSP han dado lugar a nuevas modalidades diagnosticas y terapeuticas. Se cree que el DFSP es el resultado de una translocacion entre el factor de crecimiento beta derivado de las plaquetas (PDGFB, 22q13.1) y el colageno tipo 1 (COL1A1, 17q21≈22) que conduce a una proteina de fusion (PDGFB) que estimula el receptor de PDGF. La deteccion de este desplazamiento en el tejido a traves de la reaccion en cadena de la polimerasa (PCR) o hibridacion in situ fluorescente (FISH), puede ser util en casos dificiles.
El tratamiento principal de esta entidad consiste en la escisión de la tumoración con amplios márgenes quirúrgicos (5). Es muy importante realizar una extirpación quirúrgica completa del tumor para reducir el riesgo de recidiva (3). La resección local amplia puede provocar mutilaciones y desfigurar al paciente, por ello la cirugía micrográfica de Mohs (CMM) ayuda a reducir los márgenes quirúrgicos (6). Mientras que la cirugía con resección local amplia o CMM es la base del tratamiento, el uso de la terapia dirigida con mesilatoe imatanib resulta prometedora en tumores grandes o irresecables. El conocimiento de las características clínicas, la histología, la genética y las opciones de tratamiento son importantes para la gestión exitosa de estas tumores (7).
Para ilustrar el conocimiento sobre el tema, presentamos 3 casos de DFSP tratados en nuestro centro hospitalario durante el periodo 2010-2013; todo ello con el objetivo de documentar la presentación clínica poco frecuente de esta tumoración en pacientes en edad pediátrica.
Material y método
Realizamos una revisión retrospectiva de 3 casos diagnosticados de DFSP y tratados en nuestro centro, un hospital de nivel superior de referencia regional y nacional de Cirugía Plástica Infantil, durante los años 2010-2013. Registramos los detalles del tratamiento quirúrgico, incluidos los márgenes de resección de las tumoraciones, la duración de la estancia hospitalaria, los resultados, el seguimiento postoperatorio de los pacientes y el análisis de tejido tumoral genética molecular.
RESULTADOS
Recogimos en el periodo analizado 3 casos en niñas, con una edad media de 6.75 años (SD 5.97, rango: 3 meses - 12 años), diagnosticadas de DFSP en otras instituciones y remitidas a nuestro centro más tarde. Dos de las pacientes habían sido sometidas a cirugía para resección del DFSP en dichos hospitales y remitidas posteriormente a nuestro centro tras confirmarse el resultado anatomopatológico en el primer caso, y tras recidiva en el segundo. El tercer caso, con DFSP congénito, nos fue remitido tras biopsia y sin diagnóstico claro. Detallamos a continuación los 3 casos.
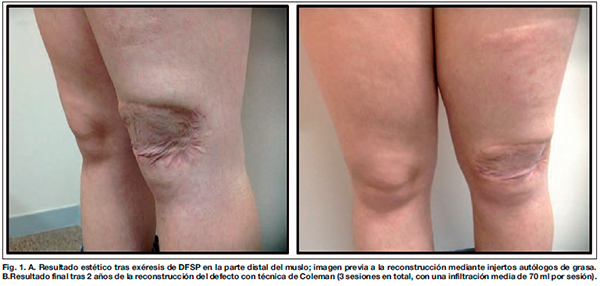
Caso 1. Niña diagnosticada de DFSP en la parte distal del muslo a la edad de 8 años, remitida desde otra institución tras comprobación del resultado histopatológico de la lesión para ampliación de bordes quirúrgicos y seguimiento. Una vez en nuestro centro se realizó biopsia de 7.5x5x1.3 cm que confirmó mediante técnica de inmuno peroxidasa y expresión de CD34+ y factor XIIIa, una neoformación tumoral en la zona cicatricial. Seguidamente se practicó ampliación de los bordes quirúrgicos de resección mediante CMM, con una extensión de 3 cm aproximadamente y en profundidad hasta fascia y músculo, y cobertura del defecto creado con dermis artificial (Integra®) e injerto autólogo. El seguimiento postoperatorio se llevó a cabo mediante controles ecográficos periódicos (Fig. 1-A); tras 1 año de vigilanciay sin signos de recurrencia tumoral, se procedió a la reconstrucción del defecto mediante injertos autólogos de grasa con técnica de Coleman: 3 sesiones en total, con una infiltración media de 70 ml. por sesión) (Fig. 1-B). Después de 2 años de seguimiento, la paciente se encuentra libre de enfermedad y sigue un régimen de vida normal acorde a su edad.
Caso 2. Niña de 10 años de edad, diagnosticada y tratada en otro centro de una tumoración congénita pediculada en línea mamaria derecha, de 2x2x1.5 cm de diámetro, con consistencia dura y compatible con DFSP, la cual fue resecada quirúrgicamente y remitida a Anatomía Patológica para confirmación de diagnóstico.
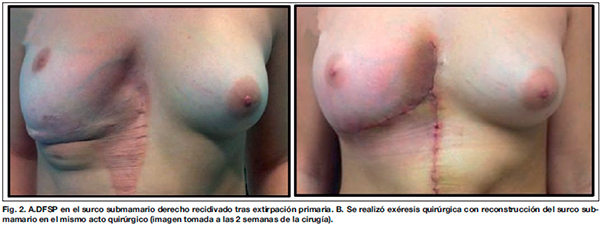
Dos años más tarde, la paciente es remitida a nuestra institución por alteración estética del surco submamario y sospecha de recidiva tumoral (Fig. 2-A). Como antecedentes personales destacan un Síndrome de Hamartomatosis Múltiple asociado al gen PTEN, aplasia aplasia de piel y tejido subcutáneo en labio vulvar mayor derecho, con ocupación de la zona por una tumoración de consistencia firme. Mediante ecografía mamaria y resonancia magnética (RM) del tronco se identificó una lesión ovoidea localizada en tejido celular subcutáneo, de características quísticas, con captación en anillo, compatible con hamartoma, y posible recidiva del tumor extirpado en el surco submamario derecho.
Se realizó exéresis quirúrgica de forma inmediata, con reconstrucción del surco submamario en el mismo tiempo quirúrgico (Fig. 2-B). Los resultados histopatológicos confirmaron la sospecha diagnóstica. Más tarde se resecó la tumoración sospechosa de hamartoma en el labio vulvar mayor derecho (Fig. 3), aunque no mostró alteraciones histológicas significativas.
Tras 2 años de seguimiento postoperatorio, la paciente está asintomática y sigue controles semestrales clínicos en Oncología y por técnica de imagen con RM.
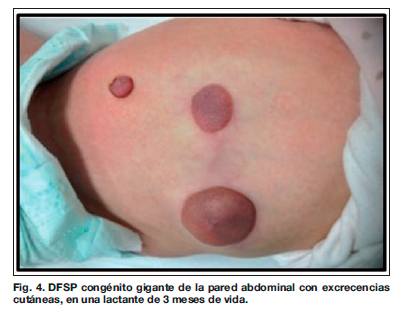
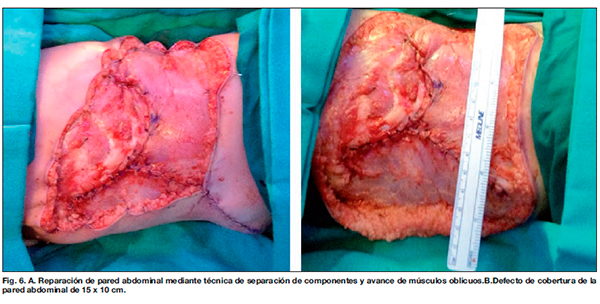
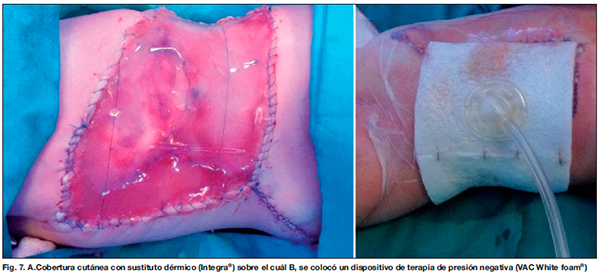
Caso 3. DFSP congénito en paciente remitida a nuestro centro a los 3 meses de vida con una tumoración abdominal gigante con excrecencias cutáneas (Fig. 4). La tumoración ya había sido biopsiada sin que se pudiera confirmar su estirpe tumoral. En nuestro centro se le realizó RM que mostró una extensa lesión focal en pared abdominal de 5.8x2x2 cm, de aspecto heterogéneo, que infiltraba recto anterior y músculos oblícuos, sugerente de lesión neoformativa. La biopsia simple confirmó el diagnóstico de DFSP congénito en base a las características clínicas e inmunohistoquímicas con positividad para CD34, expresión de vimentina, proliferación de células fusiformes y estudio citogenético, por lo que se decidió llevar a cabo intervención quirúrgica para exéresis completa del tumor. Se extirpó la tumoración, con una extensión total de resección de 12x8 cm, resecando los tejidos hasta la fascia preperitoneal (Fig. 5-7). Se realizaron muestras extemporáneas mediante CMM hasta lograr 3 cm de margen quirúrgico libre de enfermedad, quedando un defecto final de cobertura de la pared abdominal de 15x10 cm (Fig.6-B). La reparación de la pared abdominal se hizo mediante técnica de separación de componentes y avance de músculos oblicuos. La cobertura cutánea se realizó con un sustituto dérmico (Integra®), sobre el que se colocó un dispositivo de terapia de presión negativa (VAC White foam®) (Fig.7-B) a presión continua de 90 mmHg durante 1 mes, con recambios cada 4 días. El postoperatorio inmediato, durante 4 días, transcurrió en la Unidad de Cuidados Intensivos Pediátricos con evolución satisfactoria. Un mes más tarde se realizó el segundo tiempo de cobertura del sustituto dérmico con injertos de piel parcial laminares obtenidos del cuero cabelludo mediante dermatomo eléctrico. La paciente permaneció ingresada durante una semana para realizar curas diarias de la zona donante, y posteriormente fue dada de alta con controles ambulatorios y curas cada 3-4 días, durante 6 meses aproximadamente, hasta la completa resolución de las lesiones.
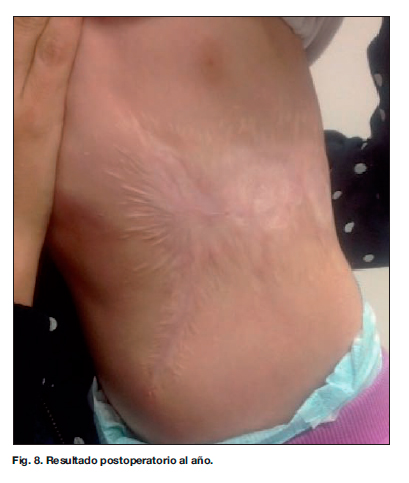
Tras 1 año de seguimiento postoperatorio (Fig. 8), la paciente sigue controles trimestrales en Oncología Pediátrica y semestrales en Cirugía Plástica Infantil, con controles ecográficos y RM periódicos, sin presentar signos de recidiva ni restos tumorales. Como complicación presenta alopecia cicatricial en la zona donante del cuero cabelludo.
Discusión
El diagnóstico final de DFSP se hizo, en todos los casos que presentamos, en base a los hallazgos histopatológicos de la pieza tras su exéresis quirúrgica completa. Ni la punción aspiración, ni la biopsia cutánea, lograron confirmar el diagnóstico. El diagnóstico fue orientativo con la RM con gadolino y finalmente se confirmó con la escisión quirúrgica de la tumoración.
Ninguna de las lesiones asoció invasión ósea, ni infiltración perineural o metástasis ganglionar o a distancia.
El tratamiento quirúrgico consistió en la extirpación completa del tumor mediante CMM, logrando márgenes de 3 cm y asociando eliminación de la primera capa anatómica no afectada en profundidad. La reconstrucción fue en cada caso adaptada para el defecto en anchura, profundidad y topografía. En la paciente con DFSP congénito, se complementó con el uso de los sistemas de cierre asistido por vacío (8,9). El dolor fue limitado y la movilidad total se mantuvo en todas las pacientes.
Las complicaciones postquirúrgicas, que se produjeron en la tercera paciente, fueron: pérdida parcial de los injertos secundaria a una infección nosocomial por Pseudomonas Aeruginosa que precisó antibioticoterapia y nuevos injertos; y una alopecia cicatricial en la zona donante pendiente de exéresis quirúrgica previa expansión cutánea a mayor edad. No hubo ninguna secuela funcional residual en los casos de nuestra serie.
En la tercera paciente se optó por tomar los injertos autólogos del cuero cabelludo a pesar de que la zona donante para los injertos de piel parcial por excelencia es la cara interna del muslo; en algunos casos en los que la necesidad de piel donante es mayor, se pueden usar la espalda y los glúteos. En el caso de niños menores de 5 años se puede optar por el cuero cabelludo ya que se trata del área de mayor tamaño relativo de su cuerpo (hasta un 10% de la superficie cutánea total) junto con el abdomen y la espalda, y presenta una baja tasa de complicaciones. Además, dada la abundancia de apéndices dérmicos y su rica vascularización, es posible reutilizar la zona donante en poco tiempo (10,11). Este tipo de injerto ofrece ventajas tales como evitar lesiones cicatriciales en la zona donante, pues al tratarse de un injerto parcial, los folículos pilosos permanecen en el cuero cabelludo y el paciente no debería sufrir alopecia cicatricial ni aparición de pelo en la zona implantada. Desgraciadamente, en nuestra paciente, la alopecia se presentó debida a infección por Pseudomonas que profundizó la zona donante.
Por último, queremos señalar también que es fundamental en estos casos la participación multidisciplinaria. La primera sospecha la tendrá el pediatra en una revisión rutinaria, y ante la aparición de una tumoración sospechosa, el paciente debe ser remitido a un centro con mejor dotación asistencial para una evaluación más profunda. Es imprescindible en estos pacientes la coordinación entre pediatras oncológicos, anatomopatólogos y cirujanos plásticos infantiles para poder llevar a cabo una exéresis óptima de la lesión y un tratamiento médico oportuno (12).
Conclusiones
El DFSP es un tipo de sarcoma raro de la piel del niño y del adulto, localmente agresivo, con una alta tasa de recidiva. El tratamiento, en la infancia, se retrasa a menudo debido a un mal diagnóstico que conduce al crecimiento localmente agresivo de la tumoración y a la escisión incompleta. Por lo tanto, los pediatras deben ser conscientes de esta entidad poco común y garantizar la escisión amplia de la lesión para reducir el riesgo de recurrencia.
Las lesiones sospechosas de DFSP justifican una evaluación histológica temprana con abordaje multidisciplinario.
La exéresis local amplia puede provocar mutilaciones y desfigurar al paciente, por ello la cirugía micrográfica de Mohs permite obtener márgenes quirúrgicos menores que la escisión amplia y debe ser considerada como tratamiento de elección en los niños con DFSP. El uso provisional de los sistemas de cierre asistido por vacío aumenta la comodidad del paciente y su rápida evolución.
Bibliografía
1. King L, López-Terrada D, Jakacky J, et al. Primary intrathoracic dermatofibrosarcoma protuberans. Am J Surg Pathol. 2012; 36(12): 1897-1902. [ Links ]
2. De Morais OO, De Araújo LC, Gomes CM, et al. Congenital dermatofibrosarcoma protuberans. Cutis. 2012; 90(6): 285-288. [ Links ]
3. Valdivielso-Ramos M, Hernanz JM. Dermatofibrosarcoma protuberans in childhood. Actas Dermosifiliogr. 2012; 103(10): 863-873. [ Links ]
4. Millare GG, Guha-Thakurta N, Sturgis EM, El-Naggar, Debnam JM. Imaging Findings of Head and Neck Dermatofibrosarcoma Protuberans. Am J Neuroradiol. 2014; 35(2): 373-378. [ Links ]
5. Abdel Wahab O, Qassemyar A, Maillet M, et al. Dermatofibrosarcoma protuberans in children. Ann Chir Plast Esthet. 2012; 57(2):140-146. [ Links ]
6. Barysch MJ, Weibel L, Neuhaus K, et al. Dermatofibrosarcoma protuberans in childhood treated with slow Mohs micrographic surgery. Pediatr Dermatol. 2013; 30(4): 462-468. [ Links ]
7. Kornik RI, Muchard LK, Teng JM. Dermatofibrosarcoma protuberans in children: an update on the diagnosis and treatment. Pediatr Dermatol. 2012; 29(6):707-713. [ Links ]
8. Garrigós X, Guisantes E, Oms L, Mato R, Ruíz D, Prat J. Combinación de distintos dispositivos de terapia V.A.C.® para el cierre de defectos abdominales complejos. Cir plást iberolatinoam. 2014; 40(3): 243-251. [ Links ]
9. Martínez-Méndez JR, Ramón Bitrián S, Leyva Rodríguez F, Casado Pérez C. Terapia de vacío como adyuvante para el uso de sustitutos dérmicos monocapa. Cir plást iberolatinoam. 2011; 37(S1): S53-S58. [ Links ]
10. Weyandt GH, Bauer B, Berens N, Hamm H, Broecker EB. Split-skin grafting from the scalp: the hidden advantage. Dermatol Surg. 2009; 35(12):1873-1879. [ Links ]
11. Wyrzykowski D, Chrzanowska B, Czauderna P. Ten years later-scalp still a primary donor site in children. Burns. 2015; 41(2): 359-363. [ Links ]
12. Goyal P, Sehgal S, Sinagh S, et al. Dermatofibrosarcoma protuberans in a child: a case report. Case Rep Dermtol Med. 2012; 2012: 796-818. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Dra. Anna Domènech Tàrrega
Servicio de Cirugía Plástica Infantil y Cirugía Pediátrica
Hospital Universitari i Politècnic La Fe
Avda. Fernando Abril Martorell Sur no 106
CP 46026, Valencia, España
annadomenechtarrega@gmail.com
Recibido (esta versión): 15 noviembre/2015
Aceptado: 20 noviembre/2015