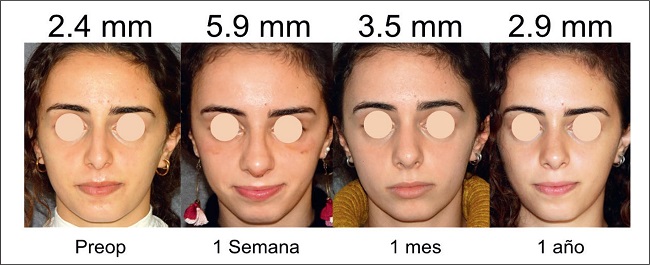
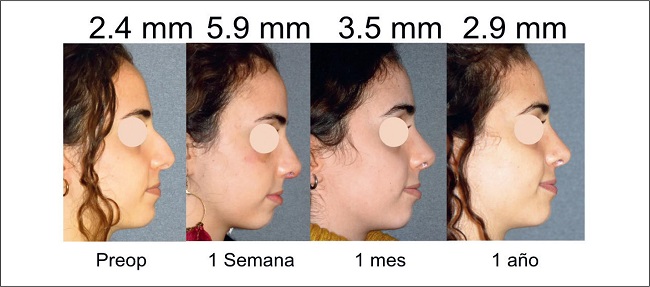
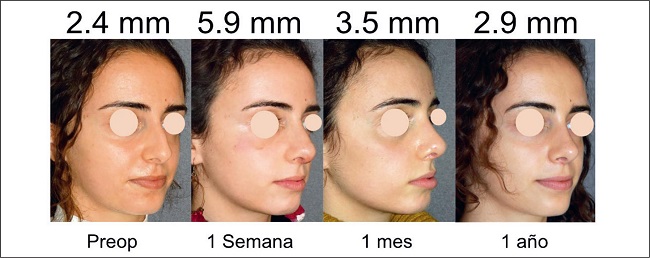
Introducción
Los defectos estéticos más comunes después de la rinoplastia estética son pequeñas irregularidades en el dorso nasal que se observan principalmente en pacientes con piel delgada. Se han utilizado diversas técnicas para intentar tratar las irregularidades perceptibles así como los bordes afilados de huesos y cartílagos nasales en estos pacientes, como por ejemplo: cartílago cortado en cubitos solo o en bloque o combinado con hidroxiapatita de calcio,(1) esponja de fibrinógeno-trombina,(2) membrana de colágeno de doble capa,(3) lipoinfiltrado,(4) cartílago inyectable, ácido hialurónico, fascia temporal, etc.
La piel dorsal delgada se ha descrito constantemente como un factor de riesgo para desarrollar irregularidades del dorso nasal después de la rinoplastia. Estas irregularidades suponen un inconveniente para el paciente y una sobrecarga y reto para el cirujano ya que conllevan reintervenciones que suponen entre un 5-15%(5) de las rinoplastias. Se ha recomendado la rinoplastia de preservación como un método para prevenir las irregularidades del dorso nasal, sin embargo, esta técnica tiene limitaciones de indicación y es posible que algunos cirujanos no estén familiarizados con ella. En algunos casos, también se han utilizado otras técnicas de preservación del dorso tal y como plantean Skoog,(6) o Cottle(7) con su método de autoinjerto del dorso nasal descrito en 1954.
Identificar aquellos pacientes con un riesgo más elevado de desarrollar irregularidades postoperatorias en el dorso nasal tras rinoplastia supone una oportunidad para prevenir su aparición mediante un tratamiento intraoperatorio accesible, que no suponga un incremento inaceptable de la morbilidad del paciente ni una prolongación del tiempo quirúrgico. En este trabajo, presentamos un enfoque metodológico de rinoplastia que incluye la evaluación preoperatoria del grosor de la piel del dorso nasal y la clasificación de los pacientes en función de dicho grosor. Buscamos de esta forma identificar aquellos pacientes con mayor riesgo de desarrollar irregularidades estéticas en el dorso nasal después de la cirugía con la finalidad de aplicar tratamientos preventivos personalizados en el intraoperatorio utilizando injertos de nanograsa enriquecidos con fibrina rica en leucocitos y plaquetas (L-PRF, Leucocyte and Platelet Rich Fibrin) en aquellos con alto riesgo, a fin de mejorar el grosor del tejido blando y prevenir irregularidades postoperatorias, optimizando así los resultados estéticos de la rinoplastia.
Material y método
Llevamos a cabo nuestro estudio sobre pacientes sometidos a rinoplastia estética que implicó la eliminación de giba dorsal mediante abordaje abierto de tipo estructural. La disección fue subperióstica. La resección mayor del dorso se realizó mediante cincel protegido clásico. Las osteotomías mediales y laterales y el limado final del dorso y de los sitios fracturarios de las osteotomías se hizo mediante el dispositivo de ultrasonidos Piezotome® Solo M+ (Salteltec, Mérignac, Francia). Los pacientes fueron operados entre enero de 2022 y enero de 2023. Todos dieron su consentimiento informado por escrito para someterse a la operación y para la publicación de sus fotografías con fines educativos.
Tomamos fotografías preoperatorias y postoperatorias en la semana 1 y a los 6 y 12 meses de la intervención.
Medimos el espesor de la envoltura de tejido blando (STE) pre y postoperatoriamente pellizcando la piel con un adipómetro digital a nivel del rinion.(8) Consideramos válida la medición al observar la palidez de la piel durante la prueba de pellizco.
Estamos de acuerdo con otros autores(8) en que el grosor ideal del tejido blando del dorso nasal se sitúa en algún punto en el rango medio donde es lo suficientemente grueso como para ocultar pequeñas irregularidades, pero lo suficientemente delgado como para transmitir los contornos esculpidos de la estructura del esqueleto nasal. Esto nos lleva a considerar que un espesor de la envoltura de tejido blando del rinion de 3 mm (R-STET: Rhinion Soft Tissue Envelope Thickness) es suficiente para ocultar las irregularidades subyacentes. Clasificamos todos los pacientes siguiendo esta valoración clínica del R-STET (Tabla I) antes de la cirugía y seguimos el siguiente protocolo:
Tabla I. Clasificación del tipo de espesor del envoltorio de tejido blando nasal medido en el rinion (R-STET: Rhinion Soft Tissue Envelope Thickness).
| Tipo de R-STET | Espesor de la piel | Tratamiento |
|---|---|---|
| Tipo I | < 3mm |
Coágulo subcutáneo de L-PRF (Leucocyte Plasma Rich Fibrine) Injerto intradérmico de nanograsa enriquecido con L-PRF |
| Tipo II | ≥ 3mm |
Esteroides intradérmicos intraoperatorios en punta nasal |
- Tipo I. Pacientes con un grosor de tejidos blandos del dorso nasal menor de 3 mm en los que se supone que R-STET es insuficiente para ocultar irregularidades, y por tanto, trataremos intraoperatoriamente con una combinación de coágulo de L-PRF subcutáneo (fibrina rica en plaquetas y leucocitos) e injerto intradérmico de nanograsa enriquecido con L-PRF.
- Tipo II. Pacientes con un grosor de tejidos blandos del dorso nasal igual o superior a 3 mm en los que consideramos que el R-STET tiene espesor suficiente. En estos, administramos coágulo de L-PRF subcutáneo en el intraoperatorio con el fin de prevenir el exceso de edema postoperatorio en la región de la punta y tratar el espesor de las pieles más gruesas para obtener mayor definición.
Técnica quirúrgica
El cirujano o un asistente capacitado toma 2 tubos IntraSpin de tapa roja sin anticoagulante de 10 cc (IntraLock®, Boca Raton, FL, EE.UU.) de sangre venosa de la extremidad superior no perfundida del paciente inmediatamente después de la fase de inducción anestésica con un sistema de venopunción Vacuette® y "holder set" (Greiner bio-one®, 4550 Kremsmünster, Austria)(3) (Fig. 1). A continuación se centrifuga la sangre con una centrífuga Hettich® EBA 200/CE a 2700 RPM / 408 RCF durante 12 minutos.(4) La rinoplastia comienza mientras se realiza la centrifugación. El asistente quirúrgico se encarga del procesamiento del L-PRF (Fig. 2).
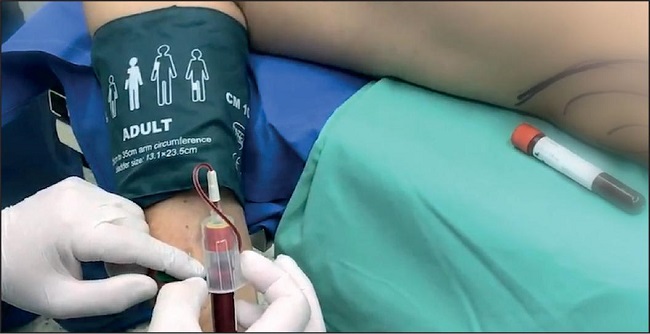
Figura 1. Extracción de las muestras de sangre del paciente para la obtención del coágulo de L-PRF (fibrina rica en plaquetas y leucocitos).
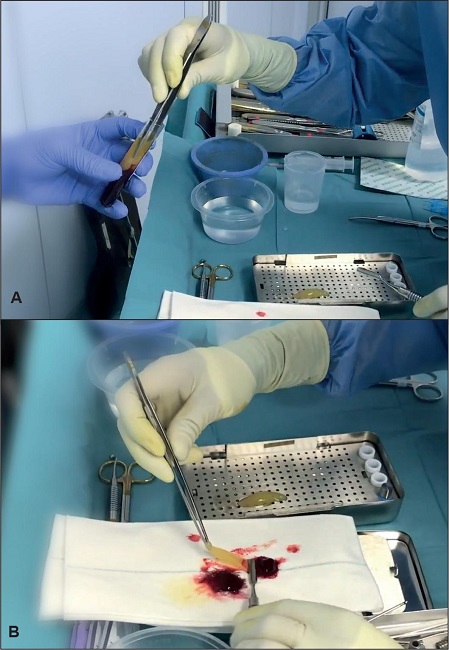
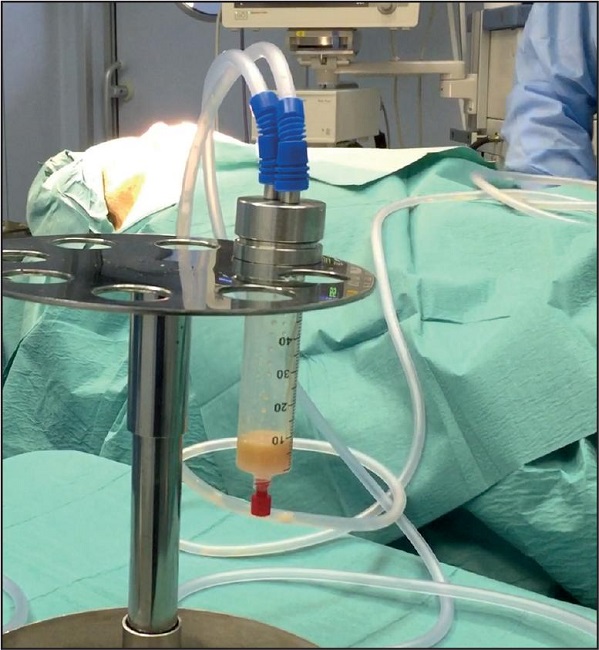
Una vez terminada la centrifugación, el auxiliar de quirófano se encarga de extraer los tubos de la centrífuga, de abrirlos y ofrecerlos al asistente quirúrgico. Este extrae de manera estéril el coágulo de fibrina sobrenadante con una pinza con dientes (Fig. 3A) y lo deposita en la parrilla de drenaje dentro la caja Xpression® (IntraLock®, Boca Raton, FL, EE.UU.) (Fig. 3A y B). La caja Xpression® es un recipiente rectangular de acero quirúrgico compuesto por una cubeta, una parrilla, una plancha de un peso determinado que se apoya sobre esta parrilla y una tapa. Es en esta parrilla donde se depositan los coágulos de L-PRF y en la cubeta donde se recoge el exudado de suero procedente de la compresión de los coágulos. La compresión del coágulo produce una membrana L-PRF(5) de 1 mm de espesor que contiene fibrina, leucocitos y plaquetas. En el fondo de la caja se obtiene un suero de plaquetas altamente concentrado. Los dos coágulos de L-PRF (uno de cada tubo) obtenidos se dejan bajo una suave presión por gravedad proporcionada por la plancha de presión del sistema Xpression® durante el tiempo que dura la rinoplastia, sobre una mesa esterilizada independiente de la mesa de instrumental quirúrgico (Fig. 4A-C).
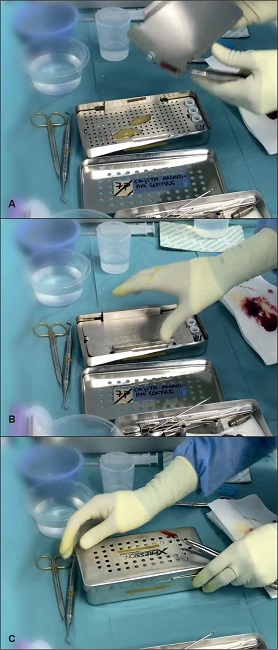
Figura 4. A-C. El coágulo se deposita en la parrilla de drenaje de la caja Xpression®. En el fondo de la caja se obtiene un suero de plaquetas altamente concentrado.
El tiempo quirúrgico promedio en nuestras manos para una rinoplastia abierta estructural estándar es de 3 horas; esto es relevante ya que se ha reportado que los coágulos de L-PRF tienen un tiempo de viabilidad de 4 horas. Si la rinoplastia se prolonga más de 4 horas, se debe tomar una nueva muestra de sangre del paciente para producir coágulos de fibrina L-PRF más frescos.
La técnica de rinoplastia abierta empleada implica disección subpericóndrica. Realizamos la resección dorsal con osteotomo clásico cuando se necesita una reducción dorsal nasal significativa, o con un Piezotome® (Sateltec®, Merignac, Francia) cuando la deformidad dorsal era moderada, seguida de un afinamiento del dorso con el mismo dispositivo ultrasónico. También empleamos el Piezotome® para realizar las osteotomías laterales y el refinamiento de las líneas de fractura. Llevamos a cabo fijación consistente de los cartílagos triangulares al tabique con o sin injerto espaciador.
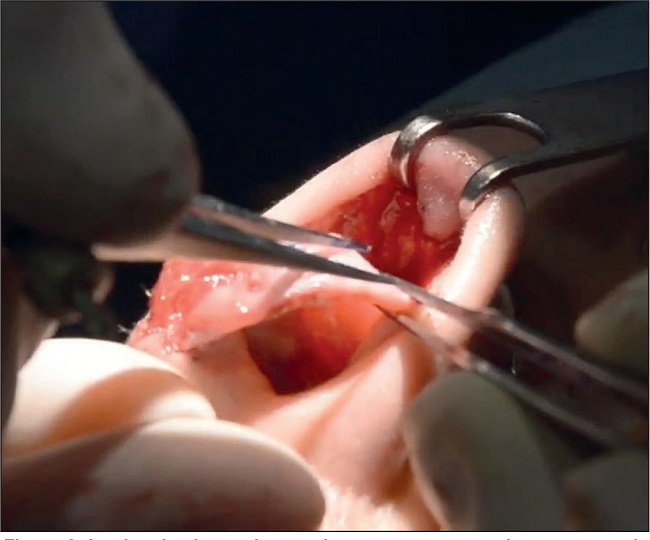
Al finalizar la rinoplastia, justo antes de cerrar la piel, colocamos las 2 membranas de L-PRF en el dorso nasal (Fig. 5 y 6) (Video 1 disponible en material suplementario solo como link material suplementario).
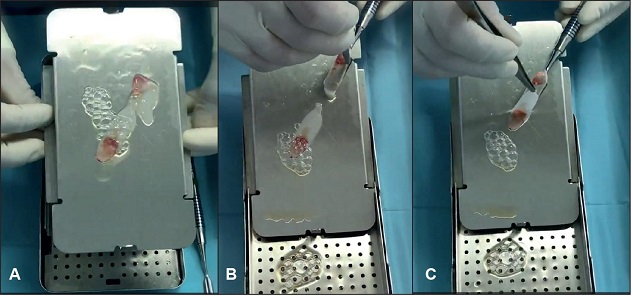
Figura 5. A y B. Apertura de la caja, extracción y preparación de los dos coágulos de L-PRF (uno de cada tubo).
En este momento preparamos el campo para la obtención del lipoaspirado, para lo cual infiltramos la región lumbar derecha (por comodidad del autor) con 50 cc de una solución compuesta por 1 L de NaCl al 0.9% con 1 mg de adrenalina y 10 ml de lidocaína al 2%. Comenzamos la sutura de las incisiones de la rinoplastia esperando 10 minutos para iniciar con la liposucción. Realizamos lipoaspiración de 10 ml con una cánula de liposucción de 2 mm utilizando un dispositivo de recolección de grasa del autor por debajo de 700 mmHg de fuerza de vacío (Fig. 7).
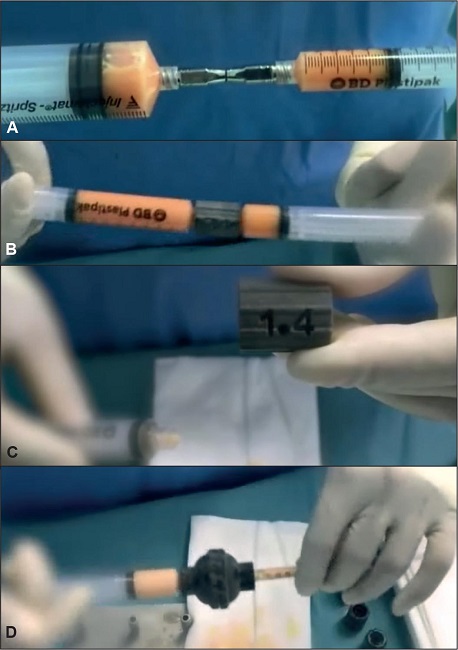
Seguidamente, un asistente capacitado procesa el lipoaspirado siguiendo 3 pasos y utilizando una serie de piezas de transducción (Fig. 8):

Figura 8. Diferentes jeringas y dispositivos de impresión 3D empleados durante la técnica para el procesado de la grasa y obtención del nanofat.
-
- Paso 1. Lavado del lipoaspirado transfiriendo desde la jeringa de recolección a otra jeringa llena de solución de 50 cc de NaCl al 0.9% tibia a través de una transferencia de 4 mm de diámetro. Después de la decantación, transferimos el lipoaspirado, directamente, a una jeringa de 10 cc (Fig. 9A).
- Paso 2. Cambio vigoroso entre 2 jeringas de 10 ml a través de un conector luer-lock hembra a hembra de 2.4 mm (Fig. 9B). Después de 30 pasadas, repetimos el mismo proceso con un conector luer-lock hembra a hembra de 1.4 mm durante otras 30 pasadas vigorosas hasta observar una decoloración blanquecina de la grasa(9) (Fig. 9C).
- Paso 3. Para la recolección de la grasa empleamos un dispositivo de diseño propio realizado en PA12 (poliamida o nylon) impreso por sinterización selectiva por láser (SLS), biocompatible y termorresistente. Se trata de un adaptador con un orificio de entrada y otro de salida de aire, que aplicado a las jeringas de 50 cc sin émbolo, las transforma en un colector de grasa que permite utilizar las jeringas como depósito de recolección, decantador y al mismo tiempo la transferencia de grasa a otras jeringas en un sistema cerrado. Realizamos filtración única final de 600 micras (Fig. 9D) Este último filtrado de grasa ha sido diseñado para minimizar el espacio muerto, de modo que la cantidad de grasa desperdiciada sea mínima y los daños por recolección de grasa se reduzcan también al mínimo. A continuación, transferimos la grasa emulsionada a 2 jeringas de 1 ml y está lista para el injerto.
Injerto de nanograsa
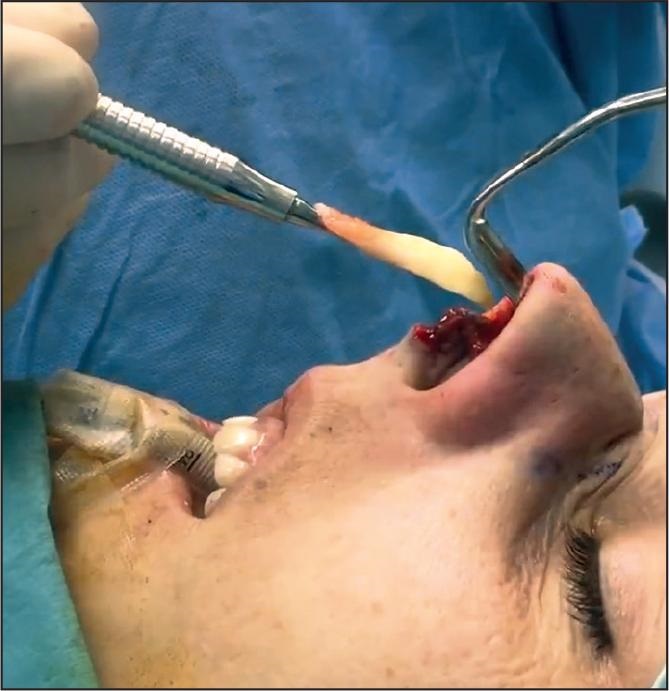
Una vez terminada la sutura de la incisión de la rinoplastia, llevamos a cabo el injerto de nanograsa. Inyectamos por vía intradérmica en la región de rinion un promedio de 1.5 ml de nanograsa por paciente, en abanico, desde cefálico a caudal con una aguja de 27G (Vídeo 2 disponible en material suplementario) cubriendo el área del rinion(7) y extendiéndola bilateralmente a lo largo del borde piriforme.
La arteria nasal dorsal corre cerca del periostio en la región del rinion, por lo que se debe evitar la capa preperióstica en esta zona,(8) evitando así la arteria dorsal y el plexo subdérmico para no provocar sangrado. Primero pasamos la aguja a través de la dermis, ligeramente acodada 10º y con el bisel de la punta hacia arriba. Una vez alcanzado el extremo más distal de posicionamiento deseado del injerto, inyectamos la nanograsa dentro de la misma dermis, aprovechando el túnel realizado por la aguja. Hemos de tener cuidado por mantener la piel intacta a lo largo de la trayectoria de la inyección para evitar la pérdida de volumen de nanograsa (Fig. 10 A-C).
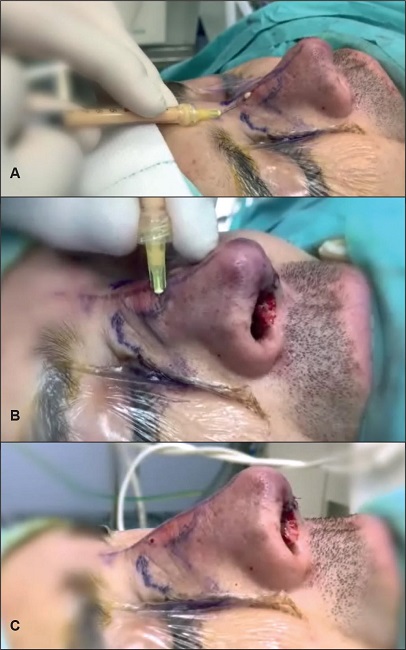
Figura 10. A y B. Aplicación de la grasa en dorso nasal, nótese la angulación de la aguja y la posición del bisel hacia arriba para evitar la inyección intraarterial. C. Aspecto del dorso nasal (ligeramente abultado y enrojecido) al terminar la infiltración de la nanograsa.
Tras el nanofat, inyectamos el exudado recogido en la cubeta de la caja Xpression®. Este exudado es conocido por tener una concentración elevada de plaquetas,(10) cuyos factores de crecimiento se liberan en la nanograsa para optimizar su viabilidad (Fig. 11) (Video 2 disponible en material suplementario).
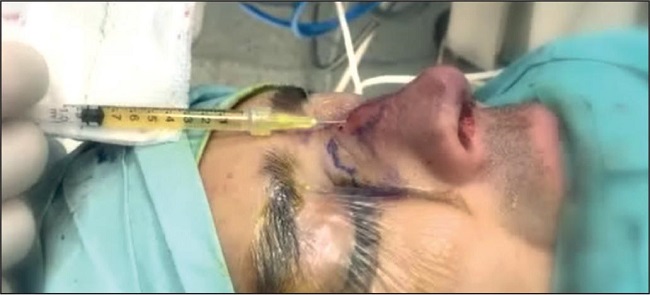
Figura 11. Finalización del procedimiento con infiltración del exudado remanente en la caja Xpression® tras obtención del coágulo de fibrina.
Para finalizar, aplicamos una lámina de cianocrilato en spray (Nobecutan®) sobre la piel nasal, esperamos a su secado y aplicamos apósitos adhesivos (Steri.Strips®) sobre el dorso y rodeando la punta nasal. Volvemos a aplicar una lámina de Nobecutan® sobre estos apósitos y tras su secado, procedemos a aplicar una férula de material termoplástico que se adhiere a los apósitos. Mantenemos esta ferulización durante 10 días.
Resultados
Analizamos 24 pacientes, 2 hombres y 22 mujeres, sometidos a rinoplastia primaria estética que incluyó la extirpación de jiba dorsal, entre enero de 2022 y enero de 2023, con una edad media de 31.21 años (máxima de 43 y mínima de 21 años). De ellos, y según nuestra clasificación del grosor preoperatorio del dorso nasal a nivel del rinion (R-STET), 22 fueron de tipo I a los que administramos intraoperatoriamente membrana más L-PRP, y 2 de tipo II a los que administramos solo membrana en la región del dorso y 0.5 ml de una disolución de acetónido de triamcinolona al 70% (esteroides) en la región de la punta con la finalidad de reducir el edema postoperatorio y el espesor de la piel en esta zona para una mayor definición de la punta nasal.
Los dos grupos diferentes de pacientes siguieron un patrón de curva similar. Los tipo I y II (Gráfico 1) respondieron con un aumento promedio de R-STET de 5 mm al día 7 de postoperatorio y de 1.9 mm al año. La disminución media del R-STET para los tipos I y II entre el día 7 y el 6º mes fue de 3 mm y desde el 6º mes hasta el final del primer año postoperatorio la disminución media fue de 0.1 mm.
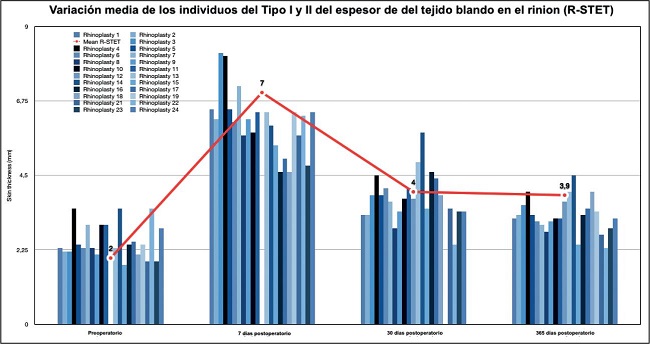
Gráfico 1. El tipo I respondió con un aumento del espesor de la piel en el rinion de 5mm. El aumento del grosor de la piel después de 1 año fue de 1.9 mm. La disminución media del espesor de la cobertura del rinion para los tipo I entre el séptimo día y el sexto mes fue · de 3 mm y desde el sexto mes hasta el final del primer año postoperatorio, la variación fue -0.1 mm.
Analizando ahora los resultados obtenidos de forma separada para cada tipo de pacientes tratados vemos que:
-
- Tipo I (Gráfico 2), respondió con un aumento del R-STET al día 7 de postoperatorio de 4.2 mm, y al año de 0.9 mm. La variación media del R-STET para el tipo I después de 1 mes en comparación con el valor preoperatorio fue de 1 mm de aumento. La variación media del R-STET para el tipo I entre el día 7 y el 6º mes de postoperatorio fue de -3,2 mm y desde el 6º mes hasta el final del primer año postoperatorio la variación fue de -0.1 mm.
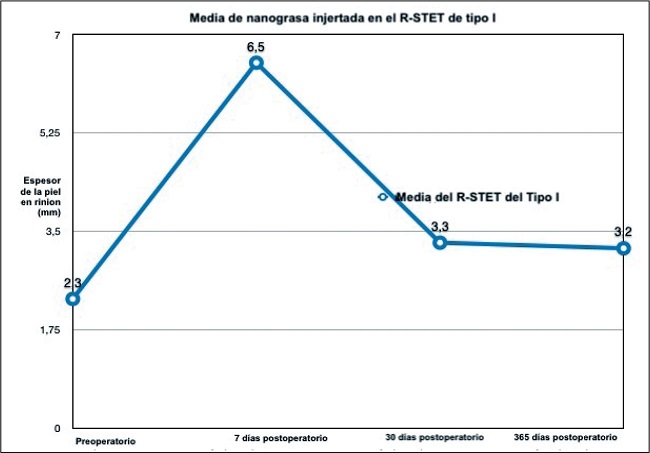
Gráfico 2. El tipo I respondió con un aumento de R-STET en el séptimo día postoperatorío de 3.2 mm. El aumento del espesor de la piel después de un año fue de 0.9 mm. La variación media de R-STET para el tipo I entre el séptimo día y el sexto mes fue de -3.2 mm y desde el sexto mes hasta el final del primer año postoperatorío la variación fue de -0.1 mm.
-
- Tipo II (Gráfico 3), respondió con un aumento del R-STET al día 7 de postoperatorio de 4.6 mm y de 0.5 mm al año. La variación media del R-STET para el tipo I después de 1 mes en comparación con el valor preoperatorio fue de 1 mm de aumento. La variación media del R-STET para el tipo I entre el día 7 y el 6º mes de postoperatorio fue de -3.5 mm, y desde el 6º mes hasta el final del primer año postoperatorio la variación fue de -0.6 mm.
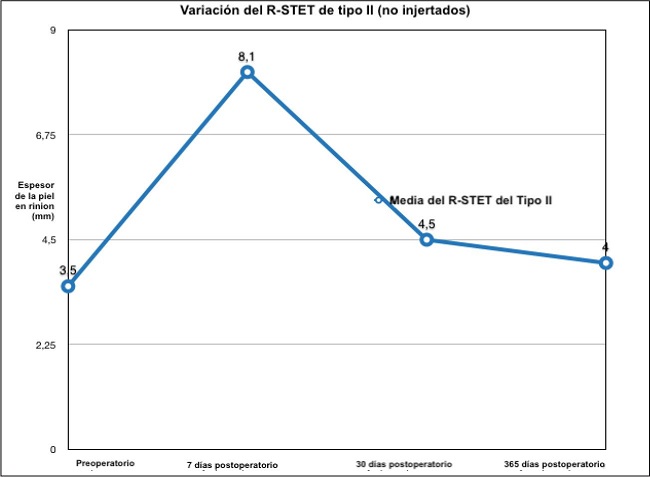
Gráfico 3. El tipo II respondió con un aumento de R-STET en el séptimo dia postoperatorio de 4.6 mm, El aumento de R-STET después de un año fue de 0.5 mm teniendo en cuenta que 2 de los casos fueron tratados intraoperativamente con acetónido de triamcinolona para prevenir y tratar la hinchazón excesiva de la piel. La variación media de R-STET para el tipo II entre el dia 7 y el sexto mes fue de -3.6 mm y desde el sexto mes hasta el final del primer afio postoperatorio la variación fue de -0.5 mm.
Así pues, los dos tipos de R-STET aumentaron en el primer año de postoperatorio de la rinoplastia, de forma que los casos promedio de R-STET Tipo I se convitieron en Tipo II al año de la intervención. Después de realizar la rinoplastia, la mayoría de los pacientes de tipo I de nuestro grupo de estudio (81.81% n=18) se convirtieron en tipo II.
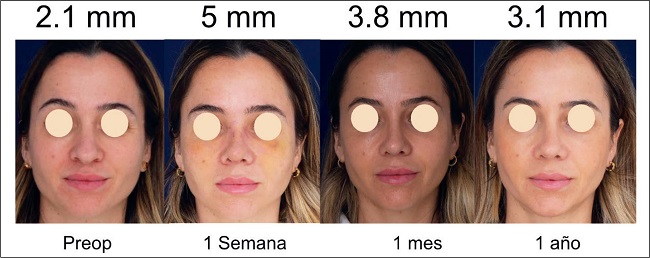
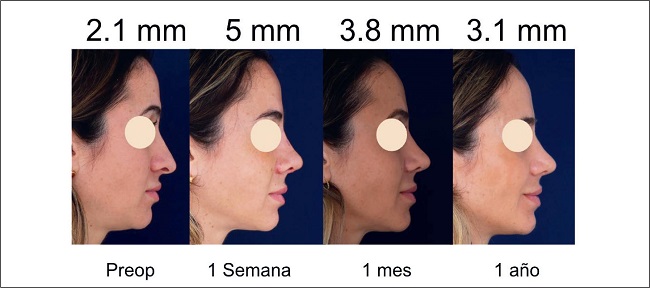
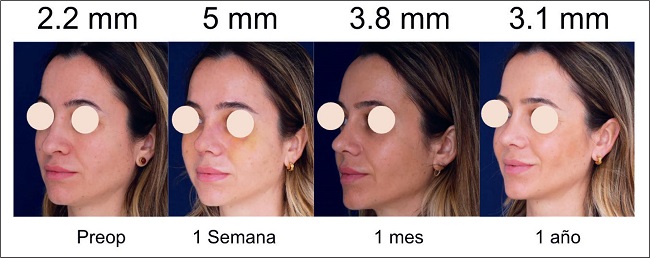
De los 24 pacientes de nuestra serie, ninguno presentó irregularidades durante el primer año de seguimiento postoperatorio. No recogimos complicaciones tipo cicatrices, hematomas, infecciones, decoloración de la piel, quistes, acné o signos de embolia, y ningún paciente precisó reintervención (Fig. 12 y 13)
Discusión
Las principales y más comunes quejas de los pacientes que solicitan una rinoplastia estética primaria se relacionan con la presencia de una giba de convexidad dorsal y, de manera similar, las irregularidades postoperatorias de la zona del dorso son las indicaciones más comunes, entre el 5% al 15%,(5) para la rinoplastia secundaria.(11) Los problemas encontrados en el dorso nasal operado incluyen gibas residuales, asimetría, muescas o protuberancias, que son especialmente evidentes en pacientes de piel fina y en casos secundarios con una anatomía muy distorsionada del dorso nasal.(12)
El grosor ideal del tejido blando del dorso nasal se sitúa en el rango medio, donde es lo suficientemente grueso como para ocultar pequeñas irregularidades, pero lo suficientemente delgado como para transmitir los contornos esculpidos de la estructura del esqueleto nasal. Dado el desafío que representa un envoltorio de tejido blando a nivel del rinion fino o grueso, consideramos de gran utilidad identificar a estos pacientes de piel fina y de piel gruesa de forma preoperatoria, ya que esto permitiría a los cirujanos brindar un mejor asesoramiento preoperatorio y una adecuada gestión de expectativas, analizando los resultados típicos y los desafíos asociados a la rinoplastia en función de las características propias de la piel de dorso nasal de cada paciente.
Es por ello que nos basamos en la clasificación R-STET que básicamente establece como piel fina la que tiene un grosor inferior a 3 mm y piel gruesa la que tiene un espesor igual o superior a 3 mm medidos a nivel del rinion, y en nuestra práctica personal, con un adipómetro manual. Empleamos el adipómetro manual por su simplicidad y economía, además de que consideramos que las mediciones que proporciona son tan válidas como las que se realizan con métodos más sofisticados y costosos, tales como el ultrasonido o la tomografía axial computarizada (TAC).(13,14) Estableciendo esta clasificación preoperatoria de los pacientes podemos facilitar la aplicación de técnicas preoperatorias, intraoperatorias y postoperatorias, que en ocasiones son infrautilizadas, para optimizar el grosor de la piel del dorso nasal y de esta forma mejorar los resultados postoperatorios y la satisfacción de los pacientes.(8,13-16) ya que el espesor de la piel nasal y de los tejidos blandos tiene efectos considerables en la planificación del procedimiento y en los resultados postoperatorios en la cirugía de rinoplastia.(17)
En cuanto a las medidas que determinan ese grosor del dorso nasal, algunos estudios han encontrado que la envoltura de tejido blando nasal (STE, Soft Tissue Envelope) es más gruesa en el nasion (1.7 mm), más delgada en el rinion (0.7 mm), engrosada sobre la suprapunta (1 mm) y punta nasal (0.6 mm), y adelgazada sobre la columela (0.4 mm).(14) Parecía pues necesario abordar el espesor de la envoltura de tejido blando, particularmente a nivel del rinion, cuando es necesario reducir una giba dorsal nasal y determinar preoperatoriamente qué paciente es un candidato con mayor riesgo de desarrollar complicaciones postoperatorias y, por tanto, candidato a algún tipo de tratamiento complementario en el intraoperatorio. Sin embargo, y hasta donde hemos podido revisar, no encontramos literatura que correlacione el grosor de la piel en el rinion con alguna forma de planificación que establezca algunas acciones preventivas para tratar de evitar complicaciones en esta región en el postoperatorio de una rinoplastia estética. Por consiguiente, la base del presente estudio fue la identificación preoperatoria del grosor de la piel del dorso nasal, medida específicamente a nivel del rinion, con el objetivo de implementar, en casos de piel delgada, procedimientos complementarios a la rinoplastia estética que optimicen el resultado estético final.
En la actualidad, existen varios métodos para medir el STE que incluyen el examen visual, la palpación y, ocasionalmente, estudios por imagen como la ecografía(8,16,18) y la TAC.(14) En nuestra práctica no creímos justificable el uso de la TAC en el contexto de una rinoplastia estética con el único fin de evaluar el STE nasal y si bien consideramos la ecografía, resulta costosa. Es por ello que optamos por una forma más práctica y disponible para medir el R-STET que fue una prueba de pellizco con adipómetro digital.(14) Con este método aplicado tal y como hemos presentado en el apartado de material y método, clasificamos el espesor de la piel dorsal a nivel del rinion para tratar aquellos pacientes con mayor riesgo por tener una piel demasiado fina y así disminuir el riesgo de complicaciones postoperatorias derivadas de irregularidades en esta zona.
Algunos estudios de TAC encuentran que el grosor de la piel del rinion de la nariz es el más delgado, con un rango de espesor que oscila entre 1.8 mm y 2.11mm. Dey y col.(14) clasifican el grosor del STE de la nariz en 5 categorías: delgado, medio-delgado, medio, medio-grueso y grueso. Utilizando una escala predictiva de 0 a 100, definen las categorías de grosor del dorso nasal de la siguiente manera: delgado (0-20), medio-delgado (20-40), medio (40-60), medio-grueso (60-80) y grueso (80-100). Camacho y col. se preocupan por la piel nasal en su totalidad y clasifican el rinion según la facilidad para separar la piel en la zona en 2 grupos: uno en el que la piel se puede elevar del hueso y otro grupo en el que la piel no se puede elevar fácilmente del hueso.(19)
Dado que la prevención de las secuelas desfavorables después de la resección del dorso en la rinoplastia de reducción mediante restauración del complejo de la bóveda nasal media se ha vuelto imperativa en la mayoría de los pacientes,(17) y las imperfecciones de la "zona clave" pueden conducir a una serie de deformidades nasales dorsales comunes y errores en la rinoplastia,(20) en nuestro estudio, y centrándonos en la prevención de las complicaciones del rinion en el contexto de la rinoplastia primaria con reducción de la giba dorsal en pacientes con una STE fina, clasificamos preoperatoriamente nuestros pacientes en 2 grupos según el grosor de su piel a nivel del rinion medida con un adipometro manual (Tabla I).
Para tener una perspectiva acerca de cuál es el papel de la técnica que describimos en nuestro trabajo, creemos interesante comentar algunos de los métodos existentes para prevenir las irregularidades del dorso nasal, razón por la cual seguidamente hablaremos de la rinoplastia de preservación y lo que implica.
En la rinoplastia de preservación dorsal (DPO), la técnica push down (PDO) realiza osteotomías laterales y mediales de la pirámide nasal combinadas con una movilización del septo para, "empujando hacia abajo", alcanzar la forma deseada, mientras que en la técnica let down (LDO) o de caída del dorso, se eliminan segmentos específicos de hueso y cartílago en la base nasal "dejando caer" el dorso a la nueva posición. Estas técnicas fueron definidas por Lothrop en 1914(21) como métodos para preservar tanto el rinion (keystone zone-zona clave) como la uniformidad de la bóveda cartilaginosa. En nuestro caso utilizamos la rinoplastia abierta estructural e incorporamos el piezotomo para refinar el resultado de las osteotomías.
Mientras que una nariz cartilaginosa es una excelente indicación para la preservación dorsal del rinion, la giba ósea muy cifótica con un ángulo nasofrontal profundo o una pirámide ósea irregular y las septorrinoplastias secundarias no son una buena indicación para la preservación dorsal. Por tanto, estas técnicas siguen siendo una indicación para pacientes seleccionados de rinoplastia primaria .(21)
Se han descrito además diversos métodos para tratar irregularidades postoperatorias del dorso nasal, como cartílago cortado en cubitos solo o en bloque o combinado con hidroxiapatita de calcio, esponja de fibrinógeno-trombina, membrana de colágeno de doble capa,(3) lipoinfiltración, cartílago inyectable, ácido hialurónico, fascia temporal, y algunos de ellos durante la rinoplastia primaria, como membranas de colágeno,(3) fascia temporal, dermis acelular, pericardio, incluso polvo de hueso. Por otro lado, el tejido adiposo se ha convertido en un recurso popular y bien establecido en la Cirugía Plástica, tanto con usos estéticos como reconstructivos. La lipoinfiltración (lipofilling) del tejido subcutáneo se ha utilizado satisfactoriamente en rinoplastia como micrograsa para corregir irregularidades menores, y más recientemente, Tonnard y col.(22) informaron sobre la eficiencia y seguridad del tratamiento del envejecimiento de la piel con nanograsa, una suspensión de grasa emulsionada diferente del trasplante de grasa tradicional, para promover el rejuvenecimiento de la piel. En este sentido, Sesé y col.(23) informan que el análisis de ADN mostró que la desagregación mecánica utilizada durante el procesamiento de producción de la nanograsa ofrece un mejor inóculo celular que los métodos de disociación enzimática convencionales, al utilizar 10 veces menos tejido graso como material de partida y ofrecer un mayor rendimiento celular.
Durante la última década, también el uso de fibrina rica en plaquetas leucocitarias (L-PRF) ha ganado un tremendo impulso en la odontología regenerativa. La fibrina rica en plaquetas (PRF) se introdujo como una fuente autógena de factores de crecimiento sanguíneo que podría servir como herramienta para la regeneración de tejidos en la medicina moderna. Los conceptos se derivan del hecho de que un concentrado de plaquetas de primera generación, denominado plasma rico en plaquetas (PRP), se estaba utilizando intensamente en diversos campos de la Medicina a pesar de tener el aspecto negativo de contener anticoagulantes, impidiendo así la cascada completa de coagulación, importante para la formación de tejido de cicatrización.
El PRF (Platelet Rich Fibrine-Fibrina Rica en Plaquetas), que desde entonces pasó a llamarse L-PRF debido a su mayor contenido de leucocitos, no contiene ningún anticoagulante y además proporciona una matriz de fibrina tridimensional que puede utilizarse como soporte para una variedad de procedimientos que cumplen la función de membrana barrera en procedimientos guiados de regeneración ósea y tisular. El PRF se utiliza en procedimientos de rinoplastia como armazón autólogo cuando se combina con cartílago para el aumento del dorso nasal, o como forma de reducir el edema y la equimosis en el posoperatorio. También se ha utilizado ampliamente en la práctica clínica para mejorar la eficacia de la lipotransferencia asistida por células (CAL- Cell Assisted Lipotransfer) y la reparación de heridas, debido a sus ventajas en la prevención del rechazo inmunológico, la producción simple y las pequeñas complicaciones.(10) Además, los cirujanos plásticos han adoptado el PRP, un predecesor del PRF, como rejuvenecedor para tratar la piel envejecida mediante inyección intradérmica. Zhi-Jie Liang y col. informan acerca de que la inyección intradérmica precisa de nanofat-PRF es segura y altamente efectiva para el rejuvenecimiento y reparación facial(24) y también como forma preventiva durante la rinoplastia contra irregularidades postoperatorias.(19)
Cárdenas y col.(25) utilizan la lipoinyección de microinjertos grasos enfocada en mejorar el contorno del dorso nasal y corregir imperfecciones menores postoperatorias. Inyectan 2-3 ml de grasa preparada en el espacio subcutáneo sobre el marco osteocartilaginoso al finalizar la cirugía, después de la sutura de las incisiones y antes de aplicar la férula. La grasa inyectada actúa como una fina capa de tejido blando, aumentando el grosor de la piel y camuflando irregularidades leves. En nuestro caso producimos 1.5 ml de nanograsa combinada con L-PRF y la infiltramos en el plano intradérmico de manera selectiva, según nuestra clasificación preoperatoria, en las rinoplastias de tipo I, a nivel del rinion, para prevenir la aparición de irregularidades postoperatorias.
En cuanto a la forma de aplicación en el dorso nasal, muchos estudios han demostrado que los principales vasos sanguíneos nasales, incluida la arteria nasal dorsal, se encuentran en las capas de grasa fibromuscular o subcutánea. Por lo tanto, la capa grasa profunda ubicada entre la capa fibromuscular y el periostio o pericondrio se considera una capa segura para la inyección de relleno nasal. Tansatit y col. demuestran que existen arterias nasales dorsales bilaterales en solo el 34% de las muestras cadavéricas de su estudio, mientras que el 28% tenía sólo una única arteria nasal dorsal grande. Además, en el 14% de sus especímenes la arteria nasal dorsal cruzó la línea media en el tercio medio de la nariz. Sus hallazgos demostraron que la inyección perpendicular a la línea media perfora la arteria en pacientes en los que la arteria atraviesa la línea media. El uso de una aguja 27G con el bisel de la punta hacia arriba y la aguja ligeramente acodada 10º, garantiza la colocación del injerto de nanograsa muy por encima del tejido subcutáneo profundo del área del rinion y de esta manera, prevenir la inyección endovenosa de la nanograsa. En nuestra práctica y mediante la utilización de esta técnica, no hemos encontrado complicaciones tipo embólico entre los pacientes de nuestro grupo de estudio.
Con la medición preoperatoria del grosor de los tejidos blandos del dorso nasal y la clasificación que proponemos de los pacientes que vamos a someter a rinoplastia estética según su envoltura de tejidos blandos del rinion, planteamos una propuesta para seleccionar aquellos que podrían tener mayor riesgo de desarrollar complicaciones postoperatorias (clasificación R-STET). De esta manera, los casos de tipo I, que definimos con un grosor de dichos tejidos menor de 3 mm, son los que consideramos de mayor riesgo y planificamos su tratamiento selectivo intraoperatorio con membranas L-PRF e injertos nasales de nanograsa enriquecidos con suero L-PRF. (Tabla I).
Consideramos que los resultados de la observación a 1 año de postoperatorio de los pacientes de nuestro grupo de estudio son prometedores e informan acerca de un aumento promedio del grosor de la envoltura de tejido blando del rinion de 0,9 mm en pacientes tipo I, sin complicaciones, y con resultados satisfactorios. De esta forma y con un mínimo incremento de tiempo operatorio de 15 minutos en nuestras manos, logramos que los pacientes con R-STET tipo I se conviertan en tipo II (grosor igual o superior a 3 mm).
Conclusiones
El espesor de la piel nasal y de la envoltura de tejidos blandos tiene efectos considerables sobre la planificación del procedimiento y los resultados postoperatorios en la cirugía de rinoplastia estética. El análisis observacional revela que los pacientes con piel más fina son propensos a sufrir irregularidades postoperatorias en la bóveda media.
Proponemos y desarrollamos una metodología y técnica quirúrgica para medir preoperatoriamente el espesor del tejido blando del dorso nasal con adipómetro manual a nivel del rinion en pacientes candidatos a rinoplastia estética, y en función del mismo clasificar a los pacientes para, en aquellos que presenten un espesor menor o igual a 3 mm, planificar un procedimiento complementario intraoperatorio que mediante la aplicación de L-PRF y nanograsa previene la aparición de irregularidades del dorso nasal en el postoperatorio.