Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Española de Cirugía Oral y Maxilofacial
versión On-line ISSN 2173-9161versión impresa ISSN 1130-0558
Rev Esp Cirug Oral y Maxilofac vol.34 no.3 Madrid jul./sep. 2012
https://dx.doi.org/10.1016/j.maxilo.2012.02.001
Manejo quirúrgico del ameloblastoma
Surgical management of ameloblastoma
Adaia Vallsa, Esther Montanéa, Coro Bescósa, Manel Saeza, Montserrat Munilla y Margarita Alberolab
aServicio de Cirugía Oral y Maxilofacial, Hospital Vall d'Hebron, Barcelona, España
bServicio de Anatomía Patológica, Hospital Vall d'Hebron, Barcelona, España
Dirección para correspondencia
RESUMEN
El ameloblastoma es un tumor odontogénico de estirpe epitelial. Aunque se clasifica como una tumoración benigna, suele ser localmente agresiva presentando elevada invasión local, con gran tendencia a la recidiva y con posibilidad metastásica ocasional.
Se manifiesta preferentemente durante la tercera, cuarta y quinta décadas de la vida, sin predilección por razón de sexo, aunque puede darse en cualquier grupo de edad, incluidos los niños. La mayoría de los ameloblastomas se encuentran sobre todo en mandíbula (al nivel del ángulo y rama). En el tratamiento se debe valorar su tipología clínica (sólido, multiquístico, uniquístico, mixto o periférico), su localización y el tamaño del tumor, así como la edad y las condiciones clínicas del paciente.
Presentamos una revisión de los pacientes afectos de ameloblastomas tratados en nuestro Centro durante los últimos 10 años. Se aportan datos acerca de su aparición clínica, sus características histológicas, el manejo terapéutico realizado y analizamos el seguimiento y comparamos la aparición de recidivas en los pacientes presentados.
Las características clínicas, incluso si se complementan con radiografías y/o muestras histológicas, no son siempre determinantes del comportamiento biológico y, por tanto tampoco lo son del pronóstico de un ameloblastoma individual.
Palabras clave: Ameloblastoma. Tumor mandibular y maxilar. Tumor benigno. Tumor agresivo. Tratamiento quirúrgico. Algoritmo de tratamiento ameloblastoma.
ABSTRACT
The ameloblastoma is an odontogenic tumour of epithelial origin. Although it is classified as benign, there is usually aggressive local invasion, a great tendency to recurrence, and occasional metastatic potential.
It generally appears during the third, fourth and fifth decades of life, without gender predilection, although it can occur at any age, including in children. Ameloblastomas are mostly found in the mandible (angle and branch). In treatment, its clinical type (solid, unicystic, desmoplastic, mixed or peripheral), its location and size, must be assessed, as well as the age and clinical condition of the patient.
We present a review of patients diagnosed and treated for ameloblastoma in our hospital during the last 10 years. We present data on clinical appearance, histological characteristics, and therapeutic management, and we analyse and compare the rate of recurrence in these patients.
The clinical features, even if they are supplemented with radiographs and/or histological samples, are not always biological determinants of its behaviour, or of the individual prognosis of the ameloblastoma.
Keybwords: Ameloblastoma. Benign tumour. Aggressive tumour. Surgical treatment. Treatment algorithm.
Introducción
El ameloblastoma es una neoplasia odontogénica de estirpe epitelial. Puede originarse a partir del órgano del esmalte, de los remanentes de la lámina dental, del epitelio de quistes dentígeros o, posiblemente, de las células basales del epitelio de la mucosa oral1. Varios elementos han sido sugeridos como precursores de la lesión: diente incluido, quiste odontogénico, extracción dentaria, traumatismo externo o virus papiloma humano2. Ninguno de ellos ha sido demostrado, aunque resulta interesante destacar que el 25% de los ameloblastomas se asocian a un diente incluido.
Se trata del tumor odontogénico más común, representando el 1% de todos los tumores y quistes maxilares y el 11% de todos los tumores odontógenos maxilares3-5. Presenta un claro predominio en mandíbula (80%), sobre todo en ángulo y rama mandibulares y no se han encontrado diferencias significativas en razón de sexo ni de raza, aunque se ha sugerido un aumento en la incidencia de ameloblastomas en el este de África.
El estudio de la lesión suele iniciarse cuando el paciente acude con una tumoración de crecimiento lento, dolor, sobreinfección de la lesión, ulceración de la mucosa, pérdida o movilidad dentaria, parestesias del nervio dentario inferior, o simplemente como hallazgo radiológico casual. El estudio suele complementarse con pruebas de imagen: ortopantomografía, escáner o resonancia magnética (figs 1 y 2).

Fig. 1. TC diagnóstico de ameloblastoma mandibuar.

Fig. 2. TC de control posquirúrgico con reconstrucción mandibular.
Radiológicamente suele describirse como una lesión quística expansiva que adelgaza o erosiona la cortical ósea. Se han descrito 3 patrones radiológicos de esta lesión: unilocular, multilocular y en panal de abejas. A pesar de dicha clasificación, no se ha encontrado ninguna correlación radiológica con la edad, el sexo, el tipo histológico ni el comportamiento o agresividad del tumor. La reabsorción radicular es altamente sugestiva de ameloblastoma.
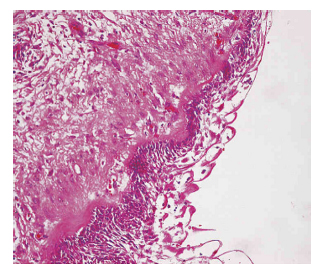
El diagnóstico definitivo debe estar basado en el estudio anatomopatológico, el cual puede ser mediante punción aspiración con aguja fina (PAAF)6 o biopsia de la lesión (fig. 3).
La OMS incluye los ameloblastomas dentro de los tumores benignos de epitelio odontogénico maduro, con estroma fibroso sin ectomesénquima odontogénico. Desde el 1992, dicha organización reconoció 3 variantes clínico-patológicas: ameloblastoma sólido, convencional o poliquístico (AS), ameloblastoma uniquístico (AU) y ameloblastoma periférico (AP). Pero en 2005 se añadieron 2 nuevas variantes en la clasificación de la OMS: el patrón desmoplásico se escinde de la variante AS y forma el ameloblastoma desmoplásico (AD). Además, las lesiones que contienen áreas con patrón desmoplásico y otras con patrón sólido, son llamadas lesiones híbridas o mixtas (AM)7. Paralelamente, debemos distinguir los ameloblastomas metastizantes (METAM) definidos como un ameloblastoma que, a pesar de su apariencia histológica benigna, metastatiza a nivel ganglionar regional y a distancia (por orden de frecuencia): pulmón, pleura, vértebras, huesos craneales, diafragma, hígado y parótida, bazo y riñones8. La incidencia reportada de METAM es del 2%, aunque se sugiere que realmente es aún inferior9,10 y no deben confundirse con los carcinomas y los sarcomas ameloblásticos, que son 2 entidades independientes de los ameloblastomas con mayor riesgo de metastatizar9,11 (Tabla 1).
El patrón de crecimiento de los ameloblastomas tiene implicaciones en las tasas de recurrencia y por tanto en la decisión del plan terapéutico12. Además, actualmente se están llevando a cabo estudios de marcadores de crecimiento y agresividad tumoral: p53, MDM2, Ki-67, PCN Ag, WNT5A,...13.
Objetivos
Este estudio pretende realizar un análisis epidemiológico, clínico, radiológico e histológico, y tipo de cirugía realizada dentro de nuestra muestra de pacientes diagnosticados de ameloblastoma de los maxilares.
Nuestro interés principal es analizar y comparar el papel de la cirugía en el manejo de cada tipo de ameloblastoma en orden de determinar factores pronósticos clínicos, patológicos y radiológicos y compararlos con los resultados publicados en la literatura.
Material y métodos
Se realiza un estudio retrospectivo de 16 pacientes tratados en el Servicio de Cirugía Oral y Maxilofacial del Hospital Vall d'Hebron desde enero del 2000 a diciembre del 2010 con el diagnóstico de ameloblastoma de maxilar superior o inferior.
Se recogen los datos del estudio clínico (edad, sexo, raza, presentación clínica), histológico (AS, AU, AP, AD, AM, METAM), de imagen (localización, tamaño y patrón radiológico), tipo de cirugía: enucleación con legrado (exéresis de la lesión con raspado de la superficie ósea), resección parcelaria (se elimina parte del hueso pero manteniendo la continuidad del mismo), resección segmentaria (se reseca todo el sector del hueso afecto, perdiendo la continuidad ósea) y tipo de reconstrucción, y evolución de cada paciente (recidiva o no). Los casos son clasificados según estos ítems para poder llevar a cabo el análisis comparativo.
Resultados
La edad media de los pacientes en el diagnóstico inicial es de 44 años (17-68 años), y en relación al sexo 11 son hombres y 5 mujeres (OR: 2:1). En cuanto al país de origen, 11 son de nacionalidad española y 5 extranjeros: Lituania, China, Marruecos, Filipinas y Georgia. (Tabla 2)
Todos los pacientes han acudido a las consultas externas o a las urgencias del Hospital Vall d'Hebron por presentar alguna de las siguientes sintomatologías: tumoración (85%), dolor/tumefacción/hinchazón (43%), parestesias (7%) o movilidad de piezas dentarias (14%). Ninguno de ellos ha sido diagnosticado como un hallazgo casual ni secundario a metástasis a distancia. Se han analizado los antecedentes patológicos clínicos de los pacientes, pero ninguno de ellos ha sido relevante.
Con las pruebas de imagen obtenemos el patrón de presentación radiológica: unilocular (25%), multilocular (56,25%) o en panal de abejas (18,75%). La localización de la lesión presenta un predominio claro por la mandíbula: 13 casos (81,25%) en comparación con los 3 casos de maxilar superior (18,75%). El tamaño medio del tumor en el momento diagnóstico en nuestra serie de pacientes es de 4×3,1cm. En 4 de los pacientes (25%) se ha hallado una pieza dental incluida intraósea e intratumoral. (fig. 4).

Fig. 4. Ortopantomografía de ameloblastoma con cordal incluido.
Es de interés destacar que en maxilar superior los ameloblastomas presentan más a menudo destrucción de la cortical ósea e invasión perilesional (66,6%). En cambio, en mandíbula este fenómeno no se presenta en nuestra serie.
Los resultados histológicos obtenidos posteriormente a la cirugía han sido: 9 casos de AS, 4 casos de AU, 2 casos de AM y 1 caso de AD.
En cuanto al tratamiento quirúrgico recibido, lo subclasificamos según el patrón histológico y localización de la lesión. (figs. 5 y 6)
• 4 AU (25%): 4 enucleaciones con 1 recidiva a nivel de coronoides (25%). Todos ellos son de localización mandibular.
• 9 AS (56,25%) tratados de la siguiente manera
· 4 resecciones segmentarias (3 de los casos en mandíbula y un caso en maxilar superior) sin recidivas (0%).
· Cinco resecciones parcelarias (4 lesiones de mandíbula y una en maxilar superior), con 3 recidivas (60%), una de ellas en el caso del maxilar superior (50% de recidivas en mandíbula y 100% de recidiva en maxilar superior con resección parcelaria).
• 2 AM (12,5%), ambos en mandíbula, uno de los casos tratado con resección parcelaria y el otro con segmentaria. Ambos persisten libres de enfermedad (0% recidiva)
• 1 AD (6,25%) localizado en el maxilar superior, el cual se trató mediante resección parcelaria y no presenta recidiva (0%)

Fig. 5. Resección quirúrgica de ameloblastoma mandibular.

Fig. 6. Pieza quirúrgica de resección del ameloblastoma.
Las reconstrucciones realizadas en el lecho quirúrgico son variadas y dependen del tamaño del defecto y su localización: colocación de miniplacas o placa de reconstrucción con colgajos microvascularizados, injertos de cresta ilíaca, materiales de sustitución y regeneración ósea tipo PRP, DBX, o colgajos de rotación de temporal para defectos del maxilar superior.
El total de recidivas (n=4, 25%) las podemos analizar según la localización de la lesión: obtenemos un 33,33% (1 de 3 casos) de recidivas en maxilar superior frente a un 23,07% (3 de 13 casos) en mandíbula.
En cuanto al estudio de recidivas relacionadas con el tipo de tratamiento recibido: enucleación mandibular=1/4 (25%), mandibulectomía parcelaria=2/5 (40%), mandibulectomía segmentaria=0/4 (0%), maxilectomía parcelaria=1/2 (50%), y maxilectomía en bloque= 0/1 (0%).
Por otra parte, también podemos estudiar las recidivas según el tipo histológico: AU=1/4 (25%), AS=3/9 (30%), AM=0/2 (0%) y AD=0/1 (0%).
Discusión
El comportamiento de los ameloblastomas ha sido descrito como el de un tumor benigno de crecimiento lento, pero localmente agresivo con tendencia a la invasión, a la destrucción y a la persistencia si no se realiza una adecuada exéresis quirúrgica14. La mayoría de las revisiones de casos publicadas coinciden en el alto índice de recurrencia y la tendencia casi nula a metastatizar de los ameloblastomas. En nuestra serie de casos observamos un 25% de recidivas en AU tratados de forma conservadora. En el resto de ameloblastomas la tasa de recidiva es del 25% con tratamiento radical.
Müller y Slootveg15 en su serie de 84 casos, describen una tasa de recurrencia en AS del 75% en pacientes tratados mediante tratamiento conservador y del 15% en pacientes tratados de forma radical. En los AU tratados de forma conservadora la tasa de recidiva es del 20%.
Nakamura et al.16 realiza una comparación de los resultados a largo plazo de los distintos manejos quirúrgicos del ameloblastoma en 78 casos, reportando una recurrencia de 7,1% posterior a un tratamiento radical y 33,3% en tratamientos conservadores.
Específicamente, el AS es agresivo, con tendencia a infiltrar de forma irregular el tejido óseo y blando adyacente. Además, presenta islas tumorales alejadas de la masa de tumor principal, por lo que se requiere de un margen mínimo de uncm de tejido sano a partir del límite clínico y radiográfico. Se ha reportado una recurrencia de ameloblastomas sólidos tratados de forma conservadora de hasta el 100%, siendo la media de 55-90%2,12,17,18. En los AS se han descrito diversos patrones histológicos: folicular, plexiforme y desmoplásico (escindido como AD). Generalmente se encuentran patrones mixtos, por lo que se clasifican según el tipo de patrón predominante19. Se duda de la implicación pronóstica del patrón histológico, pero Reichart et al. realizaron un estudio retrospectivo20 donde concluyeron que el subtipo histológico tenía implicaciones pronósticas en cuanto a la recurrencia de los ameloblastomas. De acuerdo con su estudio, el patrón folicular presentaba la mayor tasa de recurrencia, siendo aproximadamente del 29,5%, seguido por el patrón plexiforme con tasas de recurrencia del 16,7 y del 4,5% en la variante desmoplásica.
Los AU, que afectan a pacientes ligeramente más jóvenes, se clasifican en 3 subtipos: intraluminal (I) cuando las células tumorales proliferan hacia el interior de la cavidad patológica; luminal (II) cuando la lesión quística está rodeada de epitelio de ameloblastoma; y mural o intramural (III) cuando las células neoplásicas infiltran el tejido conjuntivo fibroso de la pared quística18. En general, tanto el subtipo luminal como el intraluminal pueden ser tratados efectivamente mediante enucleación, mientras que los AU intramurales, por su capacidad de infiltración, deben ser considerados como ameloblastomas sólidos18,21-23. (fig. 7).

Fig. 7. Esquema con los distintos subtipos de AU.
Los AP se manifiestan como una masa sésil o pediculada de crecimiento lento que queda confinada a la encía o a la mucosa alveolar. En general no incluye el hueso subyacente ni tiene una actividad invasiva, por lo que se suele recomendar una escisión conservadora5.
Por último, los AD son un patrón de ameloblastoma muy infrecuente y con características radiológocas diversas. Se presentan con mayor frecuencia en la región anterior de ambos maxilares, tienen un crecimiento intramedular y con límites poco definidos. En definitiva, requieren un tratamiento radical, similar al del ameloblastoma sólido24. Los mismos criterios se asumen para los AM.
En conclusión, el tratamiento que deben recibir los ameloblastomas a menudo es un tema de controversia entre los especialistas. Para tomar una decisión adecuada, debemos considerar los siguientes factores: tipo histológico, localización anatómica, proximidad a estructuras nobles, dimensiones del tumor, edad, condiciones físicas y expectativas del paciente.
El algoritmo de tratamiento sugerido por nuestro centro es el siguiente:
• Mandíbula:
· En los AU con márgenes quísticos nítidos (I,II) y en los AP: enucleación y curetaje.
· En los AS, AD, AM, AU con erosión de los márgenes quísticos (III), METAM o recidivas: amplia resección con márgenes de seguridad.
• Maxilar superior: amplia resección con márgenes de seguridad.
Notas a remarcar:
• Carcinoma y sarcoma ameloblásticos no se incluyen en el algoritmo
• Es imprescindible la biopsia de cualquier lesión sospechosa de ameloblastoma (biopsia previa cirugía o bien la intraoperatoria serían la norma). En caso de haber realizado una exéresis sin márgenes de un ameloblastoma que no sea periférico o uniquístico tipo I o II, nos debemos replantear la cirugía con márgenes o bien realizar controles de forma exhaustiva, dependiendo de la localización, tamaño, y características de la lesión y de la edad y tipología de paciente.
• Se consideran márgenes quirúrgicos de seguridad la ampliación de la resección de 1 cm a partir del límite clínico y radiográfico de la lesión de forma intraoperatoria.
• En el maxilar superior las lesiones tienen más facilidad de expansión debido a la menor resistencia de su cortical y medular óseas.
• La radioterapia en general se reserva para las lesiones no quirúrgicas desde el inicio, las recurrencias no operables y para las lesiones extirpadas con márgenes afectados a pesar de la amplia resección.
• Los controles recomendados son hasta los 10 años libres de enfermedad, y en los malignos el seguimiento debe ser más prolongado.
• En pacientes pediátricos existe un mayor porcentaje de incidencia de ameloblastomas uniquísticos. La enucleación se ha considerado un tratamiento efectivo en los casos de AU y AP. En casos de tumores uniquísticos recurrentes, ameloblastomas uniquísticos intramurales, sólidos y demás patrones, estos deben ser tratados mediante resección amplia25.
Por su parte, en el hospital Pitié-Salpêtrière26 han propuesto un algoritmo de tratamiento, donde recomiendan tratamiento conservador en lesiones menores de 5cm sin invasión periférica y tratamiento agresivo en el resto de lesiones.
Paralelamente, Sachs et al.27 recomiendan tratar los ameloblastomas mediante escisión quirúrgica más osteotomía periférica. Indica la enucleación de la mayoría de la lesión, como una sola masa mediante el uso de curetas y posteriormente se realiza ostectomía periférica de 2 a 3mm. Para la elección del plan terapéutico, valora la localización de la lesión, la extensión de la expansión, la presencia de continuidad ósea y en cierto grado, el tipo histológico.
De otro modo, algunos autores utilizan adyuvantes terapéuticos, que junto a la maniobra de extirpación elegida, procuran provocar la lisis de las células tumorales residuales y disminuir la tasa de recurrencia. Se ha demostrado que el uso de nitrógeno líquido posterior a la enucleación de ameloblastomas disminuye la tasa de recidiva. Pogrel28 reporta resultados muy buenos tratando los ameloblastomas con curetaje o resección junto a crioterapia con nitrógeno líquido. El uso de soluciones esclerosante como la de Carnoy también se han recomendado para los AU (solución descrita en 1933 para el tratamiento de quistes y fístulas, que además penetra el hueso esponjoso a una profundidad de 1,5mm).
Conclusiones
El ameloblastoma es un tumor benigno, pero localmente agresivo. A pesar de que sus marcadores histológicos de pronóstico aún están en estudio, toda lesión sospechosa debe ser biopsiada previamente a la cirugía, ya que la decisión terapéutica es difícil en los ameloblastomas ya enucleados.
En función de los criterios clínicos, histológicos y radiológicos, debemos decidir qué tipo de cirugía es la adecuada: la conservadora o la agresiva, así como el uso de otras terapias adyuvantes.
Financiación
Ninguna.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Agradecimientos
Agradecer la ayuda del Servicio de Anatomía Patológica del Hospital Vall d'Hebron de Barcelona, que siempre colabora en nuestros trabajos. También el trabajo del equipo de Cirugía Maxilofacial del Hospital Vall d'Hebron, Barcelona.
Bibliografía
1. Ghandhi D, Ayoub AF, Pogrel MA, MacDonald G, Brocklebank LM, Moos KF. Ameloblastoma: A surgeon's dilemma. J Oral Maxillofac Surg. 2006; 64:1010-4. [ Links ]
2. Correnti M, Rossi M, Avila M, Perrone M, Rivera H. Human papillomavirus in ameloblastoma. Oral Surg Oral a Med Oral Pathol oral Endod Radiolé 2010; 110:E20-4. [ Links ]
3. Goldman KE. Mandibular cysts and odontogenic tumors. eMedicine. 2006. [ Links ]
4. Slootweg PJ. Lesions of the jaws. Histopathology. 2009; 54:401-18. [ Links ]
5. Mendenhall WM, Werning JW, Fernandes R, Malyapa RS, Mendenhall NP. Ameloblastoma. Am J Clin Oncol. 2007; 30:645-8. [ Links ]
6. Bisht S, Kotwal SA, Gupta P, Dawar R. Role of fine needle aspiration cytology in preoperative diagnosis of ameloblastoma. Indian J Cancer. 2009. [ Links ]
7. Reichart PA, Philipsen HP, Sciubba JJ. The new classification of head and neck tumours (WHO): any changes?. Oral Oncol. 2006; 42:757-8. [ Links ]
8. Barnes L., Eversol J.W., Reichart P., Sidransky D., editors. World Health Organization Classification of Tumours. Pathology and Genetics Head and Neck Tumours. Lyon: IARC Press; 2005. [ Links ]
9. Dissanayake RK, Rukmal Jayasooriya P, Siriwardena DJ, Mudiyanselage Tilakaratne W. Review of metastazing (malignant) ameloblastoma (METAM): Pattern of metastasis and treatment. Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology and Endodontology. 2011. [ Links ]
10. Van Dam SD, Unni KK, Keller EE. Metastasizing (malignant) ameloblastoma: review of a unique histopathologic entity and report of Mayo Clinic experience. Oral Maxillofac Surg. 2010 Dec; 68:2962-74. [ Links ]
11. Fujita S, Anami M, Satoh N, Yamashita H, Asahina I, Ikeda T, Hayashi T. Cytopathologic features of secondary peripheral ameloblastic carcinoma: A case report. Diagnostic Cytopathology. 2011; 39:354-8. doi: 10.1002/dc.21427. [ Links ]
12. Medeiros G, Weege CF, Batista L, da Costa MC, Pereia L. Solid ameloblastomas. Retrospective clinical and histopathologic study of 54 cases. Braz J Otorhinolaryngol. 2010; 76:172-7. [ Links ]
13. Sukarawan W. WNT5A Expression in Ameloblastoma and Its Roles in Regulating Enamel Epithelium Tumorigenic Behaviors. Am J Pathol. 2010; 176-80. [ Links ]
14. Carlson ER, Marx RE. The ameloblastoma: primary, curative surgical management. J Oral Maxillofac Surg. 2006; 64:484-94. [ Links ]
15. Müller H, Slootweg PJ. The ameloblastoma, the controversial approach to therapy. J Surg Maxillofac. 1985; 13:79-84. [ Links ]
16. Nakamura N, Higuchi Y, Mitsuyasu T, Sandra F, Ohishi M. Comparison of long-term results between different approaches to ameloblastoma. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2002; 93:13-20. [ Links ]
17. Bachmann AM, Ronald LL. Ameloblastoma, Solid/Mulicystic type. Head Neck Pathol. 2009; 3:307-9. [ Links ]
18. Kessler HP. Intraosseous ameloblastoma. Oral Maxillofacial Surg Clin N Am. 2004; 16:309-22. [ Links ]
19. Slootweg PJ. Odontogenic tumours - An update. Current Diagnostic Pathology. 2006; 21:54-65. [ Links ]
20. Reichart PA, Philipsen HP, Sonner S. Ameloblastoma: biological profile of 3677 cases. Eur J Cancer Oral Oncol. 1995; 31B:86-99. [ Links ]
21. Philipsen HP, Reichart PA. Unicystic ameloblastoma. A review of 193 cases from the literature. Oral Oncology. 1998; 34:317-25. [ Links ]
22. Ackermann GL, Altini M, Shear M. The unicystic ameloblastoma: a clinicopathologic study of 57 cases. Journal of Oral Pathology. 1988; 17:541-6. [ Links ]
23. Bisinelli JC, Ioshii S, Retamoso LB, Moysés ST, Moysés SJ, Tanaka OM. Conservative treatment of unicystic ameloblastoma. Am J Orthod Dentofacial Orthop. 2010; 137:396-400. [ Links ]
24. Li B, Long X, Wang S, Cheng Y, Chen X. Clinical and radiologic features of desmoplastic ameloblastoma. J Oral Maxillofac Surg. 2011;69:2173-85. [ Links ]
25. Ord RA, Blanchaert RH, Nikitakis NG, Sauk JJ. Ameloblastoma in children. J Oral Maxillofac Surg. 2002; 60:762-70. [ Links ]
26. Escande C, Chaine A, Menard P, Ernenwein D, Ghoul S, Bouattour A, Berdal A, Bertrand JC, Ruhin-Poncet B. A treatment algorithm for adult ameloblastomas according to the Pitié-Salpêtrière Hospital experience. J Craniomaxillofac Surg. 2009; 37:363-9. Epub 2009 Jun 25. [ Links ]
27. Sachs SA. Surgical excision with peripheral ostectomy: A definitive, yet conservative, approach to the surgical management of ameloblastoma. J Oral Maxillofac Surg. 2006; 64:476-83. [ Links ]
28. Sampson DE, Pogrel MA. Management of mandibular ameloblastoma: the clinical basis for a treatment algorithm. J Oral Maxillofac Surg. 1999; 57:1074-7. discussion 1078-9. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico: adaiavalls@gmail.com
(A. Valls)
Recibido 15 Noviembre 2011
Aceptado 8 Febrero 2012