Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO  Similares en Google
Similares en Google
Compartir
Anales del Sistema Sanitario de Navarra
versión impresa ISSN 1137-6627
Anales Sis San Navarra vol.26 supl.3 Pamplona 2003
Clasificación de la osteoporosis. Factores de riesgo. Clínica y diagnóstico diferencial
Classification of osteoporosis. Risk factors. Clinical manifestations and differential diagnosis
M.T. Hermoso de Mendoza
| RESUMEN El hecho de que existan múltiples factores que pueden intervenir en la etiopatogenia de la OP, y el de su poca expresividad clínica hasta que no se producen las complicaciones –las fracturas– plantea un problema práctico en la consulta diaria a la hora de identificar a las personas con riesgo de padecer OP y a la hora de concretar nuestra actuación. Estos aspectos, junto con las dificultades para el acceso desde la atención primaria a una prueba complementaria que confirme el diagnóstico así como la sobrecarga de tareas en nuestra consulta hace que muchas veces pase desapercibida esta enfermedad. De modo que, en el apartado de orientación diagnóstica de la OP tratamos de clarificar y cohesionar este abordaje, dando unas líneas guía muy útiles para sospechar la enfermedad y unas pautas de actuación que van a permitir centrar el diagnóstico de una forma eficaz y certera. Palabras clave. Osteoporosis. Epidemiología. Factores de riesgo. Fracturas. Diagnóstico. | ABSTRACT The fact that there are multiple factors that can intervene in the ethiopathology of osteoporosis, together with its scarce clinical expression until complications –fractures– are produced, poses a practical problem in medical practice when it comes to identifying those persons at risk of osteoporosis. These aspects, together with the difficulties in obtaining access to a complementary test that would confirm the diagnosis and the overload of tasks in our clinic, mean that the disease often passes unnoticed. Hence, in the section on diagnostic orientation of osteoporosis we attempt to clarify and give cohesion to this approach, offering highly useful guidelines for suspecting the presence of the disease and patterns of action that will make it possible to diagnose in a more efficient and accurate way. Key words. Osteoporosis. Epidemiology. Risk factors. Fractures. Diagnosis. |
| Medico de Familia. Atención Primaria. C.S. Azpilagaña. Pamplona | Correspondencia: M.T. Hermoso de Mendoza Macua Centro de Salud Azpilagaña C/ Luis Morondo, 1 31006 Pamplona Tfno. 948 290480 Fax 948 290477 E-mail: mhermosm@cfnavarra.es |
DEFINICIÓN
La osteoporosis (OP) se define como una enfermedad generalizada del sistema esquelético caracterizada por la pérdida de masa ósea y por el deterioro de la microarquitectura del tejido óseo, que compromete la resistencia ósea y que condiciona como consecuencia una mayor fragilidad ósea y una mayor susceptibilidad a las fracturas1. Es una definición propuesta por el National Institute of Health (NIH) que, actualiza a la previamente establecida por consenso en 1993 en Hong-Kong2.
Cuando la masa ósea del adulto alcanza su valor máximo aproximadamente a los 35 años, la tasa de síntesis y de reabsorción ósea es equivalente. Este equilibrio normal entre la síntesis y reabsorción ósea mantiene constante la masa esquelética. A partir de los 40 años se observa una lenta reducción de la densidad de masa ósea en ambos sexos (aproximadamente 0,3-0,5% al año). Se desconocen las razones por las que se produce esta pérdida ósea con la edad, y por qué se inicia a una edad más temprana en las mujeres y sigue un curso más acelerado incluso antes de la menopausia. Sin embargo, un individuo que no alcance un pico de masa ósea óptimo durante la infancia y adolescencia puede padecer osteoporosis sin que se produzca una pérdida acelerada de masa ósea3.
La definición de OP del NIH integra dos características: la cantidad de masa ósea (componente cuantitativo) y el concepto resistencia-fragilidad ósea (componente cualitativo).
La densidad de masa ósea (DMO) se expresa en gramos de mineral por unidad de superficie (cm2). La DMO puede estimarse por una amplia variedad de técnicas4,5 entre las que se considera a la DEXA como patrón oro6.
La calidad ósea se refiere a la microarquitectura del tejido óseo que, sólo es posible objetivar mediante técnicas cruentas como la biopsia ósea lo cual, no es aplicable a la práctica clínica. Es por este motivo y por el hecho de que la DMO representa un 70% de la resistencia del hueso por lo que, en la práctica habitual aunque no sea del todo correcto, tendemos a equiparar la resistencia ósea con la DMO puesto que la disminución de la misma se asocia fuertemente a la aparición de fracturas3,7. Pero también radica en este aspecto la explicación de las diferencias en la incidencia de fracturas en pacientes con la misma DMO.
De todo lo anterior se deduce una importante limitación práctica, tanto para diagnosticar la OP, como para estimar adecuadamente el riesgo de que se complique con fracturas.
En 1994, la OMS estableció las categorías o criterios diagnósticos de la OP sobre la base de criterios epidemiológicos que tienen en cuenta la evolución de los valores de la masa ósea con la edad (evaluados con densitometría ósea como densidad mineral ósea) y la prevalencia e incidencia de las fracturas osteoporóticas en mujeres posmenopáusicas de raza blanca8. Así, se definen cuatro categorías:
– Normal: cuando la DMO es superior a –1 DE en la escala T.
– Osteopenia: cuando la DMO se sitúa entre –1 y –2,5 DE en la escala T.
– Osteoporosis: cuando la DMO es inferior a –2,5 DE en la escala T.
– Osteoporosis grave o establecida: cuando al criterio de osteoporosis se añade la presencia de fracturas.
La escala T toma como referencia la DMO de la población joven cuando se alcanza el pico máximo de masa ósea.
La puntuación en la escala Z relaciona los valores de DMO del sujeto con los correspondientes a su mismo grupo de edad y sexo. El valor Z cobra un especial interés a la hora de establecer criterios terapéuticos, sobre todo en edades avanzadas.
Hasta la fecha, esta clasificación densitométrica se considera universalmente aceptada como criterio diagnóstico, a pesar de que es una clasificación que plantea varias limitaciones (de manera estricta, sólo es adecuada para mujeres postmenopáusicas de raza blanca; no tiene en cuenta el componente cualitativo del hueso; su aplicación principal es en columna vertebral y cadera y pueden existir interferencias en la medición por patología degenerativa o calcificaciones paravertebrales9,10). Es muy probable que en un plazo no muy lejano asistamos a un cambio de esta definición.
EPIDEMIOLOGÍA
La OP es la enfermedad metabólica ósea más frecuente; sin embargo, su prevalencia real es difícil de establecer, ya que es una enfermedad asintomática hasta la aparición de complicaciones, lo que hace difícil la identificación de las personas que padecen la enfermedad. Habitualmente se usan indicadores indirectos, como son las fracturas osteoporóticas, para aproximarnos a la prevalencia de la OP11.
Según criterios de la Organización Mundial de la Salud (OMS), la prevalencia se estima en un 30% de las mujeres caucásicas y en un 8% de los varones caucásicos mayores de 50 años, y asciende hasta un 50% en mujeres de más de 70 años.
En el estudio de prevalencia densitométrica (DEXA) de OP en la población femenina española publicado por Díaz-Curiel y col12 se presentan las siguientes cifras: de 50 a 59 años un 9% OP lumbar y 1% de OP femoral; de 60 a 69 años un 24% OP lumbar y 5,7% de OP femoral; de 70 a 79 años un 40% OP lumbar y un 24% OP femoral.
Las cifras presentadas por los mismos autores para los varones de 70-79 años son de 11,3% en columna lumbar y de 2,6% en cadera13.
La incidencia de OP es mayor en las mujeres que en los varones, debido a que en los varones la masa ósea es mayor, a la ausencia de un equivalente de la menopausia, a una menor tendencia a caerse y a una esperanza de vida más corta. En consonancia con este hecho, la incidencia global de fracturas osteoporóticas es mucho mayor en las mujeres que en los varones, y esta diferencia se hace especialmente llamativa en el caso de las fracturas de hueso trabecular. La mujer presenta fracturas de hueso trabecular en una proporción 8/1 respecto al varón, frente a las fracturas de hueso cortical donde la proporción se reduce 2/1 también a favor de la mujer. En los primeros 4-8 años tras la menopausia se producen con más frecuencia las fracturas vertebrales y de radio (Colles). Posteriormente, hacia los 70-75 años aparecen las fracturas de cadera que se relacionan más con la pérdida de hueso cortical y con otros factores que predisponen a las caídas14,15.
Debido fundamentalmente a que la DMO disminuye con la edad, la incidencia de fracturas aumenta exponencialmente y llega a ser un problema alarmante en la población senil, un sector demográfico con clara tendencia ascendente. En España, se estima, que la OP afecta actualmente a 3,5 millones de personas y cada año se producen más de 100.000 fracturas osteoporóticas. Constituye pues, un problema de salud pública de gran magnitud por su prevalencia, por la morbimortalidad que ocasiona y por el consumo de recursos sanitarios que conlleva16,17.
CLASIFICACIÓN DE LA OSTEOPOROSIS
Osteoporosis primarias18,19
Constituye el grupo más amplio e incluye los casos de OP en los que no se identifica ninguna enfermedad que la justifique directamente. Se distinguen:
OP idiopática juvenil y OP del adulto joven
Afecta a niños o adultos jóvenes de ambos sexos con función gonadal normal.
La OP idiopática juvenil es un trastorno raro, que se inicia generalmente entre los 8 y los 14 años. Se manifiesta por la aparición brusca de dolor óseo y de fracturas con traumatismos mínimos. El trastorno remite por sí solo en muchos casos y la recuperación ocurre de forma espontánea en un plazo de 4 ó 5 años.
La OP idiopática del adulto joven se observa en varones jóvenes y mujeres premenopáusicas en las que no se objetiva ningún factor etiológico. El comienzo del trastorno en algunas mujeres aparece con el embarazo o poco después. Estas mujeres presentan disminuciones de la DMO del hueso trabecular que puede permanecer baja durante muchos años. Los estrógenos no son eficaces en este tipo de OP. La evolución es variable y a pesar de que los episodios de fracturas recidivantes son característicos, no se produce un deterioro progresivo en todos los enfermos.
Osteoporosis postmenopáusica. Tipo I
Ocurre en un subgrupo de mujeres posmenopáusicas de 51 a 75 años y se caracteriza por una pérdida acelerada y desproporcionada de hueso trabecular (alta remodelación ósea). Las fracturas de los cuerpos vertebrales y de la porción distal del radio son complicaciones frecuentes. Se observa disminución de la actividad PTH para compensar el aumento de la reabsorción ósea. El tratamiento antirreabsortivo es eficaz para frenar la pérdida ósea.
Osteoporosis senil. Tipo II
Se detecta en algunas mujeres y varones de más de 70 años como consecuencia de un déficit de la función de los osteoblastos (bajo remodelado óseo). Otros factores etiopatogénicos son: sedentarismo-inmovilización, peor absorción intestinal de calcio, menor insolación y trastornos nutricionales que ocasionan déficit de vitamina D e hiperparatiroidismo secundario. Se asocia con fracturas de cuello femoral, porción proximal del humero y pelvis, por afectarse tanto el hueso cortical como el trabecular. El tratamiento antirreabsortivo es menos eficaz en este tipo de OP, tal y como cabe esperar por su mecanismo patogénico.
Osteoporosis secundarias
Se clasifican en este grupo todos aquellos casos de OP que son una consecuencia o bien una manifestación acompañante de otras enfermedades o de su tratamiento. La mayoría de estas causas se recogen en la tabla 1 y como puede apreciarse son numerosas y muy diversas. Algunas de ellas se tratan en el capítulo correspondiente a este tema. La importancia de identificarlas adecuadamente radica en que esto nos permite llevar a cabo una terapia etiológica. Además, estas entidades patológicas, por lo tanto, hemos de tenerlas en cuenta como factores de riesgo de OP.
FACTORES DE RIESGO DE OSTEOPOROSIS
Por medio de estudios epidemiológicos se han identificado múltiples marcadores y factores de riesgo que conllevan una mayor probabilidad de desarrollar OP3, 18. Tienen baja sensibilidad y baja especificidad pero han de ser tenidos en cuenta para poder abordar adecuadamente la prevención, el diagnóstico y el tratamiento de la OP15,20. Diversos autores han intentado desarrollar métodos para identificar los factores de riesgo de baja masa ósea y medir el carácter predictivo de OP de cada factor para facilitar la sospecha diagnóstica de esta enfermedad. Sin embargo, no disponemos de ningún cuestionario validado para uso clínico. Aunque sabemos que los factores con mayor peso específico son: más de 10 años de menopausia, antecedente de fractura previa, historia familiar de OP y la edad. Una relación exhaustiva de estos factores de riesgo se recogen en la tabla 215
Menopausia
Supone la condición de riesgo más importante para esta enfermedad21. En el mundo occidental se mantiene la edad media de presentación de la menopausia a los 49 años mientras que, la esperanza de vida ha aumentado hasta superar los 80 años. Esto condiciona que la mujer pase más de la tercera parte de su vida en menopausia. Circunstancia que justifica que la prevalencia de la OP haya aumentado de forma notable en los últimos años. La deprivación estrogénica supone una falta de freno a la acción de los osteoclastos y esto conlleva una pérdida acelerada y desproporcionada de hueso trabecular (alto remodelado óseo). Esta acción, junto con el hecho de que el pico de masa ósea en la mujer es más precoz y de menor cuantía que en el varón justifica, en gran medida, que la OP sea mucho más frecuente en el sexo femenino. El riesgo es mayor cuanto más precoz es la edad de la menopausia, y mucho más intenso cuando la deprivación hormonal es brusca, como ocurre en la menopausia quirúrgica.
Edad
Es un factor de riesgo independiente para desarrollar una OP, pero está intensamente relacionado con la menopausia en la mujer. En el hombre la edad es un factor de riesgo más específico y de hecho, en edades por encima de los 75 años tiende a igualarse la proporción mujer/hombre con OP que pasa a ser de 2:1 cuando, en edades más jóvenes esta proporción es de 8/122. Con la edad se producen múltiples condicionantes fisiopatológicos: menor actividad osteoblástica ósea, menor absorción intestinal de calcio, defectos nutricionales, carencia de vitamina D, baja exposición solar y sedentarismo entre otros. Además, la edad no sólo influye a través del descenso fisiológico del capital óseo a partir del pico de masa ósea juvenil sino que, es un factor de riesgo independiente de la masa ósea para que se produzcan fracturas.
Genética
Aunque la OP es más frecuente en hijas de madres osteoporóticas, no se ha podido establecer un patrón de transmisión genética específico de la enfermedad. La influencia de la carga genética parece evidente en lo referente al pico de masa ósea alcanzado en las primeras décadas de la vida. Por el contrario, este factor parece menos importante en la pérdida de masa ósea a lo largo de la vida, donde los factores adquiridos tienen mucha más importancia, y esto es más marcado cuanta más edad tiene el paciente. De ahí, la importancia de controlar los hábitos de vida en la prevención de la enfermedad osteoporótica.
Masa corporal
Las pacientes con un IMC bajo (<19 Kg/m2) tienen menor DMO lo cual, parece estar en relación, por una parte, con un menor efecto osteoblástico debido a una menor carga mecánica sobre el hueso y por otra, con un menor freno de la actividad osteoclástica derivado de la menor producción de estrona por falta de panículo adiposo.
Estilos de vida
Es fundamental para conservar la masa ósea. Engloba aspectos que tienen que ver con la dieta, los hábitos tóxicos y la actividad física. Son factores que influyen con poco peso específico cada uno, pero de forma persistente a lo largo de la vida y potenciándose entre sí.
Ingesta de calcio
La ingesta de calcio en la dieta es necesaria para un metabolismo óseo normal. Durante la etapa de desarrollo del esqueleto condiciona el pico máximo de masa ósea. El adulto sano con ingesta inadecuada de calcio tiene incrementada la pérdida de masa ósea. Los estudios poblacionales han demostrado menor número de fracturas en áreas geográficas con mayor ingesta de calcio. La ingesta recomendada de calcio depende de la edad y circunstancia individual (embarazo, lactancia, crecimiento, menopausia, etc.) pero oscila alrededor de 1.000 -1.200 mg /día (Tabla 3).
Es importante, indagar a la paciente sobre la ingesta de calcio diaria, para lo cual podemos ayudarnos de una encuesta alimentaria de calcio (Tabla 4).
Conviene sensibilizar y facilitar información a la población sobre las repercusiones para la salud ósea de un aporte adecuado de calcio en la dieta, ya desde la infancia (Tabla 5). Está indicado recomendar suplementos farmacológicos sólo si existen deficiencias dietéticas.
Vitamina D
Junto con la PTH, la vitamina D es uno de los factores más importantes en la homeostasis fosfo-cálcica. Las necesidades de vitamina D están entre 400-800 U.I. diarias. En nuestro medio, una dieta variada y una exposición moderada a la luz solar es suficiente. Sólo es necesario suplementarla en situaciones deficitarias: algunos ancianos asilados, latitudes con poca incidencia de luz solar, cuadros de malabsorción de grasa.
Tanto las dietas hiperproteicas como las dietas vegetarianas muy estrictas se asocian a osteopenia.
Tabaco
Diversos estudios epidemiológicos han objetivado una relación entre el consumo de cigarrillos y una menor DMO, una mayor incidencia de fractura vertebral y de cadera, además de ser más recurrentes y precisar más tiempo para su curación. Se habla de un efecto tóxico directo del tabaco, disminuyendo la actividad osteoblástica del hueso. También sabemos que el tabaco disminuye la absorción intestinal de calcio. Pero el mecanismo etiopatogénico más importante es consecuencia de su efecto antiestrogénico. Sin embargo, también hay estudios que sugieren que la asociación entre el consumo de cigarrillos y los trastornos del metabolismo óseo son falsas, y que las diferencias que se observan son debidas a los distintos factores demográficos y de estilos de vida entre fumadoras y no fumadoras (las mujeres fumadoras son más delgadas, más sedentarias, consumen más alcohol y, tienen la menopausia más precoz que las no fumadoras). Deberían hacerse más estudios para investigar los efectos del tabaco sobre el hueso, controlando todos esos factores de confusión.
Alcohol
Es el tóxico más perjudicial. El consumo crónico de alcohol tiene efecto directo depresor sobre la actividad del osteoblasto y se asocia con alteraciones del metabolismo mineral óseo del calcio, fósforo y magnesio; altera el metabolismo de la vitamina D; provoca alteraciones endocrinas y nutricionales. Todo lo cual, aboca al paciente a una situación de OP que, junto con una mayor frecuencia de caídas, condiciona un incremento importante en el riesgo de fracturas.
Ejercicio físico
Tiene un papel importante para el crecimiento y la remodelación del hueso a lo que también contribuye la presión y tensión muscular. El hábito sedentario y todas las situaciones que conllevan inmovilización, suponen la ausencia de estos estímulos y condicionan la posibilidad de desarrollar o agravar una OP.
CLÍNICA DE LA OSTEOPOROSIS
La OP es un trastorno generalizado del esqueleto que por sí mismo no produce síntomas y que, puede ofrecer una exploración física rigurosamente normal. Las manifestaciones clínicas de la OP se asocian exclusivamente a la presencia de fracturas osteoporóticas.
Las fracturas osteoporóticas pueden producirse en cualquier localización, y es característico que surjan de forma espontánea o por un traumatismo mínimo. Cualquier fractura por fragilidad puede considerarse osteoporótica15. A mayor descenso de la DMO, mayor riesgo de fractura (por cada -1 DE de la T score, se multiplica por 2 el riesgo de fractura)7, si bien existen otros factores, además de la DMO, que condicionan la aparición de fracturas. De hecho, un porcentaje no despreciable de fracturas se producen en enfermas osteopénicas.
La fractura vertebral y de la extremidad distal de radio (Colles), debidas a una pérdida preferente de hueso trabecular, son localizaciones típicas de la OP tipo I y, su incidencia empieza a ser relevante entre los 55-65 años, es decir, de 20 a 30 años antes de alcanzarse la expectativa media de supervivencia18.
La fractura del cuello del fémur es característica de la OP tipo II o senil que incide en edades avanzadas, hacia los 70-75 años y se relaciona más con la pérdida de cortical ósea y con factores que facilitan las caídas18.
Las fracturas osteoporóticas pueden motivar una clínica aguda en forma de impotencia funcional y de dolor severo incapacitante o ser asintomáticas. Pueden cursar sin complicaciones y tener una recuperación completa, o bien, condicionar consecuencias a corto y medio plazo: dolor crónico sordo y persistente que se agrava con el movimiento; callos de fractura hipertróficos; deformidades en los huesos largos por mala alineación; deformidades y cambios en la actitud postural que suponen, desde sólo una pequeña disminución de la talla al colapso total de la columna vertebral; repercusiones viscerales (insuficiencia respiratoria restrictiva); incapacidad que variará desde la necesidad de usar un bastón hasta el encamamiento; necesidad de cuidados a domicilio; dependencia para todas las actividades básicas de la vida diaria; consecuencias psicológicas y finalmente la muerte, relacionada sobre todo con la fractura de cadera19.
El riesgo de padecer una fractura de cadera en una mujer a partir de los 50 años es de 15,6% lo cual, supone la mitad de riesgo de sufrir una fractura vertebral (32%). Y en los varones es la mitad de frecuente que en las mujeres. Sin embargo, la fractura de la extremidad proximal del fémur es la más grave puesto que, condiciona una importante morbilidad, mortalidad, consumo de recursos sanitarios y costes indirectos. A partir de los 50 años la incidencia de tales fracturas aumenta de forma exponencial; en conjunto, se calcula que es de 1,3 a 1,9 por 1.000 habitantes (30.000 fracturas de cadera al año en España), siendo la edad media de los pacientes, en la mayoría de los estudios, alrededor de los 80 años22-24. Es una incidencia media, similar a la de otros países mediterráneos e inferior a la de países del Norte de Europa. Se manifiesta de forma brusca con dolor e incapacidad del miembro inferior, generalmente, después de una caída desde la posición de pie. Siempre requiere ingreso hospitalario lo que hace que se encuentre mejor documentada que las otras fracturas osteoporóticas24. Tiene unos elevados índices de mortalidad en la fase aguda, entre 5-8%, habitualmente por complicaciones cardiovasculares y cardiopulmonares. En casi la mitad de los intervenidos hay alguna complicación; las más frecuentes son infecciones del tracto urinario, neumonías, tromboembolismo pulmonar, falta de consolidación de las fracturas, necrosis avascular de la cadera, aflojamiento de la prótesis y úlceras por decúbito. La mortalidad en el primer año tras la fractura es de un 30%, unas 3 ó 4 veces superior que la que sería de esperar por el sexo y la edad. La tasa de mortalidad permanece alta durante varios años. Además de que la tercera parte de los pacientes fallece, de los supervivientes, más del 50% quedan con una incapacidad permanente y dependencia para las actividades cotidianas. Se han identificado como factores predictores de mortalidad en la fractura de cadera: la edad mayor de 85 años, comorbilidad y riesgo operatorio alto, la demencia y el sexo masculino25,26.
La fractura distal del radio con angulación dorsal (fractura de Colles) ocurre en el 15% de mujeres caucasianas de más de 50 años. Su incidencia aumenta rápidamente a partir de los primeros 5 años tras la menopausia y alcanza su pico máximo entre los 60 y los 70 años. Se produce al caer sobre la mano extendida, con la muñeca en cierto grado de flexión dorsal. Provoca dolor e impotencia funcional, y habitualmente requieren reducción e inmovilización durante 4 ó 6 semanas. Suele presentar como complicaciones una alta incidencia de algodistrofia refleja, deformidad y rigidez residual, síndrome del túnel carpiano y artrosis secundaria. La mortalidad no es mayor en este tipo de fracturas que en la población general, pero sí incrementa el riesgo de fractura de cadera24.
La fractura vertebral es la más frecuente de las fracturas osteoporóticas. La mayoría de las publicaciones hablan de que un 32% de las mujeres mayores de 50 años presentarán fracturas vertebrales osteoporóticas a lo largo de su vida. No es fácil estimar su prevalencia correctamente debido a que muchas pasan inadvertidas al ser oligosintomáticas, a que son atribuidas a otros procesos reumáticos y a los diferentes criterios empleados en su definición radiológica23.
En España, son escasos los estudios sobre prevalencia de fractura vertebral. Uno de los más importantes es el estudio European Vertebral Osteoporotic Study (EVOS) en el que participaron cuatro ciudades españolas (Oviedo, Barcelona, Las Palmas y Madrid). Los datos obtenidos ponían de manifiesto una gran variabilidad en la prevalencia de fractura vertebral, oscilando entre un 7,7 y un 26,6% según el método usado para definir la fractura vertebral27.
Las fracturas vertebrales, aunque menos aparatosas clínicamente, no deben infravalorarse, ya que tienen un importante impacto sobre la calidad de vida y ocasionan una morbi-mortalidad nada despreciable. Sufrir una fractura vertebral osteoporótica supone 5 veces más de riesgo de que dicha paciente presente otra nueva fractura vertebral a corto plazo (1 año) y, de 2 a 4 veces más de riesgo de que se produzca una fractura de cadera en el plazo de 4 años23,28,29.
El tramo vertebral característico que se afecta es entre la D4 y la L3 (con dos puntos de máxima incidencia D9 y D12-L1). Es fundamental la exploración radiológica en proyección lateral de la columna dorsal y lumbar para documentarlas puesto que, sigue siendo la radiología convencional la técnica de elección para su diagnóstico si bien, en ocasiones no es sencillo15,17. La fractura vertebral viene definida como la pérdida de al menos un 20% de la altura vertebral global o, en su porción anterior (lo más frecuente), media o posterior, con respecto a la vértebra adyacente. También se considera valorable si disminuye más de 4 mm la altura vertebral con respecto a los controles previos. La clasificación de Genant establece tres tipos de fracturas sobre la base de la porción afectada y tres grados de severidad en función de la pérdida de altura del cuerpo vertebral, realizando la medición en los cuerpos vertebrales de D4 a L530:
1. Tipos de fractura(anterior, central y posterior).
– Aplastamiento: disminución de la altura del cuerpo vertebral de manera global.
– Biconcavidad: disminución de la altura central.
– Acuñamiento anterior: disminución de la altura anterior. El acuñamiento posterior es mucho menos frecuente.
2. Grado de severidad. Grado I: 20%, Grado II: 20-40%, Grado III: >40%.
Además son características radiológicas muy sugestivas de fractura osteoporótica: la localización dorso lumbar, la afectación vertebral múltiple, la conservación de los espacios discales, el hundimiento de las plataformas con cierta disrupción de las mismas, que se centre en el cuerpo y respete los pedículos vertebrales y el arco posterior de tal manera que, son fracturas estables y no producen compresión medular ni síntomas neurológicos, y que no haya desplazamiento anterior/posterior de los fragmentos.
Con frecuencia, están presentes otros signos radiológicos de hipertransparencia ósea muy sugestivos de OP como son: reforzamiento de los platillos vertebrales, aparente reforzamiento de las trabéculas verticales como consecuencia de una reabsorción ósea preferencial de las trabéculas horizontales y, en ocasiones, aspecto de vértebra vacía. Todas estas características radiológicas, es importante tenerlas en cuenta cuando hagamos el diagnóstico diferencial con otras causas de deformidad vertebral31.
Hasta dos terceras partes de los casos de fractura vertebral son asintomáticas. Cuando es sintomática se manifiesta con un dolor agudo, intenso e incapacitante dorso-lumbar que, a veces, irradia por el flanco hacia la cara anterior del tórax-abdomen. Se presenta después de flexiones súbitas de la espalda, levantamiento de objetos, saltos aparentemente triviales o incluso sin ningún traumatismo ni sobreesfuerzo previo. El enfermo tiene gran limitación de la movilidad y gran dificultad para mantenerse en pie. Muchos pacientes son incapaces de mantener la sedestación en la fase aguda y el dolor se incrementa con los cambios posturales o las maniobras de Valsalba. Es excepcional la clínica neurológica secundaria a compresión medular19. Es frecuente el dolor con la palpación de las espinosas de las vértebras afectadas. Precisa reposo absoluto en cama unas 2-3 semanas y tratamiento analgésico potente. El dolor remite total o parcialmente de manera paulatina y la mayoría de los pacientes son capaces de deambular sin problemas y de asumir nuevamente las actividades cotidianas al cabo de 6 semanas.
En ocasiones el enfermo no presenta manifestaciones en forma de episodios agudos de dolor e impotencia funcional sino que aqueja dolor sordo, persistente, que se agrava con maniobras de tipo mecánico al levantarse o moverse bruscamente.
Son frecuentes los episodios recidivantes de acuñamiento vertebral sobre todo en la región central de la columna dorsal, que justifican las consecuencias más llamativas de las fracturas vertebrales. Contribuyen a la disminución de la talla, a alterar la estática de la columna vertebral y a conformar una actitud postural característica: cifosis dorsal marcada e hiperextensión cervical dolorosa, rectificación de la lordosis lumbar, disminución del espacio costo-iliaco y protrusión abdominal. Todo esto conlleva una disminución de la capacidad de la caja torácica y secundariamente una alteración funcional respiratoria restrictiva32. En ocasiones, persiste un dolor ligero que quizá no sea de origen óseo sino que esté relacionado con la sobrecarga o distensión a que están sometidos los ligamentos, discos o articulaciones interapofisarias, consecutivas a la alteración estática o funcional que sufre una columna en que se han producido una o varias fracturas16.
DIAGNÓSTICO DIFERENCIAL DE LA FRACTURA VERTEBRAL
En el contexto de esta circunstancia clínica es inexcusable realizar el diagnóstico diferencial de la osteoporosis con otras entidades patológicas frecuentes o graves que pueden manifestarse con deformidades vertebrales o fracturas patológicas15,18,19. Para ello es necesario, además de las pruebas de imagen, realizar una historia clínica completa y determinaciones analíticas más o menos exhaustivas según nuestra sospecha etiológica. De entrada, no debe faltar el hemograma con VSG, calcio, fósforo, fosfatasa alcalina, proteinograma, creatinina, transaminasas, glucemia y calciuria de 24 horas.
Es necesario hacer diagnóstico diferencial con las siguientes entidades patológicos:
– Osteoporosis.
– Deformidades fisiológicas. En la columna dorsal media puede ser fisiológica una altura anterior de la vértebra de hasta un 15% inferior a la altura posterior o, viceversa en las ultimas vértebras lumbares. Una diferencia de altura entre la longitud anterior y posterior de un cuerpo vertebral dorsal superior a 4 mm, debe ser considerada como indicativa de una auténtica compresión vertebral.
– Epifisitis Juvenil Idiopática o Cifosis del Adolescente (enfermedad de Scheüerman). Aparece en un 4-8% de la población, entre los 13 y los 17 años de edad. Desde el punto de vista clínico puede ser asintomática o producir una sintomatología más o menos intensa en la columna dorsal media-baja con dolor espinal, postura defectuosa y cifosis (con o sin escoliosis). La radiografía puede mostrar una imagen de aplastamiento cuneiforme de varias vértebras dorsales contiguas, responsable de la cifosis. Se aprecian irregularidades de aspecto ondulante en los contornos de las plataformas vertebrales. Es característico observar nódulos cartilaginosos de Schomrl (herniaciones de material discal) como áreas radiotransparentes dentro del cuerpo vertebral. Normalidad analítica. El conjunto de todo el cuadro clínico debe orientar fácilmente al diagnóstico.
– Neoplasias benignas: hemangioma, granuloma eosinófilo. Normalidad analítica. Requieren estudios de imagen más exhaustivos que completen la radiología.
– Neoplasia maligna metastásica: pulmón, mama, próstata, riñón, de origen digestivo, leucemias y linfomas. Cuando afecta a las vértebras es característico encontrar signos radiológicos muy diferentes a los que muestra la OP con desestructuración del cuerpo vertebral, aplastamiento vertebral en cuña posterior de forma característica, afectación de los pedículos y arco posterior de la vértebra tanto en su morfología como en su densidad, mala definición de los platillos vertebrales y afectación vertebral cervical o por encima del nivel D5 o compromiso aislado de L5. En ocasiones, producen una pérdida difusa de hueso, especialmente hueso trabecular de la columna vertebral.
Clínicamente suele expresarse con dolor de espalda de ritmo inflamatorio, intenso y progresivo, que con frecuencia asocia sintomatología neurológica, en el contexto de un síndrome general más o menos manifiesto. En la analítica encontramos, de forma casi constante, anemia, VSG elevada y en ocasiones hipercalcemia. Es necesario completar el estudio con otras pruebas complementarias para confirmar la sospecha diagnóstica.
– Mieloma múltiple. Además de provocar fracturas vertebrales puede afectar al sistema esquelético produciendo una osteoporosis difusa y lesiones osteolíticas parcheadas en huesos hematopoyéticos (cráneo, costillas, vértebras, pelvis y epífisis de huesos largos). El dolor óseo (por osteolisis) es el síntoma más frecuente. La anemia normocítica y normocrómica, la elevación importante de la velocidad de sedimentación, la hipercalcemia y la paraproteinemia monoclonal son alteraciones asociadas casi de manera constante.
– Espondilodiscitis sépticas. Esta patología se localiza sobre todo al nivel de la columna lumbar y en ocasiones a nivel dorsal. Principalmente afecta al cuerpo vertebral con compromiso de los discos intervertebrales. A veces, tampoco respeta los pedículos y el arco posterior aunque, su afectación es mucho más rara. El proceso comienza en un foco de hueso subcondral del cuerpo vertebral y al progresar perfora la superficie vertebral y alcanza el disco intervertrebral. Suele existir historia previa de una infección primaria urinaria, respiratoria o cutánea, o de una instrumentación invasiva diagnóstica o terapéutica. El germen más frecuente es el Estafilococcus aureus. Algunas veces es por tuberculosis o brucelosis. Se debe sospechar esta entidad ante un dolor espinal grave asociado a un síndrome constitucional.
Radiológicamente se aprecian imágenes erosivas en el cuerpo vertebral y, en ocasiones, aplastamiento del cuerpo vertebral y pinzamiento discal si bien, son hallazgos tardíos. La gammagrafía con galio o la RNM son más sensibles para detectar el proceso en fases más tempranas.
– Fracturas traumáticas. Un traumatismo muy intenso justifica una fractura de hueso vertebral sano.
– Osteomalacia. Puede simular o asociarse a la OP. Se presenta en el adulto de forma insidiosa. Cuando aparecen síntomas consisten en dolor óseo difuso espontáneo y a la palpación y en una debilidad muscular proximal, a veces severa, que incapacita al paciente. Las fracturas óseas aparecen con microtraumatismos y los aplastamientos vertebrales (vértebras bicóncavas) reducen la talla del paciente.
La disminución de la DMO se acompaña de una pérdida de trabéculas y de un adelgazamiento de la cortical. El aspecto de las vértebras da una imagen de borrosidad como de vidrio esmerilado, a diferencia del enmarcado vertebral de la OP. El aplastamiento vertebral suele ser bicóncavo. El dato radiológico específico que sugiere osteomalacia es la presencia de pseudofracturas de Looser en escápula, pelvis, fémur y peroné. Estos hallazgos junto con un nivel bajo o indetectable de vitamina D [25(OH)D] sugieren el diagnóstico. Cuando se sospecha, está justificado hacer este tipo de determinaciones analíticas para detectarla, puesto que responde al tratamiento mucho mejor que la OP. El calcio y fósforo están bajos con elevación de la fosfatasa alcalina.
– Enfermedad de Paget del hueso. Es un proceso casi siempre localizado, que se caracteriza por una remodelación ósea excesiva y una formación desordenada de nuevo hueso. Habitualmente se localiza en la pelvis, el fémur, el cráneo, la tibia, la columna lumbosacra, la columna dorsal, la clavícula y/o las costillas. La enfermedad a menudo es asintomática y se sospecha a partir de la imagen de una radiografía o por una concentración elevada de fosfatasa alcalina detectada en un análisis rutinario. Cuando es sintomática se expresa de forma variada, según el hueso afectado, con dolor sordo y deformidad. Los hallazgos radiológicos reflejan la fase lítica-blástica predominante de la enfermedad. A nivel vertebral da imagen de vértebra enmarcada, con aumento de volumen, que hace que sobresalga de las inmediatas vecinas. En su interior se aprecia el desorden arquitectónico típico de esta osteítis deformante. Las fracturas vertebrales patológicas que puede producir con frecuencia tienen aspecto de vértebra bicóncava y, en ocasiones, asocian síntomas neurológicos.
– Hiperparatiroidismo primario. Es un trastorno generalizado del metabolismo del calcio, de los fosfatos y del hueso debido a un exceso de secreción de hormona paratiroidea (PTH). La prevalencia estimada es del 1% de la población general. Habitualmente se sospecha en pacientes asintomáticos a partir de una hipercalcemia detectada en un análisis rutinario. Se diagnostica mediante la cuantificación de PTH, a la vez que descartamos otros procesos responsables de elevaciones marcadas del calcio (neoplasias entre otros). Fosforemia baja. La manifestación ósea singular del hiperparatiroidismo es la osteítis fibrosa quística, consecuencia de la reabsorción subperiostica de la cortical de los huesos de las manos. Y la imagen del cráneo en sal y pimienta por lesiones líticas en sacabocados. El recambio mineral óseo es elevado en casi todos los pacientes, y la pérdida progresiva de masa ósea (sobre todo cortical) acaba produciendo osteopenia. No hay criterios que permitan distinguir la osteopenia dependiente del hiperpartiroidismo, de la OP de alto recambio de los pacientes sin hiperparatiroidismo. Constituye pues, una causa de OP secundaria. Se acepta que los pacientes hiperparatiroideos tienen incrementado el riesgo de fractura vertebral y de cadera entre otras.
Algunas veces, podemos encontrar deformidades vertebrales en forma de vértebras bicóncavas similares a las que aparecen en la OP, osteomalacia, enfermedad de Paget y en las neoplasias. En todas estas enfermedades existe una debilidad generalizada del hueso, y la vértebra debilitada se deforma como consecuencia de la presión expansiva ejercida por el disco intervertebral.
Es necesario distinguir dos situaciones clínicas: la fractura vertebral como hallazgo casual (Fig. 1) y la fractura vertebral como episodio agudo (Fig. 2).
SOSPECHA Y ORIENTACIÓN DIAGNÓSTICA DE LA OP
Es importante tener presente el esquema adjunto (Fig. 3) como una manera de englobar de forma resumida el contenido de este capítulo y la estrategia a seguir en la consulta
Etapa I. Sospecha de osteoporosis
En la práctica clínica diaria disponemos de una serie de puntos guía que, cuando están presentes, sirven de puntos de partida y anclaje de nuestra sospecha de que el paciente que tenemos delante padece una osteoporosis o tiene riesgo alto de padecerla. Básicamente los podemos agrupar en tres bloques que, ya han sido descritos de manera más exhaustiva al inicio del capítulo:
– Existencia de factores de riesgo clínicos de OP. Dado que estos factores de riesgo tienen baja sensibilidad y baja especificidad, no son por sí solos un criterio diagnóstico de OP, pero su asociación con esta enfermedad hace que sea inexcusable su valoración33. En la anamnesis, hemos de indagar de forma prioritaria aquellos factores con mayor peso relativo de riesgo de OP (Tabla 2).
– Presencia de manifestaciones clínicas producidas por las fracturas osteoporóticas y sus consecuencias.
– Hallazgos radiológicos sugestivos de OP: la radiología, también es muy poco sensible y muy poco específica para diagnosticar una OP. Es necesario que exista al menos un 30% de pérdida de la DMO para que pueda ser apreciable con la exploración radiológica. Y a la inversa, no siempre que la imagen radiográfica aparenta baja DMO se confirma en la densitometría puesto que, es muy frecuente, que se artefacte por la superposición de partes blandas, por la obesidad, por la penetración del rayo, por la calidad de la placa, por la técnica del revelado. Sin embargo, con frecuencia, encontramos múltiples signos radiológicos sugestivos de OP que son un complemento importante a la hora de sospechar el diagnóstico de OP, sobre todo ante la presencia de fracturas vertebrales.
Ante cualquiera de estas circunstancias tenemos que pensar en el diagnóstico de OP. Se trata de obordar el manejo de la OP desde una estrategia de cribado mediante la detección oportunista (case-finding) de individuos con mayor riesgo de padecer una OP, aprovechando las visitas a la consulta por otros motivos de salud15,33. A partir de aquí, hemos de completar el estudio realizando una anamnesis y exploración física completas, analítica, radiología y densitometría ósea. Con todo ello estaremos en condiciones de confirmar el diagnóstico, grado y tipo de OP; realizar el diagnóstico diferencial con otras patologías; aproximar el riesgo de fractura y plantear el tratamiento adecuado15,34,35.
Etapa II. Estudios complementarios (Tabla 6)15,34
Anamnesis
La anamnesis aporta una información de extraordinario valor para sospechar el diagnóstico y además, con gran trascendencia en el tratamiento. En primer lugar deben recogerse los factores de riesgo que pueden afectar a la masa ósea, para procurar modificar los modificables y, ponderar la presencia de los no modificables a la hora de establecer la estrategia terapéutica (Tabla 2).
La historia clínica, además, aporta información trascendental para pensar en una OP secundaria (Tabla 1), y para realizar un diagnóstico diferencial adecuado con otras patologías. Debemos indagar para poder identificar una serie de condicionantes clínicos que, pueden tener importancia a la hora de establecer la indicación terapéutica, bien porque son susceptibles de ser mejorados, bien porque pueden ser condicionantes de intolerancia o por la aparición de efectos secundarios adversos con algunos de los tratamientos farmacológicos posibles. Entre otros están: insuficiencia venosa crónica, enfermedad tromboembólica, clínica de menopausia, mastopatía, riesgo de neoplasia de mama y/o útero, problemas digestivos (hernia de hiato, ERGE, esofagitis, ulcus, etc.), hepatopatía, nefropatía crónica, hipercalcemia, litiasis renal, hipercalciuria y tratamientos previos o actuales.
Calcular de forma aproximada la ingesta de calcio dietético habitual de cada paciente permite evaluar si ésta debe ser aumentada o si el paciente va a necesitar un suplemento de calcio medicamentoso (Tablas 3, 4 y 5).
Debemos completar la anamnesis identificando los factores de riesgo de fractura que actúan independientemente de la masa ósea y que por ello, precisan medidas terapéuticas adicionales al tratamiento de la OP15. El haber padecido una fractura osteoporótica previa, es uno de los hechos que más incrementa el riesgo de fractura y podemos identificarlo fácilmente clínica o radiológicamente28,29.
Exploración física
Trataremos de obtener datos clínicos secundarios a fracturas osteoporóticas previas. La exploración física de una paciente con sospecha de OP debe ser la habitual, insistiendo en la del aparato locomotor y poniendo especial atención en la columna vertebral, realizando:
– Inspección para determinar alteraciones en la estática de la columna vertebral: hipercifosis dorsal, rectificación de la lordosis lumbar, escoliosis, disminución de la talla.
– Palpación para detectar puntos dolorosos a la presión que delimiten el nivel vertebral fracturado (centrar la radiografía en esa zona).
– Movilidad que suele estar limitada y ser dolorosa.
A otros niveles podemos observar deformidades del carpo, callos de fractura hipertróficos y mala alineación de huesos largos. Aunque, no es infrecuente que la exploración física sea completamente normal. Siempre hemos de buscar signos de otras enfermedades que ocasionan OP secundarias (hipertiroidismo, hábito cushingoide, estigmas de hepatopatía, de etilismo, etc.) y signos de enfermedades del aparato locomotor que justifiquen el dolor crónico (escoliosis, artrosis, fibromialgia, etc.).
La valoración del equilibrio, agilidad y balance muscular permite por una parte evaluar el riesgo de caída (y por tanto el riesgo de fractura) y por otra, establecer un programa de fisioterapia que permita una mejoría sintomática del paciente.
Análisis clínicos
Un paciente con sospecha de OP es tributario de que se le realicen los análisis clínicos (Tabla 7) a pesar de que, no existe ninguna prueba de laboratorio que pueda asegurar la presencia de una OP puesto que, su diagnóstico es por la DEXA.
La analítica general de sangre y orina nos proporcionará información sobre el estado de salud general y sobre la existencia de procesos causantes de OP secundaria (hipercalcemia/hiperparatiroidismo, gammapatías monoclonales/mieloma, hipertiroidismo, etc.). Así mismo, es importante para realizar el diagnóstico diferencial con otras patologías que simulan OP o que justifican el dolor del paciente (Tabla 8).
La determinación de fosfatasa alcalina total, que en ausencia de hepatopatías o enfermedad intestinal se correlaciona muy bien con la fosfatasa alcalina ósea específica y la fosfatasa ácida tartrato resistente, nos sirven de orientación respecto a la actividad metabólica ósea. Cuando sus valores están en limites altos sugieren una alta remodelación ósea. Si bien, su utilidad diagnóstica es limitada, estos parámetros ofrecen una excelente referencia en el control de la evolución de la enfermedad, sobre todo, si se instaura un tratamiento antirreabsortivo36.
La calciuria de 24 horas junto con la encuesta dietética nos ofrecerán una información importante respecto al balance del calcio. Una calciuria baja con dieta rica en calcio orienta hacia malabsorción o déficit de vitamina D. Una hipercalciuria puede ser absortiva, resortiva o de origen renal.
Los estudios hormonales más complejos deben limitarse a casos seleccionados, si bien hay que tener presente que la prevalencia del déficit de vitamina D en nuestro país, sorprendentemente, es mayor de lo que se suponía. Así mismo, los valores de referencia se están revisando al alza en personas de edad avanzada, en las que son necesarios niveles de 25 OH vitamina D superiores a 30-40 ng/ml para prevenir el desarrollo de hiperparatiroidismo secundario37.
El estudio del eje hormonal es importante en mujeres histerectomizadas en las que exista duda sobre su estado estrogénico y, es obligado en los hombres con sospecha de OP idiopática porque hasta un 25% de las OP del varón se deben a un hipogonadismo.
Radiología
El estudio radiológico de la columna vertebral dorsal (centrado en D7) y lumbar (centrado en L2) en bipedestación (de frente y de perfil), trata de valorar el estado del raquis y de documentar la presencia de fractura osteoporótica, que con frecuencia son asintomáticas, y suponen un importante marcador de riesgo de nuevas fracturas28. En ocasiones, no existen fracturas, pero sí signos radiológicos de hipertransparencia ósea coherentes con OP31. Además, contribuye a evidenciar otras causas de dolor de espalda (artrosis, escoliosis, espondilitis, etc.). También detecta focos de calcio extravertebral que pueden alterar la medición densitométrica.
Densitometría ósea
Aunque una OP es mucho más que un valor de una densitometría ósea, hoy por hoy, el diagnóstico de certeza de la OP se fundamenta en la evaluación de la masa ósea mediante densitometría ósea (DEXA)6. Esta evaluación permite cuantificar el tejido óseo a fin de poder utilizarlo como criterio de diagnóstico (de acuerdo a las categorías diagnósticas de la OP que estableció la OMS en 1994)8; como valor predictivo objetivo sobre el riesgo de fractura38; como mejor método para determinar la velocidad de la pérdida ósea y como punto de referencia en el control evolutivo de la enfermedad.
Diversos organismos de evaluación de tecnologías sanitarias han elaborado listados sobre cuándo está indicado solicitar una densitometría39, pero tal y como ellos reconocen, tan solo evalúan una parte de los riesgos y por ello, el listado que utilizamos con más frecuencia es más afín al quehacer médico de atención primaria (Tabla 9)15,20.
Se acepta mayoritariamente que las indicaciones de la DEXA deben restringirse a situaciones clínico-terapéuticas de alto riesgo; signos radiológicos sugestivos de OP y monitorización de la respuesta terapéutica. Teniendo en cuenta de antemano que los resultados de la prueba van a ser decisivos para la decisión terapéutica y que, si no fuera así, no estaría indicado realizarla (Tabla 9).
Además del diagnóstico y del grado de OP, tras haber completado todo el estudio, estaremos en condiciones de hablar de OP primaria o de OP secundaria a otra patología. De igual modo habremos realizado el diagnóstico diferencial con otros procesos que se confunden o se solapan con la OP.
Es la probabilidad de que se produzcan fracturas, la complicación clínica de la OP, lo que hace relevante esta enfermedad. Es muy importante no confundir el riesgo de OP y el riesgo de fractura osteoporótica. Así como, no asociar el criterio diagnóstico de OP con el criterio de intervención terapéutica.
La DMO es el factor determinante de fractura más importante38. Condiciona en un 70% la aparición de una fractura. El umbral de fractura se ha definido como el valor de DMO por debajo del cual se considera que aumenta el riesgo de fractura no traumática. La cifra es forzosamente arbitraria y por ello no hay una concreción unánimemente admitida. Por cada desviación estándar que disminuye el T-score de la masa ósea, aumenta 1,5 veces el riesgo relativo de producirse cualquier fractura28,29. Sin embargo, se reconocen una serie de factores de riesgo de fractura (Tabla 12)15 que actúan de manera independiente de la DMO y que, por ello, necesitan medidas terapéuticas adicionales al tratamiento específico de la OP.
Entre ellos destacan:
– Antecedentes personales de fractura previa: es uno de los factores de riesgo de fractura, independiente de la DMO, que más incrementa el riesgo y que se identifica más fácilmente. En el caso de fractura vertebral previa, el incremento del riesgo de producirse nueva fractura vertebral o de cadera es 5 veces superior28,29. De ahí la importancia de recoger información o evaluar radiológicamente la existencia de fracturas previas.
– Edad avanzada: el riesgo absoluto de fractura para un mismo valor de la DMO cambia sustancialmente con la edad. Es por tanto, un factor de riesgo de fractura independiente de la DMO.
– Antecedente familiar de OP y/o fractura osteoporótica.
– Institucionalización (encamamiento, no-exposición solar, mala nutrición, patología de base)
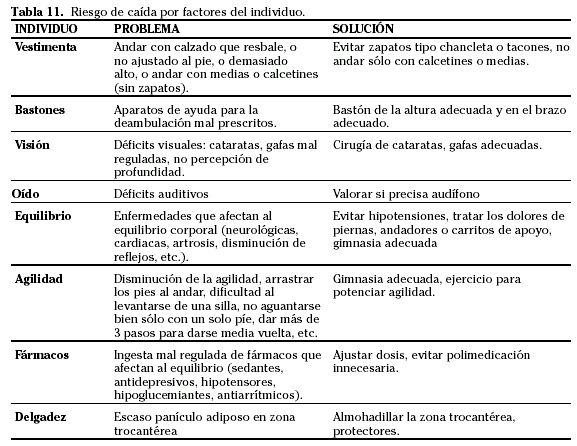
– Riesgo de caída: las caídas son uno de los factores de riesgo de fractura más importantes entre las personas de edad avanzada. Se ha sugerido que podría ser más predictivo de fractura que una baja DMO. Sobre todo conlleva riesgo de fractura de cadera (Tablas 10 y 11). La modificación de estos riesgos, tanto del entorno como los propios del individuo, consiguen una reducción importante en la incidencia de fracturas. El ejercicio físico adecuado al paciente, con el objetivo de mejorar su agilidad y su equilibrio, reduce el riesgo de caídas y reduce la incidencia de fracturas de cadera entre un 25-50% (Estudio Greeg 1998).
No tenemos ningún método bien establecido para cuantificar cada uno de estos factores y conocer el riesgo global de fractura del paciente osteoporótico. Pero se ha de realizar una valoración clínica de todos ellos para aproximarnos de la forma más fiel posible al riesgo de fractura.
La decisión de tratar debe ser individualizada en cada paciente en base a la valoración clínico-pronóstica que se haya realizado y de acuerdo con las indicaciones evidenciadas por cada una de las opciones terapéuticas.
BIBLIOGRAFÍA
1. Consensus development conference: prophylaxis and treatment of osteoporosis. Am J Med 1991; 90: 107-110. [ Links ]
2. Conferencia de consenso sobre prevencion, diagnóstico y tratamiento de la osteoporosis. Instituto Nacional de la Salud, USA. Rev Esp Enf Metab Oseas 2000; 9: 231-239. [ Links ]
3. Sosa M, Gómez de Tejada MJ, Hernández D. Prevención de la osteoporosis. Concepto, clasificacion, factores de riesgo y clinica de la osteoporosis. Rev Esp Enferm Metab Oseas 2001;10 (Supl A): 7-11. [ Links ]
4. Jergas M, Genant HK. Spinal and femoral DXA for the assessment of spinal osteoporosis. Calcif Tissue Int 1997; 61: 351-357. [ Links ]
5. Long TF, Li J, Harris S, Genant HK. Assessment of vertebral bone mineral density using volumetric quantitative CT. J Comput Assist Tomogr 1999; 23: 130-137. [ Links ]
6. Kanis JA. Assessment of bone mass and osteoporosis. En: Kanis JA, ed. Osteoporosis. Oxford: Blackwell Science, 1994; 114-147. [ Links ]
7. Marsall D, Johnell O, Wedel H. Meta-analysis of how well measures of bone mineral dendity predict occurrence of osteoporotic fractures. Br Med J 1996; 312: 1254-1259. [ Links ]
8. Worl Health Organization. Assessment of fracture risk and its application to screening for postmenopausal osteoporosis. WHO technical report series 843, 1994. Geneve, Switzerland. [ Links ]
9. Reid IR, Evans MC, Ames R, Wattie DJ. The influence of osteophytes and aortic calcification on spinal mineral density in postmenopausal women. J Clin Endocrinol Metab 1991; 72: 1372-1374. [ Links ]
10. Black DM, Palermo l, Genant HK, Cummings SR. Four reason to avoid the use of BMD T-scores in treatment decisions of osteoporosis. J Bone Miner Res 1996; 11(Supl 1) S61. [ Links ]
11. Riggs BL, Melton LJ. Osteoporosis: etiología, diagnóstico y tratamiento. Nueva York: Raven Press, 1998, 171-271. [ Links ]
12. Díaz-Curiel M, García JJ, Carrasco JL, Honorato J, Perez-Cano R, Rapado A et al. Prevalencia de osteoporosis determinada por densitometía en la población femenina española. Med Clin (Barc) 2001; 116: 86-88. [ Links ]
13. Díaz-Curiel M, Turbí C, Rapado A, García J. Prevalencia de osteopenia y osteoporosis densitométrica en la población masculina española. Rev Esp Enf Metab Óseas 1997, 6: 129-132. [ Links ]
14. Nogués X, Diez A. Definición y epidemiología de la osteoporosis. Barcelona: Profarmaco 2, editores, 2000; 3-6. [ Links ]
15. Grupo de osteoporosis de la SEMFYC. Guía práctica para el abordaje de la osteoporosis 2002. Recomendaciones SEMFYC. [ Links ]
16. Paulino J, Paulino M. Osteoporosis: importancia, epidemiología y manifestaciones clínicas. Medicine (Madrid) 2000; 8: 15-22. [ Links ]
17. Rapado A, Díaz M. Manual práctico de osteoporosis en Atención Primaria de Salud. Madrid: FHOEMO ( Fundación Hispana de Osteoporosis y Enfermedades Metabólicas Oseas), 1996. [ Links ]
18. Sosa Henriquez M. Osteoporosis: factores de riesgo, clasificación y clinica. En: Rapado Errazti A, Díaz-Curiel M, eds. Manual práctico de osteoporosis en atención primaria. FHOEMO, 1996, 35-44. [ Links ]
19. Stephen M, Krane M, Holick F. Enfermedad osea metabólica. Osteoporosis. Pricipios de Medicina Interna. Harrison. McGraw-Hill-interamericana (14ª Ed). Capítulo 355; 2557-2570. [ Links ]
20. Orozco P. Abordaje racional de la osteoporosis. Cuadernos de Gestion Sanitaria 2000; 6: 4-9. [ Links ]
21. Dempster DW, Lindsay R. Pathogenesis of osteoporosis. Lancet 1993; 341: 260-262. [ Links ]
22. Sosa Henriquez M, Navarro R, Arbelo A. Fractura de cadera: la realidad española. En: Díaz-Curiel M, ed. Actualizacion de la osteoporosis. FHOEMO, 2001; 13-22. [ Links ]
23. Naves Díaz M, Díaz López JB, Gómez Alonso C, Altadill A, Rodriguez Rebollar A, Cannata JB. Estudio de incidencia de fracturas osteoporóticas en una cohorte de individuos mayores de 50 años en Asturias tras 6 años de seguimiento. Med Clin (Barc) 2000; 115: 650-653. [ Links ]
24. Sosa M, Arbelo A, Lainez P, Navarro MC. Datos actualizados sobre la epidemiología de la fráctura osteoporótica en España. Rev Esp Enf Metab Óseas 1998; 7: 174-179. [ Links ]
25. Meyer HE, Tuerdal A, Falch JA, Pederson JI. Factors associated with mortality after hip fracture. Osteoporos Int 2000; 11: 228-232. [ Links ]
26. Cree M, Soskolne CL, Belseck E, Horning J, MC Elhaney JE, Brant R et al. Mortality and institutionalization following hip fracture. J Am Geriatr Soc 2000; 48: 283-288. [ Links ]
27. ONeill TW, Felsenberg D, Varlow J, Cooper C, Kanis JA, Silman AJ. The prevalence of vertebral deformity in european men and women: the European Vertebral osteoporosis Study. J Bone Miner Res 1996; 11: 1010-1018. [ Links ]
28. Lindsay R, Silverman SL, Cooper C, Hanley DA, Barton I, Broy SB et al. Risk of new vertebral fracture in the year following a fracture. JAMA 2001; 285: 320-323. [ Links ]
29. Ismail AA, Cockerill W, Cooper C, Finn JD, Abendroth K, Ranisi G et al. Prevalent vertebral deformity predicts incident hip toutgh not distal forearm fracture: results from the European prospective osteoporosis study. Osteoporos Int 2001; 12: 85-90. [ Links ]
30.Genant Hk, WuCY van Kkuijik C, Nevitt MC. Vertebral fracture assessment using a semiquantitative technique. J Bone Miner Res 1993; 8: 1137-1148. [ Links ]
31. Jergas MD, genat HK. Radiology of osteoporosis. En: Favaus MJ, ed. Primer on the metabolic bone diseases and disorders of mineral metabolism. Filadelfia: Lippincott Williams & Wilkins 1999; 160-169. [ Links ]
32. Muñoz Torres M, Mezquita Raya P, Escobar Jimenez F. Concepto, fisiopatología y clínica. En: Formación continuada en osteoporosis. Barcelona: Ed Mayo SA, 1999. [ Links ]
33. Orozco López P. Actualización en el abordaje y tratamiento de la osteoporosis 2001. Inf Ter Sist Nac Salud 2001; 25: 117-147. [ Links ]
34. Documento de la Sociedad Española Española de Reumatología sobre la osteoporosis postmenopaúsica. Rev Esp Reumatología 2001; 28: 148-153. [ Links ]
35. Kanis JA, Delmas P, Burkhardt P, Cooper C,Torgerson D. Guidelines for diagnosis and management of osteoporosis. Osteoporosos Int 1997; 7:390-396. [ Links ]
36. Delmas PD. The role of markers of bone turnover in the assessment of fracture risk in portmenopausal women. Osteoporos Int 1998; 8, (Suppl 1): S32-36. [ Links ]
37. Goméz Alonso C, Naves ML; Fernádez Matín JL. Vitamin D levels and prevalence of secondary hyperparathiroidism in a Spanish population-based sample aged 54 to 89. J Bone Miner Res 2001, 16: s156-s158. [ Links ]
38. United States preventive Services Task Force Screming for osteoporosis in postmenopausal women recommendations and rationale. Am Intern Med 2002; 137: 526-528. [ Links ]
39. Agencia dÁvaluació de Tecnología Médica. Guía para la indicación de la densitometría ósea en la valoración del resgo de fractura. Departamento de Sanidad y Seguridad Social. Generalitat de Catalunya. Barcelona. Junio de 1999. [ Links ]