INTRODUCCIÓN
La miastenia gravis (MG) es la patología más frecuente de la transmisión neuromuscular. En España se diagnostican cada año 700 nuevos casos aproximadamente, según la Sociedad Española de Neurología1. La prevalencia es de 0,5-20,4 pacientes/100.000 habitantes y la incidencia de 0,3 casos/100.000 habitantes2. Actualmente, la mortalidad es del 4,5%.
La MG es causada por un defecto en la transmisión de los impulsos nerviosos a los músculos. Ocurre cuando la comunicación normal entre el nervio y el músculo se interrumpe en la unión neuromuscular, el lugar de conexión entre las células nerviosas y los músculos que controlan. Normalmente, cuando los impulsos recorren el nervio, las terminaciones nerviosas segregan acetilcolina; esta se desplaza a través de la unión neuromuscular y se adhiere a sus receptores, los cuales se activan y generan una contracción del músculo. La MG es una enfermedad autoinmune cuya fisiopatología se basa en la disminución del número de receptores de acetilcolina presentes en la membrana postsináptica porque los anticuerpos bloquean, alteran o destruyen los receptores de acetilcolina en la unión neuromuscular, lo cual evita que ocurra la contracción del músculo.
Puede manifestarse a cualquier edad, aunque suele tener dos picos: uno temprano en la segunda-tercera década de la vida (de predominio femenino) y otro tardío en la octava década (de predominio masculino)1. Clínicamente, presenta dos formas: ocular y generalizada, las cuales se basan en la misma característica de debilidad muscular fluctuante3.
La forma seronegativa es relativamente rara: los autoanticuerpos antiacetilcolina (ACh) no se detectan en el 20% de pacientes con MG generalizada y el 50% de pacientes con MG ocular4,5. Ante estas formas, el diagnóstico se basará en las características clínicas de esta enfermedad, siendo confirmada por:
Presencia de alteración en la transmisión neuromuscular, demostrada en un estudio electromiográfico: se requiere una disminución rápida de más del 10% en la amplitud de las respuestas provocadas por la estimulación repetida de nervios5,6.
Respuesta al tratamiento anticolinesterásico: test farmacológico con edrofonio intravenoso o tratamiento oral con piridostigmina. Si se advierte una mejoría neta en la sintomatología, se considera como respuesta positiva.
Debe cumplir al menos uno de estos criterios junto con una clínica compatible para el diagnóstico de MG3.
La definición de paciente seronegativo clásicamente se asocia a no presentar autoanticuerpos contra receptores de ACh7. Sin embargo, después se han ido asociando a otros autoanticuerpos: antiquinasa mioespecífica (MuSK), que están presentes hasta en el 40% de pacientes seronegativos con MG generalizada, y en otra pequeña proporción de estos pacientes se han detectado autoanticuerpos anti-receptor 4 de lipoproteína de baja densidad (LRP4)5,8. El fenotipo MuSK es más frecuente en mujeres9.
CASO CLÍNICO
Presentamos el caso de un hombre de 36 años que acude a la consulta de Atención Primaria por sentir en la última semana parestesias a nivel del labio superior durante la masticación, que se acompañaba de escape de líquidos por la comisura labial de forma ocasional; la parestesia cede a los pocos minutos de terminar de comer. No contaba síntomas de disfagia ni claudicación mandibular; tampoco había alteraciones en la mímica facial del paciente.
Como únicos antecedentes personales, presenta una intervención quirúrgica de hernia inguinal derecha y ablación de venas pulmonares por taquiarritmia en 2008. No presenta otros datos de interés, ya que se trata, por lo demás, de un hombre previamente sano, sin factores de riesgo asociados, sin hábitos tóxicos ni consumo de fármacos, sin antecedentes familiares de interés ni alergias conocidas. En cuanto a la exploración neurológica, esta es anodina, la sensibilidad estaba conservada y en la exploración general tampoco encontramos datos de alteración. Ante esta situación, se deja en observación domiciliaria al paciente, a quien informamos de posibles síntomas de alarma.
Doce días después, encontrándose fuera de su domicilio habitual, acude a urgencias por disfagia y diplopía de varios días de evolución cada vez más marcada. Informa de que en los últimos días asocia disfagia de predominio para líquidos junto con diplopía binocular oblicua de predominio vespertino. En la entrevista refiere haber hecho más ejercicio del habitual en las últimas semanas, notándose más disneico y débil. No presenta otra sintomatología ni déficit neurológico. En la exploración, observamos una limitación en la abducción e hipotropía del ojo derecho con la supraversión que condiciona una diplopía oblicua, así como una debilidad de ambos orbiculares de los ojos (siendo mayor en el lado derecho). También podemos objetivar una ptosis del ojo derecho con la supraversión mantenida. Además, encontramos disminuidos los reflejos profundos o de estiramiento muscular o miotáticos REM en miembros izquierdos tanto superior como inferior; se objetiva también debilidad en los flexores del cuello. El resto de la exploración física es absolutamente normal, sin ninguna otra alteración. En la evolución, el paciente presenta disfagia a líquidos y regurgitación nasal de los mismos.
Entre las pruebas complementarias realizadas, la analítica sanguínea y serológica son negativas y con datos en rango de normalidad. En la resonancia magnética sin contraste y tras la administración del mismo no se aprecian hallazgos significativos. Sin embargo, en la tomografía axial computarizada torácica se observa una imagen sugerente de timoma en el espacio prevascular de 3 cm, de contorno bien definido y densidad heterogénea; la masa contacta con la pleura mediastínica izquierda y con el pericardio, sin claros signos de infiltración. No se aprecian adenopatías mediastínicas ni hiliares de tamaño significativo (figura 1).
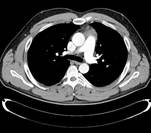
Figura 1. Tomografía axial computarizada torácica con imagen sugerencia de timoma en el espacio prevascular.
Ante el alto grado de sospecha de miastenia gravis, se solicitan anticuerpos antirreceptor de acetilcolina, los cuales resultan negativos. También fueron negativos los anticuerpos anti-Musk. Se programa intervención quirúrgica de probable timoma. Tras la intervención, la anatomía patológica confirma la presencia de un timoma tipo A Masaoka 1. Finalmente, se introduce una pauta ascendente de corticoides hasta una dosis de 60 mg de prednisona al día y piridostigmina con buena respuesta inicial por parte del paciente, no así al paso del tiempo.
La evolución no fue óptima y ha precisado en varias ocasiones ajuste de la dosis de corticoides. Como hemos visto, esta evolución es más frecuente en pacientes seronegativos; sin embargo, en este grupo de pacientes no suele haber timoma, y en nuestro caso sí lo había. Además, como ocurre normalmente, la timectomía permite disminuir la dosis de corticoides y los pacientes sufren menos crisis miasténicas, cosa que con nuestro paciente no ocurrió. El paciente no presentaba patología tiroidea ni reumatológica. A los 9 meses de evolución de la enfermedad, se observó una astenia marcada, a pesar de añadirle al tratamiento un inmunosupresor, micofenolato. Al año, y tras hacer una seroconversión con los autoanticuerpos de acetilcolina con valor de 12,55 nmol/l (positivo a partir de 1 nmol/l), presentó un cuadro de microperforación de sigma y sendos abscesos en mesosigma y psoas. Se determinó la calprotectina fecal, resultando negativa, por lo que se planteó el diagnóstico diferencial entre enfermedad inflamatoria intestinal (EII) y enfermedad diverticular.
DISCUSIÓN
Se trata de un paciente joven con sintomatología y exploración anodinas en su consulta inicial que presenta inicialmente una sintomatología que afecta a la musculatura implicada en la masticación, inervada por el V par craneal, el nervio motor de la musculatura de la masticación. Normalmente, los síntomas ceden con el reposo y son más evidentes cuando el alimento es duro de masticar, como puede ser la carne. La evolución ha sido mala: comenzó con síntomas pequeños e inespecíficos, pero acabó desarrollando síntomas muy importantes y muy asociados a la MG.
En este caso, la serología fue negativa, hecho que es más frecuente en mujeres. En esta forma de presentación el inicio de síntomas es más variable (predominan las formas tardías) y son más habituales las formas benignas. La respuesta al tratamiento suele ser peor y raramente hay remisión completa. Las anomalías tímicas no suelen estar asociadas. La seroconversión en MG anti-ACh no es rara (17%)2,3,10, y así ocurrió en este paciente.
Los pacientes con MG seronegativa tienen mayor probabilidad de presentar la forma ocular y asociaciones con otras patologías: puede considerarse un síndrome paraneoplásico de timoma, cáncer pulmonar de células pequeñas o linfoma de Hodgkin. La asociación con patologías tiroideas es común (3-10%). También tienen mayor propensión a enfermedades reumáticas autoinmunes (síndrome de Sjögren, artritis reumatoide o lupus eritematoso sistémico)10.
El timo tiene un papel fundamental en la patogénesis de la MG. La timectomía se indica en caso de timoma, pero en casos de no timoma tampoco se descarta. Permite disminuir la dosis de glucocorticoides, presentan menos episodios de crisis miasténicas y más frecuentemente episodios de remisión total o casi total11.
La MG es un trastorno neuromuscular autoinmune que produce debilidad y tendencia a la fatiga de los músculos esqueléticos, indoloro, de predominio proximal y de curso fluctuante. Un 10% de los pacientes presenta clínica de comienzo en forma de debilidad de los miembros inferiores2. La debilidad es fluctuante hasta que se instaura de forma paulatina. Este dato es importante para aquellos pacientes que consultan esto al inicio del cuadro. En ancianos puede confundirnos con un accidente cerebrovascular, en otras ocasiones nos puede parecer una patología psiquiátrica (20%)12. En el 90% de los pacientes con MG la distribución, gravedad y evolución de la enfermedad se definen dentro de los dos primeros años a partir de su inicio. Por todo ello, es imprescindible hacer una minuciosa historia clínica y una exploración neurológica completa, incluidos reflejos y sensibilidad.
Debemos pensar en la MG cuando la clínica sea atípica y, sobre todo, ante cuadros de diplopía asociada a debilidad y otras afectaciones neurológicas, o incluso en cuadros que impresionan de carácter psicosomático o somatoforme. El diagnóstico diferencial de la fatiga o cansancio es el más difícil de establecer, pudiendo ayudarnos las maniobras de fatigabilidad, como pueden ser elevar 10 veces los miembros superiores por encima de la cabeza, contar despacio hasta 30 o levantarse de una silla sin ayuda de los brazos 10 veces.
Queremos recordar esta patología que ha visto incrementado su diagnóstico desde los años ochenta del pasado siglo, debido a un mejor reconocimiento de los síntomas y al diagnóstico precoz a causa de la accesibilidad de la determinación de los anticuerpos circulantes2. Asimismo, gracias a los nuevos tratamientos y al diagnóstico precoz, la calidad de vida de estos pacientes ha mejorado.














