INTRODUCCIÓN
Los antibióticos betalactámicos son los más utilizados tanto en el ámbito de atención primaria como hospitalario y más del 90 % de los pacientes que dicen ser alérgicos a la penicilina en realidad no lo son1. Las reacciones alérgicas a los betalactámicos, específicamente a las aminopenicilinas (en concreto, la amoxicilina), son la causa más común de reacciones adversas a medicamentos notificadas en niños y adultos2.
Las penicilinas se usan comúnmente para tratar infecciones causadas por organismos tanto gram negativos como gram positivos. La alergia a la penicilina es una de las alergias a medicamentos más frecuentemente reportadas, con una prevalencia del 5 % al 10 % y entre el 11 % y 15 % en pacientes hospitalizados3,4.
Asimismo, los individuos etiquetados de alergia a penicilina tienen más probabilidades de recibir terapias alternativas, lo que puede generar gastos adicionales, estancias hospitalarias más prolongadas y un aumento de microorganismos multirresistentes como por ejemplo enterococcus resistente a la vancomicina, S. aureus resistente a la meticilina, o C. difficile, entre otros5,6.
Aproximadamente del 90 % al 95 % de los pacientes con sospecha de alergia a penicilina pueden tolerar una nueva exposición tras una evaluación adecuada por especialistas de alergología5.
CLASIFICACIÓN DE LAS REACCIONES ADVERSAS MEDICAMENTOSAS
Las reacciones adversas a fármacos se definen, según la Organización Mundial de la Salud, como cualquier efecto perjudicial y no intencionado, producido por un fármaco, que ocurre a las dosis utilizadas en humanos para la profilaxis, el diagnóstico o el tratamiento. Un fármaco es cualquier sustancia o producto empleado para modificar o explorar una función biológica o una situación patológica, que repercuta en el beneficio de la persona receptora de la misma1,5,7.
Se entiende por reacción alérgica o de hipersensibilidad la respuesta adversa a un medicamento producida por mecanismo inmunológico. Son reacciones de tipo B, en cuya patogenia participa un mecanismo inmunológico específico, conocido o supuesto. Son reproducibles incluso con dosis mínimas del agente causal y, en ocasiones, pueden ser detectadas mediante diferentes técnicas empleadas en el diagnóstico alergológico7.
Habitualmente no dependen de la dosis del fármaco, no están relacionadas con la acción farmacológica del mismo y requieren una sensibilización previa. La mayoría son impredecibles y afectan sólo a determinados individuos. La predisposición individual para presentar reacciones de hipersensibilidad depende de características genéticas en individuos susceptibles. Estas reacciones, en muchos casos graves, limitan el uso de fármacos que, por otra parte, son eficaces y pueden causar la retirada tras su comercialización. Por lo tanto, no son reacciones predecibles y son recurrentes si el paciente se expone de nuevo al fármaco1,7.
La Red Europea de Alergia a Medicamentos clasifica las reacciones de hipersensibilidad a medicamentos en dos grupos: reacciones inmediatas y reacciones no inmediatas8.
Se consideran reacciones inmediatas (tipo 1 o mediadas por IgE) cuando se presentan entre una y seis horas después de la exposición al fármaco. Las manifestaciones clínicas que involucran reacciones inmediatas van desde cuadros leves como urticaria inmediata o angioedema hasta reacciones graves como anafilaxia, incluyendo el shock anafiláctico. Pueden producirse reacciones limitadas (angioedema labial, disfonía o broncoespasmo aislado), pero son infrecuentes8.
Las reacciones no inmediatas o tardías (no mediadas por IgE) tienen lugar más de seis horas después y hasta varios días después de la última administración del fármaco y comprenden desde el exantema maculopapular o urticaria no inmediata hasta reacciones adversas cutáneas graves (conocidas con las siglas SCAR). La mayoría de las reacciones no inmediatas son leves. La manifestación clínica más común en niños es cutánea, en forma de exantema maculopapular tardío o urticaria, de hecho, el exantema maculopapular ocurre en el 5 %-10 % de los niños a los que se les prescribe amoxicilina. Por lo tanto, es necesario considerar en el diagnóstico diferencial infecciones virales como Epstein Barr, Citomegalovirus, Herpes virus Humano-6 y otras. La anafilaxia en niños es extremadamente rara y representa menos del 0,05 % de todos los casos. La gravedad de la reacción se asocia con el aumento de la edad8.
¿POR QUÉ ES IMPORTANTE CONFIRMAR EL DIAGNÓSTICO?
Si bien el diagnóstico de alergia a la penicilina generalmente se adquiere en la infancia y hasta el 20 % de la población general se autodenomina alérgica a la penicilina, solo menos del 6 % de ellas se confirman después de un estudio adecuado9. Las manifestaciones como náuseas, vómitos, diarrea, dolor de cabeza no deben ser considerados como contraindicación alergológica para recibir el fármaco ya que probablemente sean consecuencia de algún tipo de intolerancia o efecto secundario10.
Un diagnóstico erróneo conduce a la utilización de antibióticos de segunda línea, posible aumento de efectos adversos y uso de terapias alternativas menos efectivas. Esto constituye una importante amenaza para la salud pública y una significativa carga económica, ya que el uso de antibióticos de amplio espectro puede provocar infección por C. difficile, resistencia a los antibióticos y estancia hospitalaria prolongada. Por todo ello, es muy importante reconsiderar las sospechas de alergia a la penicilina y derivados y confirmarlas con estudios alergológicos5.
A la hora de realizar el estudio alergológico hay que tener en cuenta que debe realizarse de forma ambulatoria, tras cuatro o seis semanas de la reacción inicial y con el paciente estable. No es recomendable realizar el estudio durante un ingreso hospitalario.
ASPECTOS A TENER EN CUENTA
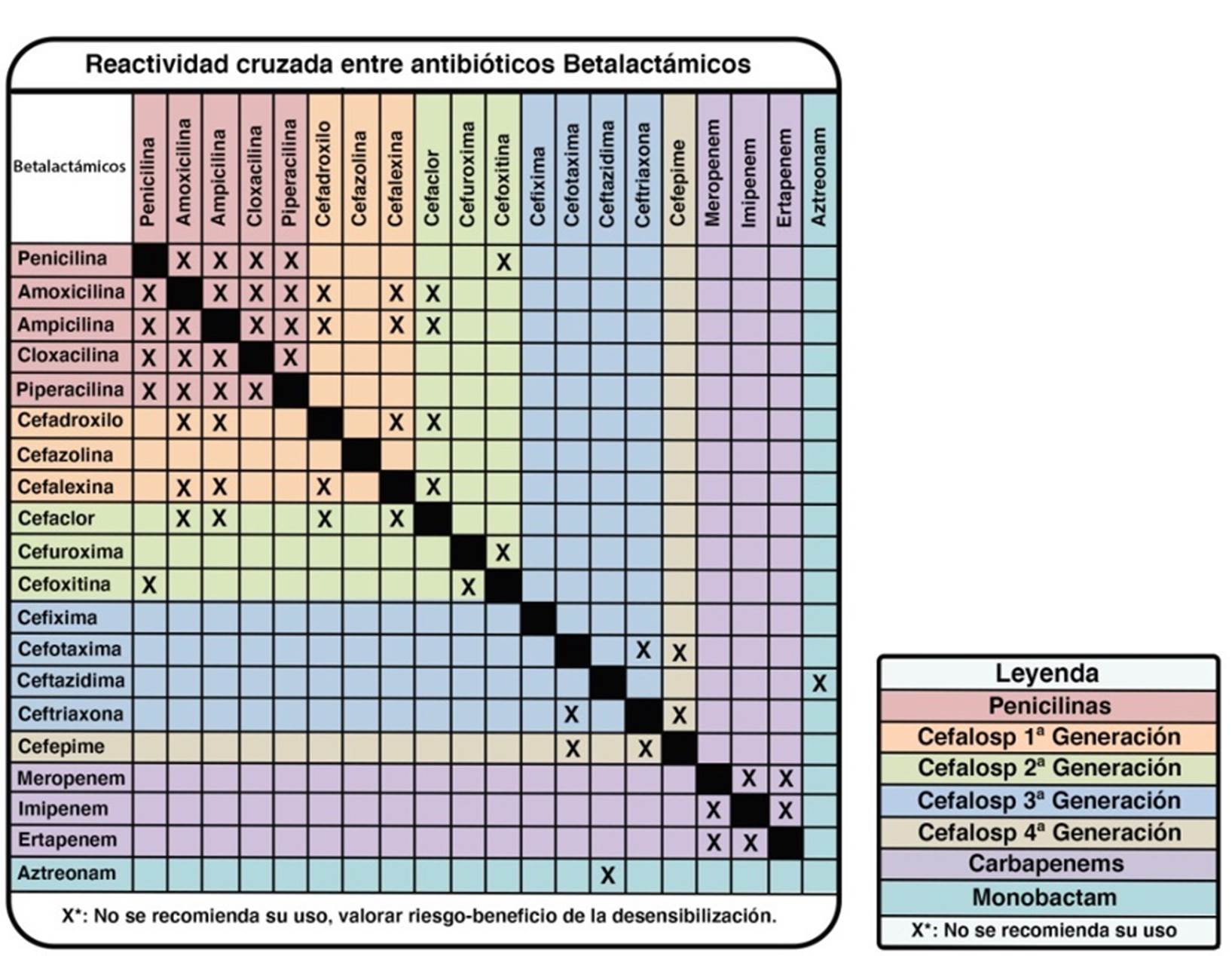
Conocer la reactividad cruzada entre antibióticos pertenecientes al grupo de los betalactámicos, para lo cual resulta necesario identificar la estructura química de éstos.
Realizar una anamnesis detallada describiendo el tipo de reacción que ha manifestado el paciente para decidir el protocolo de actuación.
Reactividad cruzada
Los fármacos betalactámicos comparten un anillo de cuatro carbonos, denominado anillo betalactámico. Además, cada tipo de betalactámico posee un anillo de grupo característico:
Anillo tiazolidínico: penicilinas
Anillo dihidrotiazina: cefalosporinas
Anillo de cinco carbonos: carbapenemes
Solo poseen anillo betalactámico: monobactámicos
Por otro lado, todos tienen al menos una cadena lateral, que puede ser idéntica a la de otros betalactámicos pese a pertenecer a diferentes grupos.
La penicilina y el resto de betalactámicos comparten el anillo betalactámico pero difieren con respecto al anillo adyacente y las cadenas laterales del grupo R: R1 y R2. Los datos publicados indican un alto grado de reactividad cruzada entre las penicilinas semisintéticas, especialmente las aminopenicilinas (amoxicilina, ampicilina, bacampicilina y pivampicilina) que comparten un grupo amino en su cadena lateral, así como entre las penicilinas semisintéticas y la bencilpenicilina11.
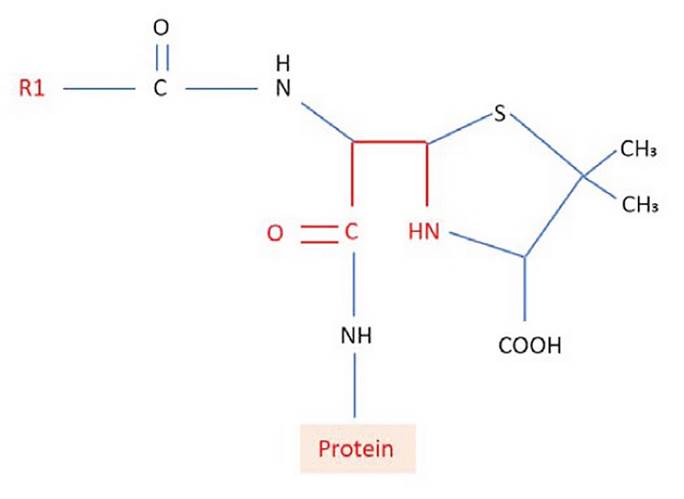
La penicilina es una molécula pequeña que se une covalentemente a las proteínas plasmáticas para crear complejos hapteno-portador. El anillo betalactámico se une a residuos de lisina en las proteínas séricas y, cuando se une a una matriz de polilisina, se genera el principal determinante antigénico peniciloil-polilisina (PPL) (figura 1). La haptenación por unión covalente a grupos carboxilo y tiol conduce a la creación de varios determinantes menores11 (MDM) (figura 2).
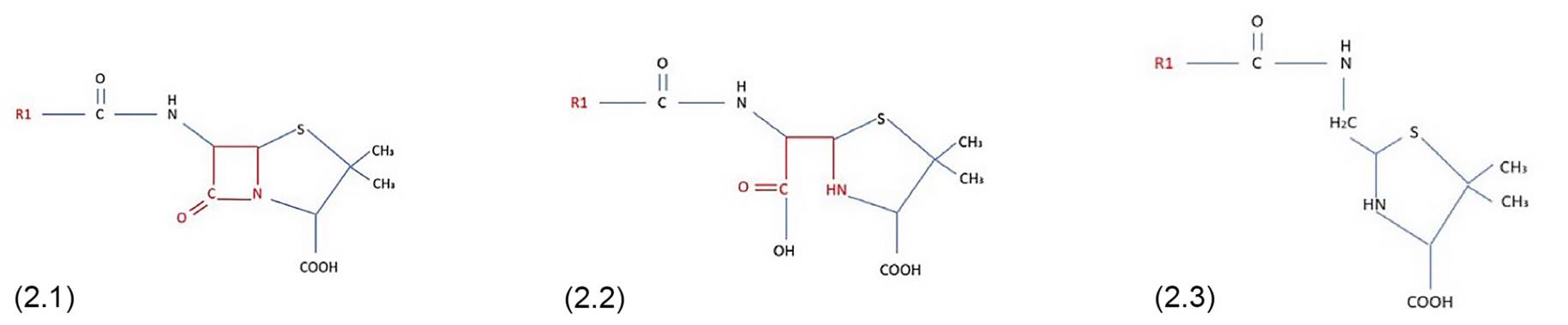
Figura 2. Estructuras químicas de la mezcla de determinantes menores (MDM): Penicilina (2.1), Penicilato (2.2), Peniloato (2.3).
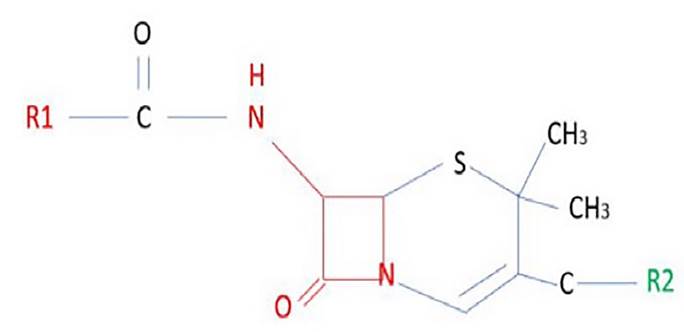
Los betalactámicos del tipo penicilina solo tienen grupos R1. Se ha demostrado que las cadenas laterales R1 compartidas entre algunas penicilinas y cefalosporinas, así como entre las propias cefalosporinas, son un importante factor de reactividad cruzada. La cadena R2 solo está presente en las cefalosporinas y, por tanto, no es causa de reactividad cruzada entre las cefalosporinas y las penicilinas11 (figuras 3, 4 y 5).
Se ha informado que, en reacciones inmediatas, existe una reactividad cruzada del 10 % entre las penicilinas y las cefalosporinas de primera generación debido a la similitud de sus cadenas laterales (excluyendo la cefazolina). Si son idénticas, la reactividad cruzada alcanza el 30 %, como ocurre con la amoxicilina y el cefadroxilo, siendo menor entre las penicilinas y las cefalosporinas de segunda generación, sobre todo con la cefuroxima. De hecho, Romano et al. informaron en su último estudio una tasa de reactividad cruzada entre penicilinas, cefamandol y aminocefalosporinas en torno al 38 %, así como la tolerabilidad de cefuroxima y ceftriaxona en todos los sujetos con hipersensibilidad a las penicilinas mediada por IgE que presentaban pruebas cutáneas negativas con estas cefalosporinas. Por el contrario, la reactividad cruzada con cefalosporinas de tercera y cuarta generación es extremadamente infrecuente12-14.
Comprender los mecanismos subyacentes de la reactividad cruzada es de suma relevancia para brindar alternativas seguras a los pacientes con alergia a antibióticos de la familia de los betalactámicos que pueden ser candidatos a recibir tratamiento con alternativas dentro del mismo grupo (tabla 1).
Reacción índice
Es esencial identificar el tipo de reacción inicial que ha presentado el paciente mediante la realización de una historia clínica detallada que recoja los siguientes datos:
Fármacos implicados en la reacción y su tolerancia previa
Tiempo de latencia transcurrido desde la toma del fármaco hasta la aparición de los síntomas
Clínica/sintomatología
Medicamentos utilizados para tratar la reacción y respuesta a los mismos
- Tiempo de curación y presencia de lesiones residuales o descamación
Fármacos tolerados con posterioridad
De esta manera será posible clasificar el tipo de reacción y programar el estudio adecuado. Es importante saber que debe transcurrir un mínimo de cuatro o seis semanas entre la reacción y la realización del estudio alergológico, dado que la sensibilidad de las pruebas disminuye si se encuentra en periodo refractario o ventana11.
En general, como ya se ha mencionado, las reacciones alérgicas a medicamentos pueden agruparse en dos tipos, inmediatas y tardías y por lo tanto, en función de la sospecha, el estudio alergológico incluirá pruebas cutáneas en prick e intradermorreacción con lectura inmediata y/o tardía, pruebas epicutáneas o de parche con lectura a las 48 y 96 horas y pruebas in vitro como la determinación de IgE específica, el test de activación de basófilos o test de transformación linfoblástica. En función del resultado de este estudio se valora la posibilidad de realizar una prueba de exposición controlada con el fármaco implicado o alternativo11.
En conclusión, dado que, tras una evaluación formal por especialistas con pruebas cutáneas y prueba de exposición, menos del 5 % de los casos sospechosos se confirma que son verdaderamente alérgicos, es evidente la trascendencia de eliminar el etiquetado de estos pacientes, ya que un diagnóstico erróneo puede tener implicaciones para la salud pública y personal. Además, en niños con reacciones leves, un algoritmo simplificado que evita las pruebas cutáneas y séricas es eficaz para descartar o confirmar el diagnóstico8,9,11.
Anexo
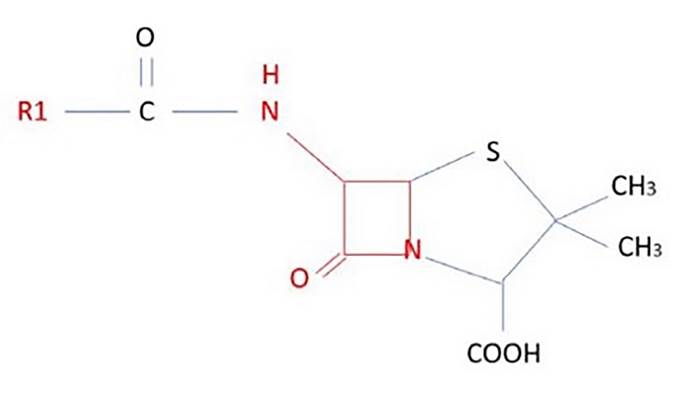
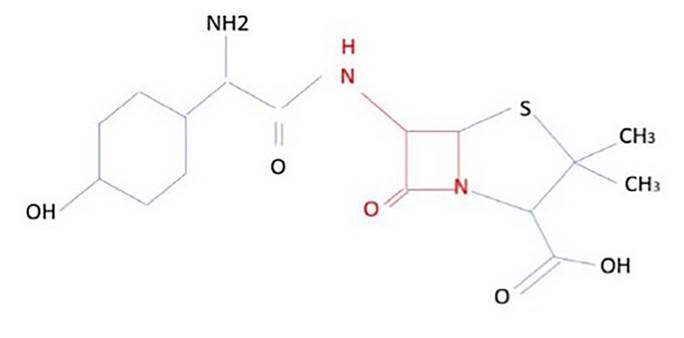
Las figuras muestran el principal determinante alergénico y la mezcla de determinantes menores que forman el anillo betalactámico, así como la estructura química de la penicilina, amoxicilina y cefalosporina.
El anillo betalactámico se muestra resaltado en color rojo. R1, también resaltado en rojo, representa el grupo R de las cadenas laterales. El anillo betalactámico (rojo) es común a los antibióticos betalactámicos y cada subclase se diferencia por el anillo adyacente (azul) y el grupo R de cadenas laterales R1 (rojas) y R2 (verde). Algunas penicilinas y cefalosporinas comparten el lado R1 cadena (reactividad cruzada).