INTRODUCCIÓN
Actualmente, los inhibidores de la aromatasa (IA) se utilizan como terapia adyuvante de primera línea para mujeres con diagnóstico de cáncer de mama con receptores hormonales positivos. Aunque su efectividad para reducir el riesgo de recurrencia y mortalidad es bien conocida1, los IA también se han asociado con efectos secundarios que pueden afectar negativamente la calidad de vida del paciente, la adherencia al tratamiento y la mortalidad asociada2.
En el tratamiento con IA, se produce una marcada reducción de los estrógenos circulantes en la mujer postmenopáusica al bloquear la conversión por la enzima aromatasa de andrógenos a estrógenos. Esta acción deja a la mujer sin estrógenos residuales, que se producen tras la menopausia, como el estradiol y la estrona. Uno de los efectos secundarios más comunes es la pérdida ósea acelerada, que se asocia con un mayor riesgo de fracturas osteoporóticas3,4. En esta línea, existen diferentes meta-análisis que incluyen ensayos clínicos controlados aleatorizados que han demostrado una asociación entre el tratamiento prolongado con IA y un aumento del riesgo de fracturas óseas, con un incremento entre el 34% y el 59%5,6.
Por otro lado, en un estudio de cohorte que incluyó a 1.775 pacientes que iniciaron la terapia con inhibidores de la aromatasa a largo plazo, el riesgo de fractura osteoporótica fue similar al de la población general. Cabe destacar que en este estudio las mujeres tratadas con IA presentaban un índice de masa corporal basal más alto, una mayor densidad mineral ósea y una menor prevalencia de fractura previa al inicio del estudio que la población general7.
La cohorte B-ABLE (Barcelona – Aromatase induced Bone Loss in Early breast cáncer) incluye pacientes postmenopáusicas con cáncer de mama receptor de estrógeno positivo (RE+), reclutadas en el momento de iniciar el tratamiento con IA. Esta cohorte se ha utilizado para realizar un estudio observacional prospectivo en que las pacientes son controladas durante todo el estudio con datos de salud ósea y factores asociados desde el inicio del tratamiento hasta un año después de finalizar dicho tratamiento3.
El objetivo de este estudio fue evaluar la incidencia de fracturas clínicas y las características de las pacientes fracturadas en la cohorte B-ABLE durante el tratamiento con IA y hasta un año después de su finalización.
Material y métodos:
Población de estudio
Se ha realizado un estudio de cohorte prospectivo, no seleccionado, observacional y clínico en la cohorte B-ABLE que incluye pacientes postmenopáusicas diagnosticadas de cáncer de mama receptor de estrógenos positivo (RE+), tratadas en el Hospital del Mar de Barcelona. Las participantes se reclutaron al inicio del tratamiento con IA (letrozol, exemestano o anastrozol) y fueron tratadas durante 5 años, de acuerdo a las recomendaciones de la American Society of Clinical Oncology, empezando dentro de las 6 semanas después de la cirugía ó 1 mes después del último ciclo de quimioterapia8. Alternativamente, aquellas pacientes que eran premenopáusicas en el momento de iniciar el tratamiento adyuvante fueron tratadas con tamoxifeno durante 2 ó 3 años, y fueron incluidas en el estudio en el momento del cambio a IA debido al inicio de la menopausia. Estas pacientes fueron tratadas con IA (3 ó 2 años, respectivamente) hasta completar los 5 años de terapia adyuvante. Además, todas las participantes recibieron suplementos de calcio y de 25(OH) vitamina D3 (1.000 mg y 800 UI al día, respectivamente), y aquellas con deficiencia de vitamina D (<30 ng/ml) recibieron una dosis adicional de 16.000 UI de calcifediol oral ó 25.000 UI de colecalciferol oral cada 2 semanas. Las pacientes diagnosticadas de osteoporosis mediante densitometría ósea (absorciometría radiológica de energía dual, DXA), fracturas por fragilidad antes de iniciar IA, y/o una densidad mineral ósea (DMO) con una T-score <-2,0 más un factor de riesgo mayor para osteoporosis, iniciaron tratamiento con bisfosfonatos orales o denosumab en el caso de intolerancia digestiva o enfermedad gastroesófagica previa. Las pacientes mantuvieron dicho tratamiento durante todo el estudio.
Los criterios de exclusión fueron: alcoholismo, insuficiencia renal > grado 3b, artritis reumatoide, enfermedades metabólicas óseas diferentes a la osteoporosis, enfermedad de Paget, osteomalacia, hiperparatiroidismo primario, hipertiroidismo, diabetes mellitus insulinodependiente, tratamiento previo o en curso con antirresortivos, corticosteroides orales o cualquier otro fármaco que pudiera afectar el metabolismo óseo, excepto tamoxifeno.
El protocolo de estudio fue aprobado por el comité de ética del Parc de Salut Mar (2016/6803/I) y se llevó a cabo de conformidad con la Declaración de Helsinki. Se obtuvieron los consentimientos informados por escrito de todos los participantes después de haber leído la hoja de información del estudio y de haber respondido cualquier pregunta. En todo momento se respetaron los derechos de privacidad de los pacientes.
Datos y mediciones de las pacientes
Se recogió información de variables clínicas y demográficas en el momento del reclutamiento y durante el estudio, incluyendo la edad, la edad de menarquia y de menopausia, el índice masa corporal (IMC), dieta y hábitos de vida, quimioterapia y radioterapia previa, tamoxifeno previo, tratamientos antirresortivos, antecedentes familiares, caídas previas, niveles séricos de 25(OH) vitamina D (VitD) y paratohormona (PTH), así como los siguientes parámetros de remodelado óseo: propéptido aminoterminal del colágeno tipo I (P1NP), el isómero beta del telopéptido carboxiterminal del colágeno tipo I (β-CTX), osteocalcina y fosfatasa alcalina ósea. Antes del inicio y anualmente hasta después de un año de la finalización del tratamiento con IA, se midió la densidad mineral ósea (DMO) a nivel lumbar (CL L1–L4), cuello femoral (CF) y cadera total (CT), utilizando el densitómetro DXA QDR 4500 SL® (Hologic, Waltham, Massachusetts, EE.UU.). El coeficiente de variación para esta técnica en nuestro centro es del 1% en CL y del 1,65% en CF. Se excluyeron en el seguimiento aquellas imágenes que presentaban artefactos, enfermedad degenerativa del disco con osteofitos, artrosis con hiperostosis de las articulaciones facetarias, fracturas vertebrales y/o calcificaciones aórticas y todas aquellas que pudieran causar un falso aumento de la DMO, de acuerdo a la descripción de Blake y cols.9 Las fracturas incidentes fueron diagnosticadas por una radiografía (Rx) lateral de columna dorsal y lumbar por un médico especializado o por informe médico de otro centro. Se evaluó el riesgo de fractura a 10 años mediante la herramienta FRAX® en la plataforma, con acceso en: https://www.sheffield.ac.uk/FRAX/tool.aspx?lang=sp. Los umbrales de valores FRAX que se utilizaron para identificar personas con alto o bajo riesgo de fractura osteoporótica principal en población femenina española fueron: riesgo bajo, <5; intermedio, entre 5 y <7,5; y alto, ≥7,510; y para fractura de cadera se consideró de alto riesgo ≥3%11.
Análisis estadístico
Se estudió el riesgo de fractura mediante un análisis de supervivencia: se calculó el estimador de Kaplan-Meier, y se realizó un modelo de los riesgos proporcionales (regresión de Cox) entre usuarias y no usuarias de bifosfonatos, y entre pacientes con tamoxifeno previo o sin tamoxifeno, ajustando por covariables de riesgo. Se comprobó la proporcionalidad del riesgo en el tiempo. Las comparaciones entre grupos se realizaron mediante la Prueba T de Student o Chi-Cuadrado. Los análisis se realizaron con SPSS versión 23 y con R 3.5.3 utilizando los paquetes foreign, plyr, survminer, Hmisc, dplyr, ggplot2.
Resultados:
Un total de 943 pacientes postmenopáusicas en tratamiento con IA fueron incluidas en el estudio. De ellas, 51 pacientes (5,4%) sufrieron una fractura incidente (Figura 1). La mayoría de las fracturas ocurrieron durante el tratamiento con IA aunque el 21,5% ocurrieron durante el primer año después de finalizar la terapia. El 82,4% de las pacientes con fractura tomaron letrozol, el 15,7% exemestano y 1 paciente tomó anastrozol. La mayoría de fracturas incidentes detectadas fueron vertebrales (29,4%) y de Colles (31,4%) (Figura 1).

Figura 1. Diagrama de flujo de las pacientes con cáncer de mama tratadas con inhibidores de la aromatasa (cohorte B-ABLE) con fractura incidente
Las características de las pacientes con fractura se muestran en la tabla 1. La mayoría de pacientes con fractura (78,5%) estaban en el rango de sobrepeso (IMC >25-29,9 kg/m2) (n=17) u obesidad (IMC >30 kg/m2) (n=24). Todas las fracturas de húmero se produjeron en pacientes con un IMC >28 kg/m2. Solo 2 pacientes tenían bajo peso (IMC <18,5 kg/m2).
Tabla 1. Características de las pacientes en el momento de la fractura incidente
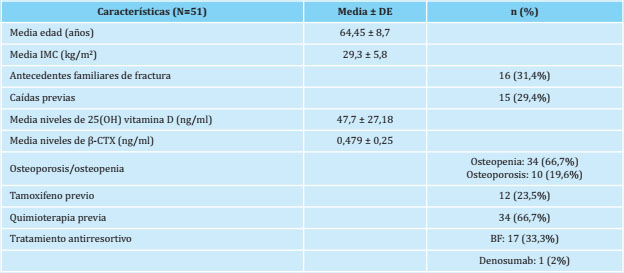
DE: desviación estándar; IMC: índice de masa corporal; BF: bifosfonatos.
Un 86,3% de las pacientes tenían diagnóstico de osteopenia u osteoporosis en el momento de la fractura, siendo un factor de riesgo clave para la fractura asociada a los IA. No se encontraron diferencias significativas en el riesgo de fractura entre pacientes con y sin tratamiento antirresortivo: HR=1,75 [IC 95%: 0,88 a 3,46] (Figura 2). Cabe destacar que las pacientes con fracturas incidentes tratadas con bisfosfonatos tenían un IMC significativamente menor que las pacientes con fractura y sin bisfosfonatos [media (DE): 26,4 (6,2) vs. 30,9 (5,2), respectivamente; p=0,01]. No se encontraron diferencias en los otros parámetros analizados: edad, quimioterapia previa y caídas previas.

Figura 2. Gráfico del riesgo acumulativo de eventos de fractura en grupos de estudio (con o sin tratamiento con antirresortivos óseos) según el riesgo de fractura. Los gráficos muestran las curvas de Kaplan-Meier que representan los resultados del estudio en términos de riesgos acumulativos. (A) durante el tratamiento con inhibidores de la aromatasa, (B) en el post-tratamiento
El 29,4% (n=15) de las pacientes habían tenido caídas previas a la fractura. De éstas, 6 tuvieron fractura vertebral y 8 fractura de Colles.
Del total de pacientes de la cohorte B-ABLE, 293 tomaron previamente tamoxifeno y el 4,1% de éstas sufrieron una fractura. Por otro lado, 650 no recibieron tamoxifeno previo y se fracturaron un 6% (Figura 3). No se encontraron diferencias significativas en el riesgo de fractura entre las pacientes que habían recibido tratamiento previo con tamoxifeno respecto las que no (HR=1,00 [IC 95%: 0,39 a 2,56]).

Figura 3. Gráfico del riesgo acumulativo de eventos de fractura en grupos de estudio (con o sin tratamiento previo con tamoxifeno) según el riesgo de fractura. Los gráficos muestran las curvas de Kaplan-Meier que representan los resultados del estudio en términos de riesgos acumulativos. (A) durante el tratamiento con inhibidores de la aromatasa, (B) en el post-tratamiento
Los niveles de VitD a tiempo basal tenían una media de 17,39±8,2 ng/ml. Todas las pacientes fueron tratadas con VitD al iniciar el tratamiento con IA, siendo la media de 48,69±42,11 ng/ml a los 3 meses de tratamiento. De esta manera, en el momento de la fractura incidente, todas las pacientes tenían niveles óptimos de VitD con una media de 47,7±27,18 ng/ml.
Según los valores de normalidad del isómero beta del telopéptido carboxiterminal del colágeno I (β-CTX) en el suero de mujeres sanas premenopáusicas en población española (0,064-0,548 ng/ml)12, el 33% de las pacientes con fractura tenían los niveles de β-CTX por encima de la normalidad. Además, si del total de las 51 pacientes con fracturas se excluyen aquellas en tratamiento con antirresortivos, la media de β-CTX se situaba en niveles por encima de la normalidad (0,585±0,228 ng/ml).
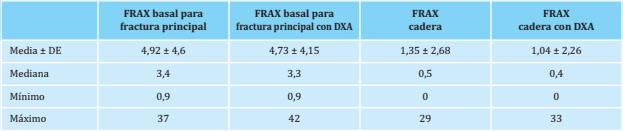
El cálculo del riesgo absoluto de fractura osteoporótica mayor y de cadera en los próximos 10 años, utilizando la herramienta FRAX® en las pacientes con fracturas incidentes, se muestra en la tabla 2. Se detectaron valores de FRAX de alto riesgo de fractura principal (≥7,5) y de fractura de cadera (≥3) en 13 y 8 pacientes, respectivamente (Figura 4). Además, al comparar las medias con las pacientes de la B-ABLE sin fractura incidente (Tabla 3), la media de FRAX en las pacientes con fractura era más elevada que las pacientes sin fractura.
Tabla 2. Valores de la herramienta FRAX® para el cálculo del riesgo de fractura a los 10 años en las pacientes con fractura de la cohorte B-ABLE

DE: desviación estándar; DXA: densitometría ósea.
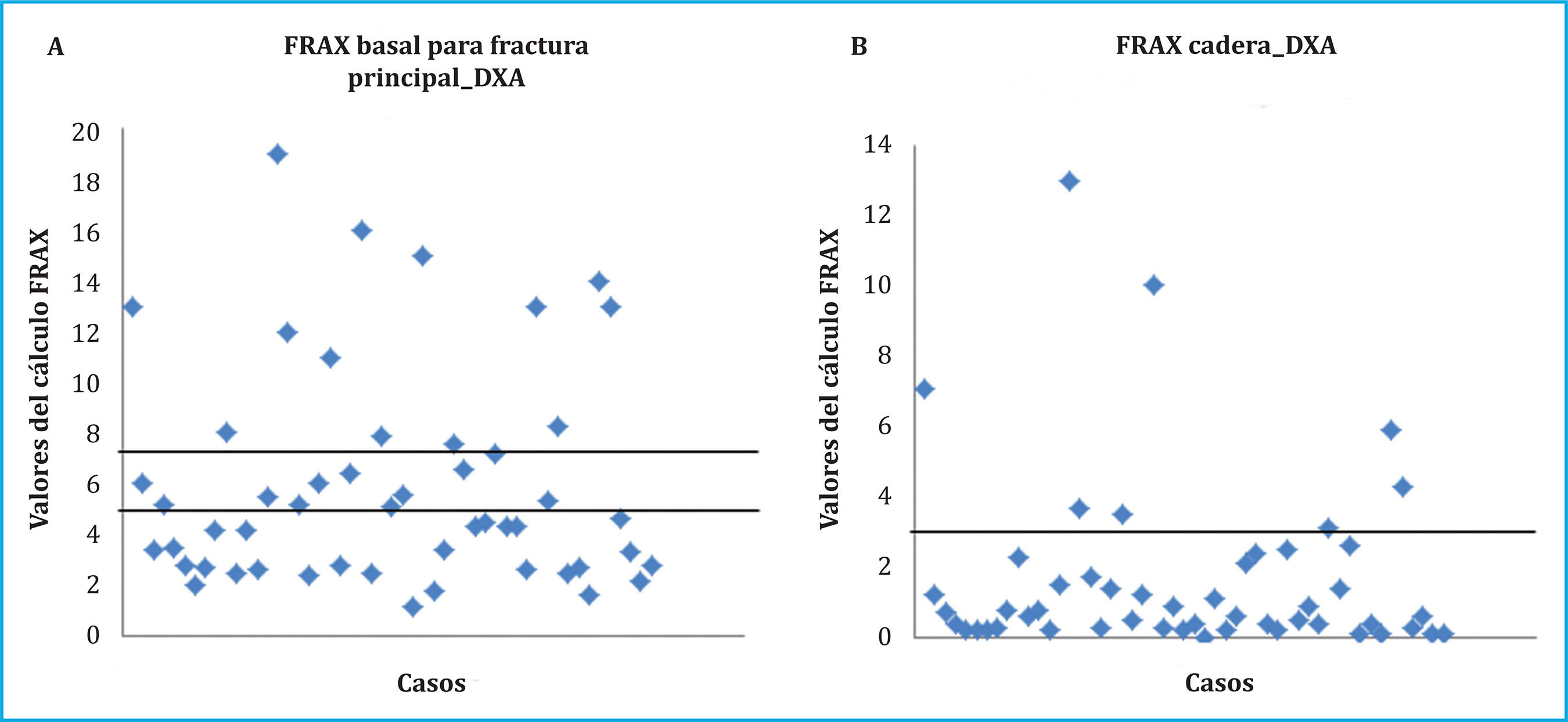
Figura 4. Valores de FRAX de cada paciente del estudio de: A) fractura principal y B) fractura de cadera, teniendo en cuenta la DMO. Las líneas horizontales de cada figura muestran el umbral establecido para el riesgo de fractura a 10 años. Los umbrales de FRAX basal para fractura principal fueron: riesgo bajo, <5; intermedio, entre 5 y <7,5; y alto, ≥7,5. Los umbrales de alto riesgo para fractura de cadera fueron ≥3
DISCUSIÓN
Los IA producen un efecto deletéreo en el tejido óseo que ya ha sido demostrado en los ensayos clínicos de referencia5. Sin embargo existen pocos datos de estudios prospectivos clínicos no aleatorizados en la clínica habitual. Este estudio se ha centrado en la evaluación de los factores de riesgo de fractura incidente en la cohorte B-ABLE, que incluye mujeres postmenopáusicas con cáncer de mama RE (+) tratadas con inhibidores de la aromatasa. El principal factor de riesgo detectado es el diagnóstico de osteopenia u osteoporosis seguido de los valores de β-CTX elevados. El sobrepeso también surgió como factor de riesgo para la identificación de pacientes con fractura de húmero. Asimismo, el cálculo del FRAX resultó útil para identificar algunos pacientes con alto riesgo de fractura principal y de cadera.
Todas las pacientes de la cohorte B-ABLE iniciaron tratamiento con suplementos de vitamina D desde el momento de su inclusión en el estudio si tenían valores por debajo de 30 ng/ml y, por consiguiente, en la mayoría de los casos los niveles de vitamina D se situaron en valores óptimos durante el periodo de la terapia con IA. De esta manera, el 86,3% de las pacientes tenían valores de vitamina D superiores a 20 ng/ml en el momento de la fractura situando una media en 47,7 ng/ml. Esto descarta niveles subóptimos de vitamina D como factor de riesgo de fracturas en estas pacientes. Cabe destacar que la mayoría de las pacientes (66,6%) tenían niveles menores de 20 ng/ml en el momento de iniciar la terapia con IA por lo que no podemos saber si estos bajos niveles podrían incidir en futuras fracturas. Además, las pacientes de alto riesgo de fractura a nivel basal se trataron con antirresortivos óseos desde el primer momento en que iniciaron la terapia con IA por lo que debido al tratamiento antirresortivo disminuían el riesgo de fractura, que se equiparaba así a la incidencia de fractura de las pacientes sin tratamiento con antirresortivos. Este dato está en consonancia con un estudio reciente en la cohorte SIDIAP (Sistema de Información para el Desarrollo de la Investigación en Atención Primaria), en el que las mujeres tratadas con bifosfonatos reducían significativamente su riesgo a padecer una fractura osteoporótica4. De todas maneras, más de un 30% de las fracturas se detectaron en pacientes en tratamiento con antirresortivos. De manera interesante, estas mujeres tratadas con bisfosfonatos tenían un IMC más bajo que las mujeres sin tratamiento antirresortivo.
Aunque es bien sabido que tener un historial de caídas previas es un predictor relevante del riesgo de la fractura osteoporótica13, la mayoría de las pacientes de nuestra cohorte (más de un 70%) no reportaron caídas previas a la fractura incidente. Cabe destacar que en las pacientes con fractura incidente durante el tratamiento con IA y que reportaron un historial de caídas, la fractura más frecuente fue la vertebral y/o fractura de Colles.
Tampoco se han detectado diferencias en el riesgo de fractura entre las pacientes con tratamiento previo con tamoxifeno y las que solo recibieron IA. Sin embargo, no se ha podido descartar un posible insuficiente tamaño muestral para detectar estas diferencias.
También se evaluó el riesgo de fractura con la herramienta FRAX a tiempo basal (previo tratamiento con IA) situando la mayoría de estas pacientes en niveles de riesgo intermedios/bajos en el momento que entran en el estudio. Una limitación de la herramienta es que no tiene en cuenta el tratamiento con inhibidores de la aromatasa, con lo que posiblemente el riesgo de fractura se encuentra infraestimado en nuestra cohorte. De todas maneras, el 25% de las pacientes con fractura tenían valores de alto riesgo con lo que este índice podría tenerse en cuenta a la hora de detectar pacientes de riesgo.
En conclusión, el diagnóstico de osteopenia u osteoporosis, junto con niveles elevados de β-CTX podría detectar pacientes tratadas con IA con riesgo alto de padecer una fractura incidente. El tratamiento previo con tamoxifeno parece no afectar al riesgo de fractura.











 texto en
texto en