La osteocalcina es una proteína sintetizada por el osteoblasto que fue identificada a finales de los años 70, y que en el humano contiene 49 aminoácidos1. Antes de ser liberada a la matriz extracelular, la osteocalcina sufre una gamma-carboxilación, al unirse en las posiciones 17, 21 y 24 el ácido gamma-carboxi-glutámico. En esta reacción interviene una gamma-carboxilasa y es necesaria la presencia de la vitamina K (Figura 1). La presencia de los dos grupos carboxilo provoca que la osteocalcina gamma-carboxilada tenga una gran afinidad por el calcio y que, al liberarse al medio extracelular, se una en gran proporción a la hidroxiapatita del hueso. En la circulación queda una parte de esta osteocalcina gamma-carboxilada y también osteocalcina no carboxilada2. Solo un 10-30% de la osteocalcina sintetizada alcanza la circulación, y el resto se queda unido a la matriz ósea. La osteocalcina no carboxilada representa 1/3 de la osteocalcina total. Durante la resorción, al destruirse la matriz ósea, parte de la osteocalcina que está unida al hueso pasa a la circulación2. La osteocalcina es únicamente sintetizada por los osteoblastos y es la proteína no colágena más abundante de la matriz extracelular y es la décima proteína más abundante en los vertebrados3. Desde el principio de su conocimiento sus niveles se correlacionaron con la formación ósea4. Para todos los investigadores del metabolismo del hueso supuso un avance contar con un nuevo marcador de formación ósea cuando los únicos marcadores de remodelado que se tenían hasta el momento eran la hidroxiprolina y la fosfatasa alcalina total. La isoenzima ósea de la fosfatasa alcalina también se podía medir por un método bastante complejo mediante electroforesis. La osteocalcina se ha utilizado durante muchos años como marcador de formación ósea en prácticamente todos los trabajos que se realizaban al respecto. Se utiliza menos desde el año 2011 en que la International Osteoporosis Foundation (IOF) y la International Federation of Clinical Chemistry and Laboratory Medicine (IFCC) recomendaron que se utilizaran el propéptido N-terminal del colágeno tipo I (PINP) como marcador de formación y el β-telopéptido C-terminal del colágeno tipo I o β-crosslaps (β-CTX) como marcador de resorción en los estudios clínicos sobre osteoporosis5.
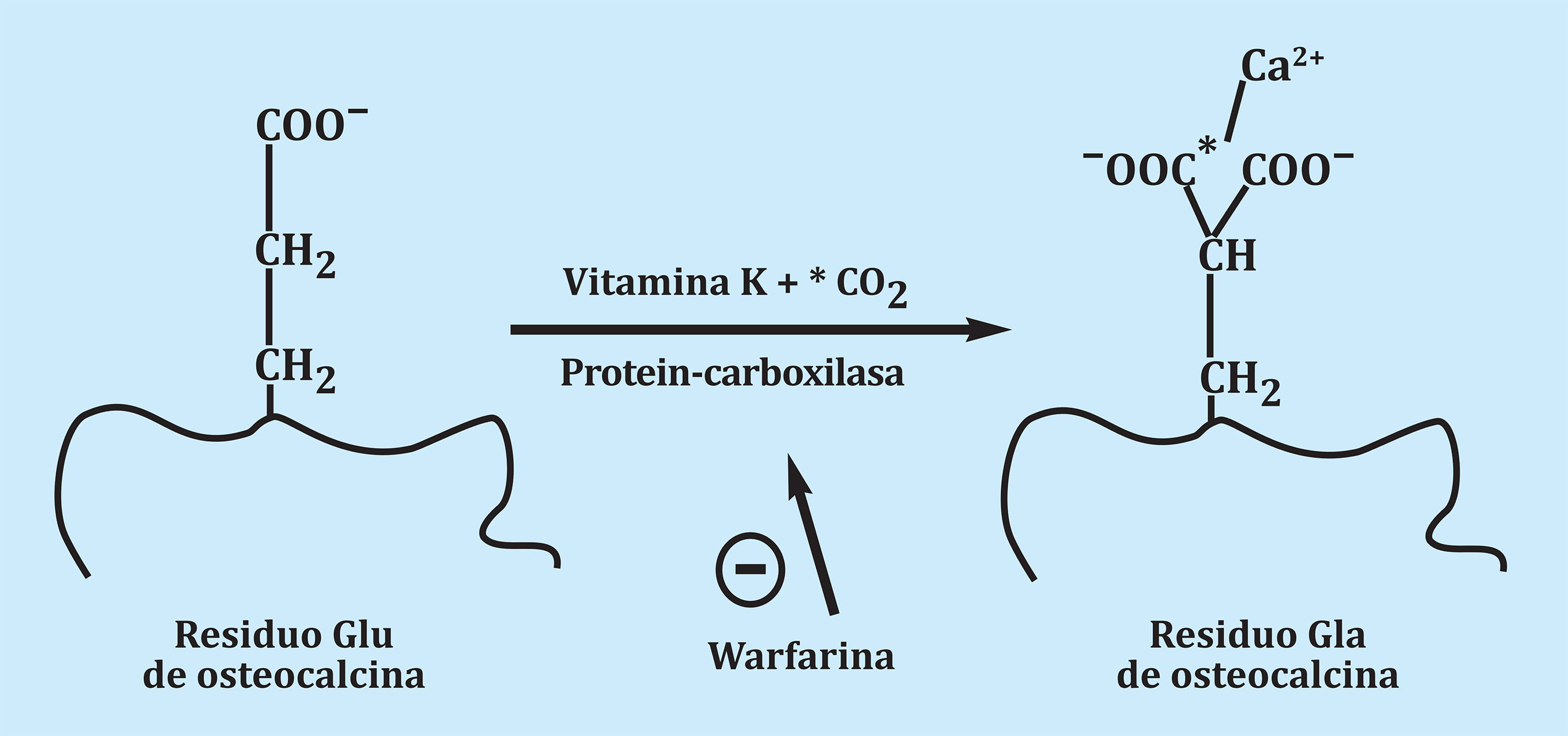
Figura 1. Mediante una carboxilación post-traslacional el ácido glutámico de la osteocalcina se transforma en ácido gamma-carboxi-glutámico. La presencia de los dos grupos carboxilos provoca una gran afinidad por la unión al calcio Ca2+ de la matriz extracelular
Durante muchos años y a pesar de su abundancia se ignoraba cuál era el papel de la osteocalcina en el organismo. Debido a su modificación post-traslacional se pensó que estaba implicada en la mineralización del hueso. Pero cuando se consiguieron ratones sin osteocalcina (osteocalcina-/-) se evidenció que estos mutantes presentaban una mineralización totalmente normal, por lo cual quedaba claro que la función de la osteocalcina no estaba relacionada con la mineralización ósea6.
El hueso contiene osteoclastos, células cuya función es destruir hueso, y esta destrucción activa del hueso mineralizado requiere energía7. La formación ósea también requiere energía8. Debido a ello, grupos de investigadores como Karsenty y cols.9,10 plantearon la hipótesis de que el modelado y remodelado óseo deben estar asociados a la regulación del metabolismo energético. Probablemente, la cantidad de energía de la destrucción activa del hueso es proporcional a la superficie ocupada por el mismo. Este requerimiento energético es probablemente muy elevado, puesto que la resorción ósea no se produce como un hecho aislado, sino en el contexto de que debe de haber una regulación coordinada de una función bifásica llamada modelado durante la infancia y remodelado en la vida adulta. Por ello, es por lo que los autores mencionados anteriormente plantearon la hipótesis de que el modelado y el remodelado óseo deben de estar unidos a la regulación del metabolismo energético. Esta visión de una regulación coordinada de la masa ósea y del metabolismo energético está apoyada por evidencias clínicas. Por ejemplo, el crecimiento longitudinal del hueso se detiene en los niños y la masa ósea desciende en los adultos con acceso severamente limitado a la comida (es decir, a la energía)11. Además, otro nexo de unión entre remodelado óseo y metabolismo energético es que la masa ósea siempre declina en ambos sexos cuando disminuye la función gonadal. Considerando estas observaciones, se llega a la conclusión de que debe haber una regulación coordinada del crecimiento/masa del hueso, metabolismo energético y reproducción9.
Anteriormente mencionábamos que los ratones (osteocalcina-/-) tenían los huesos mineralizados normalmente, pero desarrollan algunos fenotipos que solo pueden ser explicados, dado el sitio de síntesis de la osteocalcina y su abundancia, si esta molécula estuviera actuando como una hormona. En efecto, los ratones mutantes (osteocalcina-/-) tenían más grasa visceral que los controles y además tenían menos crías. El estudio sistemático de estos fenotipos estableció que el hueso debía de ser un órgano endocrino y que la hormona que segrega, la osteocalcina, afecta al metabolismo energético y a la fertilidad. Es decir, que existe una regulación coordinada, endocrina en naturaleza del metabolismo energético y la reproducción. Una parte fundamental es que el hueso sería un órgano endocrino y no el receptor de la acción de las hormonas.
En este momento, el conocimiento de los mecanismos de acción de la osteocalcina en sus órganos diana es un trabajo que se está desarrollando. Por ejemplo, la adiposidad aumentada de los ratones (osteocalcina-/-) podría estar asociada a un descenso en el gasto energético y no a un incremento del apetito (otra función regulada por el hueso). La base molecular de este fenómeno no ha sido descubierta todavía10.
OSTEOCALCINA Y HOMEOSTASIS DE LA GLUCOSA
En un estudio de Wei y cols.9, en el que cultivaron osteoblastos de ratón con islotes pancreáticos, se observó que había un aumento de la expresión de insulina en los islotes. Los osteoblastos no incrementaban la expresión de ninguna otra hormona segregada por los islotes pancreáticos. Cuando se añadía osteoblastos procedentes de ratones (osteocalcina-/-) no se producía esta expresión de insulina. Así se demostró que los osteoblastos son células endocrinas que regulan la expresión de insulina y que la osteocalcina es la hormona responsable de esta acción. También se observó que los ratones (osteocalcina-/-) con una dieta normal eran hiperglucémicos e hipoinsulinémicos. La secreción de insulina estaba disminuida en ausencia de osteocalcina.
En este mismo estudio, un test de tolerancia a la glucosa demostró que los ratones (osteocalcina-/-) eran intolerantes a la glucosa porque tenían un descenso en la expresión de insulina. Wei y cols.9 expresaron que el hecho de que la osteocalcina regule el metabolismo de la glucosa no es sinónimo de que el hueso sea el origen de la diabetes. Simplemente, aumenta el panorama de regulación del metabolismo de la glucosa.
Investigaciones llevadas a cabo en ratas con dieta normal muestran que la osteocalcina es necesaria y suficiente para promover la proliferación de las células β en los islotes pancreáticos, para promover la expresión y la secreción de insulina y para favorecer la captación de glucosa en los tejidos periféricos y por lo tanto la homeostasis de la glucosa12.
El receptor que media la señal de la osteocalcina en las células β-pancreáticas y otros tejidos periféricos es un receptor acoplado a la proteína G denominado GPR6a13. La eliminación específica de genes y otros experimentos de genética han establecido que, in vivo, la osteocalcina es, sin lugar a dudas, el ligando que explica la regulación de la homeostasis de la glucosa a través del GPR6a10. La importancia biológica de la regulación de la osteocalcina en la homeostasis de la glucosa se ha verificado en ratones normales alimentados con una dieta alta en grasas. La osteocalcina exógena rescata casi completamente la intolerancia a la glucosa de estos animales14.
Era muy importante saber si estas acciones las producía la osteocalcina carboxilada o la descarboxilada. En las bacterias no existe gamma-carboxilación y así se pudo producir osteocalcina bacteriana recombinante que no estaba gamma-carboxilada. Esta osteocalcina nocarboxilada fue capaz de inducir expresión de insulina en los islotes pancreáticos, indicando que la forma no carboxilada de la osteocalcina es la que actúa como hormona9.
Los osteoblastos tienen en su superficie receptores de la insulina, y es de gran interés que la insulina y la osteocalcina están implicadas en un loop regulador, de tal modo que la señal de la insulina en los osteoblastos es necesaria para la buena homeostasis de la glucosa en todo el organismo9.
Los ratones que no tienen receptores de la insulina en los osteoblastos, cuando toman una dieta normal, sufren un descenso en la forma circulante activa de la osteocalcina, un descenso en la secreción de insulina, intolerancia a la glucosa y resistencia a la insulina. La señal de la insulina sobre los osteoblastos inhibe la expresión de osteoprotegerina y favorece la resorción ósea. El bajo pH que se produce bajo los osteoclastos favorece la formación de osteocalcina descarboxilada, que es la forma activa de la osteocalcina. Esta osteocalcina activa vuelve a actuar sobre las células β-pancreáticas y se forma nueva insulina que vuelve a actuar sobre el osteoblasto y comienza de nuevo el ciclo (Figura 2)15.

Figura 2. Ciclo osteocalcina-insulina. La osteocalcina descarboxilada, forma activa, se une al receptor GPRC6a de las células ß pancreáticas, provocando la liberación de insulina. La insulina se une entonces al receptor de la insulina en el osteoblasto, provocando una disminución de la síntesis de osteoprotegerina y un aumento de la resorción ósea. En el ambiente ácido del osteoclasto, la osteocalcina inactiva, gamma carboxilada, se convierte en activa, nocarboxilada. La osteocalcina activa vuelve a comenzar el ciclo uniéndose a las células ß de los islotes pancreáticos
OSTEOCALCINA Y MÚSCULO ESQUELÉTICO
Una simple inyección de osteocalcina exógena inmediatamente antes del ejercicio o la administración crónica de esta hormona durante 1 mes, no solo incrementa la capacidad de ejercicio de los ratones jóvenes sino también restaura la capacidad de ejercicio de los ratones de más edad16. Al mismo tiempo que incrementa la fuerza muscular en los ratones de edad, la administración crónica de osteocalcina favorece la ganancia en masa muscular17. Es decir, que la osteocalcina exógena es no solamente necesaria sino suficiente para revertir el descenso en la capacidad de ejercicio y en la masa muscular observada en los ratones de más edad18.
La señal de la osteocalcina sobre el músculo esquelético se realiza a través del receptor GPR6a18. Se ha observado que la osteocalcina regula la captación y catabolismo de nutrientes en el músculo durante el ejercicio. La glucosa que es el principal nutriente utilizado por el músculo esquelético para generar energía durante el ejercicio se almacena en las miofibras en forma de glucógeno. La degradación del glucógeno en el músculo esquelético durante el ejercicio es menor en los ratones que no tienen el receptor GPR6a y en los ratones (osteocalcina-/-), demostrando que la osteocalcina favorece la glucogenolisis.
También se ha observado que la acumulación de intermediarios del ciclo tricarboxílico en el músculo esquelético que se ve en los ratones después del ejercicio no se observa en los ratones (GPR6a-/-), lo que indica que no hay entrada de ATP procedente del ciclo tricarboxílico. Durante un periodo largo de ejercicio, cuando los animales terminan su reserva de glucógeno, la captación y catabolismo de los ácidos grasos se incrementa en el músculo esquelético19. La osteocalcina favorece la oxidación de los ácidos grasos en las miofibras. La señal de la osteocalcina en las miofibras promueve la captación y el catabolismo de la glucosa y de los ácidos grasos durante el ejercicio, por eso se observa un descenso de actividad física en los ratones (osteocalcina-/-) y (GPR6a-/-) cuando se comparan con los controles20.
Se conoce desde hace décadas que el ejercicio induce cambios en el sistema inmune21. La interleucina 6 (IL6) fue la primera molécula que se vio que se liberaba a la sangre en respuesta a la contracción muscular22. La IL6 promueve la captación de glucosa y la oxidación de los ácidos grasos en el músculo esquelético, aumentando la producción de glucosa en el hígado y la lipolisis en el tejido adiposo23.
El ejercicio induce la resorción ósea y la producción de osteocalcina bioactiva. Los ratones (IL6-/-) después del ejercicio no aumentan los marcadores de resorción ósea ni la osteocalcina bioactiva, como pasa en ratones sanos. Esto sugiere la existencia de un loop entre el hueso (vía osteocalcina) y el músculo (vía IL6) que promueve la adaptación al ejercicio20. Así pues:
- La osteocalcina aumenta la captación de nutrientes y su catabolismo en el músculo esquelético.
- La osteocalcina aumenta la secreción de IL6 en el músculo esquelético. Esto da lugar a la generación de glucosa extra-muscular y ácidos grasos24.
- La IL6 aumenta la producción de osteocalcina bioactiva20.
La IL6 y la osteocalcina regulan aspectos similares del metabolismo esquelético durante el ejercicio, incrementando la glucosa y el catabolismo de los ácidos grasos. Pero, ¿actúa la osteocalcina independientemente de la IL6 en estos procesos? Mera y cols.16 estudiaron la acción de la osteocalcina sobe un cultivo de miofibras en ratones normales y ratones (IL6-/-). La osteocalcina indujo estas funciones en los dos tipos de cultivo, lo que revela que la IL6 no es requerida para la acción catabólica de la osteocalcina en el músculo esquelético.
La identificación de un puente entre el hueso, vía osteocalcina, y el músculo esquelético, vía IL6, que es necesario y suficiente para promover la adaptación al ejercicio en animales jóvenes y mayores, representa un avance significativo en nuestro conocimiento de cómo el sistema muscular esquelético controla una función que es esencial para la supervivencia de todos los vertebrados20.
La osteocalcina es necesaria para el desarrollo del cerebro y para su funcionamiento. Su ausencia en ratones produce un profundo déficit en el conocimiento espacial y la memoria y una exacerbación de la ansiedad. La ostecalcina podría prevenir el descenso de conocimientos debido a la edad25.
El factor neurotrófico BDNF, una molécula muy conocida que participa en la memoria, dependiente del hipocampo, es el mediador de la regulación de la osteocalcina sobre la función cognitiva26. La osteocalcina no carboxilada es capaz de estimular la dinámica del transporte de vesículas de BDNF hacia la sipnasis en las neuronas de ratas25.
Khrimian y cols.27 identificaron el receptor que traslada la señal de la osteocalcina a las neuronas. Es el Gpr158, un receptor unido a la proteína G expresado en las neuronas en la región CA3 del hipocampo, que transmite la señal de la osteocalcina a través del inositol 1,4,5-trifosfato y un factor neurotrófico derivado del cerebro. Esto es muy importante de cara a futuras acciones terapéuticas.
OSTEOCALCINA Y FERTILIDAD MASCULINA
La osteocalcina descarboxilada actúa sobre las células de Leydig de los testículos favoreciendo la biosíntesis de testosterona28. La osteocalcina descarboxilada actúa a través del receptor GPRC6a, al igual que lo hacía sobre las células β-pancreáticas.
Tambien se ha demostardo que la osteocalcina actúa vía un eje páncreas-hueso-testículos que regula, independientemente y en paralelo al eje hipotálamo-pituitaria-testículos, la función reproductiva masculina, promoviendo la biosíntesis de testosterona29.
OSTEOCALCINA Y ESTEATOSIS HEPÁTICA
En ratones con una dieta rica en grasa, inyecciones diarias de osteocalcina de 3 ó 30 ng/g de peso/día restauran par-En la “paradoja calcificación ósea-vascular” existe una elevada calcificación en los vasos, conduciendo a rigidez arterial y enfermedad cardio-vascular y una reducida calcificación en el hueso que conduce a osteoporosis y fractura ósea. Ésto conduce a la hipótesis de que los desórdenes en el metabolismo óseo y los cardiovasculares podrían tener vías patogénicas comunes, conduciendo a la expresión “eje óseo-vascular”30. Varias moléculas parecen jugar un papel en este eje, y una de ellas sería la osteocalcina.
Rashdan y cols. mantienen la hipótesis de que la osteocalcina regula la calcificación de las células del músculo liso vascular31. La inmunohistoquímica revela la co-localización de la osteocalcina con la calcificación de las células del músculo liso vascular en placas calcificadas de arterias carótidas. La implicación de la osteocalcina en el desarrollo de arteriosclerosis está avalada por un reciente metaanálisis de Millar y cols.32, en el que se observa una relación entre la osteocalcina y los marcadores de arterioesclerosis en muestras histológicas. En este mismo estudio, los autores no encontraron diferencias entre los niveles de osteocalcina en pacientes con y sin eventos vasculares. Es decir, que la osteocalcina parece ser un marcador sólo del proceso de calcificación.
OSTEOCALCINA EN HUMANOS
Hasta ahora, toda la revisión realizada sobre el papel de la osteocalcina como hormona se ha centrado en experimentos en ratones o ratas. Resulta de extraordinaria importancia conocer si estos hechos se pueden trasladar al humano, con las implicaciones clínicas que ello conllevaría.
Una revisión sistemática de la literatura realizada entre el año 2007 y el 2014 identificó 82 estudios que observaban que los niveles séricos de osteocalcina descarboxilada o total se correlacionan negativamente con la glucosa sanguínea, la resistencia a la insulina, la obesidad o marcadores del síndrome metabólico. Más aún, algunos de los datos obtenidos en humanos apoyan un papel de la osteocalcina en la secreción de insulina33.
Se ha observado que el tratamiento con bifosfonatos desciende la osteocalcina no carboxilada en el suero y que los niveles de la misma y/o los marcadores de la sensibilidad o la secreción de insulina se correlacionan positivamente con los marcadores de resorción ósea en humanos34.
Se ha visto también que pacientes con una forma dominante de osteopetrosis debido a un defecto en la actividad del osteoclasto se caracterizan por niveles descendidos de osteocalcina descarboxilada e hipoinsulinemia15.
Cambios en los niveles de osteocalcina, siguiendo tratamientos con bifosfonatos, se asocian con cambios en la masa y la grasa corporal35.
Oury y cols. analizaron una cohorte de pacientes con fallo testicular, e identificaron 2 individuos con una variante en uno de los dominios del GPRC6a. Estos pacientes presentaban intolerancia a la glucosa y resistencia a la insulina36.
Se han comparado los niveles de osteocalcina entre pacientes con diabetes mellitus tipo 2 y población no diabética, teniendo los diabéticos menores niveles de osteocalcina37. Los pacientes con síndrome metabólico también tienen menos niveles de osteocalcina total que los individuos sanos. Además existe una correlación entre osteocalcina total y descarboxilada con marcadores del estado glicémico y otros parámetros cardio-metabólicos38. Estos autores señalan la necesidad de profundizar en estos hallazgos y su posible participación en la salud humana, así como analizar su posible potencial terapéutico.
Un estudio observacional evaluó la asociación entre niveles séricos de osteocalcina y capacidad de conocimiento en adultos sanos, demostrando que se correlaciona positivamente con medidas de conocimiento global en mujeres ancianas39. En niños y adolescentes con hígado graso no alcohólico, la concentración de osteocalcina se correlaciona inversamente con las enzimas hepáticas y con la severidad de la enfermedad40.
Smith y cols., en un trabajo realizado en 202041, han estudiado los valores normales de osteocalcina descarboxilada y carboxilada en hombres adultos. Estos valores deberían ser introducidos en futuros estudios en los ensayos clínicos y asociarlos a la predicción de sucesos como fracturas o riesgo de diabetes. La cantidad de evidencias sobre los efectos multiorgánicos de la osteocalcina descarboxilada, apoyados en los hechos demostrados in vivo e in vitro, señalan la necesidad de profundizar en estos hallazgos y su posible participación en la salud humana, así como analizar su posible potencial terapéutico.
CONCLUSIONES
Resultan verdaderamente sorprendentes los descubrimientos que se han hecho estos últimos años sobre el papel de la osteocalcina como hormona y del hueso como órgano endocrino. La osteocalcina, que para los investigadores del metabolismo óseo era simplemente un marcador de formación ósea sin ninguna función conocida.
En ratones, la osteocalcina está implicada en la homeostasis de la glucosa, en el funcionamiento del músculo esquelético, en el desarrollo cerebral, en la esteatosis hepática, en la fertilidad masculina y en la calcificación arterial.
Empezamos a conocer trabajos que parecen anticipar que esto podría suceder también en el hombre.
Resulta de extraordinaria importancia abordar este tipo de investigación en el humano, porque si lo sucedido en el hombre fuera semejante a lo que ocurre con la osteocalcina en los ratones, las implicaciones terapéuticas de este compuesto serían extraordinariamente interesantes.











 texto en
texto en 


