INTRODUCCIÓN
El sistema óseo depende de un equilibrio entre la formación y la reabsorción ósea. Cuando este equilibrio se ve interrumpido por un traumatismo en forma de fractura ósea, este tejido tiene la capacidad de autorrenovación (1). En este proceso de cicatrización, intervienen distintos tipos celulares, matrices extracelulares y moléculas de señalización (2), a lo largo de las tres principales fases que tienen lugar: fase de inflamación, fase reparativa y fase de remodelado. En la fase reparativa, las células osteoprogenitoras y las células mesenquimales indiferenciadas son inducidas a diferenciarse a osteoblastos, en lugar de a otros tipos celulares, como los adipocitos (3). Además, en el proceso regenerativo es fundamental la formación de nuevos vasos sanguíneos que aporten el oxígeno y nutrientes necesarios para la formación ósea (2). Sin embargo, en algunos casos, pueden producirse retrasos en la cicatrización, fracturas no consolidadas o enfermedades óseas (osteoporosis, osteonecrosis o cáncer). Las cuales, presentan una morbilidad significativa y merman sustancialmente la actividad y calidad de vida de los pacientes que las sufren. Por ello, es necesario nuevas estrategias terapéuticas que puedan reducir la inmovilización prolongada o las intervenciones quirúrgicas repetidas. Estas podrían además suponer un coste significativo para los sistemas sanitarios y la sociedad (4).
Recientes avances en la ingeniería de tejidos han propuesto la combinación de diferentes tipos celulares con biomateriales sintéticos, como alternativa a los injertos óseos. Concretamente, las células madre estromales mesenquimales (MSC) derivadas de médula ósea, han sido propuestas para tratar diversas patologías, debido a su capacidad de diferenciación, regenerativa e inmunomoduladora (5). Sin embargo, aunque pueden obtenerse de terceros donantes, la posibilidad de la persistencia de las MSC implantadas en los pacientes receptores o la formación de tejidos ectópicos han frenado su aplicación para la curación de lesiones óseas (6). Además, entre otras limitaciones para su aplicación se encuentran la dificultad para mantener una potencia y viabilidad óptima durante la expansión celular, y la forma de administración al paciente (7). Estudios recientes han revelado que el potencial de las MSC en la regeneración tisular está ligado a su actividad paracrina, la cual, depende en parte, de las vesículas extracelulares (VE) derivadas del secretoma. Así, se ha propuesto el uso de estas VE en medicina regenerativa como una estrategia terapéutica libre de células (8).
Las VE tienen una función de comunicación intercelular y contienen gran variedad de moléculas biológicamente activas, como proteínas, lípidos y distintos tipos de ácidos nucleicos que pueden ser relevantes en la respuesta inflamatoria y en la regeneración tisular a través de señales que se transmiten a células receptoras (9). En función de su tamaño, las VE pueden ser clasificadas como microvesículas, exosomas y cuerpos apoptóticos. Concretamente, los exosomas, oscilan entre 40 y 100 nm, tienen un origen endosomal y son liberados por exocitosis de cuerpos multivesiculares a través de membranas plasmáticas (7). Así, pueden ser administrados por vía intravenosa y circular a través de fluidos corporales, como la sangre, la orina o la saliva (10). Estos exosomas parecen transmitir los efectos terapéuticos de la célula de origen, a la vez que solventan las limitaciones propias del uso de células en medicina regenerativa (7,9). Pueden ser aislados de múltiples fluidos corporales como semen, sangre, orina, saliva, leche materna, líquido amniótico, ascítico o cefalorraquídeo y bilis (11). El contenido de estas VE circulantes depende del estado del organismo, por lo que son una fuente de biomoarcadores y de factores que pueden ser utilizados incluso para aplicaciones terapéuticas, como alternativa a la VE derivadas de MSC. Efectivamente, la utilización de VE de MSC supone la manipulación de cultivos celulares in vitro, lo cual puede provocar pérdida de propiedades de las MSC e inestabilidad genética al efectuarse fuera de su nicho natural (12). Esto puede ser evitado en parte mediante líneas estables e inmortalizadas de MSC obtenidas por manipulación genética, induciendo por ejemplo la expresión de la telomerasa transcriptasa inversa humana (hTERT). Este procedimiento ha producido MSC con una alta capacidad de proliferación y expansión, manteniendo sus propiedades inmunomoduladoras, de diferenciación y regenerativas (13,14). Aunque diversos estudios en animales han mostrado que con el tiempo MSC inmortalizadas no se transforman en células tumorales y por lo tanto concluyen que pueden ser consideradas como seguras para su posible uso clínico, estos estudios tienen ciertas limitaciones. Entre ellas se encuentran la falta de ensayos clínicos y el desconocimiento aún sobre si las MSC inmortalizadas pueden acumular mutaciones no deseadas tras largos periodos de expansión. Por ello, se ha sugerido que el uso de estas células, tanto en terapia celular como en terapia libre de células basada en el uso de VE, debe estar sujeto a controles estrictos durante su cultivo (15). Esto aumenta la complejidad del procedimiento debido a la necesidad de mantener las líneas de MSC estables y el diseño de biorreactores para la producción a gran escala de VE. Por ello es interesantes estudiar otras fuentes alternativas de VE con capacidad regenerativa, entre las que se encuentran las VE circulantes en sangre, las cuales pueden ser obtenidas sin necesidad de expandir y mantener células en cultivo (16). Además, la cantidad de VE obtenidas en plasma, puede ser entre 10 y más de 100 veces superior a la obtenida a partir de cultivos celulares (17). Una posible fuente es la sangre de cordón umbilical. La cual tiene una composición similar a la de la médula ósea en adultos, pero a diferencia de esta, también contiene una serie de células inmunosupresoras, que le permite reducir los niveles de citoquinas inflamatorias (18). En humanos se ha observado que las VE derivadas de sangre de cordón umbilical (veCU), en relación con las de sangre periférica de adultos (veAD), poseen una mayor expresión de miRNA involucrados en el embarazo, la supresión de la leucemia, la inhibición de la inflamación, la movilidad celular y el desarrollo del sistema nervioso, además de factores relacionados con el desarrollo embrionario (19,20), lo que sugiere un alto potencial regenerativo. En cuanto a las veAD, diversos estudios han mostrado su potencial terapéutico para el tratamiento de procesos isquémicos y cicatrización de heridas (21). Así, el objetivo del presente estudio ha sido evaluar los potenciales efectos veCU y veAD sobre la angiogénesis de células endoteliales y la diferenciación osteoblástica y adipogénica de MSC.
MATERIAL Y MÉTODOS
EXTRACCIÓN DE VESÍCULAS EXTRACELULARES DE PLASMA SANGUÍNEO
Tras firma de consentimiento informado, mujeres sanas, sin patologías crónicas y en edad adulta (entre 26 y 31 años) fueron sometidas a una única extracción de sangre. La sangre de cordón umbilical fue donada por madres que cumplían los mismos criterios de inclusión que las adultas sanas, y del mismo modo, firmaron su consentimiento de participación.
Las muestras de sangre se centrifugaron a 3000 rpm 10 minutos para la obtención del plasma. Un mililitro de plasma se pasó por columnas de cromatografías de exclusión de tamaño PURE-EVs (HansaBioMed Life Sciences Ltd.) utilizando disolución salina tamponada con fosfato (PBS) como vehículo. Los 3 mililitros en los que eluyeron las VE se concentraron mediante ultrafiltración con concentradores de 10 MWCO (Vivaspin 6 centrifugal concentrator, Sartorius) hasta un volumen de 300-350 µl que se almacenaron a -20 °C hasta su uso. La concentración y tamaño de los exosomas obtenidos de cada muestra se determinaron con un analizador de seguimiento de nanopartículas (Nanosight NS300) basado en la tecnología "Nanoparticle Tracking Analysis" (NTA) en el Instituto Universitario de Nanoquímica (IUNAN) de la Universidad de Córdoba.
CARACTERIZACIÓN DE LAS VE MEDIANTE WESTERN BLOT
Las VE se caracterizaron mediante Western blot. Para ello, 10 ug de cada muestra fueron cargados en un gel de acrilamida 8-16 % (nUView Tris-Glycine Precast Gels, NuSeP) en condiciones desnaturalizantes y separados por electroforesis usando el sistema "Mini-Protean" (Bio-Rad). Tras ello, las proteínas se transfirieren a una membrana de difluoruro de polivinilidina (PVDF) (Bio-Rad) mediante Trans-Blot Tranfer System (Bio-Rad). La membrana fue bloqueada con una solución al 5 % de leche desnatada en polvo en tampón TTBS (20 nM Tril-CL pH 7.6, 150 mM NaCl, 0,05 % Tween) durante 1 h a temperatura ambiente y se incubó a 4 °C durante toda la noche, con los anticuerpos primarios anti-CD81 (25kDa, 1:500; ref.: 10630D), CD9 (25kDa, 1:1000; ref.: 10626D) y anti-CD63 (30-60 kDa, 1:1000; ref.: 10628D), todos ellos en 1 % en leche con TTBS. Tras ello, se lavó con TTBS y se incubó durante 1h con el anticuerpo secundario anti-mouse (1:4000; ref.: 32430), en 2 % de leche con TTBS. Todos los anticuerpos utilizados fueron de Invitrogen, ThermoFisher Scientific. La detección se realizó utilizando el sustrato quimioluminiscente Clarity Western ECL Substrate (Bio-Rad) y las imágenes se adquirieron con el sistema ChemiDoc™ XRS+ (Bio-Rad) mediante el software Image Lab 6.1 del mismo fabricante.
CULTIVOS CELULARES DE MSC Y HUVEC
Las MSC utilizadas se aislaron a partir de células mononucleares criopreservadas comerciales (Stemcell Technologies, Colonia, Alemania) según el protocolo descrito previamente por nuestro grupo (22). Fueron expandidas en medio esencial mínimo alfa (αMEM) de Biowest (Nuaillé, Francia), que contenía 2 mM de ultraglutamina (Biowest), 10 % de suero bovino fetal (FBS; Gibco-Thermo Fisher Scientific), 100 U de penicilina, 0,1 mg de estreptomicina/ml y 1 ng/ml de factor de crecimiento de fibroblastos (FGF-2) de Sigma-Aldrich (Saint Louis, MO, EE. UU.). Las células endoteliales de vena de cordón umbilical (HUVEC) de Lonza (Basilea, Suiza) fueron crecidas en medio basal endotelial (EBM), con suplementos y factores de crecimiento, conocido como medio de crecimiento endotelial (EGM) de Lonza. Este contenía 10 % de FBS, hidrocortisona, gentamicina, factor de crecimiento epidérmico humano (hEGF) y extracto de cerebro bovino.
Tanto los cultivos de MSC como de HUVEC se incubaron a 37 °C con 95 % de humedad y 5 % de CO2. Cuando alcanzaron el 90 % de confluencia, las células fueron levantadas con tripsina-EDTA (Gibco) y sembradas en placas de cultivo (Nalgene-Nunc-Thermo Fisher Scientific) de 12 (P12), 24 (P24) o 96 pocillos (P96) para los diferentes experimentos.
ENSAYO DE VIABILIDAD CELULAR
La viabilidad celular se determinó utilizando el ensayo de bromuro de 3-(4,5-dimetiltiazolil-2)-2,5-difeniltetrazolio (MTT; Sigma-Aldrich). Las MSC y HUVEC se sembraron en P96, a una densidad de 4000 y 8000 células por pocillo, respectivamente, en el medio de cultivo correspondiente a cada tipo celular, según lo descrito en el apartado anterior. Tras 24 horas, el medio se sustituyó por medio con FBS libre de exosomas, suplementado con distintas concentraciones de veCU o veAD (10 × 106, 20 × 106, 40 × 106, 80 × 106 y 160 × 106 partículas/ml). Después de 72 h, se retiró el medio y se añadieron 50 µl/pocillo de medio de Eagle modificado por Dulbecco (DMEM) sin rojo fenol suplementado con 1 mg de MTT/ml (ambos de Sigma-Aldrich). Después de 2 h de incubación, el medio fue retirado y, los cristales de formazán producidos, disueltos en isopropanol. En la solución resultante, se midió la absorbancia a 570 nm, utilizando la absorbancia a 650 nm como referencia, con un espectrofotómetro de microplacas PowerWave XS de BioTek Instruments (Winooski, VT, EE. UU.).
ENSAYO DE MIGRACIÓN CELULAR
La migración se estudió mediante el ensayo Scratch en P24. En cultivos en confluencia, se generó una zona libre de células utilizando la punta de una pipeta P200, y se adicionaron al medio distintas concentraciones de veCU o de veAD (10 × 106 y 160 × 106 partículas/ml). Los cultivos se mantuvieron hasta 24 h, obteniendo imágenes a distintos tiempos a través de un IncuCyte Zoom Imain System, Sartorius. Imágenes a 18 y 15 h de migración para MSC y HUVEC, respectivamente, fueron analizadas con el software ImageJ V1.53f51 (NIH; Bethesda, MD, USA). Los tiempos fueron seleccionados debido a que en tiempos posteriores la zona libre de células había sido totalmente ocupada por las células, lo que impedía identificar diferencias entre tratamientos. La migración se cuantificó en relación al porcentaje del área inicial no ocupada por las células.
DIFERENCIACIÓN DE MSC A OSTEOBLASTOS Y ADIPOCITOS
En cultivos de MSC al 60-80 % de confluencia, se indujo la diferenciación a osteoblastos o adipocitos. La diferenciación osteoblástica se mantuvo durante 21 días en medio suplementado con 10 nM de dexametasona, 0,2 mM de ácido ascórbico y 10 mM de β-glicerolfosfato (Sigma-Aldrich), en presencia o ausencia de las distintas concentraciones de VE evaluadas (10 × 106 y 160 × 106 partículas/ml). Por otro lado, la diferenciación hacia adipocitos fue inducida con 500 nM de dexametasona, 0,5 mM de isobutilmetilxantina y 50 µM de indometacina (todos de Sigma-Aldrich), manteniéndose durante 14 días, en presencia o ausencia de las distintas concentraciones de VE.
TINCIONES CITOQUÍMICAS
La tinción con rojo de alizarina a los 21 días de la diferenciación osteoblástica se utilizó para la visualización y cuantificación de la mineralización de la matriz extracelular. Cultivos en P12 se fijaron con formaldehído al 3,7 % durante 10 min y posteriormente fueron teñidos con 40 mM de rojo de alizarina en agua, pH 4,15 (Sigma-Aldrich) durante 10 min. A continuación, los pocillos se lavaron varias veces con isopropanol al 60 %, se secaron y se visualizaron con microscopio óptico. Las mediciones de depósitos de rojo de alizarina se llevaron a cabo después de la elución con ácido acético al 10 %, la neutralización con hidróxido de amonio al 10 % y la cuantificación por espectrofotometría a 405 nm de absorbancia de la solución resultante.
La formación de vesícula de grasa en los cultivos inducidos a diferenciarse en adipocitos se evaluó mediante tinción Oil Red O. Para ello, las células se fijaron con formaldehído 3,7 % durante 15 min, se lavaron con 60 % de isopropanol en agua y se tiñeron durante 15-20 min con una solución del 0,3 % de Oil Red O (peso/volumen) en 60 % de isopropanol. A continuación, las células se lavaron dos veces en agua destilada, se tiñeron con hematoxilina y se tomaron imágenes, al menos nueve por pocillo, con un microscopio óptico. La tinción de las vesículas de grasa fue cuantificada con el software ImageJ (NIH) y los valores fueron normalizados con el número de células por imagen. La acumulación de lípidos en los cultivos se expresó como: (área teñida con Oil Red O / n.º de células).
AISLAMIENTO DE ARN Y CUANTIFICACIÓN DE LA EXPRESIÓN GÉNICA
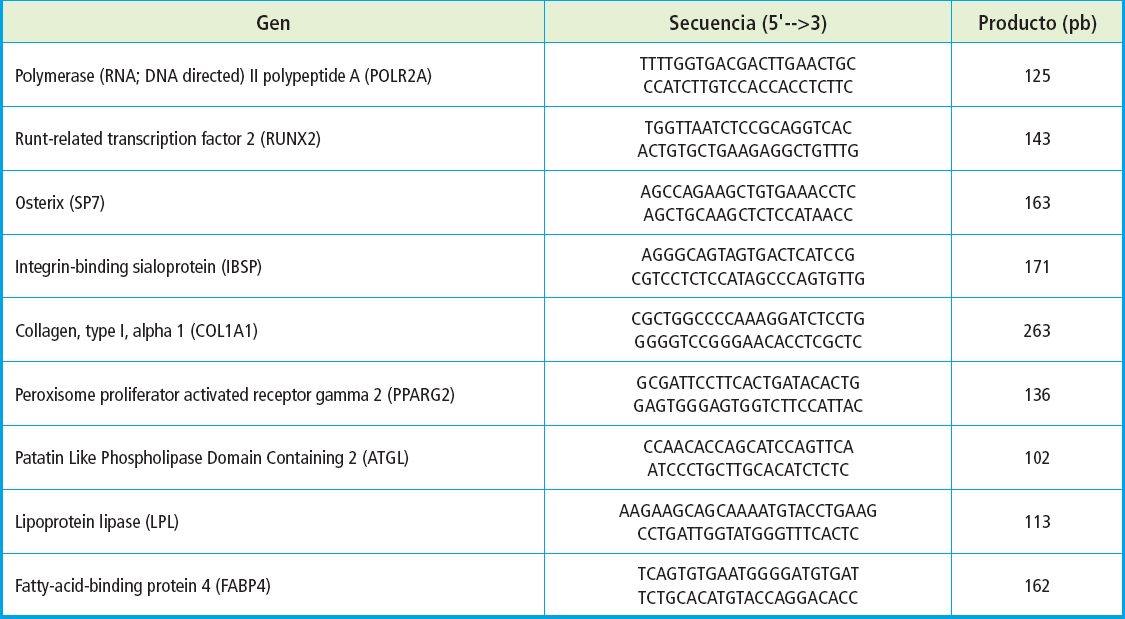
Se tomaron muestras para el aislamiento de ARN y el posterior análisis de genes marcadores de la adipogénesis y osteoblastogénesis, de cultivos de MSC, a los 10 días de ser inducidas a diferenciarse a osteoblastos o adipocitos. El ARN se aisló siguiendo las instrucciones del fabricante utilizando el kit NZY total RNA isolation (NZYTech, Lisboa, Portugal) y cuantificado con un espectrofotómetro NanoDrop ND-1000 (Thermo Fisher Scientific). A continuación, 900 ng se retrotranscribieron con el kit de síntesis de ADNc iScript de Bio-Rad (Hercules,CA, EE. UU.). Pruebas de reacción en cadena de la polimerasa cuantitativa en tiempo real (RT-qPCR) se llevaron a cabo en un CFX96 Connect (Bio-Rad). Cada reacción contenía 1 µL de ADNc, 10 pmol de cada par de cebadores (Tabla I) y SensiFAST Sybr No-Rox Mix de Bioline (Londres, Reino Unido). El programa de amplificación de PCR incluyó un ciclo a 95 °C durante 2 min (desnaturalización del ADN y activación de la ADN polimerasa) y 44 ciclos de amplificación: 95 °C durante 5 s (desnaturalización del ADN) y 65 °C durante 30 s (hibridación y extensión). Los resultados se analizaron con el software CFX Maestro V 2.3. (Bio-Rad) para la obtención de los ciclos umbrales (Ct) Como gen constitutivo se utilizó el gen codificante de la RNA polimerasa II subunidad A (POLR2A) y la expresión relativa respecto a las muestras control se expresaron como unidades arbitrarias calculadas a través del método 2-(∆∆Ct), donde ∆∆Ct= ∆Ct (muestra) - ∆Ct (muestra control); y ∆Ct (muestra) = Ct (muestra gen interes) - Ct (muestra gen constitutivo) y ∆Ct (muestra control) = Ct (muestra control gen interes) - Ct (muestra control gen constitutivo).
ENSAYO DE ANGIOGÉNESIS EN HUVEC
Con el objetivo de evaluar el efecto de las veCU y veAD sobre la angiogénesis en HUVEC, se realizó un ensayo de formación de estructuras tubulares en matrigel. Células HUVEC fueron pretratadas durante 24h con distintas concentraciones de veCU o veAD (10 × 106 y 160 × 106 partículas/ml) en medio EGM + 10 % FBS sin exosomas. Para el ensayo de angiogénesis, 10 µl de Matrigel reducido en factores de crecimiento (Corning, NY, EE. UU.) a 4 °C fue añadido a microplacas P96 de Greiner Bio-One (Kremsmunster, Austria), dejándose gelificar a temperatura ambiente. A continuación, de cada cultivo de HUVEC pretratado con las distintas VE, se añadieron 15 000 células por pocillo, resuspendidas en 70 µl de EBM + 2 % FBS sin exosomas, suplementado con el tipo y concentración de VE correspondiente. Las células se mantuvieron en condiciones de cultivo durante 4 h a 37 °C y 5 % CO2. Tras este periodo de tiempo, se tomaron imágenes al microscopio óptico que se analizaron con la extensión Angiogenesis Analyzer del software ImageJ. Como control negativo de angiogénesis, se utilizaron cultivos mantenidos en medio de cultivo sin suplementar con VE y, como control positivo, el medio fue suplementado con 30 ng/ml del inductor angiogénico factor de crecimiento fibroblástico 2 (FGF-2).
ANÁLISIS ESTADÍSTICO
Los datos se muestran como la media más el error estándar de la media (media ± SEM). En todos los experimentos el número de replicados para cada parámetro estudiado fue de al menos 3. La comparación entre los distintos tratamientos se realizó mediante la prueba ANOVA para detectar cambios significativos, seguida de una prueba de Tukey para identificar diferencias significativas entre pares de tratamientos. Se han considerado cambios significativos para p < 0,05.
RESULTADOS
CARACTERIZACIÓN DE LAS VE CIRCULANTES DEL PLASMA SANGUÍNEO DE CORDÓN UMBILICAL O DE ADULTOS
El análisis del tamaño de las veCU y veAD por Nanoparticle Tracking Analysis muestra que la mayoría de las VE obtenidas tienen un diámetro comprendido entre 50 y 150 nm (Figs. 1 A y B). La concentración de partículas por ml de plasma de cordón umbilical estuvo comprendida entre 0,7 × 1011 y 1,3 × 1011, y la de plasma de sangre de adulto entre 3,2 × 1011 y 1.1 × 1012. Por otro lado, la caracterización de la expresión proteica de los marcadores CD81, CD9 y CD63, mediante Western blot indicó que, ambos tipos de VE, expresan dichos marcadores (Fig. 1C). Estos resultados muestran cómo tras el procesamiento de las muestras de plasma de sangre de cordón umbilical o de adulto, se obtuvieron VE circulantes.
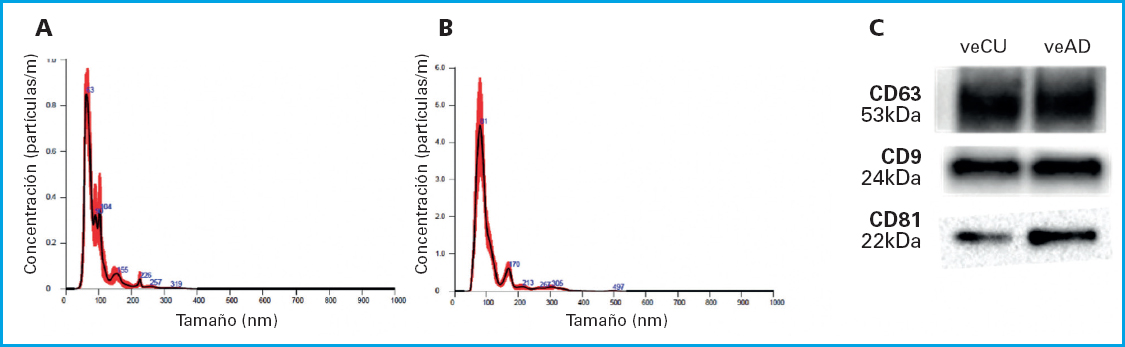
Figura 1. Cuantificación y caracterización de los exosomas circulantes aislados de plasma de sangre de cordón umbilical (veCU) o de sangre periférica de adultos sanos (veAD). A y B. Muestran el análisis mediante de la distribución del tamaño de las partículas obtenidas de veCU y veAD, respectivamente. C. Muestra la expresión proteica mediante Western blot de los marcadores de VE CD63, CD9 y CD81, en veCU y veAD.
EFECTO DE LAS veCU Y veAD SOBRE LA VIABILIDAD CELULAR DE MSC Y HUVEC
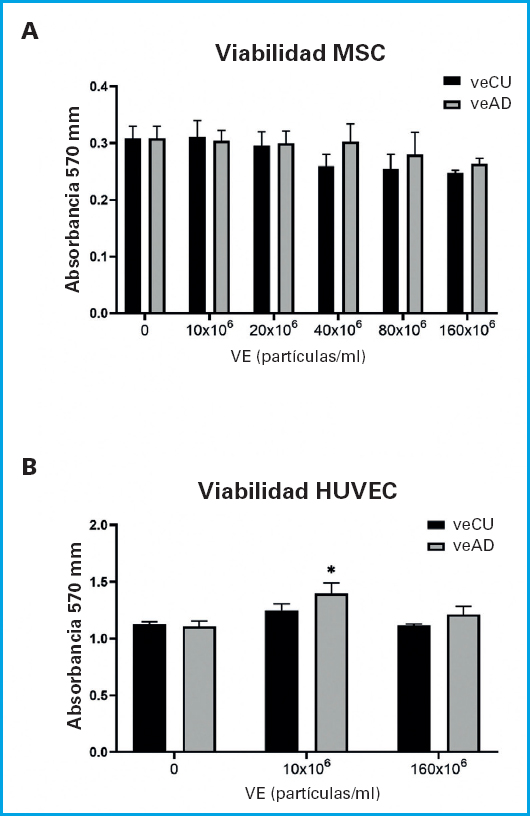
Para evaluar el efecto de veCU y veAD, en la viabilidad celular de cultivos de MSC, las células fueron tratadas con diferentes concentraciones de VE (10 × 106, 20 × 106, 40 × 106, 80 × 106 y 160 × 106 partículas/ml) durante 48 h. Los resultados mostraron que la viabilidad no se vio afectada significativamente con ninguna de las dosis y tipo de VE (Fig. 2A). En base a estos resultados, en cultivos de HUVEC, se evaluó el efecto de la menor y mayor concentración de VE utilizadas en el estudio sobre la viabilidad en MSC (10 × 106 y 160 × 106 partículas/ml). En este caso, se observó un aumento significativo de la viabilidad cuando las células fueron tratadas con la concentración más pequeña (10 × 106) de partículas/ml de veAD (Fig. 2B).
EFECTO DE LAS veCU Y veAD SOBRE LA MIGRACIÓN DE MSC Y HUVEC
En el ensayo de migración celular, la presencia de 10 × 106 o 160 × 106 partículas/ml de ambos tipos de VE (veCU y veAD), disminuyeron la migración en cultivos de MSC y de HUVEC, tras 18 h o 15 h, respectivamente (Fig. 3). La disminución tendió a ser mayor en presencia de veAD (Fig. 3).
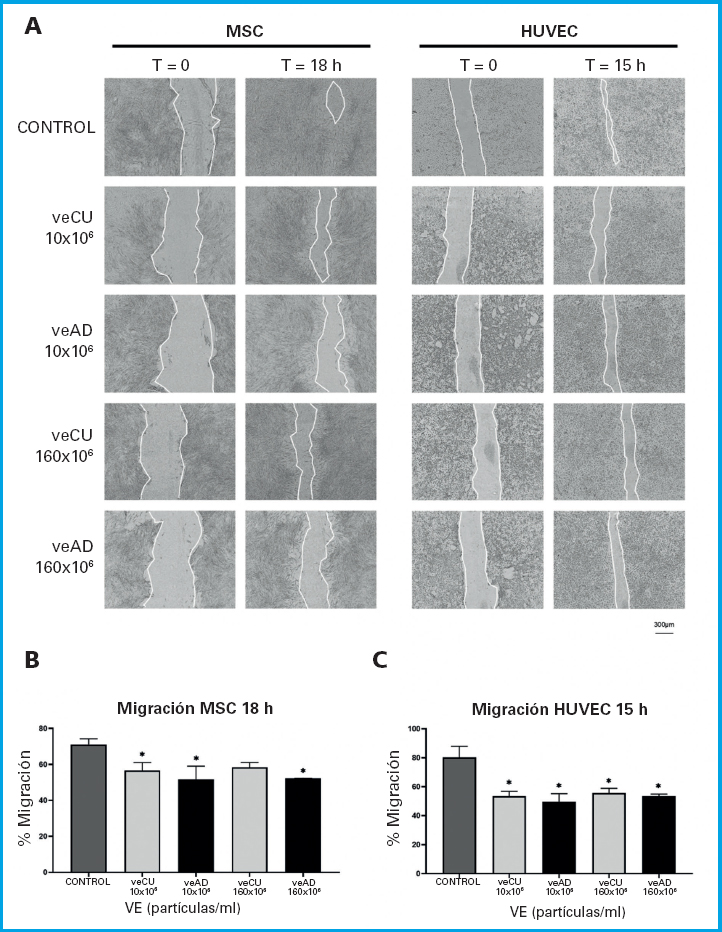
Figura 3. Efecto de veCU y veAD en la migración celular. A. Imágenes representativas de cultivos de MSC o HUVEC, en el tiempo 0 de haber realizado una línea libre de células en la placa, y a las 18 o 15 h de cultivo, respectivamente, en presencia o ausencia de distintas concentraciones de veCU o veAD. B. Cuantificación del porcentaje del área de migración en MSC a las 18 h de tratamiento. C. Igual que en B, a las 15 h con HUVEC. *p < 0,05 respecto a los cultivos no tratados (control).
EFECTO DE LAS veCU Y veAD SOBRE LA DIFERENCIACIÓN DE MSC
Diferenciación osteogénica
Los resultados de mineralización de la matriz extracelular después de 21 días de diferenciación osteogénica en las MSC inducidas a diferenciarse a osteoblastos en presencia de distintas concentraciones de veCU y veAD, muestran que ninguna de las concentraciones utilizadas afectó a dicha mineralización (Figs. 4 A y B).
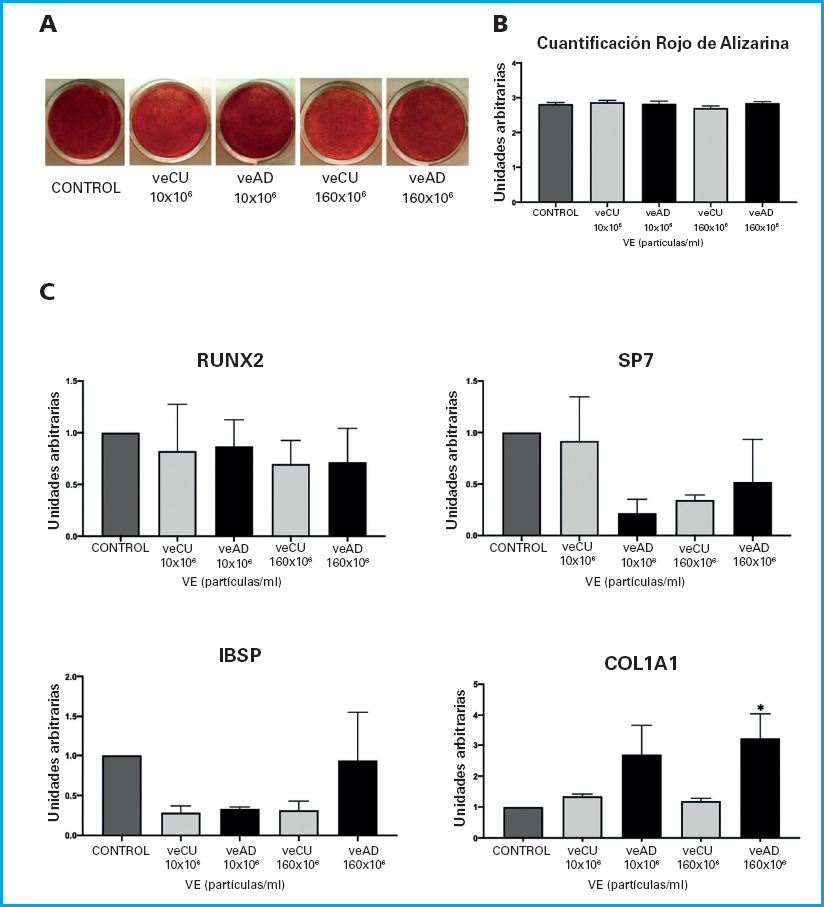
Figura 4. Estudio de la capacidad de diferenciación osteoblástica de MSC tratadas con diferentes concentraciones de veCU y veAD. A. Imágenes representativas de la tinción con rojo de alizarina para la mineralización de la matriz extracelular, de cultivos de MSC inducidos a osteoblastos y tratados con distintas concentraciones de veCU o veAD durante 21 días. B. Cuantificación de la tinción con rojo de alizarina. C. Expresión génica de genes marcadores osteoblásticos (RUNX2, SP7, IBSP y COL1A1), de cultivos de MSC tratadas con veCU o veAD, a los 10 días de la inducción a diferenciarse a osteoblastos. *p < 0,05 respecto a los cultivos no tratados (control).
A los 10 días de diferenciación osteoblástica, también se estudió en estos cultivos la expresión de genes marcadores osteoblásticos como el factor de transcripción 2 relacionado con runt (RUNX2) y osterix (SP7), codificantes de dos factores de transcripción responsables de la diferenciación osteogénica, e sialoproteína de unión a integrina (IBSP) y colágeno alfa-1, tipo I (COL1A1), codificantes de proteínas de la matriz extracelular. Los resultados mostrados en la figura 4C indican que, al igual que en la mineralización, el tratamiento con los distintos tipos de VE no produjo cambios significativos en la expresión de estos genes osteoblásticos. Tan solo, en la expresión de COL1A1 se observó un aumento en los cultivos tratados con la mayor concentración de VE (Fig. 4C).
Diferenciación adipogénica
En MSC diferenciados a adipocitos, los resultados del análisis de la tinción Oil Red O mostró que la presencia de veCU o de veAD en el medio adipogénico, disminuyó la formación de vesículas de grasa respecto a los cultivos no tratados (Fig. 5B). En cuanto a la expresión del gen codificante del principal factor de transcripción responsable de la diferenciación adipogénica, el receptor de peroxisoma-proliferador-activado gamma 2 (PPARG2), no se observaron diferencias significativas entre los distintos tratamientos a los 10 días de diferenciación adipogénica. Cambios fueron observados en la expresión de genes involucrados en el metabolismo grasos, como adipo-triglicérido-lipasa (ATGL) y la proteína 4 de unión a ácido graso (FABP4). Los niveles de ARNm de ATGL disminuyeron en los cultivos tratados con 160 × 106 partículas/ml de veCU y la expresión génica de FABP4 fue inhibida con las dos concentraciones usadas de veAD (Fig. 5C). La disminución de la expresión de los genes ATGL y FABP4 pueden ser relacionados con la disminución de la formación de vesículas de grasa y con distintos mecanismos de acción de las veCU y veAD sobre los cultivos de MSC diferenciados a adipocitos.
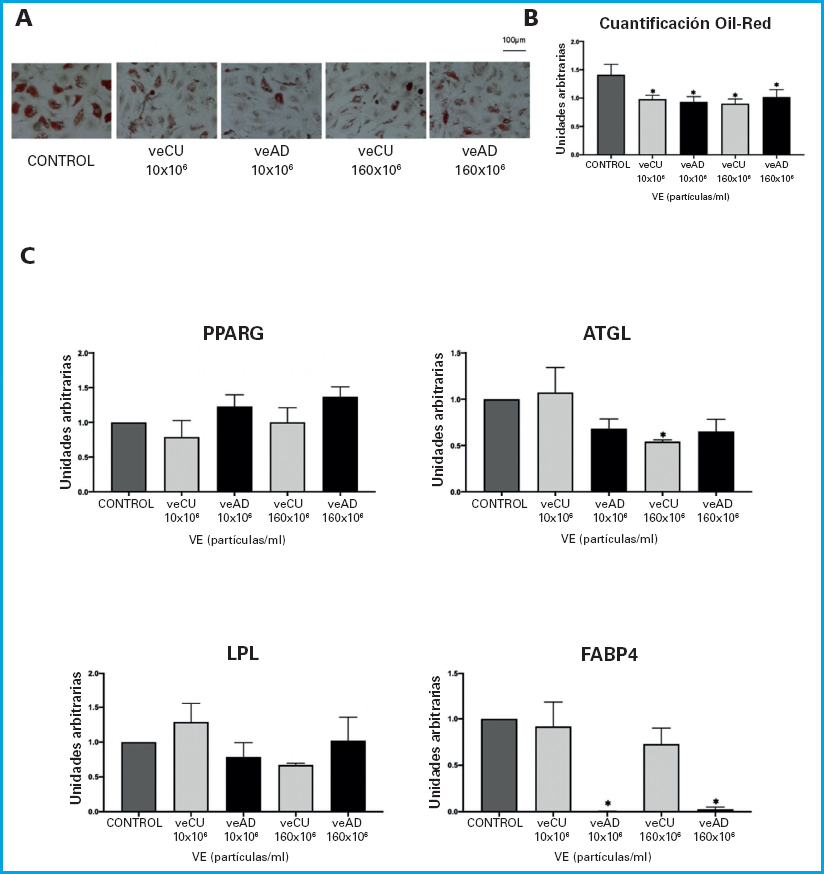
Figura 5. Estudio de la capacidad de diferenciación adipogénica de MSC tratadas con diferentes concentraciones de de veCU y veAD. A. Imágenes representativas de la tinción con "Oil Red O" de vesículas de grasa, de cultivos de MSC inducidos a adipocitos y tratados con distintas concentraciones de veCU o veAD durante 14 días. B. Cuantificación de la tinción "Oil Red O". C. Expresión génica de genes marcadores adipogénicos (PPARG, ATGL, LPL y FABP4), de cultivos de MSC tratadas con veCU o veAD, a los 10 días de la inducción a diferenciarse a adipocitos. *p < 0,05 respecto a los cultivos no tratados (control).
ESTUDIO DEL EFECTO DE LAS VECU Y VEAD SOBRE LA ANGIOGÉNESIS
Los resultados de la cuantificación de la longitud total de segmentos y la de estructuras tubulares indican que todos los tratamientos con VE aumentaron la angiogénesis respecto a la HUVEC no tratadas (Control -). Este aumento fue más significativo con los tratamientos con veCU (Figs. 6 B y C).
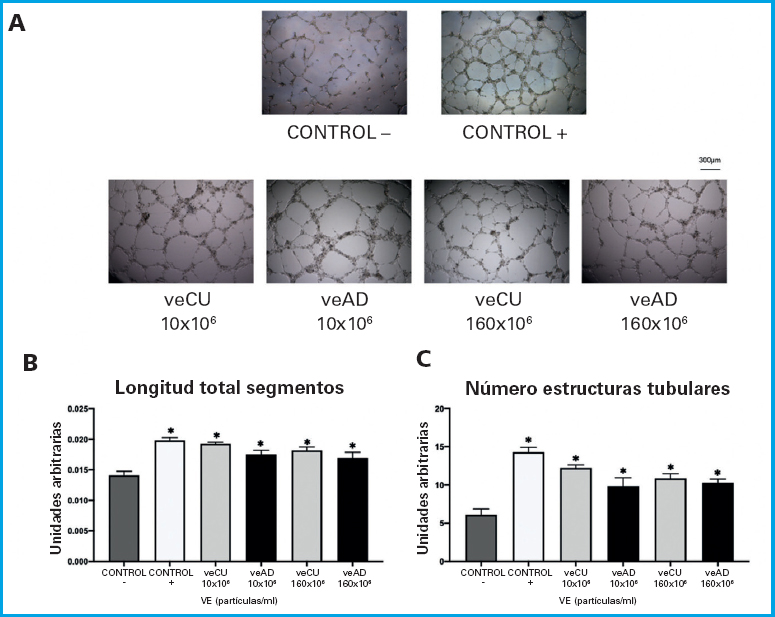
Figura 6. Estudio de la angiogénesis en cultivos de HUVEC. A. Imágenes representativas de la formación de estructuras tubulares en cultivos HUVEC sobre matrigel y tratados con diferentes concentraciones de veCU o veAD. El control (-) corresponde a cultivos no tratados y el control (+) a cultivos tratados con bFGF (30 ng/ml) como factor angiogénico. B y C. Representación gráfica de la cuantificación en el ensayo de angiogénesis de la longitud total de segmentos, y el número de estructuras tubulares, respectivamente. *p < 0,05 respecto a los cultivos no tratados (control [-]).
DISCUSIÓN
La medicina regenerativa aplicada al hueso tiene un gran potencial para el tratamiento de patologías como la osteoporosis, la artrosis, la osteonecrosis y las fracturas traumáticas. Aunque la terapia celular ha sido ampliamente evaluada en la regeneración ósea con resultados prometedores (23), actualmente se considera que el uso de VE derivadas de MSC como herramienta terapéutica libre de células, puede evitar los inconvenientes de la producción e implantación de células progenitoras con fines terapéuticos en hueso (7). Sin embargo, la obtención de VE derivadas de MSC, incluso de líneas celulares inmortalizadas, supone el establecimiento y mantenimiento de cultivos celulares estables. Lo cual, aumenta la complejidad de su aislamiento y requiere de instalaciones adecuadas para su uso clínico. Por lo tanto, es conveniente evaluar la posible capacidad terapéutica de otras fuentes de VE que cumplan que sean fácil de acceder, abundantes y su obtención no presente aspectos éticos importantes.
Así, el objetivo de este trabajo fue evaluar el efecto de VE derivadas de sangre de cordón umbilical y de personas adultas sanas, sobre procesos relacionados con la regeneración ósea, como la angiogénesis de células endoteliales y la diferenciación osteoblástica y adipogénica de MSC derivadas de médula ósea.
Nuestros resultados han mostrado que ambos tipos de VE no afectan significativamente a la diferenciación osteogénica, pero disminuyen la adipogénesis en MSC y aumentan la angiogénesis de HUVEC. Aunque las veCU parecen favorecer más la angiogénesis y las veAD pueden intervenir de manera más significativa en el metabolismo graso, a través de su inhibición sobre FABP4, no hemos detectado otras diferencias importantes entre ambos tipos de VE. Ello podría ser en parte debido a que además de nutrientes y oxigeno procedentes de la sangre maternal, la sangre de vena de cordón umbilical, transporte VE procedentes de la madre (24). Con lo cual, además de exosomas de origen fetal habría exosomas de adulto.
La respuesta a un daño tisular requiere de una serie de eventos moleculares y celulares que incluyen a la migración celular entre otras (25). Según los resultados obtenidos, la migración de MSC y HUVEC disminuyó, aunque con las veCU el descenso de la migración celular fue menor que con las veAD. Estos resultados sugieren que el contenido de ambos tipos de VE, favoreció la diferenciación, pero disminuyó la migración celular. Dicho efecto ha sido descrito previamente por otros autores, que mostraron como durante la diferenciación osteogénica y condrogénica de MSC, la migración disminuyó conforme progresaba la diferenciación (26). Además, también otros autores han descrito que VE derivados de plasma de individuos sanos inhiben la migración de células endoteliales microvasculares (27).
La diferenciación osteogénica de las MSC es un proceso complejo regulado por varios factores, como el microambiente óseo, el cual influye notablemente en la osteogénesis (28) y donde participan las VE, regulando distintos aspectos fisiológicos de las células madre (29). En este contexto, nuestros resultados han mostrado que la expresión génica del gen COL1A1 aumentó en los cultivos tratados con veAD, lo cual, podría favorecer la mineralización (30). Sin embargo, en la expresión de otros genes osteoblásticos, no se observaron cambios significativos con los tratamientos con veAD o veCU. Esto se puede relacionar con que ninguna de las VE evaluadas afecto a la mineralización de MSC diferenciadas a osteoblastos. La inducción de la formación ósea por VE derivadas de MSC se ha observado en numerosos estudios previos (31). Sin embargo, la aplicación de exosomas derivados de plasma de adolescentes sanos sobre MSC no inducidas a diferenciarse no afecta significativamente a la diferenciación osteogénica, aunque cuando se trataron cultivos primarios de osteoblastos, si se observó un aumento de la actividad de la fosfatasa alcalina (ALPL) (7). No obstante, en ese estudio la mineralización no fue estudiada, por lo que no se puede concluir el posible efecto de esos exosomas sobre la maduración final de los osteoblastos tratados. En otro estudio si han demostrado que el tratamiento de cultivos de MSC derivadas de médula ósea con VE de plasma de sangre de cordón umbilical aumenta la mineralización (32). Las diferencias con los resultados obtenidos en el presente estudio podrían ser debido a la concentración de exosomas utilizada (no pueda ser comparada pues esta expresada en µg/ml) y a que las MSC proceden de ratón y no de humanos.
En relación con la diferenciación adipogénica, el tratamiento con las VE circulantes evaluadas produjo una disminución en la formación de vesículas de grasa. Ello fue acompañado por una disminución de la expresión del gen ATGL en los cultivos tratados con veCU y del FABP4 en veAD, involucrados en el metabolismo graso y en la formación de vesículas de grasa (33,34). Es interesante señalar que la expresión del gen PPARG, no fue afectada con los tratamientos, lo que sugiere que las VE utilizadas pueden afectar más a la maduración que a la diferenciación temprana de los adipocitos.
El hecho de que cada uno de los tipos de VE circulantes evaluadas haya afectado a la expresión de distintos genes adipogénicos, sugiere diferencias en su cargo entre las cuales podría estar el contenido en miRNA. Así, se ha demostrado que la expresión de FABP4 puede inhibirse por varios miRNA, como miR-369-5p y miR-455 (35) mientras que ATGL puede inhibirse por el hsa-miR-214-3p (36). Por lo tanto, en estudios posteriores sería interesante determinar las diferencias de cargo entre las veCU y veAD para identificar posibles mecanismos de acción sobre la diferenciación de las MSC. También hay que destacar, que sobre el efecto de las VE circulantes sobre la adipogénesis es importante conocer la naturaleza y salud de los donantes. Así, exosomas circulantes de adolescentes obesos favorecen la diferenciación adipogénica más que la osteogénica, en relación a los derivados de adolescentes sanos de peso normal (31).
Ha sido descrito que el aumento de la adiposidad de la médula ósea durante el envejecimiento es producido como consecuencias de cambios en el microambiente medular, que favorecen la diferenciación de las MSC a adipocitos en lugar de osteoblastos (37). Por lo tanto, aunque nuestros resultados no muestran un efecto de las veCU y de las veAD sobre la osteoblastogénesis, si han mostrado su capacidad de disminuir la adipogénesis. Por lo tanto, la aplicación de estas vesículas podría prevenir el aumento de la adiposidad de la médula ósea y como consecuencia favorecer la formación ósea a través de un potencial aumento de osteoprogenitores. Esto está apoyado por estudios que han mostrado que la inyección intravenosa de VE de sangre de cordón umbilical en ratones viejos durante dos meses, una vez por semana, disminuyen la pérdida de hueso relacionada con la edad, estimulando la formación e inhibiendo la resorción ósea (32).
La formación de vasos sanguíneos es fundamental en los procesos regenerativos para proporcionar el aporte de nutrientes, oxígeno y facilitar la llegada de células progenitoras e inmunitarias. Nuestros resultados indican que las VE circulantes evaluadas aumentan la angiogénesis de HUVEC. Resultados de otros autores han mostrado un efecto angiogénico de veCU en cerdos (38) y en otros modelos animales. Estudios in vitro han mostrado que VE derivadas de sangre de cordón umbilical y de la madre, aumentan la angiogénesis de células endoteliales microvasculares humanas (HMEC) (39) y de HUVEC (40). También exosomas derivados de suero de humanos sanos de entre 20 y 30 años tienen efecto proangiogénico a través de la inhibición de la inflamación de los macrófagos. Así, la aplicación local de estos exosomas junto con injertos óseos, favoreció la regeneración de hueso en un modelo de defectos óseos mandibulares en ratas, a través de la disminución de la inflamación y el aumento de la angiogénesis (41). Por lo tanto, nuestros resultados están en línea con estos estudios y apoyan que tanto la sangre de adultos sanos como la de cordón umbilical podrían suponer una fuente abundante de VE con fines terapéuticos. Entre las posibles aplicaciones terapéuticas se encontrarían los relacionados con la formación ósea, debido a sus efectos sobre la diferenciación de MSC y la inducción de la angiogénesis.
CONCLUSIONES
En conclusión, ambos tipos de VE no afectaron a la mineralización en MSC diferenciadas a osteoblastos, pero disminuyeron la adipogénesis en MSC y aumentaron la angiogénesis de HUVEC. Así, estos hallazgos sugieren que ambos tipos de VE, procedentes de fuentes abundantes, sin aspectos éticos importantes y fáciles de aislar, tienen un alto potencial en medicina regenerativa aplicada al hueso, inhibiendo la adiposidad de la médula ósea y favoreciendo la angiogénesis.











 texto en
texto en