INTRODUCCIÓN
La patología aórtica infecciosa (aortitis) es una entidad rara. En ausencia de intervención tiene un pronóstico infausto, con una mortalidad que excede el 55% (1).
Las bacterias que más frecuentemente se asocian a nivel torácico son las grampositivo, aunque en aortitis infecciosas abdominales es más frecuente encontrar bacterias gramnegativo (2). Campylobacter jejuni se ha documentado como bacteria causante de aortitis infecciosa abdominal en varias ocasiones (3), aunque ninguna torácica. Coxiella burnetti está asociada a fiebre-Q. Son excepcionales los casos de afectación de la pared aórtica nativa (5%) (4). El manejo estándar de esta patología incluye antibioterapia y tratamiento quirúrgico, con una elevada tasa de morbimortalidad asociada a la cirugía abierta (5).
La reparación aórtica endovascular (EVAR) ha emergido en la última década (6-8) como una opción mínimamente invasiva de exclusión de la pared vascular con resultados satisfactorios, aunque controvertida, porque el material protésico se encuentra en contacto con el tejido infectado.
Presentamos dos casos clínicos que muestran la resolución del componente inflamatorio de la aorta torácica mediante la exclusión endoprotésica de la pared y el mantenimiento de antibioterapia específica durante largo tiempo. Uno se trataba de una paciente inmunodeprimida con una aortitis torácica secundaria a C. jejuni (excepcional por su localización) y otro, a una infección persistente por C. burnetti.
CASO CLÍNICO 1
Una mujer diabética de 64 años fue tratada mediante quimioterapia debido a un linfoma folicular que había requerido un trasplante autólogo de progenitores hematopoyéticos. Durante la quimioterapia de mantenimiento de una recidiva, se implantó un catéter Hickman; en el contexto de su manipulación presentó fiebre y escalofríos, lo que motivó su ingreso hospitalario. No presentaba antecedentes de clínica respiratoria de vías altas o diarrea.
Se prescribió terapia antibiótica empírica con piperacilina-tazobactam (4/0,5 g cada 12 horas), vancomicina (1 g cada 24 horas) y amikacina (1 g cada 24 horas) en espera de los cultivos bacterianos. Sin embargo, la situación clínica de la paciente empeoró rápidamente hacia un shock séptico y fue ingresada en la Unidad de Cuidados Intensivos (UCI). La analítica inicial demostró una pancitopenia severa (plaquetas 50 × 1000 μl, neutrófilos 1,3 × 1000 μl y monocitos 0,00 × 1000 μl) y elevación de la PCR de 29,30 mg/dl. Los hemocultivos iniciales fueron positivos para C. jejuni resistente a quinolonas y cefalosporinas de tercera generación, pero sensibles a amoxicilina-ácido clavulánico, por lo que la terapia antimicrobiana se modificó (2000/2200 mg cada 8 horas).
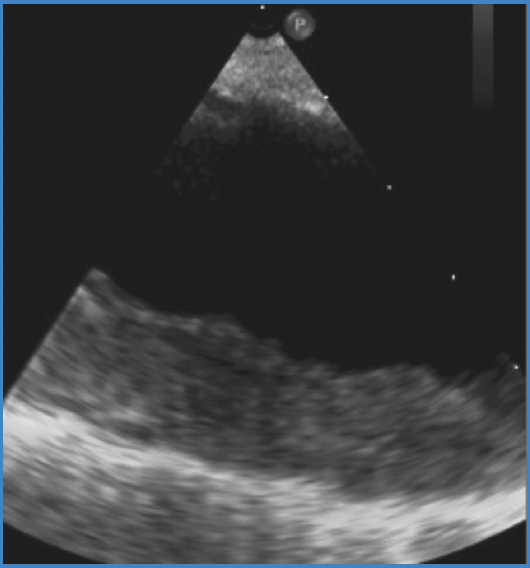
Se solicitó un ecocardiograma transtorácico y transesofágico para descartar endocarditis, pero los hallazgos revelaron una placa de ateroma complicada en la aorta torácica descendente con engrosamiento intimal, sin apreciar signos de valvulopatía o vegetaciones valvulares (Fig. 1).
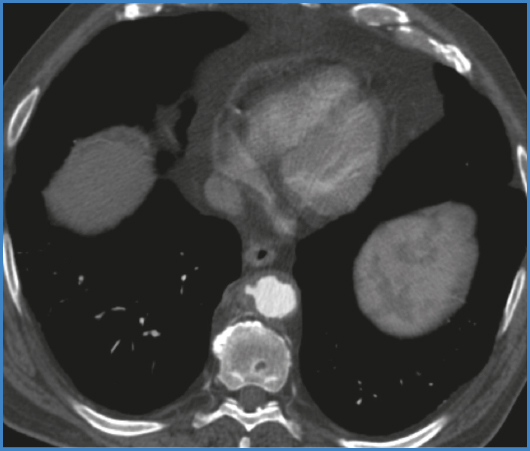
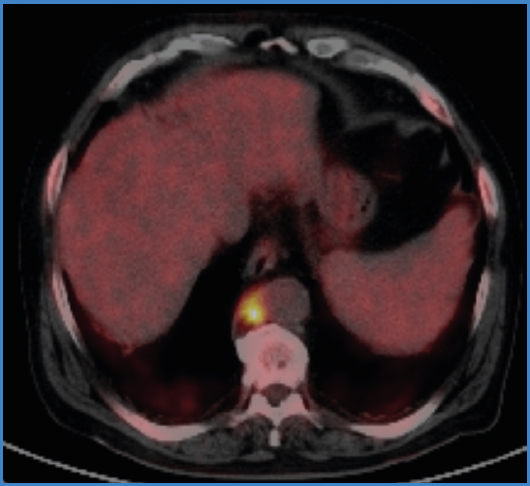
Un angio TAC de confirmación reveló un engrosamiento mural de la aorta torácica descendente con incremento de la densidad de la grasa periaórtica compatible con aortitis. Además, se observó que la paciente presentaba una arteria subclavia derecha aberrante y un tromboembolismo pulmonar subsegmentario bibasal. A pesar de la antibioterapia dirigida, los hemocultivos de control continuaron siendo positivos para C. jejuni, y un nuevo angio TAC de control a las 2 semanas mostró una progresión de la enfermedad y la aparición de nuevas ulceras aórticas (Fig. 2). Un PET-TAC-FDG (Fig. 3A) mostró intensa captación en la pared aórtica (SUVmax 6,3), lo que sugirió la presencia de una aortitis activa. Ante dichos hallazgos, se escaló el tratamiento empírico a meropenem (1 g cada 8 horas) en asociación con gentamicina (7 mg/kg cada 24 horas).
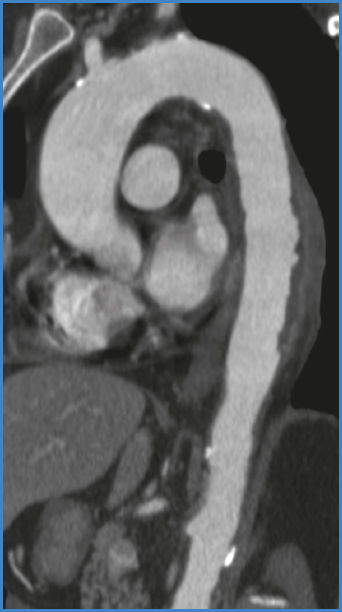
Figura 2. Corte sagital de angio TAC torácico. Progresión de la aortitis a úlceras aórticas (segmento de 10 cm de longitud).
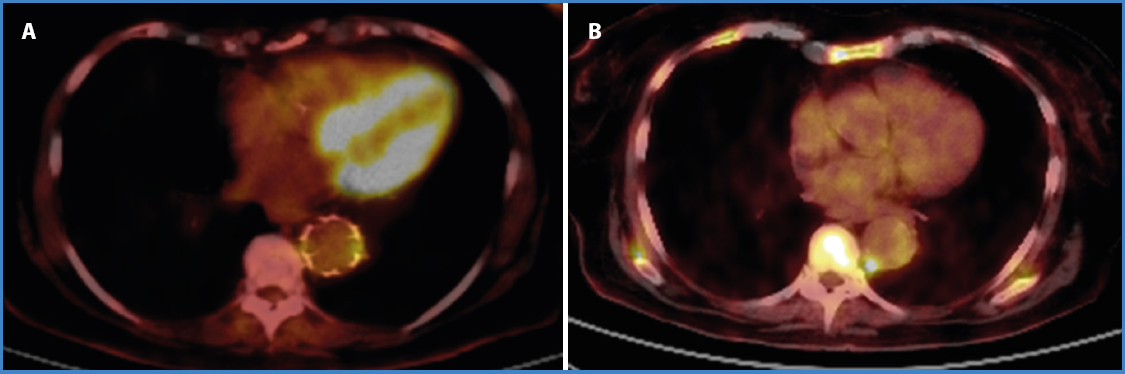
Figura 3. A. Corte axial de PET-TC-FDG torácico. Intensa captación de FDG en pared aortica. B. Corte axial de PET-TC-FDG torácico a los 18 meses de seguimiento. Disminución metabólica del marcador.
La paciente continuó mostrando pancitopenia, por lo que se inició terapia con factor estimulante de colonias de granulocitos (G-CSF, Neupogen®). Después de 35 días de terapia antibiótica continuada con meropenem y gentamicina, los hemocultivos se negativizaron y se implantó una endoprótesis aórtica (Zenith Alpha Thoracic ZTA 32 × 32 × 150 mm Cook, Inc., Bloomington, Indiana, Estados Unidos) mediante acceso femoral derecho con una correcta exclusión de la lesión parietal aórtica.
Cuando la paciente fue dada de alta por Hematología, y de acuerdo con la Unidad de Enfermedades Infecciosas, se prescribió tratamiento crónico con amoxicilina-ácido clavulánico (1000-1125 mg cada 12 horas) de forma indefinida. La paciente ha permanecido asintomática desde entonces (seguimiento 24 meses) y con normalización de la actividad metabólica de la pared aórtica en el PET-TC-FDG a los 18 meses (SUVmax 3,57) (Fig. 3B).
CASO CLÍNICO 2
Un varón de 75 años con antecedentes de isquemia arterial crónica, fibrilación auricular paroxística, accidente isquémico transitorio de origen cardioembólico y fiebre botonosa mediterránea (Rikettsia conorii) tratada ingresó por un síndrome febril y lesiones cutáneas necróticas. El paciente refería astenia, anorexia, pérdida de peso y sensación distérmica con escalofríos en los últimos días. Convivía con 5 perros y otros animales domésticos.
La radiografía de tórax era normal y la analítica mostraba una colestasis (GGT 70U/I, fosfatasa alcalina, 148 U/I; bilirrubina, 2,2 mg/ dl), elevación de PCR (19,10 mg/ dl) sin leucocitosis. Se solicitaron urocultivo, hemocultivos y serologías para sífilis, VIH, Brucella, Rickettsia y otros. Los resultados fueron negativos salvo para serología de Coxiella (fase I: IgG 1/1024; fase II: IgG 1/8192).
La ecocardiografía transtorácica descartó valvulopatías y derrame pericárdico. El ecocardiograma transesofágico no mostró endocarditis, pero se observó una ateromatosis severa de aorta torá- cica descendente con engrosamiento periaórtico en la confluencia torácico-abdominal. Un PET-TC-FDG (Fig. 4) mostró actividad metabólica patológica de la pared de la aorta torácica descendente (SUVmax al diagnóstico de 13,22).
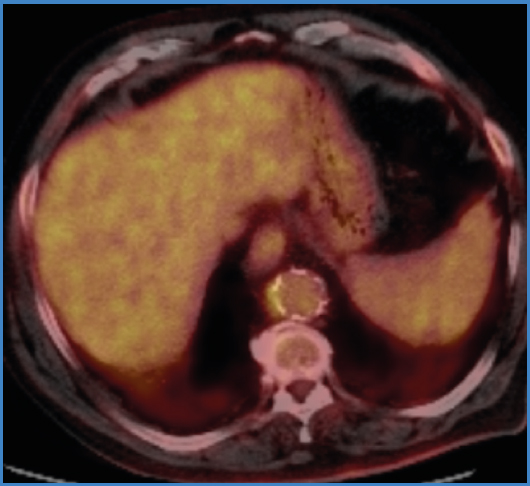
Figura 4. Corte axial PET-TC-FDG torácico. Intensa captación de FDG en aorta torácica descendente (SUVmax 13,22).
En el contexto de fiebre de origen desconocido con serología positiva a títulos muy elevados y embolismos sépticos cutáneos se asumió una infección persistente vascular por C. burnetii, a pesar de que no mostraba lesión cardíaca manifiesta. Después de cuatro semanas de tratamiento con doxiciclina (100 mg cada 12 h) e hidroxicloroquina (200 mg cada 8 h), el paciente mejoró clínicamente.
Un nuevo angio TAC (Fig. 5) mostró un empeoramiento con una úlcera aórtica en la aorta torácica descendente; además, se constató la persistencia de la elevación de PCR (2,80 mg/dl). El paciente fue tratado entonces con una exclusión endovascular de la zona lesionada con una endoprótesis (Valiant Captivia Medtronic 30 × 30 × 150 mm Medtronic, Inc., Minneapolis, Estados Unidos) y se decidió completar el tratamiento con doxiclina (100 mg cada 12 h vía oral) e hidroxicloroquina (200 mg cada 8 h vía oral). Tras la implantación de la prótesis, se objetivó normalización de los reactantes de fase aguda y descenso importante de los títulos de IgG de fase I y II (1/512 y 1/2048, respectivamente). La evolución clínica posterior fue favorable –el paciente quedó afebril–, así como la evolución radiológica y la de los parámetros de inflamación. Se objetivó repunte y persistencia de títulos altos de IgG de fase II tras la suspensión de hidroxicloroquina a los 24 meses, pero el PET-TC-FDG (Fig. 6) mostró respuesta metabólica prácticamente completa (SUVmax de 3,48). Se completó tratamiento con doxiciclina hasta 30 meses.
DISCUSIÓN
La aortitis infecciosa es una entidad rara, típicamente localizada sobre la pared arterial ateroesclerótica, pero muy peligrosa, ya que puede degenerar a úlcera aórtica, aneurisma micótico, disección, rotura y/o bacteriemias de repetición con posibles embolismos sépticos. Afecta frecuentemente a la aorta torácica o abdominal (2,9). Los pacientes inmunodeprimidos presentan una predisposición a la colonización bacteriana de placas de ateroma. Aunque los patrones bacteriológicos siguen cambiando día a día, los organismos con mayor afinidad hacia la pared arterial son Staphylococcus y Salmonella (2). El C. jejuni se ha documentado como causa de aortitis infecciosa abdominal en muchos casos (3), pero en ningún caso a nivel torácico La infección persistente vascular por C. burnetti es igualmente infrecuente, y es excepcional la pared de la aorta nativa (4).
La bacteriemia por Campylobacter es una condición grave potencialmente mortal, normalmente asociada a pacientes inmunodeprimidos. Previamente, estuvo asociada al sida (VIH avanzada). Actualmente, los trasplantes de órganos, inmunodeficiencias o neoplasias hematológicas son las condiciones concomitantes más comunes. En estos casos, la bacteriemia tiene un origen abdominal en aproximadamente un tercio de los pacientes (un 25% tiene un origen desconocido y un 16,7% un origen pulmonar). Las infecciones por Campylobacter relacionadas con catéteres intravenosos son extremadamente raras.
La infección por C. burnetti es la responsable de la fiebre Q, zoonosis de distribución mundial. La infección por C. burnetti cursa típicamente en dos fases, que no están presentes en todos los pacientes. La fase aguda o fiebre Q puede cursar con síndrome febril, neumonía, hepatitis o endocarditis. En un porcentaje de pacientes la infección se cronifica (infección persistente por Coxiella, antiguamente denominada fiebre Q crónica) en forma de endocarditis, infección vascular o infección osteoarticular. El diagnóstico está basado en los métodos serológicos debido a que el aislamiento de muestras clínicas es difícil, si bien se utilizan también la PCR en sangre y en muestras quirúrgicas en caso de endocarditis. El tratamiento principal es con antibióticos. Con frecuencia se utiliza la combinación de doxiciclina e hidroxicloroquina, habitualmente durante muchos meses. A nivel vascular periférico se han descrito varios casos (10 11-12). Debido a la asociación de estas enfermedades infecciosas con bacteriemia y metástasis sistémicas, en todos los pacientes se recomienda un ecocardiograma transtorácico o idealmente transesofágico para descartar una posible endocarditis, pero, dado que puede asociarse a otras complicaciones arteriales, un angio TAC con contraste es la técnica de imagen de elección (13), si bien algunos autores recomiendan PET-TC en todos los casos por Coxiella (14).
El antibiótico inicial suele ser empírico, en espera de la confirmación microbiológica y el antibiograma. Dada la creciente tasa de resistencias suele ser un carbapenémico en caso de Campylobacter y una tetraciclina en caso de la Coxiella. Un ciclo prolongado de antibióticos debería garantizarse en pacientes inmunosuprimidos, así como en los casos en los que se determine bacteriemia persistente, metástasis sépticas o los marcadores bioquímicos de inflamación no recuperen valores normales (15).
El manejo óptimo de la aortitis infecciosa permanece desconocido y es controvertido. Dado que la terapia médica aislada tiene una tasa de persistencia de la enfermedad y de la mortalidad superior al 90%, se recomienda un manejo combinado: médico y quirúrgico (16). A pesar de ser discutible el uso de procedimientos endovasculares (endoprótesis) sobre un lecho arterial contaminado, estas técnicas han ganado aceptación y proliferación general dada su menor morbilidad (7,17,18).
Aunque la cirugía abierta con resección del fragmento aórtico infectado se estima curativa, en nuestro caso esta opción se excluyó por el alto riesgo y el mal estado general de ambos pacientes, por lo que se optó por una terapia endovascular mediante la exclusión de la pared aórtica con endoprótesis y un tratamiento antibiótico específico según el germen causal.
En un pequeño y reciente estudio multicéntrico (19) se ha reportado un 91% de supervivencia a los 30 días; el 19% de las complicaciones relacionadas a la infección ocurrieron durante el primer año postoperatorio; la supervivencia a largo plazo fue del 55% a 5 años con pocas complicaciones tardías relacionadas con la infección. Estas complicaciones ocurren, en la mayoría de los casos, después de la suspensión de los antibióticos, lo que sugiere que la terapia antimicrobiana a largo plazo, al menos 12 meses y posiblemente para toda la vida, es necesaria para un tratamiento endovascular con éxito (15). En el caso de la infección persistente por Coxiella, se recomienda un tratamiento antibiótico de cómo mínimo 24 meses.
CONCLUSIONES
La singularidad de nuestros casos, además de las bacterias implicadas, es la observación de que la exclusión endovascular con endoprótesis y la asociación antibiótica mantenida son seguras y eficaces al contribuir a la desaparición del componente inflamatorio e infeccioso de la pared aórtica. No obstante, estos pacientes deben someterse a un protocolo de vigilancia de por vida para monitorizar la infección recurrente.
La escasa prevalencia de esta patología (aortitis infecciosa) no permite extraer conclusiones con evidencia médica e imposibilita la realización de estudios prospectivos. Un registro de endoprótesis usadas para tratamiento de este tipo de patologías ayudaría a clarificar el papel de la terapia endovascular en el tratamiento de esta rara patología.