INTRODUCCIÓN
La técnica de stent paralelo, es decir la utilización de stents convencionales colocados de manera paralela a la endoprótesis principal para mantener flujo en las ramas colaterales de la aorta, es una técnica endovascular utilizada en la reparación de los aneurismas complejos de la aorta abdominal con afectación o gran proximidad a las arterias viscerales (renales y mesentérica superior) y/o hipogástricas.
Nacida en 2001 como un procedimiento de rescate ante una oclusión accidental de una arteria renal tras un EVAR estándar, su uso como procedimiento electivo ha ido extendiéndose cada día más debido a sus buenos resultados (1-3), su relativa sencillez técnica y la posibilidad de realización incluso en casos urgentes o preferentes sin requerir la utilización de dispositivos hechos a medida.
Sus principales inconvenientes se basan en el riesgo inherente de endofuga entre los dispositivos (a través de gutters o canales) y a la relativa falta de estandarización de la técnica, basándose en su mayoría en recomendaciones de expertos y series clínicas.
Este estudio pretende analizar experimentalmente mediante modelos in vitro, parámetros técnicos fundamentales (el mejor grado de sobredimensión, la mejor manera de medirla y la mejor combinación de materiales) en dos configuraciones de stent paralelo: a) con 2 y 3 chimeneas para la reparación de los aneurismas sin cuello infrarrenal; y b) tipo sándwich para preservar la arteria hipogástrica en la reparación de los aneurismas sin cuello iliaco o distal.
MATERIAL Y MÉTODOS
Para este estudio se crearon dos modelos in vitro de stent paralelo: uno de ellos para analizar la configuración en chimenea con 2 y 3 stents viscerales y otro de un procedimiento de sándwich iliaco para preservar la arteria hipogástrica. La utilización de modelos in vitro se debió a la posibilidad de los mismos para testar cualquier parámetro, incluso con valores extremos, sin asociar riesgo alguno hacia el paciente.
El estudio fue registrado con número “HCB/2016/ 0459” y aprobado por el Comité Ético de Investigación Clínica del Hospital Clínic de Barcelona. No existió ningún conflicto de interés entre los autores y las compañías suministradoras de los dispositivos utilizados y estas donaciones de muestras fueron no estériles.
Modelo de stent paralelo con 2-3 chimeneas (chEVAR) para reparación de aneurismas sin cuello proximal
Para poder reproducir in vitro el chEVAR, se construyó un modelo de aorta visceral mediante tubos de silicona reforzados (para corregir la excesiva laxitud de la silicona intentando simular la consistencia de la pared aortica) de 18, 20, 22, 25 y 27 mm de diámetro interno. Dichos diámetros fueron seleccionados de manera específica para obtener determinados grados de sobredimensión con la endoprótesis principal a utilizar.
En cada modelo aórtico se conectaron dos segmentos tubulares sintéticos a cada lado (20 mm de longitud, 6 mm de diámetro y orientación 30° descendente) siguiendo las características anatómicas habituales de las arterias renales. Para los modelos con 3 chimeneas se añadió además un nuevo tubo de 8 mm de diámetro en la cara anterior con la misma longitud y orientación descendente simulando así la arteria mesentérica superior.
En cada modelo se introdujeron los diferentes dispositivos (stents paralelos y endoprótesis) siguiendo las consideraciones técnicas habitualmente usadas para este tipo de procedimiento: stents paralelos colocados unos 15-20 mm dentro de la rama visceral, endoprótesis principal unos 10 mm por encima de los ostia de las arterias viscerales a cubrir, y extremo proximal del stent paralelo unos 10 mm por encima de del extremo más proximal de la parte cubierta de la endoprótesis principal (Fig. 1).
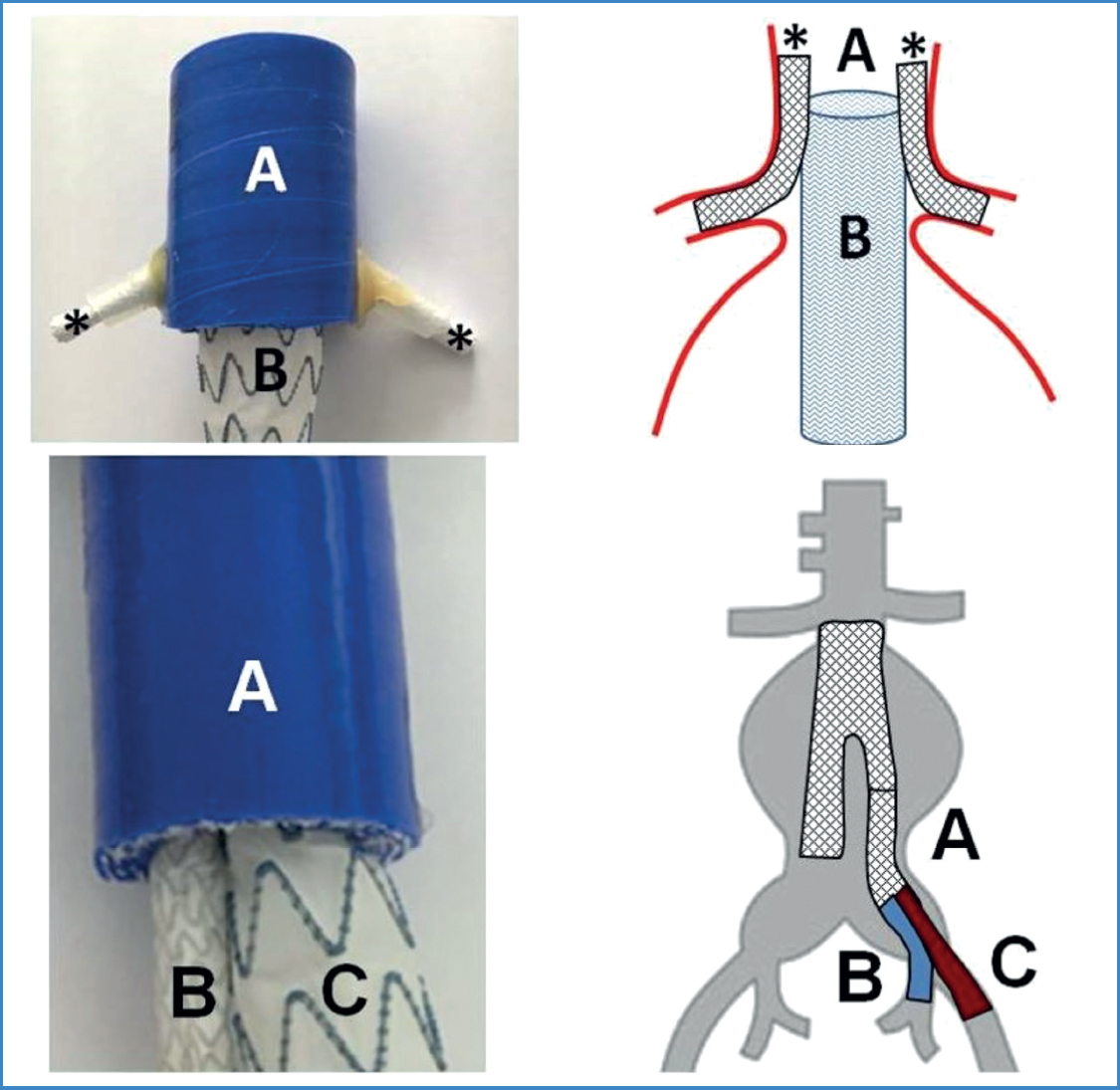
Figura 1. Modelos in vitro de stent paralelo utilizados en el estudio. Arriba: modelo en configuración tipo chimenea con 2 stents para las arterias renales (*) colocados dentro de un modelo de aorta visceral (A) en paralelo con la endoprótesis principal (B). Abajo: modelo en configuración tipo sándwich iliaco y su correspondencia con un esquema de tratamiento de un caso teórico siendo (A) el equivalente a la rama para la arteria iliaca común (B), el stent paralelo para la arteria hipogástrica y (C) el dispositivo para la arteria iliaca externa.
Como endoprótesis principal se utilizaron 2 dispositivos distintos:
– Cuerpos principales de Endurant-II (Medtronic Endurant Abdominal Stent Graft, Medtronic AVE, Santa Rosa, CA, USA) de 25, 28 y 32 mm de diámetro proximal.
– Cuerpos principales de Gore Excluder (Gore Excluder Abdominal Aortic Aneurysm Endoprosthesis, W.L. Gore & Associates, Flagstaff, AZ, USA) de 26, 28,5 y 31 mm de diámetro proximal.
La selección de dichos dispositivos concretos fue debida a su elevada prevalencia para este tipo de procedimientos en la práctica habitual (4,5), así como por sus diferentes características en cuanto a composición y fuerza radial (tela de poliéster, stent de alta fuerza radial y fijación suprarrenal en Endurant; tela de PTFE, stent de baja fuerza radial y ausencia de fijación suprarrenal en Excluder).
Como stents paralelos para las arterias viscerales se utilizaron:
– Stents Viabahn (Gore Viabahn Endoprosthesis, W.L. Gore & Associates, Flagstaff, AZ, USA).
– Stents Begraft (Bentley InnoMed, Hechingen, Germany).
Los diámetros utilizados para los stents fueron de 6 mm en los modelos con solo 2 chimeneas para las renales y de 6 y 8 mm en aquellos modelos con 3 chimeneas (6 mm para ambas arterias renales y 8 mm para la arteria mesentérica superior) igual que los habitualmente utilizados en la práctica clínica habitual (6,7).
Modelo de sándwich iliaco para reparación de aneurismas sin cuello iliaco o distal
Para el reproducir el procedimiento del sándwich iliaco, se utilizaron también tubos de silicona externamente reforzada de distintos diámetros, aunque en este caso simulando una rama endoprotésica para la arteria iliaca común. Los diámetros utilizados para dichos modelos fueron 10, 12, 14, 16 y 18 mm, siendo seleccionados de manera específica para obtener distintos grados de sobredimensión con los dispositivos para la iliaca externa y la arteria hipogástrica.
Para cada modelo de silicona se introdujeron de manera paralela dos dispositivos: uno correspondiente a una extensión para la arteria iliaca externa y otro correspondiente a la rama para la arteria hipogástrica manteniendo un solapamiento de al menos 50 mm siguiendo las recomendaciones técnicas habituales (2) (Fig. 1).
Los dispositivos utilizados para la rama de la arteria iliaca externa fueron:
– Ramas iliacas Endurant de 16 mm (Medtronic Endurant Abdominal Stent Graft, Medtronic AVE, Santa Rosa, CA, USA).
– Ramas iliacas de 12 mm Aorfix (Lombard Medical Abdominal Stent Graft, Laguna Canyon RD, Irvine, CA, USA).
– Stent Viabahn 11 mm y 13 mm (Gore Viabahn Endoprosthesis, W.L. Gore & Associates, Flagstaff, AZ, USA).
La selección del tipo de dispositivos fue por ser los más reportados en los artículos previamente publicados (1,8,9). Respecto al diámetro, se utilizaron stents Viabahn de 11 y 13 mm suponiendo un sello en una arteria iliaca externa estándar entre 9 y 12 mm y extensiones de Endurant y Aorfix de tamaño igual al diámetro proximal habitual de todas las extensiones iliacas para este tipo de plataformas (16 mm en Endurant y 12 mm en Aorfix respectivamente).
Se utilizaron dos tipos de stents para simular la rama paralela a la arteria hipogástrica:
– Stent Viabahn (Gore Viabahn Endoprosthesis, W.L. Gore & Associates, Flagstaff, AZ, USA).
– Stent V12 (Atrium Advanta V12, Atrium Medical Corporation, Hudson, NH, USA).
La elección de stents tipo Viabahn fue igualmente por ser el más reportado para la arteria hipogástrica en los procedimientos de sándwich iliaco (1,2,8,99). V12 se eligió como comparación a Viabahn y ambos stents eran diferentes tanto en su composición y su fuerza radial (Viabahn como stent autoexpandible, de nitinol y baja fuerza radial versus V12 como stent balón expandible, de acero inoxidable y alta fuerza radial). En ambos casos, se utilizaron stents de 8 mm al ser los más reportados en este tipo de procedimientos.
Análisis de los modelos
Los modelos con sus correspondientes dispositivos se sumergieron dentro de un baño de salino fisiológico a 37 °C para recrear así la composición básica y la temperatura de la sangre.
Posteriormente se remodeló toda la reconstrucción con baloneado simultáneo, mediante un balón no compliante (Reliant stent graft balloon catheter; Medtronic Inc.) y balones convencionales de angioplastia (Bentley InnoMed, Hechingen Alemania) para los stents para las ramas viscerales y la arteria hipogástrica.
Se analizaron cada uno de los modelos obtenidos mediante la realización de un TC Toshiba Aquilion One multidetector (Toshiba Medical Systems Corp, Otawara-shi, Japón). Los cortes axiales obtenidos fueron guardados de manera ciega y posteriormente exportados para un análisis externo por en dos ocasiones por dos observadores independientes (para poder obtener la concordancia inter e intraobservador) a través de un programa de tratamiento de imágenes radiológicas (OsiriX Imaging Software v 3.8.1, 32 bit Pixmeo, Geneva, Switzerland).
Una vez realizado el TC de cada modelo, los dispositivos utilizados fueron extraídos y examinados meticulosamente. En caso de no observar daño estructural (rotura del stent, perforación de la tela, doblado de la estructura o cualquier otro daño no evidenciando previamente) se reutilizaron para otros modelos. En caso contrario (daño estructural evidenciando) fueron reemplazados por dispositivos nuevos.
Para cada modelo se seleccionó un corte axial representativo de toda la reconstrucción en la zona media de solapamiento, evitando interferencias de las marcas radioopacas de los extremos de los stents o zonas de angulación en la entrada de los ostia de las ramas viscerales. Sobre dicha imagen se analizaron las siguientes variables (Fig. 2):
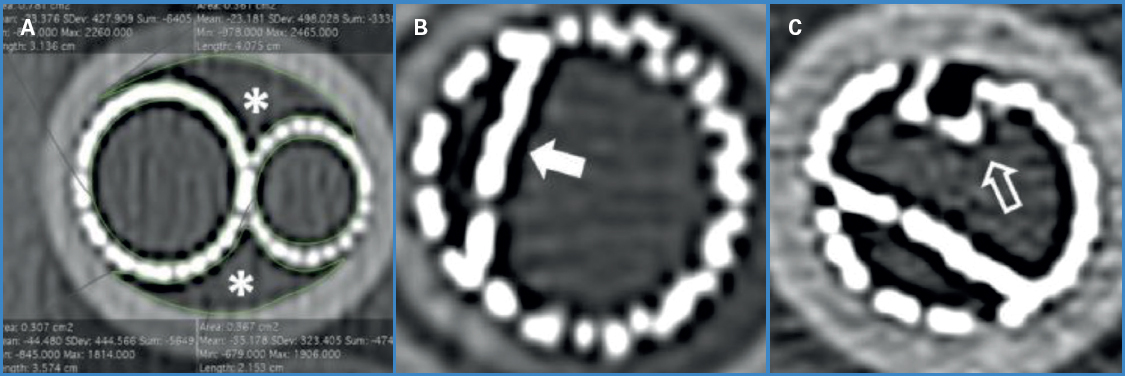
Figura 2. Variables analizadas en el estudio tras análisis TC de los modelos. A. Cálculo de gutters o áreas de mal sellado (*). B Modelo con compresión de stent visceral (flecha). C. Modelo con replegado (flecha hueca).
– Canales (gutters) o zonas de mal sellado (mm2): suma de todas las áreas internas (calculadas mediante la función close polygon de OsiriX) de cada uno de los modelos de silicona no cubiertas ni por la endoprótesis principal ni por los distintos stents paralelos.
– Compresión del stent paralelo (%): área interna de cada stent paralelo dividida por el área interna del mismo stent valorado en un TC independiente, con el stent fuera del modelo y totalmente expandido.
– Replegado o infolding (%): colapso parcial o ausencia de total expansión de la endoprótesis principal creando más zonas de mal sellado. Esta variable solo se describió de manera cualitativa (presencia o ausencia) dada su imposibilidad de cuantificación.
En los modelos de sándwich iliaco se analizó además el porcentaje de sobredimensión de los stents paralelos (para la iliaca externa e interna), respecto a la rama para la iliaca común mediante tres métodos distintos:
– Sobredimensión de áreas (%): el método más descrito previamente (9-12). Calculada como la suma de las áreas de cada stent paralelo (a1 + a2) obtenidas mediante la fórmula matemática del área de una circunferencia (π x radio2), menos el área (calculada de la misma manera) del modelo de silicona (a3), dividido nuevamente por el área del modelo (a3). { [(a1 + a2) - a3] / a3 } x 100.
– Sobredimensión de perímetros (13) (%): calculada como la suma de los perímetros (p1 + p2) de cada stent paralelo, obtenidos mediante la fórmula matemática del perímetro de una circunferencia (2 x π x radio), menos la suma del diámetro de ambos stents paralelos (d1 + d2) con el fin de rechazar la parte interior del sándwich donde ambos stents se solapan, menos el perímetro del modelo de iliaca común (p3), y finalmente dividido por el perímetro del modelo iliaco (p3). { [(p1 + p2) - (d1 + d2) ] –p3 } / p3 x 100.
– Sobredimensión de diámetros (%): un nuevo método hasta ahora no descrito basado directamente en el diámetro nominal de los stents a utilizar. Es calculada como la suma de ambos diámetros nominales de cada stent paralelo (d1 + d2), menos el diámetro nominal del modelo de silicona (d3), dividida por el diámetro de dicho modelo (d3). { [(d1 + d2) - d3] / d3 } x 100.
Análisis estadístico
Se obtuvieron para todos los datos la mediana, el rango y las frecuencias mediante el paquete estadístico SPSS v 20.0 (IBM Corp, Armonk, New York, USA). Las concordancias intra e interobservador se calcularon utilizando el coeficiente de correlación interclase para acuerdo absoluto. Dado el alto grado de concordancia evidenciado (concordancia intraobsevador de 0,993 [95% CI 0,982-0,997] y 0,991 [95% CI: 0,985-0,994]) e interobservador de 0,905 [95% CI: 0,844-0,940] y 0,988 [95% CI: 0,981-0,992] respectivamente para los modelos de 2-3 chimeneas viscerales y sándwich iliaco); las medias de las medidas de ambos observadores fueron las que se utilizaron para los posteriores análisis. Las comparaciones entre las zonas de mal sellado, la compresión de stent paralelo y presencia de replegado en función de grados de sobredimensión, combinaciones de materiales y número de stents paralelos se realizaron utilizando los test no paramétricos de Kruskal-Wallis, de Mann-Whitney, y la prueba exacta de Fisher. Las comparaciones entre los distintos métodos de medida de la sobredimensión (por área, perímetro y diámetro en los modelos de sándwich iliaco) se realizaron mediante la correlación rho de Spearman y las predicciones entre diferentes métodos de medición se realizaron mediante un estudio de regresión lineal. El valor de p < 0,05 se consideró como estadísticamente significativo.
RESULTADOS
Resultados del análisis de los modelos de stent paralelo con 2-3 chimeneas
Respecto el grado de sobredimensión de la endoprótesis principal, nuestros resultados (14) (Tabla I) indican que a mayor sobredimensión de la endoprótesis principal, mejor adaptación de los componentes con una tendencia no significativa a una reducción de las zonas de mal sellado, aunque asociando un incremento del riesgo de compresión del stent paralelo y sobre todo de aparición de replegado. Este último es especialmente importante en los modelos con 3 stents paralelos y en aquellos con dispositivos de baja fuerza radial (Endoprótesis Excluder y stents paralelos tipo Viabahn), presentando valores “prohibitivos” a sobredimensiones ≥ 30 % (67 y 100 % en modelos con sobredimensión del 30 y el 40 %, respectivamente).
Tabla I. Zonas de mal sellado, compresión del stent paralelo y porcentaje de replegado a diferentes grados de sobredimensión y distinta combinación de materiales en los modelos de stent paralelo tipo chimenea
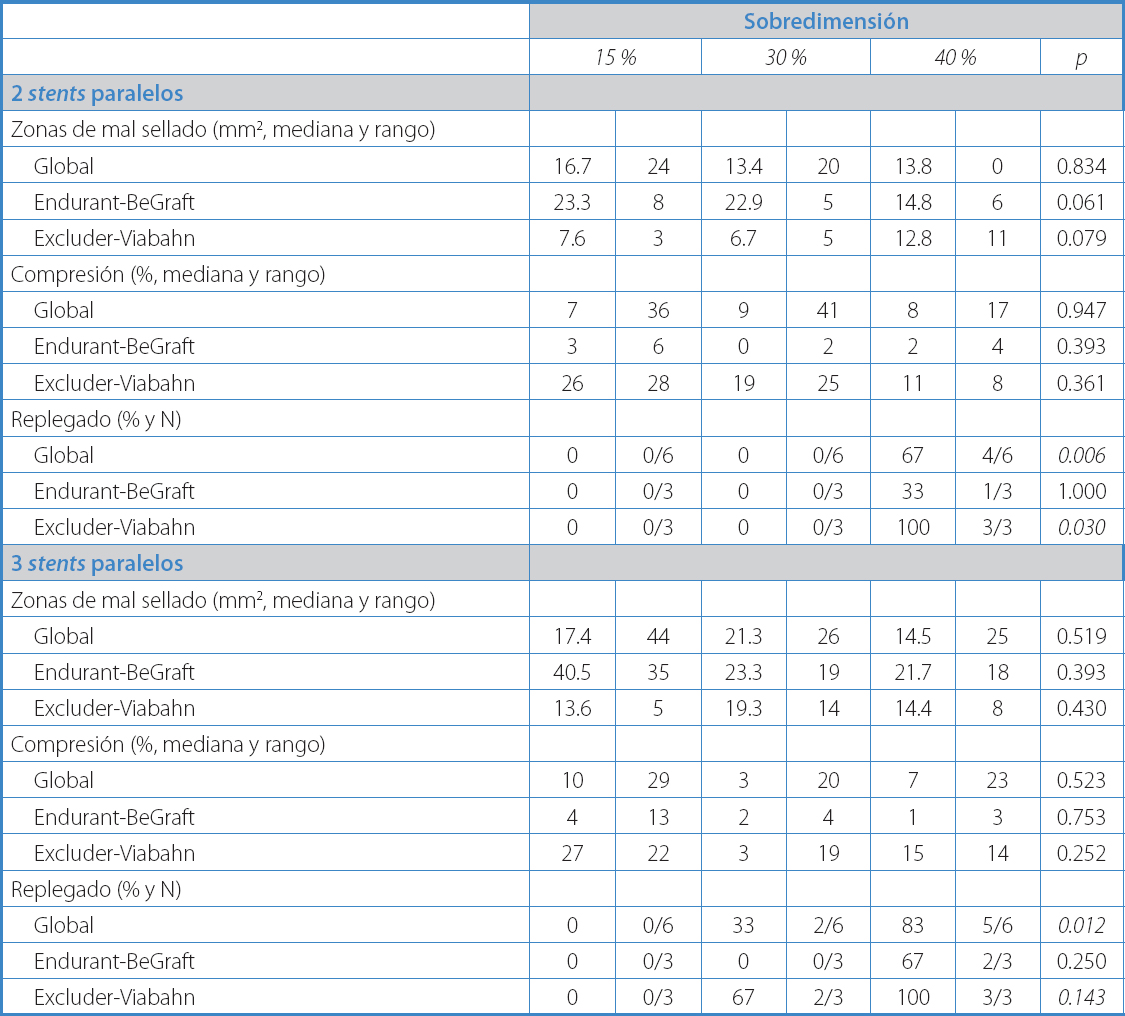
Analizando las distintas combinaciones de materiales, nuestros resultados muestran (14) que tanto para 2 como para 3 chimeneas, los stents balón expandibles (como BeGraft), se comprimen menos que los stents autoexpandibles (como Viabahn) debido probablemente a sus diferencias en cuanto a composición y fuerza radial. Si los analizamos en conjunto con la endoprótesis principal, se observa que aquellas combinaciones con materiales de alta fuerza radial (como sería la combinación Endurant-BeGraft) también presentan una menor tasa de compresión del stent paralelo (2 % vs. 18 % y 2 % vs. 15 % de compresión para 2 y 3 stents paralelos respectivamente), aunque parece a expensas de una peor adaptabilidad de la endoprótesis principal, con un significativo mayor mal sellado (22,6 vs. 8,2 mm2 y 23,3 vs. 14,4 mm2 para 2 y 3 stents paralelos respectivamente) en comparación con aquellas combinaciones de baja fuerza radial.
Resultados del análisis de los modelos de stent paralelo tipo sándwich iliaco
Respecto a la mejor manera de calcular la sobredimensión, nuestros resultados muestran (15) que los tres métodos están altamente interrelacionados con un coeficiente de correlación rho prácticamente perfecto (sobredimensión de diámetros en relación con sobredimensión de perímetros y de áreas de 0,097 y de 0,098 respectivamente, p < 0,001). Además, son altamente predecibles entre sí pudiéndose extrapolar los resultados de un método a través de los otros mediante regresión lineal: sobredimensión de diámetro = 63,66 + sobredimensión de perímetro (IC 95% y p no aplicables al ser matemáticamente equivalentes) y sobredimensión de diámetro = 36,62 + 0,534 x sobredimensión de área (IC 95% 34,57-38,66, p < 0,001 y 0,51-0,56, p < 0,001, respectivamente).
Dada la elevada equivalencia entre todos los métodos de medida y su mayor sencillez de cálculo, la sobredimensión de diámetros fue el parámetro de medición utilizado para el resto de comparaciones del estudio mediante la realización de 4 categorías distintas: > 30 %, 30-55 %, 55-75 % y > 75 %.
Respecto el grado óptimo de sobredimensión, nuestros resultados muestran que, a mayor sobredimensión de diámetro, mejor adaptación de los componentes, con una reducción progresiva de las zonas de mal sellado (38,9, 12,3, 5,5 y 2,6 mm2 a sobredimensiones < 30 %, 30-55 %, 55-75 % y > 75 %, respectivamente) aunque a expensas de una mayor compresión del stent paralelo y de un mayor porcentaje de replegado, sobretodo en grados de extremos (> al 55 %) (15) (Tabla II y Fig. 3).
Tabla II. Zonas de mal sellado, compresión y replegado a diferentes valores de sobredimensión de diámetro en los modelos de stent paralelo tipo sándwich


Figura 3. Compresión del stent paralelo (*) y replegado de la endoprótesis principal (flecha) en modelos con 3 stents tipo Viabahn combinados con una endoprótesis Excluder a una sobredimensión del 30% (A) y del 40 % (B).
Se analizó también la mejor combinación de dispositivos evidenciando que, para la iliaca interna, los stents autoexpandibles y los expandibles por balón funcionan de manera similar con una tasa de mal sellado y compresión parecida aunque con una tendencia no significativa (10 vs. 35 %, p = 0,127) a un menor replegado con los stents autoexpandibles como Viabahn (15).
No se evidenció una diferencia estadísticamente significativa respecto a mayor o menor área de mal sellado, compresión o aparición de replegado entre los distintos dispositivos utilizados como stent paralelo para la arteria iliaca externa (endoprótesis Excluder, Aorfix o stents Viabahn).
DISCUSIÓN
Respecto la configuración en chimenea para el tratamiento de los aneurismas sin cuello infrarrenal, se ha evaluado el comportamiento de modelos de chEVAR con 2 y con 3 stents paralelos. Evaluando el grado de sobredimensión, nuestros resultados indican que, a mayor sobredimensión, mejor adaptación de los componentes con una tendencia no significativa a una reducción progresiva las zonas de mal sellado, aunque a expensas de un mayor riesgo de compresión del stent paralelo y sobre todo de replegado, especialmente en los modelos con 3 stents paralelos y sobredimensiones > 30 % (Tabla I).
Por ello, para 2 como para 3 stents paralelos y según nuestros resultados, una sobredimensión de la endoprótesis principal entorno al 30 % se consideraría ideal debido a que asegura el mejor sellado sin asociar un aumento significativo de la compresión del stent paralelo y ni de la aparición de replegado. Este resultado es similar a lo publicado en estudios previos para un único stent paralelo, tanto in vitro (16) como series in vivo (3,17) por lo que el hecho de utilizar más (2 o incluso 3 stents) no debería requerir un cambio en el grado de sobredimensión habitual del 30 %.
Por otro lado, nuestro estudio evidencia peores resultados (peor sellado, más compresión o más replegado) en aquellas combinaciones con 3 stents paralelos respecto aquellas con solo 2. Esto es especialmente importante cuando se usan combinaciones de materiales de baja fuerza radial, como por ejemplo Excluder-Viabahn, a altos grados de sobredimensión con tasas de compresión del stent paralelo y de replegado del 67 % y 100 % de los modelos testados a sobredimensiones del 30 y el 40 % respectivamente (Fig. 3). Estos hallazgos son también acordes a los publicados en el registro clínicos registro PERICLES (4) y el estudio PROTAGORAS (3) donde no se recomienda de rutina la utilización de 3 o más stents paralelos debido a un aumento significativo de oclusión de la rama visceral (relacionado probablemente con un mayor grado de compresión), de endofuga tipo Ia (relacionado probablemente con un mayor replegado) e incluso de mortalidad (5). Así, según nuestros resultados, en caso de plantear la realización de un chEVAR con 3 o más chimeneas, se sugeriría evitar los dispositivos de baja fuerza radial y la sobredimensión excesiva valorando incluso la posibilidad de reducir la misma al 15-30 % (similares zonas de mal sellado y riesgo de compresión que con una sobredimensión estándar del 30 % pero con una mínima probabilidad de replegado).
Respecto a las distintas combinaciones de materiales, nuestros resultados muestran que tanto para 2 como para 3 chimeneas, los stents balón expandibles, se comprimen menos que los stents autoexpandibles. Si los analizamos en conjunto con la endoprótesis principal, se observa que aquellas combinaciones con materiales de alta fuerza radial (como sería la combinación Endurant-BeGraft) también presentan una menor tasa de compresión del stent paralelo, aunque parece a expensas de una peor adaptabilidad de la endoprótesis principal, con un peor sellado en comparación con aquellas combinaciones de baja fuerza radial (Tabla I). Este peor sellado evidenciado no se correlaciona con los hallazgos reportados en registros in vivo (3) sin evidenciar diferencias significativas en cuanto a la tasa de endofugas entre distintos tipos de stent. Esto puede explicarse al hecho que para que una endofuga aparezca no depende exclusivamente de cómo se adaptan los dispositivos entre sí (aunque obviamente a peor adaptación más riesgo), sino que además va condicionado la dinámica de presiones y flujos dentro del saco aneurismático, así como las propiedades fisiológicas de la sangre.
Por tanto, basándonos en nuestros resultados, en los casos de chEVAR con 2 y 3 chimeneas viscerales parece recomendable plantear el uso rutinario de stents balón expandibles como el stent paralelo de elección especialmente en combinación con endoprótesis de alta fuerza radial. Aunque no se ha analizado específicamente en nuestro estudio, se recomienda evitar la combinación de stents autoexpandibles con endoprótesis de alta fuerza radial (como seria por ejemplo la combinación Endurant-Viabahn) por el alto riesgo de compresión del stent paralelo y por tanto de oclusión de la rama visceral.
La segunda parte de este estudio se ha basado en el análisis de un procedimiento de sándwich iliaco, una técnica con unos buenos resultados publicados (1,8,9), aunque muy heterogéneos, y en gran parte basada en experiencias personales con una importante variabilidad en cuanto a materiales y técnica de realización se refiere.
Respecto a la mejor manera de medir la sobredimensión, nuestros resultados muestran una elevada equivalencia entre los tres métodos descritos (sobredimensión de áreas, perímetros o diámetros) con coeficiente de correlación prácticamente perfecto y siendo además altamente predecibles entre sí a través de regresión lineal. Así, según nuestros resultados, el cómputo de la sobredimensión se podría realizar exclusivamente mediante diámetros y su cálculo sería mucho más sencillo (sin tener que calcular perímetros ni áreas), incluso realizable mentalmente.
Basándonos en la sobredimensión de diámetro, se ha analizado también cuál es el mejor grado para conseguir un mejor resultado en el sándwich iliaco (mejor sellado con mejor compresión). Nuestros resultados muestran que a mayor sobredimensión de diámetro mejor adaptación de los componentes, con una reducción progresiva de las zonas de mal sellado, aunque a expensas de una mayor compresión del stent paralelo y de un riesgo mayor de replegado, sobre todo en grados de extremos de sobredimensión (> al 55 %). Así, el grado de sobredimensión ideal debería ser entorno al 30-55 % al asegurar el mejor sellado sin asociar un alto grado de compresión ni de aparición de replegado (Tabla II y Fig. 4).
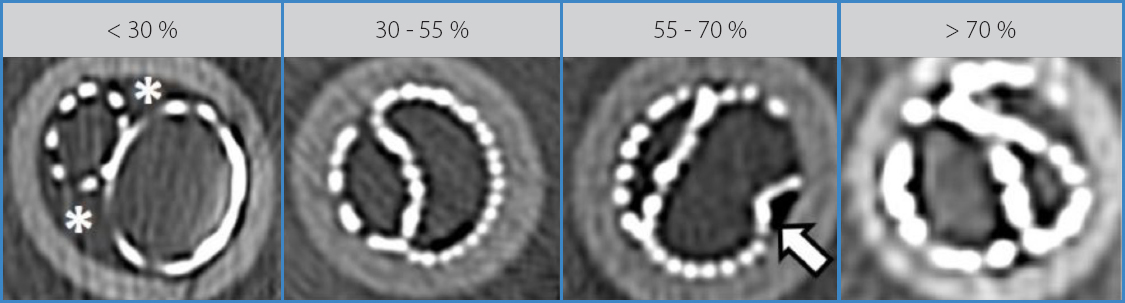
Figura 4. Modelos de sándwich iliaco a diferentes grados de sobredimensión de diámetro, siendo 30-55 % el grado aparentemente ideal consiguiendo el mejor sellado sin aparición de compresión o replegado (flecha).
Es difícil contrastar estos hallazgos con los previamente publicados en la literatura ante la ya comentada escasez y heterogeneidad de la información al respecto. A pesar de ello, si analizamos los dispositivos utilizados en determinadas series clínicas, podemos calcular el grado de sobredimensión de diámetro realizado. Por ejemplo, la serie de Lim (8), reporta la utilización de stents Viabahn entre 6 y 11 mm para la iliaca interna paralelamente a una extensión iliaca externa Aorfix personalizada de 20 mm proximal y 12 mm distal; además ambas están dispuestas en el interior de una extensión iliaca común de 20 mm de diámetro. Si a través de estos datos calculamos la sobredimensión de diámetro (mediante la fórmula {[(d1 + d2) - d3] / d3} x 100) obtenemos un valor de 30-55 % respectivamente en función del stent hipogástrico utilizado, siendo totalmente coincidente con nuestros resultados obtenidos.
Respecto a los materiales a utilizar, nuestro estudio no muestra diferencias significativas entre los distintos dispositivos utilizados salvo una tendencia no significativa a un menor replegado con los stents autoexpandibles como dispositivo para la arteria iliaca interna.
Lamentablemente, tampoco podemos comparar nuestros resultados con lo previamente publicado ya que no existe una recomendación clara en la literatura de cuáles son los mejores dispositivos a utilizar, aunque la mayoría de autores reporta la utilización de stents autoexpandibles, fundamentalmente Viabahn para la iliaca interna (debido a su adaptabilidad) sin un consenso claro en cuanto al dispositivo a utilizar para la iliaca externa.
En este estudio in vitro hemos intentado simular las condiciones anatómicas y técnicas existentes en procedimientos reales de stent paralelo: mismos dispositivos y diámetros, misma técnica quirúrgica, baño salino fisiológico a temperatura corporal, etc. Sin embargo, son evidentes las limitaciones comparativas con un caso real debido a la distinta elasticidad de modelos en comparación con la aorta, la ausencia de presión y flujo pulsátil, las diferencias de composición entre el salino fisiológico y la sangre, la ausencia de angulaciones… Por otra parte, el estudio se ha centrado en el análisis de la mejor combinación de materiales y la mejor sobredimensión pero existen otros parámetros técnicos de igual importancia no evaluados como por ejemplo la distancia de solapamiento entre los dispositivos en los procedimientos de sándwich iliaco. Además, la posibilidad de un evento clínico como una endofuga o la trombosis de un stent visceral no depende exclusivamente de la presencia de mayores zonas de mal sellado o de una mayor compresión del stent sino, también, de condiciones derivadas de las dinámicas de flujos (de entrada y salida al saco aneurismático) y de las propiedades fisiológicas de la sangre, por lo que la extrapolación de nuestros resultados a la práctica clínica diaria debe ser realizada con prudencia.
CONCLUSIONES
En el stent paralelo con 2-3 chimeneas viscerales, la sobredimensión del 30 % se consideraría la idónea al reducir al mínimo las zonas de mal sellado sin generar compresión significativa de la rama visceral ni tampoco replegado. Respecto la mejor combinación de materiales, los dispositivos de alta fuerza radial se comprimen menos, aunque a expensas de una significativa mayor área de zonas de mal sellado sin poder por tanto extrapolar una recomendación clínica específica al respecto.
En la reparación mediante sándwich iliaco, el mejor grado de sobredimensionamiento es una sobredimensión de diámetros entre el 30 y el 55 % al reducir al mínimo las zonas de mal sellado sin generar compresión significativa de la rama visceral ni tampoco replegado. Respecto los materiales, no hay diferencias que apoyen la utilización de una determinada combinación. Con respecto el cálculo de la sobredimensión, las distintas formas de medición evaluadas (áreas, perímetros y diámetros) son equivalentes entre sí, y se recomienda el uso de la sobredimensión de diámetros al simplificar de manera importante el cálculo de la misma.














