INTRODUCCIÓN
La trombosis venosa profunda (TVP) es una patología que puede manifestarse desde edema y dolor de la extremidad hasta producir un embolismo pulmonar (TEP), con una importante morbimortalidad asociada.
Presenta una incidencia anual de entre 50-100 por cada 100 000 habitantes (1). Es más frecuente en mujeres entre los 20 y 40 años, aunque en la franja de 54-60 años es más común en hombres (1).
Su fisiopatología se explica por la tríada de Virchow: estado de hipercoagulabilidad, estasis venoso y daño endotelial, y sus principales factores de riesgo son: cáncer, enfermedad aguda, cirugía, trauma, inmovilidad, obesidad, enfermedades infecciosas o inflamatorias, terapia hormonal, embarazo y trombofilia (1).
OBJETIVOS
El objetivo principal de este estudio es comparar dos estrategias diagnósticas en cuanto a costes y a efectividad:
Estrategia 1: realizar el análisis del dímero D a todos los pacientes con sospecha de TVP efectuando una exploración con eco Doppler a aquellos que resulten positivos.
Estrategia 2: realizar la escala de Wells a todos los pacientes con sospecha de TVP efectuando un análisis del dímero D a aquellos con probabilidad baja y eco Doppler a aquellos con probabilidad modera o alta y a los que presenten un dímero D positivo.
El objetivo secundario, analizar el coste generado en nuestro centro para el diagnóstico de TVP, así como aquellos factores que se hayan asociado a su presentación.
MATERIAL Y MÉTODOS
Se trata de un estudio prospectivo en el que se incluyen los pacientes atendidos por nuestro servicio con sospecha de TVP de extremidad inferior en un periodo de seis meses, entre mayo y octubre de 2019. Se analizaron las variables: encamamiento, parálisis o paresia, cirugía reciente, cáncer activo, trombofilia, antecedente de TVP/TEP, embarazo, clínica de edema, empastamiento, aumento de circulación colateral, diagnóstico alternativo, valor en la escala Wells, presencia de TEP asociado, resultado del dímero D, resultado del eco Doppler venoso y costes generados.
Respecto a los costes, se calcularon según el coste dividido en: atención en urgencias, reactivo del dímero D y realización de eco Doppler, obtenidos del Boletín Oficial de la comunidad (BOCYL) y de la unidad de cobros del hospital.
El análisis estadístico se realizó con el programa SPSS. Se empleó el análisis de χ2 cuando comparamos dos variables cualitativas dicotómicas y el test exacto de Fisher cuando se trataba de una variable cualitativa dicotómica y otra variable cuantitativa. Para analizar la efectividad de las estrategias se calcularon la sensibilidad, la especificidad y los valores predictivos positivo y negativo. Se analizaron los gastos generados por paciente y los gastos que se hubiesen generado con las dos estrategias propuestas.
RESULTADOS
Se obtuvieron 249 pacientes, con una edad media de 70 años (21-95), de los que el 46,59 % (116) presentaron TVP.
En aquellos pacientes con TVP, fue estadísticamente significativo frente a aquellos que no tuvieron TVP la presencia de: género masculino, cáncer, dolor, edema, empastamiento, TEP, obesidad y un menor diagnóstico alternativo (Tabla I).
Tabla I. Características de los pacientes (total de sospechas de TVP) con TVP frente a aquellos sin TVP.

Los costes globales generados en el diagnóstico o descarte de TVP fueron de 47 934,63 € (Tabla II), que entre los 249 individuos de la muestra resultaron de 192,5 € / paciente.
Tras aplicar la escala de Wells, 116 pacientes (46,58 %) tenían una probabilidad baja de presentar TVP, mientras que 133 (53,41 %) tenían una probabilidad media-alta. De los primeros, aquellos con probabilidad clínica pretest baja de TVP, solo 11 (9,4 %) presentaron TVP frente a 105 (78,94 %) de aquellos con probabilidad clínica pretest media-alta.
Para el objetivo primario, se incluyeron solo los pacientes a los que se les había medido el valor de dímero D (n = 144), para así tener una muestra homogénea en ambas estrategias (Fig. 1). Los costes de cada una de ellas fueron los siguientes:
En la estrategia 1:
144 × 101,41 € (atención en Urgencias por sospecha de TVP) + 144 × 3,85 € (dímero D a todas las sospechas) + 138 × 88,86 € (eco Doppler solo a dímeros D positivos) = 14 603,04 € + 554,4 € + 12 262,68 € = 27 420,12 € → 190,41 € / paciente.
En la estrategia 2:
144 × 101,41 € (atención en Urgencias por sospecha de TVP) + 71 × 88,86 € (eco Doppler solo a probabilidad media-alta) + 73 × 3,85 (dímero D a probabilidad baja) + 67 × 88,86 € (eco Doppler a probabilidad baja con dímero D positivo) = 14 603,04 € + 6309,06 € + 281,05 € + 5953,62 € = 27 146,77 → 188,51 € / paciente.
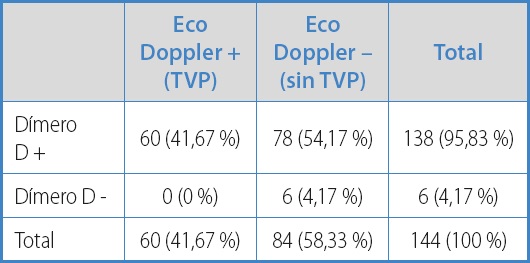
En cuanto al estudio de efectividad de ambas estrategias, la estrategia 1 (Tabla III), basada en el empleo directo del dímero D, obtuvo una sensibilidad del 100 % (los 60 pacientes con TVP presentaban dímero D positivo), una especificidad del 7,1 % (de los 84 pacientes sin TVP, 6 presentaban dímero D negativo), un valor predictivo positivo del 43 % (de los 138 pacientes con dímero D positivo, 60 presentaban TVP) y un valor predictivo negativo del 100 % (los 6 pacientes con dímero D negativo no presentaban ninguno TVP).
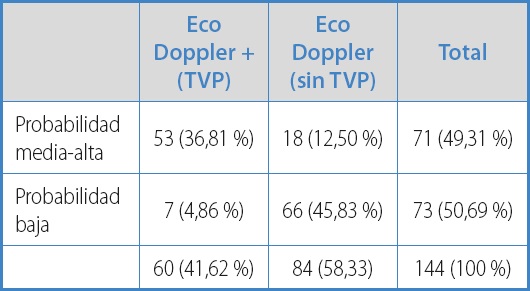
La estrategia 2 (Tabla IV), basada en el empleo de la probabilidad clínica pretest (escala de Wells), obtuvo una sensibilidad del 88,3 % (de los 60 pacientes con TVP, 53 tenían una probabilidad media-alta), una especificidad del 78,57 % (de los 84 pacientes sin TVP, 66 tenían una probabilidad baja), un valor predictivo positivo del 74 % (de los 71 pacientes con probabilidad media-alta, 53 tenían TVP) y un valor predictivo negativo del 90 % (de los 73 pacientes con probabilidad baja, 66 no tenían TVP).
DISCUSIÓN
El coste anual total de la enfermedad tromboembólica venosa se estima de 1,5-12,2 billones de euros en Europa y de 7-10 billones de dólares en Estados Unidos (1-3). Esto supone una importante carga económica para los sistemas sanitarios.
El empleo de algoritmos diagnósticos, en concreto la combinación de la probabilidad clínica con el dímero D antes de la realización del eco Doppler, ha demostrado ser coste-efectivo (4).
En nuestro país, Fuentes y cols. (5) realizaron un estudio coste-efectividad del proceso diagnóstico de la TVP, aunque con características poco comparables al nuestro: como haberse realizado desde Atención Primaria frente al medio hospitalario, los distintos criterios de exclusión y los diferentes costes tanto de la realización de las pruebas diagnósticas como de la atención en Urgencias, al haberse realizado en dos sistemas de salud diferentes. No obstante, concluyen también que el empleo de algoritmos diagnósticos en el diagnóstico de TVP es coste-efectivo.
La sensibilidad descrita del dímero D es aproximadamente del 95 %, con un valor predictivo negativo del 99-100 %, mientras que la especificidad es del 35-55 % (6). En nuestra muestra se ha obtenido una sensibilidad y un valor predictivo negativo del 100 %; sin embargo, la especificidad observada ha resultado menor, del 7,1 %, probablemente debido a las características de la muestra y a sus criterios de inclusión, con un número bajo de pacientes con dímero D negativo atendidos por nuestro servicio, que, aunque es fruto del despistaje inicial en otros servicios, de haberse seguido el algoritmo recomendado debería haber sido ninguno. Es de esperar que en la población general la especificidad sea mayor.
La sensibilidad del eco Doppler se ha descrito del 97 % para TVP proximales y del 73 % para las venas de la pantorrilla (4,7). En nuestra muestra, se ha supuesto una sensibilidad del 100 %, puesto que el resultado positivo en el eco Doppler lo hemos equiparado a la presencia de TVP.
La presencia de falsos negativos en la escala de Wells (para probabilidad baja) se ha descrito en torno al 5 % (8). En nuestra muestra, resultó más alta y el 9,4 % de los pacientes con probabilidad baja presentó TVP.
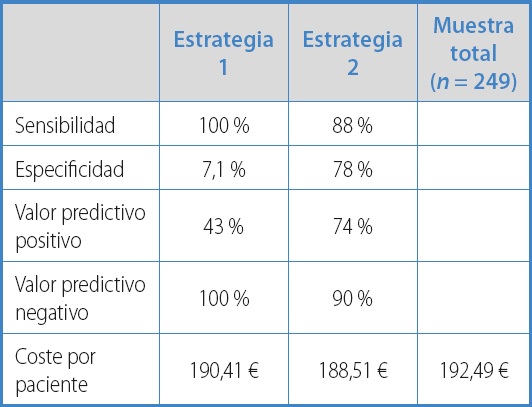
La tabla V muestra una comparación entre las dos estrategias analizadas:
La estrategia 1, que se identifica con el valor del dímero D, tiene su valor en la alta sensibilidad y en el valor predictivo negativo, si bien su baja especificidad y su valor predictivo positivo suponen que su empleo indiscriminado conlleve la realización de mayores pruebas diagnósticas (eco Doppler) a pacientes sin TVP, con el consiguiente aumento del gasto sanitario.
La estrategia 2, que emplea inicialmente la probabilidad clínica pretest (escala de Wells), lo que condiciona a su resultado el análisis o no del dímero D, se identifica con el algoritmo diagnóstico recomendado por las actuales guías de práctica clínica (1,9), lo que corrobora que en nuestro estudio haya demostrado mejores resultados, con una mayor efectividad y menores costes.
La estrategia 2 resultó un 2 % más económica que el gasto generado en nuestro centro. Incluso la estrategia 1, errónea, resultó también más económica, un 1 %, lo que puede deberse al hecho de que se solicitase la valoración y el eco Doppler de 6 pacientes con dímero D negativo.
A pesar de la existencia de dichos algoritmos, la práctica clínica habitual no se adecúa a ellos, lo que produce un sobrecoste y una sobrecarga al sistema, principalmente por la realización de pruebas diagnósticas innecesarias, bien por desconocimiento de dichos algoritmos o por el empleo de medicina defensiva. En nuestra muestra, podría haberse ahorrado un 2 % del gasto generado por paciente.
CONCLUSIÓN
El empleo de algoritmos diagnósticos (en el caso de la TVP, la estratificación de probabilidad clínica inicial [escala de Wells] combinada con el análisis del dímero D en los casos de probabilidad baja) supone una estrategia coste-efectiva para la elección de aquellos pacientes a los que deba realizárseles un eco Doppler.
Se hace necesaria una mayor concienciación sobre la importancia de adecuar el proceso diagnóstico de la TVP por parte de los diferentes profesionales que de él participan, en el que los cirujanos vasculares frecuentemente constituyen tan solo el último escalón.











 texto en
texto en