My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Archivos Españoles de Urología (Ed. impresa)
Print version ISSN 0004-0614
Arch. Esp. Urol. vol.60 n.4 May. 2007
Cirugía robótica en urología pediátrica.
Robotic surgery in pediatric urology.
Carlos R. Estrada y Carlo C. Passerotti.
Childrens Hospital Boston & Harvard Medical School. Boston. MA. USA.
Dirección para correspondencia
RESUMEN
Objetivos: Revisar el uso de la cirugía robótica en urología pediátrica y proporcionar una plataforma desde la que pueda surgir debate con respecto a esta tecnología.
Métodos: Se revisó la literatura disponible y la experiencia en la institución del autor para examinar las aplicaciones de la cirugía robótica en la urología pediátrica. Se realizó una búsqueda en MEDLINE, usando las palabras clave: robot, robótica, laparoscopia, cirugía, niño, y pediatría.
Resultados: La literatura disponible se compone principalmente de casos clínicos y series de casos. Dos grupos han publicado pequeños análisis comparando la pieloplastia laparoscópica asistida por robot con la pieloplastia abierta. En nuestra institución, hemos utilizado el sistema quirúrgico robótico da Vinci® para realizar los siguientes procedimientos quirúrgicos: orquidopexia de testes intraabdominales, nefrectomía total y parcial, pieloplastia desmembrada, pielolitotomía, excisión de divertículos caliciales, ureterostomía, ureteropielostomía, reimplantación ureteral intra y extra vesical, remodelamiento y reimplantación de megaureter, adrenalectomía, derivación cateterizable continente tipo Mitrofanoff, y extirpación de restos pélvicos Mullerianos.
Conclusiones: La cirugía robótica en urología pediátrica es una tecnología en desarrollo y muy prometedora, con posible aplicación en la mayoría de las cirugías urológicas. Los refinamientos en el equipo mejorarán la eficiencia de estos sistemas. En última instancia la eficacia y el papel de los sistemas quirúrgicos robóticos necesitan ser definidos con estudios prospectivos rigurosos que proporcionen comparaciones con las técnicas gold standard, ya sea la cirugía abierta o la laparoscópica convencional.
Palabras clave: Pediátrica. Laparoscopia. Robótica. Cirugía.
SUMMARY
Objectives: To review the use of robotic surgery in pediatric urology and provide a platform from which discussions regarding this technology can arise.
Methods: The available literature and the experience at the authors institution were reviewed to examine the applications of robotic surgery in pediatric urology. MEDLINE was queried using the following key words: robot, robotic, laparoscopy, surgery, child, and pediatrics.
Results: The available literature is comprised mainly of case reports and case series. Two groups have published small analyses comparing robotic assisted laparoscopic pyeloplasty and open pyeloplasty. At our institution, we have utilized the daVinci robotic surgical system to perform the following surgical procedures: orchidopexy of the intraabdominal testis, total and partial nephrectomy, dismembered pyeloplasty, pyelolithotomy, excision of calyceal diverticula, ureteroureterostomy, ureteropyelostomy, intra- and extravesical ureteral reimplantation, megaureter tapering and reimplantation, adrenelectomy, creation of a Mitrofanoff continent catheterizable channel, and resection of pelvic Mullerian remnants.
Conclusions: Robotic surgery in pediatric urology is an evolving technology that holds promise for application to most urological surgeries. Refinements in equipment will improve the efficiency of these systems. Ultimately, the efficacy and role of robotic surgical systems need to be defined with rigorous prospective studies that provide comparisons to gold standard techniques, be they open surgery or conventional laparoscopy.
Key words: Pediatric. Laparoscopy. Robotic. Surgery.
Introducción
La cirugía laparoscópica fue introducida en la urología pediátrica a finales de los 70 por Cortesi y cols., quien describió su utilidad en la evaluación de los testículos no palpables (1). Desde entonces, los abordajes laparoscópicos convencionales han sido utilizados en numerosas cirugías urológicas pediátricas, incluyendo la orquidopexia de testes intra-abdominales (2-15), varicocelectomía (16-23), nefrectomía total y parcial (24-33), pieloplastía (34-40), reimplantación ureteral (41,42), y cirugía reconstructiva de la vejiga (43-45). A pesar de la amplitud de estos procedimientos, los urólogos pediátricos han utilizado la laparoscopia convencional sobre todo para el diagnóstico o cirugía de exéresis y en el manejo de los testículos intra-abdominales. Este tipo de casos tienen en común el no requerir sutura intracorpórea, lo que reduce considerablemente su demanda técnica. Ciertamente, la destreza necesaria para la cirugía laparoscópica urológica reconstructora es alcanzable, pero la curva de aprendizaje es típicamente difícil (46).
Los instrumentos robóticos o asistidos por ordenador (47), fueron introducidos con el objetivo de mejorar la visualización, aumentar la precisión, y reducir la curva de aprendizaje en comparación con la laparoscopia convencional. El sistema quirúrgico robótico disponible en la actualidad, el da Vinci® (Intuitive Surgical, Sunnyvale, CA), ha cumplido estos objetivos en gran parte y ha proporcionado un medio para que incluso los cirujanos laparoscópicamente inexpertos realicen procedimientos reconstructivos complejos. Además, la tecnología proporciona una oportunidad para poner nuevas técnicas en práctica y para que los cirujanos con experiencia laparoscópica mejoren sus capacidades (48). Estos beneficios se deben a la visualización tri-dimensional, los movimientos libres de temblor, la amplitud de los mismos y los seis grados de libertad que proporciona el sistema.
La cirugía pediátrica laparoscópica asistida por robot más extendida es la pieloplastia desmembrada. La eficacia clínica de este procedimiento ha sido demostrada en un estudio reciente que comparó dos cohortes de pacientes de edad similar sometidos a pieloplastia abierta o a pieloplastia laparoscópica asistida por robot (49). Los datos disponibles de otras aplicaciones del sistema robótico da Vinci® en urología pediátrica son limitados, pero nuestro grupo y otros han realizado una variedad de otros procedimientos, incluyendo orquidopexia de testículos intra-abdominales, nefrectomía total y parcial, pieloplastia desmembrada, pielolitotomía, excisión de divertículos calíciales, ureteroureterostomía, ureteropielostomía, reimplantación ureterovesical, remodelamiento y reimplante de megauréter, adrenelectomía, creación de un reservorio urinario continente tipo Mitrofanoff, y resección de restos pélvicos Mullerianos. Los beneficios del sistema robótico en las cirugías antes mencionadas que no requieren sutura intracorpórea son modestos, pero incluyen facilidad de uso para los laparoscopistas menos experimentados y visualización mejorada.
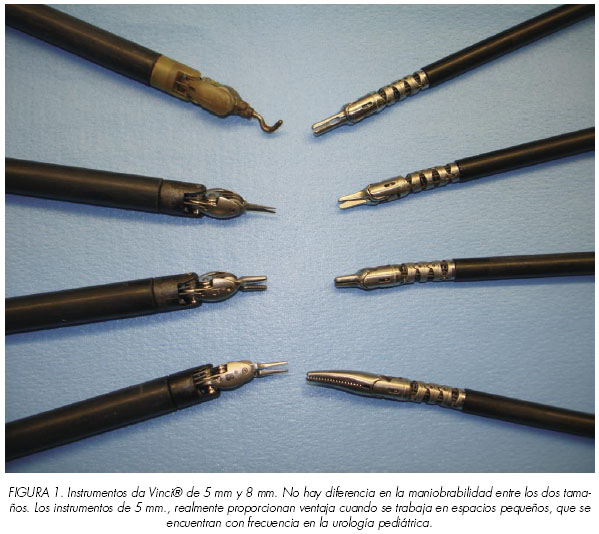
El desarrollo de instrumentos de trabajo más pequeños (5 mm), ha contribuido a la aplicación general del sistema robótico en la cirugía pediátrica (Figura 1). Estos instrumentos proporcionan una importante ventaja sobre los más grandes de 8 mm., cuando se trabaja en espacios y estructuras más pequeños que frecuentemente son el objeto de la urología pediátrica. Además, también está disponible la cámara de 5 mm., aunque la visualización tri-dimensional requiere una óptica de 12mm.
Este artículo revisa la literatura disponible y la experiencia de la institución del autor en cirugía robótica en urología pediátrica. De esta manera, esperamos poder proporcionar una completa y concisa referencia, así como una plataforma desde la que puedan surgir discusiones académicas relacionadas con la cirugía robótica en la urología pediátrica.
Materiales y métodos
La cirugía robótica en urología pediátrica está dando sus primeros pasos. Para revisar los datos sobre esta tecnología, se revisó la literatura disponible y la experiencia de la institución del autor.
La literatura se buscó usando MEDLINE, a través de las siguientes palabras clave: robot, robótica, cirugía, laparoscopia, niño, y pediatría.
En la institución del autor se realizaron las siguientes cirugías robóticas: orquidopexia de testes intra-abdominales, nefrectomía total o parcial, pieloplastia desmembrada, pielolitotomía, excisión de divertículos caliciales, ureteroureterostomía, ureteropielostomía, ureteropielostomía, reimplantación intra y extra vesical, reimplantación y remodelamiento de megauréter, adrenelectomía, creación de un reservorio urinario continente tipo Mitrofanoff, y resección de restos pélvicos Mullerianos. Describiremos en detalle dos de las cirugías robóticas más comúnmente realizadas: la pieloplastia desmembrada y la reimplantación ureteral extravesical.
Resultados y discusión
Revisión de la Literatura
Los trabajos de cirugía robótica en urología pediátrica son limitados. Hay disponibles en la literatura, cinco artículos originales (35, 49-52) cuatro casos clínicos (53-56), y varios artículos de revisión (48, 57). De los cinco manuscritos originales, cuatro tratan de la pieloplastia laparoscópica asistida por robot. Dado el grado de dificultad de la pieloplastia laparoscópica convencional y la frecuencia con la que los urólogos pediátricos tratan estenosis de la unión ureteropélvica (UPU), las ventajas proporcionadas por el sistema robótico hacen de la pieloplastia robótica una opción interesante y por tanto, el objetivo principal de la mayoría de las publicaciones.
En 2005 Atug y cols. (50), informaron por primera vez de la realización de una pieloplastia laparoscópica asistida por robot. En su trabajo inicial, siete pacientes de edades entre 6 y 15 años se sometieron a pieloplastia laparoscópica asistida por robot. Con un seguimiento limitado (mediana de 10.9 meses), seis de los siete pacientes evaluados tuvieron un mejor drenaje, resolución de los síntomas, y evidencia de la ausencia de obstrucción. Ellos concluyeron que la pieloplastia robótica permitía resultados comparables a los de la pieloplastia abierta. Kutikov y cols. informaron de su experiencia en pieloplastia robótica en lactantes con una edad media de 5.6 meses. Los tiempos quirúrgicos fueron cortos (promedio 122 minutos) y sin complicaciones. De los nueve pacientes, en siete (78%) se resolvió o mejoró la hidronefrosis, y todos los pacientes tuvieron evidencia de no obstrucción en el renograma con sobrecarga diurética postoperatorio. Concluyeron que la pieloplastia robótica es un abordaje seguro y viable, incluso en lactantes que necesitan una intervención por estenosis de UPU.
En 2006, dos grupos informaron sobre comparaciones entre pieloplastia robótica y abierta. Lee y cols. (57) realizaron un estudio retrospectivo de 33 pacientes de edades similares, sometidos a pieloplastia robótica y 33 a pieloplastia abierta (49). Informaron de que el abordaje robótico se asoció a una estancia hospitalaria más baja, menor uso de analgésicos y tiempos quirúrgicos similares a los de la cirugía abierta. Con una media de seguimiento de 10 meses, 31 de 33 (94%) pacientes tuvieron resultados satisfactorios en el grupo de pieloplastia robótica. Esto, comparado con el 100% de pacientes con resultados exitosos en la cohorte de cirugía abierta con un seguimiento medio de 12 meses. Aunque el periodo de seguimiento es corto, este análisis demuestra la eficacia y seguridad de la pieloplastia robótica. Yee y cols. informaron de resultados similares cuando compararon también pacientes con edades similares sometidos a pieloplastia robótica (n=8) y a pieloplastia abierta (n=8) (35). Al igual que Lee y cols., informaron que la pieloplastia robótica se asoció con menor estancia hospitalaria y menores requerimientos analgésicos. A diferencia del estudio anterior, estos autores informaron de unos tiempos quirúrgicos considerablemente más largos. Tras un seguimiento medio de 14.7 meses, todos los pacientes de ambos grupos tuvieron resultados exitosos.
Estos datos son esperanzadores e indican que la pieloplastia laparoscópica asistida por robot es una técnica emergente que promete mucho. Ciertamente, se necesitan estudios a largo plazo para evaluar a fondo la eficacia de esta tecnología. Serían ideales ensayos prospectivos y rigurosos comparando la pieloplastia abierta, laparoscópica y robótica, pero difíciles de realizar. La existencia de análisis retrospectivos caracteriza gran parte de la literatura quirúrgica, y si están bien concebidos, bien controlados y son minuciosos, estos estudios pueden definir el futuro de la práctica urológica. Es un hecho, la necesidad de estudios rigurosos para cada aplicación robótica, que informen sobre reproductibilidad y eficacia. Desafortunadamente, el número limitado de centros pediátricos retrasará este deseo. Según se vaya difundiendo la tecnología y los centros actuales acumulen casos, la experiencia colectiva de la comunidad urológica pediátrica necesitará ser comparada y sintetizada para proporcionar recomendaciones fiables.
Experiencia del Childrens Hospital de Boston
Proporcionamos una descripción detallada de dos procedimientos laparoscópicos asistidos por robot que hemos realizado en nuestra institución desde que adquirimos el sistema da Vinci® en el año 2001: pieloplastia desmembrada y reimplante ureteral extravesical.
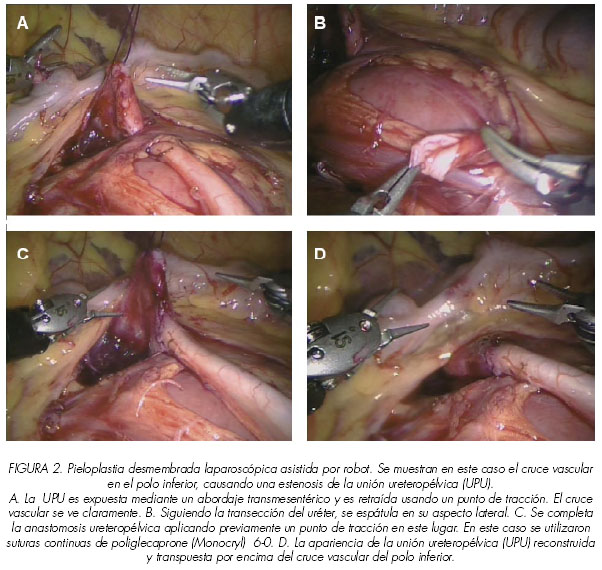
Pieloplastia (Figura 2)
La pieloplastia laparoscópica asistida por robot puede realizarse vía abordaje transperitoneal o retroperitoneal. Hemos utilizado, casi exclusivamente el abordaje transperitoneal; el único caso que fue realizado vía retroperitoneal fue técnicamente difícil por el pequeño espacio de trabajo no pudiendo controlar el cruce vascular en el polo inferior que resultó en una reparación infructuosa. En el abordaje transperitoneal, una vez anestesiado el paciente, se coloca una sonda Foley, y el paciente en decúbito supino. Se coloca una cuña de 30º bajo la teórica localización de la UPU del lado afecto, y se asegura el paciente a la mesa. Se prepara el campo quirúrgico desde el apéndice xifoides a la sínfisis púbica. Se colocan tres puertos: un puerto para la cámara sobre el ombligo, un puerto de trabajo en la línea media entre el ombligo y el apéndice xifoides y un segundo puerto de trabajo en la línea medio clavicular debajo del ombligo. Preferimos la técnica abierta para la colocación del primer puerto, y los demás bajo visión directa. Aseguramos todos los puertos con suturas fasciales que al final se usarán para cerrar la fascia. Se puede colocar un cuarto puerto para ayudar en la retracción, cambio de agujas, etc., pero lo encontramos innecesario. Además en los sistemas da Vinci® equipados con un cuarto brazo robótico, se puede colocar un tercer brazo de trabajo para su utilización. Nuestro sistema robótico es, sin embargo, el original de tres brazos, y por lo tanto no tenemos experiencia con el de cuatro.
Después de la colocación de los puertos, se inclina al paciente 60º y se acopla el robot sobre el hombro ipsilateral. La exposición de la unión ureteropélvica (UPU) se realiza a través de un abordaje trans-mesentérico por la izquierda o mediante maniobra de decolación. Se realiza entonces la disección del uréter y de la pelvis renal de la misma manera que se haría en cirugía abierta. Además se mantienen los mismos principios de manejo delicado y cuidadoso del tejido. Para ayudar en la visualización y reconstrucción de la unión ureteropélvica, se coloca un punto de tracción sobre la pelvis renal para elevarla. Este punto se puede continuar a través de la pared abdominal y asegurarlo fuera del paciente con ajustes realizados por el cirujano ayudante de ese lado, o se asegura internamente a la pared abdominal.
Se hace una incisión en la pelvis renal, e inmediatamente se espátula el uréter lateralmente para preservar su orientación. La anastomosis ureteropélvica se realiza usando sutura absorbible 5-0, 6-0 ó 7-0. Se puede utilizar suturas continuas o puntos sueltos. Después de que se ha completado el aspecto posterior de la anastomosis, se debe considerar el drenaje a utilizar. Nosotros rutinariamente drenamos nuestras pieloplastias robóticas usando stents ureterales doble J. El stent se puede colocar de manera anterograda continuando la introducción del mismo stent en la cavidad abdominal por medio de un angiocatéter. El catéter doble -J del tamaño apropiado se avanza distalmente dentro del uréter con la ayuda de una guía. Se retira luego la guía y la parte proximal del stent se coloca en la pelvis renal. Para confirmar su correcta colocación, se puede llenar la vejiga con azul de metileno diluido y el reflujo del mismo se debería ver en extremo proximal del catéter. Como alternativa, se puede colocar inmediatamente antes de la cirugía por medio de un abordaje cistoscópico retrógrado. En casi todos los casos, utilizamos la técnica de colocación anterógrada. Tras la colocación del catéter, se completa el resto de la anastomosis. Otra opción posible es la utilización del catéter renal tipo Kiss (58). Este abordaje proporciona drenaje percutáneo, permitiendo el flujo anterógrado de orina a través de la anastomosis, con la opción de realizar estudios de contraste anterógrados. Nosotros no usamos de forma rutinaria los drenajes tipo Penrose.
El catéter Foley se retira a las 24 horas y la mayoría de los pacientes se encuentran en condiciones de ser dados de alta en uno o dos días. Si se deja catéter ureteral doble J, se retirará en 4 semanas. Los resultados de este abordaje en nuestra institución y en otras son excelentes y comparables a los de la cirugía abierta (35, 49, 50, 52).
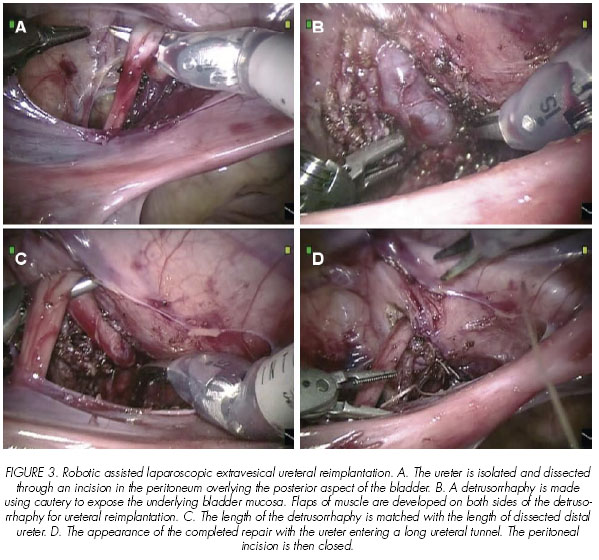
Reimplantación Ureteral Extravesical (Figura 3)
La reimplantación ureteral extravesical se realiza esencialmente igual que la abierta con la técnica de Lich-Gregoir. Robóticamente se puede realizar uni o bilateralmente. A diferencia del Lich-Gregoir abierto bilateral, no hemos experimentado retención urinaria postoperatoria como complicación (observación sin publicar).
El paciente una vez anestesiado es colocado en posición supina sobre la mesa de quirófano. Se separan las piernas y se prepara al paciente desde el apéndice xifoides al periné. Se coloca una sonda de Foley que permita su movilización durante la cirugía. Al igual que en otras cirugías robóticas, preferimos colocar el puerto de la cámara umbilical usando técnica abierta (Hasson). Dos puertos de trabajo se colocan en la línea medio clavicular, aproximadamente a 1 cm., por debajo del ombligo. Se aseguran todos los puertos con suturas de la pared abdominal que son usadas para cerrar la fascia al final del caso. Tras ello, se coloca al paciente en posición de Trendelenburg, y el robot se acopla sobre los pies del paciente. Se moviliza el intestino proximalmente para exponer el fondo de la pelvis, y se hace una incisión transversal en el peritoneo anterior al útero y sobre la pared posterior de la vejiga. El uréter se localiza lateral a la vejiga y se diseca en una longitud de 4-6 cm., con cuidado para mantener su suministro de sangre intacto. Se aplica un punto de tracción en la pared posterior de la vejiga y se fija a la pared abdominal anterior para ayudar en la exposición durante la realización de la detrusorrafia.
La detrusorrafía se realiza de la misma forma que en la técnica abierta de Lich Gregoir. Se secciona y coagula el detrusor hasta el nivel de la mucosa, que debería permanecer intacta. Si se perforara la mucosa, se cerrará con una sutura crómica 5-0. La longitud del túnel debe ser suficiente para cubrir la longitud del uréter distal disecada, 3-4 cm., son normalmente suficientes. Se crean flaps musculares a ambos lados de la detrusorrafia, y se cierran sobre el uréter con puntos sueltos de polyglactin (Vicryl®) 4-0. El cierre debe avanzar desde distal a proximal o proximal a distal. Se debe tener cuidado de no cerrar el túnel demasiado, y no retorcer el uréter, ya que cualquiera de ellas podría resultar en obstrucción ureteral. Se cierra la incisión peritoneal con una sutura continua absorbible.
No se necesita un catéter Foley postoperatorio a menos que se haya perforado la mucosa, en cuyo caso el catéter permanece 24 horas. Los pacientes estarán listos para ser dados de alta al día siguiente de la cirugía o en el día uno del postoperatorio.
Conclusiones
La cirugía robótica en la urología pediátrica es una disciplina en desarrollo que parece muy prometedora. Permite la reconstrucción de los tejidos más delicados de una forma que parece beneficiar tanto al paciente como a su familia. La eficacia y eficiencia de la cirugía robótica en nuestro campo necesita todavía definirse y se requieren estudios bien concebidos, construidos y ejecutados para definir su papel. Las mejoras del equipo así como el aumento de la disponibilidad internacional de aparatos permitirán y fomentará una utilización más amplia y confirmará la relativamente pequeña experiencia colectiva informada en la actualidad.
Agradecimientos
Los autores agradecen al Dr. Craig Peters, pionero de la cirugía laparoscópica y robótica en el Childrens Hospital Boston. Gran parte de la experiencia en nuestra institución es suya, y su consejo e innovación han enseñado e inspirado a la nueva generación de urólogos pediátricos a ejercer la cirugía mínimamente invasiva.
Bibliografía y lecturas recomendadas (*lectura de interés y ** lectura fundamental)
*1. CORTESI, N.; FERRARI, P.; ZAMBARDA, E. y cols.: Diagnosis of bilateral abdominal cryptorchidism by laparoscopy. Endoscopy, 8: 33, 1976. [ Links ]
*2. ABOLYOSR, A.: Laparoscopic versus open orchiopexy in the management of abdominal testis: a descriptive study. Int. J. Urol., 13: 1421, 2006. [ Links ]
*3. ESPOSITO, C.; DAMIANO, R.; GONZALEZ SABIN, M.A. y cols.: Laparoscopy-assisted orchidopexy: an ideal treatment for children with intra-abdominal testes. J. Endourol., 16: 659, 2002. [ Links ]
*4. ESPOSITO, C.; GARIPOLI, V.: The value of 2-step laparoscopic Fowler-Stephens orchiopexy for intra-abdominal testes. J. Urol., 158: 1952, 1997. [ Links ]
*5. GILL, I.S.; ROSS, J.H.; SUNG, G.T. y cols.: Needlescopic surgery for cryptorchidism: the initial series. J. Pediatr. Surg., 35: 1426, 2000. [ Links ]
*6. HAY, S.A.; SOLIMAN, H.A.; ABDEL RAHMAN, A.H. y cols.: Laparoscopic classification and treatment of the impalpable testis. Pediatr. Surg. Int., 15: 570, 1999. [ Links ]
*7. HUMKE, U.; SIEMER, S.; BONNET, L. y cols.: Pediatric laparoscopy for nonpalpable testes with new miniaturized instruments. J. Endourol., 12: 445, 1998. [ Links ]
*8. LAW, G.S.; PEREZ, L.M.; JOSEPH, D.B.: Two-stage Fowler-Stephens orchiopexy with laparoscopic clipping of the spermatic vessels. J. Urol., 158: 1205,1997. [ Links ]
*9. LINDGREN, B.W.; DARBY, E.C.; FAIELLA, L. y cols.: Laparoscopic orchiopexy: procedure of choice for the nonpalpable testis?. J. Urol., 159: 2132, 1998. [ Links ]
*10. PAPPARELLA, A.; PARMEGGIANI, P.; COBELLIS, G. y cols.: Laparoscopic management of nonpalpable testes: a multicenter study of the Italian Society of Video Surgery in Infancy. J. Pediatr. Surg., 40: 696, 2005. [ Links ]
*11. POENARU, D.; HOMSY, Y.L.; PELOQUIN, F. y cols.: Laparoscopic management of the impalpable abdominal testis. Urology, 42: 574, 1993. [ Links ]
*12. RADMAYR, C.; OSWALD, J.; SCHWENTNER, C. y cols.: Long-term outcome of laparoscopically managed nonpalpable testes. J. Urol., 170: 2409, 2003. [ Links ]
*13. SAMADI, A.A.; PALMER, L.S.; FRANCO, I.: Laparoscopic orchiopexy: report of 203 cases with review of diagnosis, operative technique, and lessons learned. J. Endourol., 17: 365, 2003. [ Links ]
*14. TACKETT, L.D.; WACKSMAN, J.; BILLMIRE, D. y cols.: The high intra-abdominal testis: technique and long-term success of laparoscopic testicular autotransplantation. J. Endourol., 16: 359, 2002. [ Links ]
*15. WACKSMAN, J.; BILLMIRE, D.A.; LEWIS, A.G. y cols.: Laparoscopically assisted testicular autotransplantation for management of the intraabdominal undescended testis. J. Urol. 156: 772, 1996. [ Links ]
*16. BARQAWI, A.; FURNESS, P.; KOYLE, M.: Laparoscopic Palomo varicocelectomy in the adolescent is safe after previous ipsilateral inguinal surgery. BJU Int., 89: 269, 2002. [ Links ]
*17. ESPOSITO, C.; MONGUZZI, G.; GONZALEZ-SABIN, M.A. y cols.: Results and complications of laparoscopic surgery for pediatric varicocele. J. Pediatr. Surg. 36: 767, 2001. [ Links ]
*18. ESPOSITO, C.; MONGUZZI, G.L.; GONZALEZ- SABIN, M.A. y cols.: Laparoscopic treatment of pediatric varicocele: a multicenter study of the italian society of video surgery in infancy. J. Urol., 163: 1944, 2000. [ Links ]
*19. KOYLE, M.A.; OOTTAMASATHIEN, S.; BARQAWI, A. y cols.: Laparoscopic Palomo varicocele ligation in children and adolescents: results of 103 cases. J. Urol., 172: 1749, 2004. [ Links ]
*20. NG, W.T.; WONG, M.K.; BOOK, K.S. y cols.: Laparoscopic varicocelectomy in pediatric patients. Urology, 46: 121, 1995. [ Links ]
*21. PINTUS, C.; RODRIGUEZ MATAS, M.J.; MANZONI, C. y cols.: Varicocele in pediatric patients: comparative assessment of different therapeutic approaches. Urology, 57: 154, 2001. [ Links ]
*22. PODDOUBNYI, I.V.; DRONOV, A.F.; KOVARSKII, S.L. y cols.: Laparoscopic ligation of testicular veins for varicocele in children. A report of 180 cases. Surg. Endosc., 14: 1107, 2000. [ Links ]
*23. SUN, N.; CHEUNG, T.T.; KHONG, P.L. y cols.: Varicocele: Laparoscopic clipping and color Doppler follow-up. J. Pediatr. Surg., 36: 1704, 2001. [ Links ]
*24. CHEE-AWAI, R.A.; CHANDHOKE, P.S.; KOYLE, M.A.: Laparoscopic nephrectomy in children. Semin. Laparosc. Surg., 5: 47, 1998. [ Links ]
*25. DAS, S.; KEIZUR, J.J.; TASHIMA, M.: Laparoscopic nephroureterectomy for end-stage reflux nephropathy in a child. Surg. Laparosc. Endosc., 3: 462, 1993. [ Links ]
*26. DIAMOND, D.A.; PRICE, H.M.; McDOUGALL, E.M. y cols.: Retroperitoneal laparoscopic nephrectomy in children. J. Urol., 153: 1966, 1995. [ Links ]
*27. EL-GHONEIMI, A.; VALLA, J.S.; STEYAERT, H. y cols.: Laparoscopic renal surgery via a retroperitoneal approach in children. J. Urol., 160: 1138, 1998. [ Links ]
*28. FIGENSHAU, R.S.; CLAYMAN, R.V.; KERBL, K. y cols.: Laparoscopic nephroureterectomy in the child: initial case report. J. Urol., 151: 740, 1994. [ Links ]
*29. JANETSCHEK, G.; SEIBOLD, J.; RADMAYR, C. y cols.: Laparoscopic heminephroureterectomy in pediatric patients. J. Urol., 158: 1928, 1997. [ Links ]
*30. SYDORAK, R.M.; SHAUL, D.B.: Laparoscopic partial nephrectomy in infants and toddlers. J. Pediatr. Surg., 40: 1945, 2005. [ Links ]
*31. YAO, D.; POPPAS, D.P.: A clinical series of laparoscopic nephrectomy, nephroureterectomy and heminephroureterectomy in the pediatric population. J. Urol., 163: 1531, 2000. [ Links ]
*32. LEE, R.S.; RETIK, A.B.; BORER. J.G. y cols.: Pediatric retroperitoneal laparoscopic partial nephrectomy: comparison with an age matched cohort of open surgery. J. Urol., 174: 708, 2005. [ Links ]
*33. KOYLE, M.A.; WOO, H.H.; KAVOUSSI, L.R.: Laparoscopic nephrectomy in the first year of life. J. Pediatr. Surg., 28: 693, 1993. [ Links ]
*34. KUTIKOV, A.; RESNICK, M.; CASALE, P.: Laparoscopic pyeloplasty in the infant younger than 6 months--is it technically possible?. J. Urol. 175: 1477, 2006. [ Links ]
**35. YEE, D.S.; SHANBERG, A.M.; DUEL, B.P. y cols.: Initial comparison of robotic-assisted laparoscopic versus open pyeloplasty in children. Urology, 67: 599, 2006. [ Links ]
*36. SCHWAB, C.W.; HYUN, G.; GARIBAY-GONZALEZ, F. y cols.: Transperitoneal laparoscopic pyeloplasty for pelvic kidneys with ureteropelvic junction obstruction in children: technique and preliminary outcomes. Jsls, 10: 307, 2006. [ Links ]
*37. SCHWAB, C.W.; CASALE, P.: Bilateral dismembered laparoscopic pediatric pyeloplasty via a transperitoneal 4-port approach. J. Urol., 174: 1091, 2005. [ Links ]
*38. SCHIER, F.: Laparoscopic Anderson-Hynes pyeloplasty in children. Pediatr. Surg. Int., 13: 497, 1998. [ Links ]
*39. PETERS, C.A.; SCHLUSSEL, R.N.; RETIK, A.B.: Pediatric laparoscopic dismembered pyeloplasty. J. Urol., 153: 1962, 1995. [ Links ]
*40. METZELDER, M.L.; SCHIER, F.; PETERSEN, C. y cols.: Laparoscopic transabdominal pyeloplasty in children is feasible irrespective of age. J. Urol., 175: 688, 2006. [ Links ]
*41. BALDWIN, D.D.; POPE, J.C.; ALBERTS, G.L. y cols.: Simplified technique for laparoscopic extravesical ureteral reimplantation in the porcine model. J. Endourol., 19: 502, 2005. [ Links ]
*42. EHRLICH, R.M.; GERSHMAN, A.; FUCHS, G.: Laparoscopic vesicoureteroplasty in children: initial case reports. Urology, 43: 255, 1994. [ Links ]
*43. POPPAS, D.P.; UZZO, R.G.; BRITANISKY, R.G. y cols.: Laparoscopic laser assisted auto-augmentation of the pediatric neurogenic bladder: early experience with urodynamic followup. J. Urol., 155: 1057, 1996. [ Links ]
*44. KOK, K.Y.; SENEVIRATNE, H.S.; CHUA, H.B. y cols.: Laparoscopic excision of congenital bladder diverticulum in a child. Surg. Endosc., 14: 501, 2000. [ Links ]
45. HEDICAN, S.P.; SCHULAM, P.G.; DOCIMO, S.G.: Laparoscopic assisted reconstructive surgery. J. Urol., 161: 267, 1999. [ Links ]
46. PETERS, C.: Laparoscopy in paediatric urology: adoption of innovative technology. BJU Int., 92: 52, 2003. [ Links ]
**47. GUILLONNEAU, B.: What robotics in urology? A current point of view. Eur. Urol., 43: 103, 2003. [ Links ]
**48. PASSEROTTI, C.; PETERS, C.A.: Robotic-assisted laparoscopy applied to reconstructive surgeries in children. World J. Urol., 24: 193, 2006. [ Links ]
**49. LEE, R.S.; RETIK, A.B.; BORER, J.G. y cols.: Pediatric robot assisted laparoscopic dismembered pyeloplasty: comparison with a cohort of open surgery. J. Urol., 175: 683, 2006. [ Links ]
**50. ATUG, F.; WOODS, M.; BURGESS, S.V. y cols.: Robotic assisted laparoscopic pyeloplasty in children. J. Urol., 174: 1440, 2005. [ Links ]
**51. PETERS, C.A.; WOO, R.: Intravesical robotically assisted bilateral ureteral reimplantation. J. Endourol., 19: 618, 2005. [ Links ]
**52. KUTIKOV, A.; NGUYEN, M.; GUZZO, T. y cols.: Robot assisted pyeloplasty in the infant-lessons learned. J. Urol., 176: 2237, 2006. [ Links ]
*53. PEDRAZA, R.; PALMER, L.; MOSS, V. y cols.: Bilateral robotic assisted laparoscopic heminephroureterectomy. J. Urol., 171: 2394, 2004. [ Links ]
*54. YEE, D.S.; KLEIN, R.B.; SHANBERG, A.M.: Case report: robot-assisted laparoscopic reconstruction of a ureteropelvic junction disruption. J. Endourol., 20: 326, 2006. [ Links ]
*55. YEE, D.S.; SHANBERG, A.M.: Robotic-assisted laparoscopic ureteroureterostomy in an adolescent with an obstructed upper pole system and crossed renal ectopia with fusion. Urology, 68: 673, 2006. [ Links ]
*56. PEDRAZA, R.; WEISER, A.; FRANCO, I.: Laparoscopic appendicovesicostomy (Mitrofanoff procedure) in a child using the Da Vinci robotic system. J. Urol., 171: 1652, 2004. [ Links ]
*57. LEE, R.S.; BORER, J.G.: Robotic surgery for ureteropelvic junction obstruction. Curr. Opin. Urol., 16: 291, 2006. [ Links ]
*58. ZRITCHIE, E.; REISMAN, E.M.; ZAONTZ, M.R. y cols.: Use of kidney internal splint/stent (KISS) catheter in urinary diversion after pyeloplasty. Urology, 42: 55, 1993. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Carlos R. Estrada
Childrens Hospital Boston
Dept. of Urology
300 Longwood Avenue, HU390
Boston, MA 02115. U.S.A.
carlos.estrada@childrens.harvard.edu











 text in
text in