Introducción
La enfermedad renal crónica (ERC) es considerada un problema de salud pública a nivel mundial. Se estima que una de cada 10 personas sufre algún grado de disfunción renal que progresa de manera silenciosa, con mayor frecuencia de manifestaciones clínicas en estadios avanzados, las cuales generalmente son irreversibles y afectan de manera significativa la calidad de vida1. Para el año 2010 la prevalencia global de la enfermedad se estimó en el 10,4% en los hombres y en el 11,8% en mujeres; además, el número total de personas con ERC reportadas alrededor del mundo para ese año fue de más de 400 millones, la mayoría provenientes de países en desarrollo2.
El progreso de esta entidad está asociado al desarrollo de enfermedad renal crónica terminal (ERCT) y posterior terapia de reemplazo renal (TRR), además de a un gran deterioro cardiovascular, metabólico, cognitivo y al aumento en la mortalidad dentro de este grupo de pacientes3.
El aumento en la incidencia de diabetes mellitus (DM) e hipertensión arterial (HTA), así como el pobre control de lípidos y hábitos como el tabaquismo se correlacionan con el registro acelerado de nuevos casos de enfermedad renal4,5, la gran mayoría aún en estadios iniciales6, lo que significa que en muchos pacientes se pueden aplicar estrategias para prevenir el progreso a fases terminales mediante un control y tratamiento oportunos, incluso en los que, aún sin la enfermedad, se encuentran en riesgo y son susceptibles también a mecanismos de prevención. En Latinoamérica la prevalencia de ERCT con TRR ha aumentado significativamente; para el año 2010, la prevalencia de diálisis en países latinoamericanos fue de 660 por cada millón de habitantes; el trasplante renal se estimó en 19,1 casos por cada millón de habitantes7.
La Organización Mundial de la Salud (OMS) propuso implementar programas de protección renal (PPR) con el objetivo de impactar en la carga global de ERC, mejorar sus indicadores e implementar medidas de control y prevención8. En consecuencia, se encuentran grandes estudios como el KEEP y el NHANES III, cuyo objetivo ha sido la detección temprana de la enfermedad, con énfasis en las poblaciones más susceptibles, que identifican factores de riesgo y de pronóstico con el fin de reducir el impacto en la salud de estos pacientes9. En Latinoamérica se han creado estrategias similares: en México se creó una versión del KEEP10, mientras que países como Uruguay y Chile, entre otros, han creado programas nacionales que promueven el diagnóstico temprano, la atención oportuna y la prevención del deterioro de la enfermedad y de la calidad de vida11-14.
En Colombia, la ERC se entiende como una enfermedad de alto costo desde 1993. De acuerdo con la legislación colombiana, las entidades promotoras de salud (EPS) afilian a los pacientes al Sistema de Seguridad Social y, en general, proveen prevención secundaria y TRR15. Este estudio pretendió evaluar la efectividad de un PPR en Colombia, determinada mediante el progreso de estadio en ERC y el requerimiento de TRR.
Métodos
Diseño del estudio
Estudio analítico con seguimiento a 2 cohortes dinámicas de pacientes con diagnóstico de ERC, que pretende comparar el comportamiento de los indicadores clínicos, de laboratorio y de deterioro renal entre los pacientes expuestos a un PPR y quienes estaban bajo TC.
Ambiente y participantes
La población estudiada fue el censo de usuarios de 2 EPS colombianas. De manera retrospectiva, se recogió información registrada en las historias clínicas electrónicas de ambas aseguradoras desde el año en que empezó el PPR hasta el momento en que comenzó el estudio. Luego, en forma prospectiva hasta completar 5 años de seguimiento. Los criterios de inclusión fueron: el haber estado afiliado a la EPS durante el tiempo de seguimiento y cumplir criterios KDOQI para ERC16,17. Se excluyó a los menores de 15 años y a quienes hubiesen estado registrados en ambas instituciones en algún momento del estudio. El inicio del seguimiento se entendió como el momento de diagnóstico de ERC o el ingreso al PPR. Se contó con el aval ético del IRB/IEC de las instituciones involucradas.
Programa de protección renal vs. tratamiento convencional
El PPR es una estrategia de prevención secundaria compuesta por un protocolo de citas educativas y asistenciales, con exámenes clínicos y de laboratorio periódicos, además, se concentra en la búsqueda activa de pacientes en riesgo. Está conformada por un primer nivel de atención, el cual hace seguimiento a pacientes en estadios tempranos de ERC con médicos generales y enfermeras, además de 2 citas por año con Medicina Interna y Nutrición. El segundo nivel atiende a pacientes desde el estadio 3, con citas por Medicina Interna, Nefrología y Nutrición en forma trianual o bimensual según el estadio. Los exámenes de laboratorio se realizan el mes anterior a la cita, según la guía técnica del PPR.
Por otro lado, el TC brinda atención de primer nivel tanto para los pacientes en riesgo como para los que tenían diagnóstico de ERC; la remisión a un especialista se realiza según el criterio del médico general tratante, una vez el paciente consultaba a necesidad. No se aplica una guía o protocolo de atención; tampoco hay búsqueda activa de pacientes.
Variables
De exposición: estar expuesto a PPR versus el TC.
Las variables consideradas como criterios para el diagnóstico de ERC fueron: depuración de creatinina menor de 60 ml/min (medida por la prueba de Cockroft-Gault), alteración de la ecografía renal, proteinuria mayor de 150 mg/día, alteración del sedimento urinario y, en diabéticos, microalbuminuria mayor de 30 mg16,17.
Variables dependientes: tiempo desde el diagnóstico hasta el primer progreso de estadio y tiempo desde el diagnóstico hasta el requerimiento de TRR.
Variables independientes: las características clínicas y de laboratorio.
Fuente de datos y mediciones
Se extrajo información a partir de las bases de datos suministradas por cada EPS, y por los datos provenientes de la captación progresiva desde las historias clínicas de los pacientes durante el tiempo del estudio.
Tamaño del estudio
Se analizó el censo de población de ambas aseguradoras que cumplía criterios diagnósticos de ERC según KDOQI.
Variables cuantitativas: los marcadores clínicos presión arterial sistólica, presión arterial diastólica, glucemia en ayunas, hemoglobina glucosilada (HbA1c), colesterol total, triglicéridos, lipoproteínas de baja y alta densidad (LDL, HDL) y creatinina, se recodificaron en forma dicotómica como controlado/no controlado a partir de lo reconocido en la literatura científica para cada parámetro clínico en relación con el padecimiento de ERC. El valor de referencia para definir a una variable como controlada fueron: presión arterial sistólica menor de 130 mmHg, presión arterial distólica menor de 80 mmHg, glucemia menor de 140 mg/dL, HbA1c menor de 7%, colesterol total menor de 200 mg/dL, triglicéridos menor de 150 mg/dL, LDL menor de 100 mg/dL, HDL mayor de 40 mg/dL y creatinina menor de 1,2 mg/dL16,17. La tasa de filtación glomerular se tuvo en cuenta como variable de progresión en función de cada uno de los estadios. En algunos de los análisis se prefirió agrupar variables como la edad, el estado civil, el estadio, el total de citas y los marcadores clínicos.
Métodos estadísticos
Se caracterizó a la población al diagnóstico de ERC mediante distribuciones de frecuencia y proporciones para las variables cualitativas; para las cuantitativas se utilizaron medidas de estadística descriptiva y de dispersión; adicionalmente se observó la distribución mediante la prueba de normalidad de Kolmogorov-Smirnov o de Shapiro Wilk. Para establecer diferencias entre PPR y TC se usaron las pruebas t de Student o U de Mann-Whitney según la distribución de las variables.
Se calculó la tasa de incidencia para los diferentes desenlaces entre PPR y TC. Para esto, en el numerador se tuvo en cuenta el número de casos nuevos tanto de primer progreso como de requerimiento de TRR registrados en cada cohorte y como denominador, los años de exposición a partir del diagnóstico de ERC, respectivamente. Además, se estimó la razón de tasas de incidencia con sus intervalos de confianza (IC) al 95%.
Se analizaron las curvas de supervivencia de Kaplan Meier para progreso de estadio y requerimiento de TRR por aseguradora, ambos modelos ajustados por las diferentes covariables y, además, por 2 subgrupos según estadios: 1 y 2 como entradas tempranas y 3 y 4 como tardías; el estadio, la edad y el sexo en forma comparativa (prueba de log rank), para comparar el progreso de cada estadio. La influencia de la exposición al PPR sobre cada una de las variables dependientes ajustadas por las demás variables de interés se determinó mediante un análisis de riesgos proporcionales de Cox. En este caso, para la comparación de progreso, se asumieron como referencia los estadios 3 y 4 como estadios tardíos que progresaban menos y no se tuvo en cuenta el estadio 5, pues no progresaba más. Por el contrario, para comparar el requerimiento de TRR se asumieron como referencia los estadios tempranos 1 y 2, pues los tardíos representaron mayor riesgo del desenlace. Las covariables fueron incluidas en los modelos a partir de criterios clínico y estadístico (Hosmer Lemeshow: p < 0,25). Se verificó el cumplimiento del supuesto de proporcionalidad de los riesgos gráficamente y con análisis de residuales de Scaledsch y Schoenfeld en Stata 11.
Resultados
Participantes y datos descriptivos
Se consultaron 9.887 historias clínicas, de las cuales el 56,5% correspondían a pacientes del PPR, mientras que 43,5% eran del TC. En total, 5.663 pacientes cumplieron criterios de inclusión, el 74,2% provenían del PPR y el 25,8% del TC. Durante el tiempo de seguimiento se registraron 509 retiros (8,9%), 1.010 pérdidas (17,8%) y 312 muertes (5,5%). Las personas pertenecientes al PPR tenían edades significativamente menores que las que fueron tratadas con TC, con una mediana de 66 (16-100) y 70 (20-97) años, respectivamente. El grupo de TC presentó mayor proporción de hombres (64,5%; p < 0,001).
Las comorbilidades de mayor frecuencia para ambos grupos fueron, en su orden, la hipertensión (HTA) (94,67% para PPR y 85,01% para TC; p < 0,001); la dislipidemia (60,42% en PPR y 63,8% en TC; p = 0,023) y la DM (36,2% en PPR y 32,65% en TC; p = 0,014). Más del 30% de los pacientes pertenecientes al PPR se encontraban en estadios 1 y 2, mientras que se encontraban en dichos estadios únicamente el 16,7% de los pacientes con TC.
Resultados principales
Los pacientes expuestos al PPR se demoraron más en hacer el primer progreso de estadio, en requerir la primera hospitalización y en requerir TRR, comparados con los del TC. Todas estas diferencias fueron clínica y estadísticamente significativas (tabla 1).
Tabla 1 Meses desde el diagnóstico hasta diferentes desenlaces en pacientes con ERC en 2 EPS colombianas
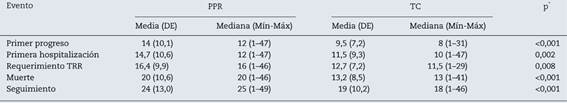
DE: desviación estándar; Máx: máximo; Min: mínimo.
*Prueba U de Mann-Whitney.
Dentro del grupo expuesto a PPR, el 24% progresaron de estadio, y solo progresó un 17,7% de los pacientes en TC (p < 0,001). Por otra parte, la proporción de pacientes que requirieron TRR al final del seguimiento fue mayor en TC (5,1%) que en PPR (4,8%) (p = 0,802).
Progreso de estadio y tasa de filtración glomerular
Los pacientes del PPR progresaron más en los primeros estadios. Adicionalmente, en estadios tardíos, ambas cohortes mostraron la tendencia a permanecer; sin embargo, los pertenecientes a PPR lograban un mejor control del deterioro renal, al conseguir, en mayor proporción, el retroceso de estadio (fig. 1).
Se observó menor afectación en la tasa de filtración glomerular de los pacientes del PPR al diagnóstico, al primer y al último cambio de estadio (tabla 2). Al analizar únicamente a los pacientes que progresaron durante el seguimiento, se encontró que los pertenecientes al PPR presentaron, tanto al diagnóstico como al primer y último cambio de estadio, tasas de filtración glomerular más favorables que los del TC. Dichas diferencias son clínica y estadísticamente significativas (prueba U de Mann-Whitney con p < 0,001 para los 3 momentos).
Tabla 2 Evolución de la TFG en pacientes, con ERC en 2 EPS colombianas

DE: desviación estándar; Máx: máximo; Min: mínimo.
*Prueba U de Mann-Whitney.
En el grupo de pacientes que requirieron TRR durante el seguimiento, se observó que los pertenecientes al PPR presentaron, tanto al diagnóstico como al primer y último cambio de estadio, mejores tasas de filtración glomerular que los del TC, aunque solo la primera de dichas diferencias fue estadísticamente significativa (prueba U de Mann-Whitney con p = 0,022; 0,191; 0,051, respectivamente).
Incidencia de progreso y requerimiento de terapia de reemplazo renal
Al finalizar el tiempo del estudio, se registraron diferencias en las tasas de incidencia (TI) para progreso de estadio y requerimiento de TRR en ambos grupos. En el PPR 204 pacientes necesitaron TRR mientras que en TC fueron 74. Como resultado, se evidencia una TI para progreso con mayor afectación para TC (0,050; IC 95% 0,040-0,064) que para PPR (0,034; IC 95%: 0,030-0,039), la razón de la tasa de incidencia para dicho desenlace fue 1,480 (IC 95%: 1,21-1,90). La tasa de incidencia de progreso de estadio no mostró diferencias significativas entre los grupos.
Supervivencia
En las curvas de Kaplan Meier ajustadas por subgrupos y a las demás covariables, se encuentra, en ambos modelos, que quienes pertenecían al PPR progresaron menos y presentaron menor requerimiento de TRR (figs. 2 y 3).
Modelo de riesgos proporcionales de Cox
Progreso de estadio: en el modelo de riesgos, ajustado por subgrupos según estadio y por las diferentes covariables, se observó que la exposición al PPR resultaba protectora para el progreso de estadio (HR: 0,855; IC 95%: 0,740-0,988), lo cual fue estadísticamente significativo; se evidenció la influencia de la edad (HR: 1,623; IC 95%: 1,429-1,843), HTA (HR: 1,55; IC 95%: 1,209-1,988) y DM (HR: 1,216; IC 95%: 1,085-1,362) sobre el progreso de estadio. Además, quienes pertenecían a estadios tempranos tenían mayor riesgo instantáneo de progresar (HR: 4,039; IC 95%: 3,554-4,590) y la dislipidemia resultó protectora (tabla 3).
Tabla 3 Riesgo instantáneo para primer progreso de estadio ajustado a covariables en pacientes con ERC
| HR | IC 95% | p | |
|---|---|---|---|
| Programa de protección renal | 0,855 | 0,740-0,988 | 0,034 |
| Estadio 1-2 | 4,039 | 3,554-4,590 | <0,001 |
| Edad | 1,623 | 1,429-1,843 | <0,001 |
| Hipertensión arterial | 1,550 | 1,209-1,988 | 0,001 |
| Diabetes mellitus | 1,216 | 1,085-1,362 | 0,001 |
| Dislipidemia | 0,891 | 0,794-0,999 | 0,048 |
| Sexo (hombres) | 0,896 | 0,803-1,000 | 0,051 |
Requerimiento de terapia de reemplazo renal
El riesgo instantáneo de requerir TRR fue menor en PPR (HR: 0,797; IC 95%: 0,606-1,049), sin embargo, no fue estadísticamente significativo. Por otro lado, el estar en estadios tardíos de la enfermedad aumentaba de manera clara el riesgo de requerir TRR (HR: 4,909; IC 95%: 3,10-7,776). Esta diferencia fue estadísticamente significativa. Comorbilidades como la DM aumentaron el riesgo instantáneo de requerir TRR (HR: 2,080; IC 95%: 1,637-2,643). La edad y el sexo, aunque suponían un riesgo mayor para este desenlace, no fueron estadísticamente significativas. Por otra parte, la dislipidemia se tornó protectora (tabla 4).
Tabla 4 Riesgo instantáneo para requerimiento de TRR ajustado a covariables en pacientes con ERC
| HR | IC 95% | p | |
|---|---|---|---|
| Programa de protección renal | 0,797 | 0,606-1,049 | 0,106 |
| Estadio 3-4 | 4,909 | 3,100-7,776 | <0,001 |
| Edad | 0,778 | 0,605-1,001 | 0,051 |
| Hipertensión arterial | 1,545 | 0,784-3-043 | 0,209 |
| Diabetes mellitus | 2,080 | 1,637-2-643 | <0,001 |
| Dislipidemia | 0,657 | 0,516-0,837 | 0,001 |
| Sexo (hombres) | 0,852 | 0,672-1,080 | 0,187 |
Discusión
Este estudio muestra como un PPR representa una estrategia de prevención secundaria en pacientes con ERC, pues disminuye de manera efectiva el deterioro renal en esta población en términos de progreso de estadio, desarrollo de ERCT y posterior requerimiento de TRR. Adicionalmente, evidencia que la estrategia de captación temprana de estos pacientes se relaciona directamente con dichos desenlaces.
Para tratarse de un estudio realizado en Latinoamérica, contamos con un número nada despreciable de pacientes diagnosticados con ERC (5.663), comparado con los estudios de referencia como el KEEP y el NHANES III en los que se incluyó a 16.689 y 2.734 pacientes con diagnóstico de ERC, respectivamente9. Como referentes en Latinoamérica, están el KEEP México que contó con 3.539 participantes con ERC10 y Uruguay, con 2.219 pacientes11. Como factor común para cada uno de estos estudios, al igual que en nuestro caso, entre las comorbilidades más prevalentes estaban la HTA y la DM.
Ambas cohortes del estudio fueron similares desde el punto de vista socioeconómico, pues cada aseguradora cubría a población vinculada laboralmente, de la misma región del país y, para efectos de nuestro análisis, ambas cohortes cumplieron criterios diagnósticos para ERC y presentaron comorbilidades proporcionalmente parecidas, como se evidenció en los resultados. Sin embargo, en términos de accesibilidad, es importante resaltar que la diferencia radicó en que el PPR realizaba búsqueda activa, mientras que en el TC se usaba el método de consulta a demanda. Lo anterior no debe ser entendido como existencia de barreras diferenciales de acceso a los servicios para ambas poblaciones: el PPR brindaba una atención mediante protocolos estructurados, lo cual se vio reflejado en desenlaces más favorecedores, de ahí nuestra intención de mostrar que, en la medida en que los agentes sanitarios consigan implementar dichos programas y se capte tempranamente a los pacientes, se podrán lograr mejores resultados en salud.
Quienes hacían parte del PPR tenían edades significativamente menores que los del TC, y también se encontraban en estadios más tempranos de la enfermedad; por la estrategia de captación temprana de pacientes con diagnóstico de ERC o en riesgo, era esperable que su población fuera más joven y estuviera en estadios iniciales. El concepto de captación temprana es el punto de partida para el manejo oportuno de una gran mayoría de las enfermedades, pues de este depende el éxito del diagnóstico y tratamiento de los pacientes. Brown et al. reconocieron la importancia de la captación temprana en poblaciones susceptibles a padecer ERC, basados en que existe una gran proporción de pacientes con factores de riesgo poco controlados, incluyendo tasas de filtración glomerular disminuidas, que no están identificados como posibles enfermos renales18.
Quienes pertenecían al PPR tardaron más tiempo en hacer el primer progreso de estadio, requerir la primera hospitalización y TRR. Sin embargo, por tratarse de una estrategia de captación temprana se registraron más progresos en estadios tempranos dentro de esta aseguradora. Se esperaba que quienes pertenecían al PPR, por ser captados más jóvenes y en estadios más tempranos, presentaran más posibilidades de progresar de estadio, mientras que los estadios avanzados, incluso en ambas aseguradoras, progresaran poco o nada, pues a partir de estos (4 y 5) se habla de etapas finales de la enfermedad, en las que el último desenlace es la TRR. Sin embargo, nuestro estudio evidenció el potencial de las estrategias de prevención para retrasar dicho progreso.
El deterioro renal, medido en términos de TFG, fue menor entre los pacientes del PPR, pues estos registraron menores TFG tanto al diagnóstico como al primer y último cambio de estadio. Adicionalmente, la tasa de incidencia de requerimiento de TRR fue menor en dicha aseguradora. Lo anterior evidencia que estar expuesto a un PPR mejora de manera significativa las condiciones clínicas y el pronóstico de pacientes con ERC, pues cursan con mejores TFG, entre otros marcadores clínicos de importancia, además de que hay una menor proporción de pacientes que requieren TRR.
Se observó que el riesgo de progresar de estadio fue mayor en PPR. Lo anterior debido a que dicha aseguradora, a través de la estrategia de captación temprana, contaba con la mayoría de sus pacientes en estadios 1, 2 y 3, por lo tanto, progresaban más comparados con los que estaban en TC. Sin embargo, el riesgo de requerir TRR fue mayor en TC, esto debido igualmente a la captación temprana ausente en dicha aseguradora, por lo que la mayoría de sus pacientes se encontraban en estadios avanzados y con un pobre acceso a atención multidisciplinaria, pues no hacía parte del protocolo de dicha estrategia. Por lo tanto, se esperaba que progresaran más.
Cuando se analizó el riesgo ajustado de progresar de estadio y el riesgo de requerir TRR, se encontró la HTA y la DM como factores de riesgo importantes para dichos desenlaces. Sin embargo, la dislipidemia se encontró protectora, lo cual corresponde al fenómeno de epidemiología inversa, pues aunque la dislipidemia es ampliamente conocida como un estado que potencia la morbimortalidad, en el caso de pacientes con ERC, especialmente en estadios avanzados, representa un claro factor protector. Iseki et al. encontraron que los bajos niveles de lípidos se comportaban como marcador de inflamación y desnutrición en enfermos renales19. Además, Kilpatrick et al. establecieron que los altos niveles de colesterol total, LDL y triglicéridos representaban un mejor pronóstico en pacientes en diálisis. Lo anterior, basado en que los niveles séricos de lípidos, entendidos como medida indirecta de la reserva energética, resultan más favorecedores incluso estando en los límites superiores, pues contrarrestan los efectos del estado proinflamatorio y los bajos niveles de albúmina derivados de las pobres condiciones nutricionales por las que generalmente cursan los pacientes con enfermedad avanzada20. Jurkovitz et al. estudiaron los factores de riesgo asociados a la progresión de la ERC en los pacientes del KEEP. Encontraron que, al igual que en nuestro estudio, la HTA, la DM y la dislipidemia eran las comorbilidades de mayor prevalencia en pacientes con ERC. Esta población no contaba con un adecuado control de dichos factores de riesgo cardiovasculares: únicamente los pacientes que cursaban los estadios finales de la enfermedad mostraron tener un mejor control de dichas comorbilidades, pues eran quienes accedían con mayor frecuencia a la atención con nefrólogo y otros especialistas. Los pacientes en estadios iniciales generalmente no eran evaluados por Nefrología ni por otra especialidad, por lo que contaban con un pobre control de los factores de riesgo21.
Como limitaciones del estudio se encuentran posibles sesgos de medición, pues se siguió más a una de las poblaciones, por lo que se espera un mayor número de desenlaces, además de la ausencia de registro de dichos desenlaces en la población seguida por menos tiempo.
Este estudio representa un aporte acerca de la efectividad de programas de prevención secundaria en pacientes diagnosticados con ERC. Los resultados evidencian el potencial protector que brinda un PPR para el deterioro renal en esta población; cuando se entiende la necesidad de la captación temprana teniendo en cuenta los factores de riesgo y las comorbilidades asociadas en este grupo de pacientes, se logran adaptar las estrategias que determinan de manera positiva la evolución de la enfermedad, reducir el número de pacientes que progresan a estadios avanzados e incluso disminir el riesgo de desarrollar ERCT de y requerir TRR. De esta manera se logra una mejor y más oportuna atención, que mejora la supervivencia y las condiciones de vida de estos pacientes.

















