My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Nutrición Hospitalaria
On-line version ISSN 1699-5198Print version ISSN 0212-1611
Nutr. Hosp. vol.22 n.4 Madrid Jul./Aug. 2007
Nutrición parenteral modular: ¿un nuevo concepto?
Modular parenteral nutrition: a new concept?
J. M. Llop Talaverón. J. J. Machí Ribes, B. Gracia García, M.ª B. Badía Tahull, M.ª Tubau Molas y R. Jódar Masanes
Servicio de Farmacia. Hospital Universitari de Bellvitge. Hospitalet de Llobregat. Barcelona. España.
Dirección para correspondencia
RESUMEN
Introducción: Definimos Nutrición Parenteral Modular (NPM) como las mezclas de nutrición parenteral (NP) obtenidas a partir de la adición de diferentes macronutrientes a preparados estándar (NPE) tanto binarios (aminoácidos y glucosa) como ternarios (aminoácidos, lípidos y glucosa).
Objetivos: El objetivo de este estudio es demostrar que utilizando la NPM se pueden ajustar las fórmulas de NP a las necesidades individuales de cada paciente y disminuir la carga de trabajo.
Material y métodos: Estudio retrospectivo de casos y controles de las NP preparadas durante el primer semestre de los años 1995, 2000 y 2005. Las NP se subdividen en: estándar (NPE) -dispensadas sin manipular-, individualizadas (NPI) y modulares. Se comparan los protocolos en los diferentes periodos, y para evaluar la carga de trabajo se relaciona el volumen de fluido trasvasado con el volumen total preparado. Se aplican los tests de chi cuadrado y t de Student con significación para p < 0,05.
Resultados: En 1995 prácticamente sólo se utilizaban fórmulas individualizadas. En el año 2000 se introdujeron NPE y NPM para las fórmulas de mantenimiento y las de estrés moderado. Finalmente, en el año 2005 se ha incluido el concepto modular para fórmulas de estrés severo y/o inmunomoduladoras. Como consecuencia de estos cambios, en el protocolo se observa una disminución de las NPI debido a la introducción progresiva de las NPM. En 1995 la NPM representaba un 2,6% del total de elaboraciones, aumentando a un 64,7% en el 2000 y a un 74,7% en el 2005. Este hecho se ha traducido en una disminución en el volumen trasvasado a través del sistema volumétrico de elaboración. En 1995 se trasvasó el 87,3% del volumen total, en el 2000 el 34,3% y finalmente en el 2005 pasó a ser sólo de un 20,6% (diferencias estadísticamente significativas entre los tres periodos; p < 0,05).
En el año 2005 se elaboraron 543 NPI, de las cuales 169 (31,1%) fueron para pacientes con encafalopatía hepática o con insuficiencia renal aguda no dializados. A las NPM elaboradas durante este mismo periodo, se ha incorporado: glutamina, emulsiones lipídicas de aceite de pescado, lípidos estructurados, lípidos de patrón de oliva, soluciones poliiónicas y micronutrientes específicos.
Discusión: La NPM permite adecuar las fórmulas de NP a un amplio abanico de situaciones clínicas, aunque en determinadas patologías siguen siendo imprescindibles las formulaciones individualizadas. La utilización de NPM se traduce en una disminución de fórmulas individualizadas que se refleja en una menor carga de trabajo.
Palabras clave: Nutrición parenteral modular. Preparados estándar. Fórmulas individualizadas. Protocolo parenteral. Necesidades individuales.
ABSTRACT
Introduction: We may define Modular Parenteral Nutrition (MPN) as parenteral nutrition (PN) mixtures obtained from adding different macronutrients to standard formulations (SPN) both binary (amino acids and glucose) and ternary (amino acids, lipids, and glucose).
Objectives: The aim of this study is to demonstrate that PN formulations may be adapted to individual needs of each patient and workload may be reduced by using MPN.
Material and methods: Case-control retrospective study of PN prepared during the first semester of the years 1995, 2000, and 2005. PN are categorized in: standard (SPN) -given without manipulation-, individualized (IPN), and modular parenteral nutrition (MPN). The protocols are compared at the different periods, and the volume of transferred fluid is related with total prepared volume in order to calculate the workload. The Chi squared and student's t tests with a significance level of p < 0.05 are used.
Results: In 1995, virtually only individualized formulations were used. In the year 2000, SPN and MPN were introduced as maintenance formulas as well as those for moderate stress. Finally, in the year 2005, the modular concept has been introduced for severe stress and/or immunomodulatory formulas. As a result of these changes, we observe in the protocol a decrease in IPN due to progressive introduction of MPN. In 1995, MPN represented 2.6% of all elaborations, increasing up to 64.7% in 2000, and to 74.7% in 2005. This fact has resulted in a decrease in transferred volume through the volumetric elaboration system. In 1995, 87.3% of the total volume was transferred, in the year 2000 34.3%, and finally in 2005 only 20.6% (the differences between the three periods are statistically significant; p < 0.05).
In the year 2005, 543 IPN were elaborated, of which 169 (31.1%) were for patients with liver encephalopathy or non-dialyzed acute renal failure. The following ingredients have been added to MPN during that same period: glutamine, fish oil lipid emulsions lipídicas, structured lipids, olive-pattern lipids, polyionic solutions, and specific micronutrients.
Discussion: MPN allows for adapting PN formulas to a wide range of clinical situations, although individualized formulations still are irreplaceable for some pathologies. The use of MPN is associated with a decrease in individualized formulas that reflects in lower workload.
Key words: Modular Parenteral Nutrition. Standard products. Individualized formulas. Parenteral protocol. Individual needs.
Introducción
El aumento de la presión asistencial, junto con el establecimiento de guías de nutrición clínica, ha dado lugar a la elaboración de protocolos y a la estandarización de las formulaciones de nutrición parenteral (NP)1,2. Esta situación ha impulsado la comercialización de preparados estándar binarios (aporte proteico y glucídico) y terciarios o "todo en uno" (aporte de nitrogenado, glúcidos y lípidos)3. La composición de estas fórmulas se basa en las recomendaciones de consenso generales de soporte nutricional por lo que con su administración se puede cubrir una amplia gama de situaciones clínicas y metabólicas4. Por lo tanto, en el momento actual nos encontramos ante dos alternativas para la NP: la utilización de productos estandarizados (NPE) o la intervención nutricional mediante formulaciones individualizadas (NPI). Así, mientras que el mayor conocimiento de las alteraciones metabólicas específicas de ciertas situaciones clínicas permite un abordaje individualizado, la utilización de fórmulas estandarizadas supone un ahorro de tiempo y dinero sin que, en ausencia de una situación clínica compleja (insuficiencia renal, encefalopatía), se comprometa el estado clínico del paciente. Sin embargo, entre estos dos escenarios nos encontramos con un abanico de situaciones clínicas y metabólicas en las que la utilización de preparados estándar presenta algunos inconvenientes, como son la no incorporación de nutrientes específicos (farmaconutrientes) o la rigidez en la composición que hace que no se adapten a perfiles clínicos más específicos (estrés, sepsis, hipoalbuminemia severa, alteraciones hepáticos, hipertriglilceridemias, alteraciones electrolíticas)2,5,6.
Nuestro protocolo de NP se basa en un número limitado de fórmulas establecidas según las características y la situación clínica del paciente. Para dar respuesta a la mayor complejidad clínica y metabólica del paciente, el protocolo está en constante evolución incorporando tanto nuevos preparados estándar, como la evidencia científica acerca de la utilización de inmunonutrientes y los cambios de las guías de práctica clínica. En un intento de adaptar mejor las fórmulas de NP a las diferentes situaciones clínicas y complicaciones metabólicas introducimos el concepto Nutrición Parenteral Modular (NPM) que definimos como mezclas de NP obtenidas a partir de la adición de diferentes macronutrientes a preparados estándar.
Por otra parte, respondiendo a la normativa de calidad en la preparación de NP (RD 175/2001 de 23 de febrero7), hemos introducido un sistema automatizado de control volumétrico para la elaboración de fórmulas (Bomba MicroMacro® 23 Baxa Compounder) en sustitución del sistema manual de mezclas que suponía múltiples manipulaciones y que limitada el control final al control visual del volumen transferido. Esta tecnología automatizada implica mayor exactitud en la composición final y garantiza la trazabilidad del proceso tanto en productos como en manipuladores8,9. En contrapartida, el nuevo sistema de elaboración enlentece el proceso, de tal forma que el volumen de líquidos perfundido es proporcional al tiempo de elaboración de la fórmula y a la carga de trabajo del personal técnico.
Por tanto, con la introducción del nuevo concepto de NPM conseguimos por un lado ajustar la NP a la situación clínica y metabólica del paciente sin recurrir a la NPI y por otro lado reducir la carga de trabajo ya que el volumen de líquido a trasvasar es menor.
El objetivo de este estudio es demostrar que utilizando la NPM se pueden ajustar las fórmulas de NP a las necesidades individuales de cada paciente y disminuir la carga de trabajo.
Material y métodos
Se realiza un estudio retrospectivo de casos y controles de las NP preparadas en el Hospital Universitario de Bellvitge para los pacientes hospitalizados, durante el primer semestre de los años 1995, 2000 y 2005. Se utilizan como controles las NP elaboradas en el primer semestre de 1995. Las NP se subdividen en: NPE (dispensadas sin manipular), NPM (obtenidas al añadir componentes específicos a la bolsa estándar) y NPI (elaboradas a partir de la adición de los componentes por separado).
La prescripción inicial de la NP se realizó según el protocolo en curso que aparece reflejado en la hoja de petición de NP y en la orden médica informatizada. Se optó por uno de los tres tipos de elaboraciones en función de la situación clínica y metabólica del paciente. Durante el seguimiento metabólico realizado desde el servicio de farmacia se evaluaron semanalmente las analíticas (bioquímicas y hematológicas) de los pacientes y se adaptó la composición de la fórmula según el protocolo interno establecido.
Se compararon los protocolos de los tres períodos estudiados. Para evaluar la carga de trabajo se relaciona el volumen de fluido trasvasado con el volumen total preparado. La significación estadística de los cambios producidos en las NP elaboradas de cada tipo y en los volúmenes trasvasados se calculó mediante los tests de chi cuadrado y t de Student con significación para p < 0,05.
Resultados
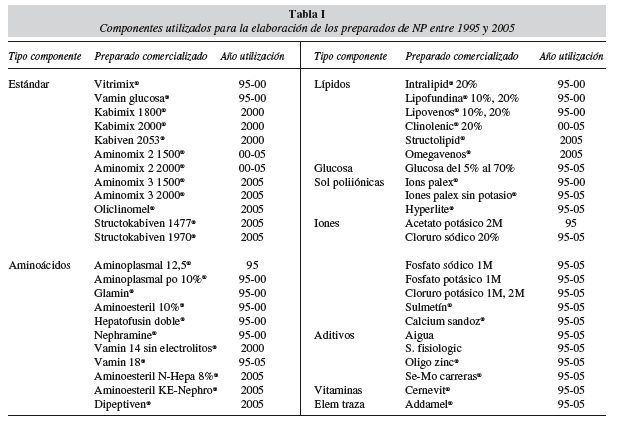
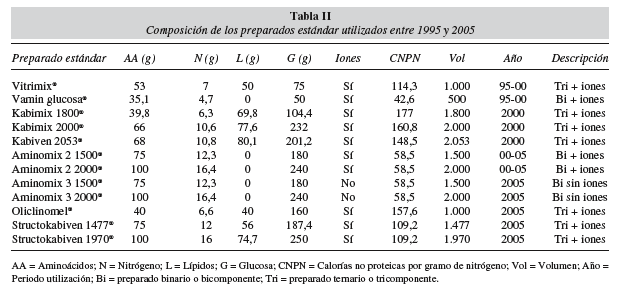
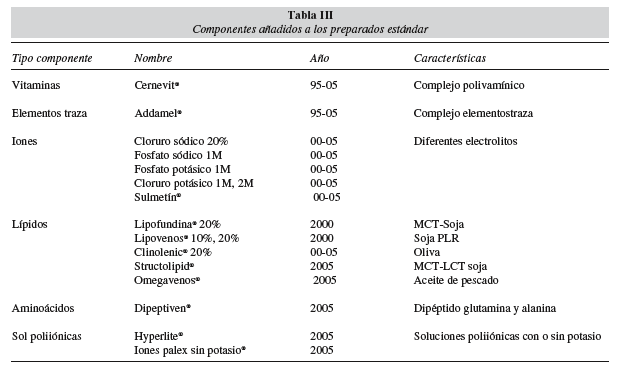
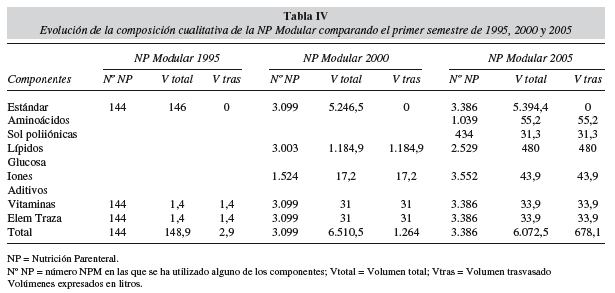
Los componentes utilizados para elaborar los preparados de NP en los tres períodos estudiados se detallan en la tabla I. La composición de las fórmulas estándares utilizadas como base y los componentes adicionados para obtener la fórmula de NPM final durante los tres periodos estudiados se incluyen en las tablas II y III. En la tabla IV se muestra la evolución de la NPM en función de los componentes utilizados para conseguir adaptar la fórmula de NP a las necesidades del paciente durante los tres periodos estudiados.
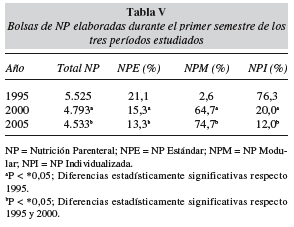
En la tabla V se muestra la distribución de los tipos de NP elaborados en los períodos estudiados. En 1995 prácticamente sólo se utilizaron fórmulas individualizadas (76,3%) y el pequeño porcentaje de preparados estándar (21,1%) se utilizó en situaciones de inicio de NP o para nutrición mixta con enteral/oral (Vamin glucosa® y principalmente Vitrimix®). En este año se introducen los primeros preparados de NPM, obtenidos por la adición de vitaminas y elementos traza a los preparados estándar disponibles.
En el 2000 se produce el primer cambio cualitativa y cuantitativamente importante, debido a la posibilidad de adecuar NPE y NPM para nutrir en fases de mantenimiento y de estrés moderado. Se incorporaron nuevos preparados estándar binarios (Aminomix 2®) y ternarios (Kabimix®, Kabiven®) con electrolitos y mayor cantidad de nitrógeno y glucosa. A estos preparados estándar, además de vitaminas y elementos traza, se les añaden iones para cubrir los trastornos electrolíticos y, sobre todo, se combinan preparados binarios con emulsiones lipídicas para obtener el patrón lipídico más adaptado a la situación del paciente. Con este cambio en el protocolo, aumenta la proporción de NPM (64,7%).
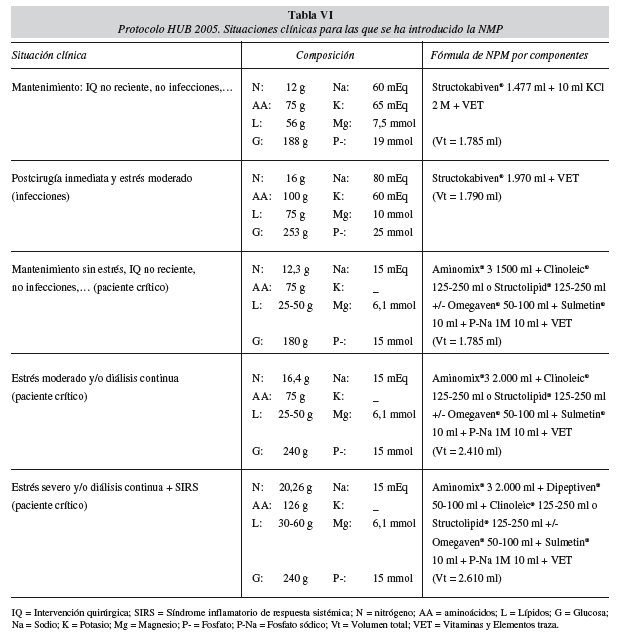
En el 2005 ha sido posible utilizar NPM en situaciones clínicas más complejas, como puede verse en el protocolo de la tabla VI, incrementando la proporción NPM (74%). En este período se introdujeron preparados estándar ternarios (Oliclinomel® y Structokabiven®) con mejor ratio de calorias no proteicas por gramo de nitrógeno y con un perfil lipídico (oleico y estructurado MCT/LCT) adecuado a una amplia gama de situaciones de estrés. Además, con la introducción de emulsiones con lípidos estructurados (Structolipid®) más fáciles de metabolizar se consiguió incluir en la NPM a los pacientes críticos de cuidados intensivos. Posteriormente, para poder dar una respuesta rápida a los desequilibrios hidroelectrolíticos de estos pacientes se introdujeron los preparados binarios sin electrolitos (Aminomix 3®), paralelamente a las soluciones poliiónicas con o sin potasio (Hyperlite® e Iones palex sin potasio®). Finalmente, con la incorporación al protocolo de dos componentes catalogados como farmaconutrientes, Dipeptiven® (dipéptido de glutaminaalanina) y Omegaven® (aceite de pescado con alto contenido de ácidos grasos omega 3) se consiguió diseñar NPM con propiedades inmunomoduladoras, sin tener que recurrir a NPI. La adición de Dipeptiven® a preparados ternarios (Structokabiven®) permite aumentar el aporte de nitrógeno en pacientes con hipoalbuminemia severa. De hecho, en la tabla IV, en el apartado referente a NPM 2005, los 55,2 litros de volumen trasvasado del componente aminoácido corresponden en su totalidad a Dipeptiven®.
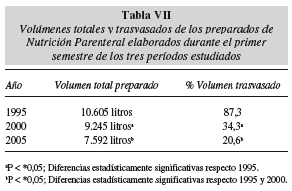
Analizando los datos globalmente, debido a los cambios en el protocolo se observa una sustitución progresiva de las NPI por NPM que se corresponde con una disminución estadísticamente significativa en el volumen trasvasado a través del sistema automatizado de control volumétrico (Bomba MicroMacro® 23 Baxa Compounder) (tabla VII).
De las 543 NPI elaboradas en 2005, 169 (31,1%) fueron para pacientes con encefalopatía hepática o con insuficiencia renal aguda no dializados, ya que no existen NPE que cubran el perfil de aminoácidos necesarios en estas situaciones clínicas.
Discusión
En el momento actual, en muchos casos todavía se contemplan la NPE y la NPI como las dos únicas opciones para abordar el soporte nutricional por vía parenteral. Así nos encontramos que, aunque en líneas generales el aporte calórico total, las necesidades de nutrientes específicos, la relación de calorías no proteicas por gramo de nitrógeno y la relación glucosa/lípidos se ha estandarizado para la mayoría de situaciones clínicas, la variabilidad clínica del paciente hace que la NPE no pueda generalizarse y que pacientes en situaciones clínicas complejas necesiten un soporte nutricional individualizado y específico5,6. Por lo tanto, lo que nosotros definimos como NPM, es un paso intermedio que permite la incorporación de diversos nutrientes a los preparados estándar binarios y ternarios para conseguir adecuar las fórmulas a la mayoría de las situaciones clínicas con requerimientos específicos.
El único componente proteico incorporado a la NPM es el Dipeptiven (dipéptido glutamina-alanina). La glutamina es el aminoácido libre que está en mayor proporción en el cuerpo humano. Es un precursor que proporciona nitrógeno para la síntesis de purinas, pirimidinas, nucleótidos, aminoglucósidos y glutatión; siendo además el sustrato más importante para la amoniogénesis renal (regulación ácido-base). La glutamina es un transportador de nitrógeno entre diferentes tejidos y representa el mayor recurso energético en las células del tracto gastrointestinal. Su adición tiene un papel destacado en la reversión de hipoalbuminemias moderadas y severas, en pacientes con hipercatabolismo y/o inflamación. La suplementación con glutamina en las fórmulas convencionales ha demostrado efectos beneficiosos sobre la inflamación, las complicaciones infecciosas, la duración de la NP y la estancia hospitalaria10-12. La utilización de las diferentes emulsiones lipídicas, puede tener implicaciones tanto en la respuesta clínica como en la posible aparición de complicaciones asociadas13-15. La versatilidad en la adición de lípidos a preparados binarios nos permite adecuarnos a la situación clínica del paciente. En nuestro protocolo, los lípidos de patrón de soja (Lipovenos®, Intralipid®) utilizados tradicionalmente como aporte de ácidos grasos esenciales y fuente de energía, se han sustituido por el patrón de oliva (Clinoleic®), emulsión de aceites de oliva y de soja (80/20%) que proporciona una relación ácidos grasos saturados/monoinsturados/ esenciales de 15/65/20%. Las ventajas de este patrón son: la elevada proporción de monoinsaturados que confiere menor riesgo de peroxidación, importante sobre todo en pacientes críticos, y el menor efecto inmunosupresor por el bajo porcentaje de poliinsaturados16-18.
Cuando el paciente presenta hipertrigliceridemia y/o disfunción hepática optamos por la reducción del aporte lipídico o por la utilización de mezclas de triglicéridos LCT/MCT llamados estructurados (Structolipid®) que son emulsiones con tamaño de partícula y propiedades biológicas, similares a las de los quilomicrones endógenos, pero sin ésteres de colesterol ni apolipoproteínas. Esta emulsión aporta ácidos grasos esenciales (ácidos grasos de cadena larga ó LCFA) y un substrato energético en forma de LCFA y ácidos grasos de cadena media (MCFA). Este tipo de emulsiones lipídicas estructuradas son de fácil metabolismo por lo que las administramos preferentemente a pacientes críticos, hipercatabólicos o con disfunción hepática19-21.
Otro componente lipídico que añadimos es el aceite de pescado (Omegaven®), compuesto fundamentalmente por ácidos grasos omega-3 eicosapentaenoico (EPA) y docosahexaenoico (DHA) que pueden mejorar las respuestas inflamatoria e inmune, disminuyendo la probabilidad de infección22. El mecanismo de acción propuesto se basa en que al competir con el ácido araquidónico por los sistemas enzimáticos que intervienen en la génesis de prostanoides, reducen los niveles plasmáticos y tisulares de éstos (prostaglandinas, leucotrienos y tromboxanos) produciendo efectos proinflamatorios, inmunosupresores y vasoconstrictores. Además, sin que se conozca completamente el mecanismo, esta serie de ácidos grasos modifican la producción de citoquinas que participan en la inflamación. Por tanto, su adición juega un papel importante en pacientes críticos y en estados inflamatorios.
Las soluciones iónicas añadidas a las NPE nos proporcionan agilidad para evitar o corregir alteraciones electrolíticas. En nuestro protocolo utilizamos como aporte de iones: cloruro sódico, fosfato sódico y potásico, cloruro potásico y sulfato de magnesio; y como soluciones poliiónicas con y sin potasio Hyperlite® e iones Palex sin potasio®. Estos productos nos permiten realizar un amplio número de combinaciones para abarcar la mayoría de las situaciones de desequilibrio electrolítico23.
Finalmente, la adición de vitaminas (Cernevit®) para prevenir las hipovitaminosis y de elementos traza (Addamel®) para prevenir la depleción de oligoelementos forma parte de la dinámica habitual y ambos preparados se añaden a todas las fórmulas de NPM desde su inicio.
Con la progresiva incorporación de la NPM en nuestro protocolo hemos conseguido ajustar las fórmulas de NP a las necesidades del paciente dando respuesta a situaciones clínicas y metabólicas que la NPE no puede abarcar, y al mismo tiempo reducir al máximo el uso de la NPI. En nuestro hospital, esta disminución de la NPI se refleja en una menor carga de trabajo al tener que transfundir menor volumen de líquido a través del sistema automatizado de control volumétrico (Bomba MicroMacro® 23 Baxa Compounder) con la consecuente disminución del tiempo empleado en la elaboración. Por tanto, la NPM es una opción versátil, que junto con la introducción de la bomba volumétrica aumenta la eficiencia y calidad del sistema de atención al paciente.
No obstante, en pacientes con encafalopatía hepática o con insuficiencia renal es difícil utilizar la NPM, ya que, aunque sin una evidencia totalmente contrastada24, históricamente se ha propuesto que estos pacientes necesitan un perfil especial de aminoácidos (ramificados para encefalopatía hepática y esenciales enriquecidos con histidina para la insuficiencia renal) que no están contemplados en la NPE actualmente comercializada.
En el estudio se pone de manifiesto que con pequeños volúmenes de adición a los preparados estándar comercializados, y por tanto con una menor carga de trabajo, se consiguen preparados finales con características nutricionales muy similares a los que se pueden preparar de forma individualizada. En nuestra experiencia la reducción de la NPI hasta el 12% actual, refleja las amplias posibilidades de intervención mediante preparados modulares.
Referencias
1.Guidelines for the use of Parenteral and Enteral Nutricion in Adult and Pediatric Patients-ASPEN Board of Directors and the clinical guidelines task force. JPEN-Journal of Parenteral and Enteral Nutrition 2002; 26(Supl. 1). [ Links ]
2. Martínez Romero G, Pérez Ruixo JJ, Jiménez Torres NV. Nutrición parenteral e identificación de subpoblaciones con necesidades nutricionales similares. Nutr Hosp 2002; 17(2):80-92. [ Links ]
3. Pichard Schwarz G, Frei A, Kyle U, Jolliet P, Morel P, Romand JA, Sierro C. Economic investigation of the use of three compartiment total parenteral nutrition bag: prospective randomized unblinded controlled study. Clin Nut 2002; 19(4):245-51. [ Links ]
4. Ruano M, Recuenco I, Torrecilla A, Sosa P, Carrión C, Gutiérrez R, Montanés P, Gómez Candela C, Cos A, Jiménez Caballero ME. Fórmulas estándar de nutrición parenteral. Estudio de su utilización en un hospital general. Nutr Hosp 1993; 8(4):242-8. [ Links ]
5. Llop Talaverón JM, Berlana Martín D, Badía Tahull MB, Fort Casamartina E, Vinent Genestar JL, Tubau Mola M y Jódar Massanés R. Preparados estándar de nutrición parenteral en situaciones clínicas complejas. Nutr Hosp 2004; 19(4): 229-235. [ Links ]
6. Zauner C, Schuster BI, Schneeweiss B. Similar metabolic responses to standardized total parenteral nutrition of septic and nonseptic critically ill patients. Am J Clin Nutr 2001; 74:265-70. [ Links ]
7. Real Decreto 175/2001, de 23 de febrero. [ Links ]
8. ASHP council on professional affairs. ASHP Guidelines on the safe use of automated compounding devices for the preparation of parenteral nutrition admixtures. Am J Health-Syst Pharm 2000; 57:1343-48. [ Links ]
9. Jeffrey J, Fishwick JJ, Murphy CC, Riesenberg MC, Malone RJ. Weight-based accuracy of parenteral nutrient solutions prepared with an automated compounder. Am J Health-Syst Pharm 1997; 54:678-679. [ Links ]
10. Lin MT, Kung SP, Yeh SL, Lin C, Lin TH, Chen KH, Liaw KY, Lee PH, Chang KJ, Chen WJ. The effect of glutamine suplemented total parenteral nutrition on nitrogen economy depends on severity of diseases in surgical patients. Clin Nutr 2002; 21(3):213-8. [ Links ]
11. Novak F, Heylan DK, Avenell A, Drover JW. Glutamine supplementation in serious illness: a systematic review of the evidence. Crit Care Med 2002; 30(9):2022-9. [ Links ]
12. Culebras-Fernández JM, De Paz-Arias J, Jorquera-Plaza F, García de Lorenzo A. Nutrición en el paciente quirúrgico: inmunonutrición. Nutr Hosp 2001; 16(3):67-77. [ Links ]
13. Camacho J, Shou J, Ortiz y cols. Lipids ans inmune function. Nutr Hosp 1996; 11:230-237. [ Links ]
14. Boncompain MG, Claudel JP, Gaussorgues y cols. Hepatic Cytolytic and Cholestatic Changes Related to a Change of Lipid Emulsions in Four Long-Term Parenteral Nutrition with Short Bowel. JPEN 1992; 16:78-83. [ Links ]
15. Morán Penco JM, Salas Martínez J, Maciá Botejara E. ¿Qué sucede en el hígado durante la alimentación artificial? Nutr Hosp 2001; 16(5):145-51. [ Links ]
16. Washington C, Koosha F y Davis SS. Phsicochemical properties of parenteral fat emulsions containing 20% triglyceride; Intralipid and Ivelip. J Clin Pharm Ther 1993; 18(2):123-31. [ Links ]
17. Kinsella J, Lokesh B, Broughton S y cols. Dietary polyunsatured fatty acids and eicosanoids: Potential effects on the modulation of inflammatory and immune cells; An overview. Nutrition 1990; 6:24-43. [ Links ]
18. Jauch KW, Günther B, Hailer S, Wolfram G. Different fat emulsions in postoperative total parenteral nutrition. Clin Nutr 1987; 6:S44. [ Links ]
19. Ythier-Moury P, Boutet G, Duquenne C y cols. Are LCT emulsions equivalents in tems of safety? A comparative study of three emulsions using a new toxicological model in the dog. Clin Nutr 1990; 9(s):32. [ Links ]
20. Garnacho J, Ortiz C, Jiménez F y cols. Estudio comparativo de dos emulsiones lipídicas en nutrición parenteral del enfermo séptico. Nutr Hosp 1996; 11:47-53. [ Links ]
21. Planas M, Farriol M, Porta y cols. Metabolic effects of long chain triglycerides and medium chain triglycerides vs long chain triglycerides in patients with sepsis. Clin Nutr & Gastroenterology 1991; 6:69-73. [ Links ]
22. Heller AR, Rossler S, Litz RJ y cols. Omega-3 fatty acids improve the diagnosis-related clinical outcome. Crit Care Med 2006; 34(4):972-9. [ Links ]
23. Kraft MD, Btaiche IF, Sacks GS, Kudsk KA. Treatment of electrolyte disorders in adult patients in the intensive care unit. Am J Health Syst Pharm 2005; 62(16):1663-82. [ Links ]
24. Melink G. Value of specialty intravenous amino acid solutions. Am J Health-Syst Pharm 1996; 53:671-4. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Josep Manel Llop Talaverón.
Servicio de Farmacia.
Hospital Universitari de Bellvitge.
Feixa Llarga, s/n.
08197 Hospitalet de Llobregat. Barcelona.
E-mail: josep.llop@csub.scs.es
Recibido: 2-IX-2006.
Aceptado: 5-III-2007.