Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.28 no.3 Madrid may./jun. 2013
ORIGINAL
Respuesta glucémica e insulinémica a dos fórmulas enterales isocalóricas en pacientes con diabetes mellitus tipo 2
Blood glucose and insulin responses to two hypocaloric enteral formulas in patients with diabetes mellitus type 2
D. A. de Luis, O. Izaola, B. de la Fuente y K. Araújo
Center of Investigation of Endocrinology and Nutrition. Medicine School and Unit of Investigation Hospital Río Hortega. University of Valladolid. Valladolid. Spain. Medical Affairs. Nestle Health Science Spain.
Dirección para correspondencia
RESUMEN
Objetivos: El objetivo del presente estudio es comparar la respuesta glucémica e insulinémica de pacientes diabéticos tipo 2 tras la administración oral de 250 ml de dos formulas enterales: una formula especifica (Novasource® Diabet Smartflex®) frente a una fórmula isocalórica estándar.
Material y métodos: El diseño fue cruzado, recibiendo los pacientes diabéticos (n = 15) de manera aleatoria las dos fórmulas. Se realizó una curva de glucemia e insulinemia en los tiempos 0, 10,20, 30,60, 90, 120,150 y 180 minutos. Las variables analizadas fueron, el área bajo la curva (AUC0-t), la concentración máxima (Cmax), el tiempo en que se alcanza la concentración máxima (Tmax) y las concentraciones de los parámetros bioquímicos en cada período del estudio.
Resultados: Se estudiaron 11 varones (73.3%) y 4 mujeres (26.7%), la edad media fue de 56,9 ± 10,9 años. Los pacientes que recibieron Novasource® Diabet presentan una media menor de AUC0-t, diferencia entre medias de glucemia -4.753,26 mg/min/dl (IC 95%: -7.256,7 a -2.249,82), también presentaron una media de insulinemia significativamente menor de AUC0-t, diferencia de medias: -930,27 uU/min/ml (IC 95%: -1.696,34 a -164,2). La Cmax mostró unas medias de glucemia significativamente menores con la fórmula específica, diferencia de medias -26,89 mg/dl (IC 95% 42,11 a -11,67) e insulinemia, diferencia de medias: -5,39 uU/ml (IC 95%: -10,37 a -1,43). El análisis de Tmax muestra que las medias de glucemia con la fórmula específica son significativamente menores, diferencia de medias -19,82 min (IC 95%: -32,11 a -7,33), sin diferencia significativa en la Tmax de insulinemia. Finalmente el análisis de las concentraciones de glucosa en el total del estudio muestra que el grupo con la formula específica tiene una media menor de glucosa 25,77 mg/dl (IC 95%: 18,29 a 33,25), sucediendo lo mismo con la insulinemia 4,39 U/ml (IC 95%: 0,927 a 7,87).
Conclusiones: Los pacientes diabéticos tipo 2 que recibieron Novasource® Diabet presentan significativamente menores medias de AUC0-t, Cmax y Tmx en las curvas de glucemia, también presentaron menores medias de AUC0-t y Cmax en las curvas de insulinemia.
Palabras clave: Glucosa. Niveles de insulina. Fórmula enteral específica.
ABSTRACT
Objectives: The aim of this study is to compare the glycaemic and insulinemic response of type 2 diabetic patients after oral administration of 250 ml of two enteral formulas: a specific formula (Novasource® Diabet Smartflex®) against a standard isocaloric formula.
Methods: The design was a cross-over study, with the diabetic patients (n = 15) receiving one of the two formulas in random order. Glycaemia and insulinemia curves were performed at 0, 10, 20, 30,60, 90,120,150 and 180 minutes. The variables studied were the area under the curve (AUC0-t), maximum concentration (Cmax), the time to reach maximum concentration (Tmax) and the concentrations of biochemical parameters in each study period.
Results: We studied 11 males (73.3%) and 4 females (26.7%), the mean age was 56.9 ± 10.9 years. Patients receiving Novasource® Diabet showed a lower mean AUC0-t of glucose, mean difference -4,753.26 mg/min/dl (95% CI: -7,256.7 to -2,249.82), also showed a mean insulinemia significantly lower AUC0-t, mean difference: 930.27 uU/min/ml (95% CI -1,696.34 to -164.2). The Cmax showed a significantly lower mean blood glucose levels with the specific formula, mean difference -26.89 mg/dl (95% CI -42.11 to -11.67) and insulin, mean difference: -5.39 uU/ml (95% CI: -10.37 to -1.43). The analysis shows that the mean Tmax of glucose with the specific formula are significantly lower, mean difference -19.82 min (95% CI: -32.11 to -7.33), however there was no difference in Tmax of insulin. Finally the analysis of glucose concentrations in the total study shows that the group with the specific formula has a lower mean glucose 25.77 mg / dl (95% CI 18.29 to 33.25), the same fact was detected with insulinemia 4.39 mU/ml (95% CI: 0.927 to 7.87).
Conclusions: Diabetic patients treated diabet Novasource® had significantly lower mean AUC0-t, Cmax and Tmax in blood glucose curves, also had lower mean AUC0-t and Cmax in insulin curves.
Key words: Glucose. Insulin levels. Enteral specific formulas.
Introducción
La diabetes mellitus es una enfermedad común que afecta a un 6% de la población española. La diabetes mellitus tipo 2 es especialmente frecuente en la población de mayor edad. Por encima del 20% de las personas de 60 años o de mayor edad padecen esta enfermedad1. El control estricto de la glucemia tiene un impacto positivo a largo plazo en la situación clínica de los pacientes con diabetes, retrasando la progresión de las complicaciones asociadas con la enfremedad2. El objetivo principal de la la dieta en los pacientes diabéticos es alcanzar la práctica normalidad de los niveles de glucemia en ayunas y en la fase postprandial, asi como controlar otros factores de riesgo, como los niveles de tensión arterial y lípidos séricos. Asimismo, la presencia de diabetes mellitus constituye un factor de riesgo para presentar desnutrición relacionada con la enfermedad, hecho reflejado en un reciente estudio multicéntrico en España en el que se observa que un 30% de los pacientes diabéticos presentan desnutrición al ingreso y/o al alta hospitalaria3. Esto condiciona la necesidad de dar soporte nutricional intrahospitalario o domiciliario a muchos de estos pacientes4-5.
Normalmente, las fórmulas más utilizadas en el soporte nutricional, son fórmulas enterales estandares con elevado porcentaje en carbohidratos y bajo porcentaje de grasas y fibra. Las fórmulas con esta composición de macronutrientes suelen producir una rápida absorción de los hidratos de carbono con una gran respuesta insulinémica5-6. En los últimos años han aparecido nuevas fórmulas para los pacientes diabéticos, estas fórmulas específicas incorporan diferentes nutrientes, ácidos grasos monoinsaturados7, fibra8 y fructosa9 con el objetivo de facilitar el control glucémico. Una revisión sistemática de los estudios que utilizan estas fórmulas específicas para diabetes en comparación con las fórmulas estándar ha demostrado de manera consistente unos menores niveles de glucosa postprandial y de la glucemia bajo la curva (AUC)10. Las recomendaciones dietéticas actuales para las personas con diabetes se centran en las cantidades relativas y tipos de carbohidratos y lípidos11. Puesto que la diabetes es cada vez más frecuente, el desarrollo de un producto especializado que minimice la hiperglucemia postprandial y favorezca el control de la diabetes y de los valores de lípidos en sangre es muy beneficioso.
Por ello, el objetivo de nuestro trabajo fue comparar la respuesta glucémica e insulinémica de pacientes diabéticos tipo 2 tras la administración oral de dos fórmulas enterales: una formula estándar y una fórmula específica.
Material y métodos
Sujetos
El estudio se realizó en 15 pacientes diabéticos tipo 2. Antes de iniciar el estudio se les practicó un examen físico estándar a fin de establecer el estado basal de salud de los pacientes, comprobar los criterios de inclusión y descartar la presencia de criterios de exclusión. Se incluyeron pacientes de ambos sexos entre 18 y 80 años de edad, con diabetes mellitus tipo 2 controlada (consejo dietético o antidiabéticos orales), con una hemoglobina glicosilada menor a 9,0% (HbAlC < 9,0%), glucemia en ayunas menor a 180 mg/dl y firma del consentimiento informado por parte del paciente. Se excluyeron pacientes con función tiroidea anormal, creatinina sérica > 2,0 mg/dl, enfermedad gastrointestinal definida como la presencia de úlcera gástrica, gastritis, diarrea, gastroparesia, vómitos y/o dolor abdominal, diabetes actualmente no controlada, pacientes en tratamiento farmacológico que a juicio del investigador pueda interferir con el metabolismo de la glucosa, pacientes embarazadas y la presencia de alergias o intolerancias a cualquiera de los componentes de la fórmula en estudio.
En una primera visita, cada sujeto recibió 250 ml de Novasource® Diabet y/o Fórmula estándar (tabla I) administrada por vía oral durante 15 minutos, de una manera aleatoria. Tras la toma, se extrajeron muestras sanguíneas para la determinación de glucemia e insulinemia a los 10, 20, 30, 60, 90, 120, 150 y 180 minutos. Después de un período de lavado de 7 días y tras la extracción de la muestra basal, cada sujeto recibió 250 ml de Novasource Diabet® y/o Fórmula estándar (la fórmula que no había recibido en la primera toma) administrada por vía oral en 15 minutos, extrayéndose las mismas muestras sanguíneas que la primera toma. El estudio fue aprobado por el Comité de Ensayos Clínicos del HURH y los pacientes firmaron un consentimiento informado antes de iniciar el protocolo de estudio.
Procedimientos
A todos los pacientes se les pesó, talló (Modelo Omron®, LA, CA) y calculó el índice de masa corporal (IMC= peso/kg2). Los niveles de glucosa de determinaron mediante el uso de un método de glucosa oxidasa automatizado (Roche Hitachi® 917, Roche Diagnostics, Mannheim, Alemania). Los niveles de insulina fueron determiandos mediante un método enzimatico colorimetrico (Insulin Modelo, WAKO Pure-Chemical Industries, Osaka, Japan).
Análisis estadístico
Para el análisis, se ha utilizado la prueba de MannWhitney para variables continuas y la prueba de Chi-cuadrado para variables categóricas. Sin embargo cuando no se cumplían las condiciones de aplicación de la prueba de Chi-cuadrado, se utilizó el estadístico exacto de Fisher. Las diferencias entre grupos para las variables continuas se resumieron mediante el intervalo de confianza al 95% de la diferencia de medias. El análisis principal consistió en comparar las diferencias entre dos fórmulas de nutrición enteral (específica y estándar) en la evolución de los niveles de glucosa e insulina en sangre. Los parámetros analíticos fueron evaluados en el periodo basal, a los 10, 20, 30, 60, 90, 120, 150 y 180 minutos. Por tanto, la hipótesis nula del estudio es que los pacientes no presentaran diferencias en la evolución de los niveles de glucosa e insulina, excluyendo los diferentes efectos asociados al diseño del estudio, también se analizó el efecto periodo y el efecto secuencia.
Para evaluar los efectos de la nutrición sobre las concentraciones de insulina y glucosa, las variables analizadas fueron el área bajo la curva concentración-tiempo desde la administración de la nutrición, hasta la última muestra con concentración medible (AUC0-t), la concentración máxima (Cmax), el tiempo en que se alcanza la concentración máxima (Tmax) y las concentraciones de los parámetros bioquímicos en cada periodo del estudio. La AUC0-t fue calculada por el método trapezoidal, las Cmax y Tmax fueron extrapoladas directamente de los datos. El análisis de la AUC0-t, Cmax, Tmax y los parámetros bioquímicos en cada uno de los periodos del tratamiento se realizaron mediante análisis multivariantes de la varianza (MANOVA). El supuesto de homogeneidad de la matriz de covarianzas se comprobó con la prueba de Box M, el supuesto de esfericidad se confirmó con la prueba de Mauchly, el supuesto de normalidad de los errores se confirmó con el test de Kolmogorov-Smirnoff para los residuales del modelo. Las desviaciones de estos supuestos se corrigieron para el efecto del tratamiento mediante F conservadora [F(1,Ni-1,α)]. El nivel de significación utilizado fué 0.05 bilateral. El análisis se ha realizado con programa estadístico SPSS V17 (IL, USA).
Resultados
Parámetros generales
Con respecto a las características basales, se incluyeron 11 (73,33%) hombres y 4 mujeres (26,57%). La edad media de todos los pacientes fue de 56,89 (10,90) años y el rango de edades osciló entre los 44,4 y los 75,30 años. Todos los pacientes habían sido diagnosticados de diabetes mellitus tipo 2 según los criterios de la Asociacion Americana de Diabetes. Todos los diabéticos recibieron los 2 tratamientos del estudio. Un total 7 pacientes (46,7%) recibieron la fórmula específica en el primer periodo y la estándar en el segundo periodo. Por el contrario 8 (53,33%) pacientes recibieron la fórmula estándar en el primer periodo y específica en el segundo periodo. En 13 (86,67%) pacientes el periodo de lavado fue de 7 días y en los 2 (13,33%) restantes de 8 días. Las enfermedades concomitantes más frecuentes fueron la hipertensión arterial que se había diagnosticado en 8 (53,33%) pacientes y la dislipemia en 6 (40%) pacientes.
El análisis de las características antropométricas reveló que el peso actual de los pacientes que componían la muestra fue de 73,2 DS (21,9) kg. El peso habitual fue de 73,1 DS (21,9) kg. Por lo que no se observó una variación importante en las medias de peso actual y habitual de los pacientes. El índice de masa corporal fue de 28,4 DS (7,8) kg/m2.
Análisis de glucemia
El análisis de los parámetros cinéticos de la concentración de glucosa, indica que los pacientes tratados con la fórmula específica presentan una media significativamente (p = 0,001) menor de AUC0-t que los pacientes que reciben la fórmula estándar (diferencia de medias: -4.753,26 [IC 95%: -7.256,69 a -2.249,82)] (tabla II y fig. 1). Además no se observan diferencias significativas en los efectos periodo y secuencia. Cuando se analiza la Cmax, también se observa que las medias de la fórmula específica son significativamente (p = 0,008) menores que los pacientes que reciben la fórmula estándar (diferencia de medias: -26,89 (IC 95%: -42,11 a -11,67) (tabla II). Además no se observan diferencias significativas en los efectos periodo y secuencia. En el análisis de la Tmax se observa que las medias de la fórmula específica son significativamente (p = 0,007) menores que los pacientes que reciben la fórmula estándar (diferencia de medias: -19,82 (IC 95%: -32,11 a -7,33) (tabla II). No se observan diferencias significativas en los efectos periodo y secuencia. Los niveles de glucemia en los tiempos 60, 90, 120, 150 y 180 min fueron significativamente inferiores con la fórmula especifica (fig. 1). Finalmente, el análisis de las concentraciones de glucosa en el total del estudio revela que el grupo con fórmula específica tiene una media de glucosa 16,62 mg/dl (IC 95%:3,41 a 29,83) menor que el grupo con fórmula estándar.
Niveles de insulina
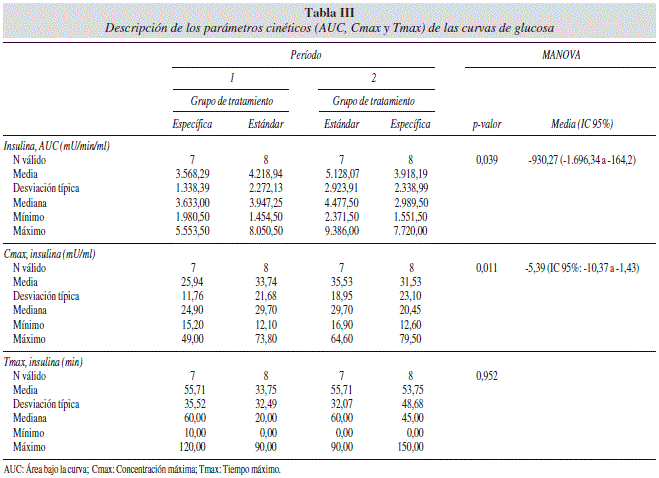
El análisis de los parámetros cinéticos de la concentración de insulina, indica que los pacientes tratados con la fórmula específica presentan una media significativamente (p = 0,039) menor de AUC0-t que los pacientes que reciben la fórmula estándar (diferencia de medias: -930,27 [IC 95%:-1.696,34 a -164,2)] (tabla III y fig. 2). Además no se observan diferencias significativas en los efectos periodo y secuencia. Cuando se analiza la CmáxCmax, también se observa que las medias de la fórmula específica son significativamente (p = 0,011) menores que los pacientes que reciben la fórmula estándar (diferencia de medias: -5,39 (IC 95%: -10,37 a -1,43). Además no se observan diferencias significativas en los efectos periodo y secuencia. El análisis de la Tmax no revela diferencias significativas entre las fórmulas estudiadas (p = 0,952). Tampoco se observan diferencias significativas en los efectos periodo y secuencia. Cuando se analizó la evolución de los valores de insulina a lo largo del estudio. No se observaron diferencias significativas respecto a los niveles de insulina en la determinación basal (efecto tratamiento p= 0,763, efecto periodo = 0,844 y efecto secuencia p = 0,290). También, se analizaron las concentraciones de insulina en cada periodo. Se observó que la fórmula específica mostraba menores niveles de insulina en sangre que la estándar entre los minutos 60 y 90 (fig. 2). Finalmente, el análisis de las concentraciones de insulina en el total del estudio revela que el grupo con fórmula específica tiene una media de 4,39 μU/ml (IC 95%:0,927 a 7,87) menor que el grupo con fórmula estándar en todo el estudio.
Por último, no se registraron acontecimientos adversos, ni discontinuaciones, en ninguno de los pacientes incluidos en el estudio.
Discusión
Los resultados del presente ensayo confirman que los pacientes diabéticos tratados con Novasource® Diabet presentan significativamente menores medias de AUC0-t, Cmax y Tmx en las curvas de glucemia, también presentaron menores medias de AUC0-t y Cmax en las curvas de insulina.
En la literatura existen diversos estudios12-16 que han demostrado el efecto beneficioso de las fórmulas enterales especificas para diabéticos en parámetros metabólicos como la HbA1c, estos estudios se han realizado fundamentalmente con fórmulas con alto contenido en ácidos grasos monoinsaturados. En este caso la base fisiológica que se ha argumentado para explicar los beneficios es que la sustitución de los hidratos de carbono por este tipo de grasas producía una respuesta más favorable de insulina y del control glucémico. En algunos trabajos se ha mostardo incluso disminución de las dosis requeridas de insulina12,14,17. En el trabajo de Alish et al.18 se ha demostrado que las fórmulas específicas para diabéticos producen menor variabilidad glucémicas, junto a unos menores requerimientos de insulina. Por otra parte estas formulas enterales especificas son bien toleradas en periodos de tiempo prolongados19.
En nuestro estudio, el análisis de los parámetros cinéticos de la concentración de glucosa indica que los pacientes que recibieron la fórmula específica presentan significativamente menores medias de AUC0-t, Cmax y Tmax. Lo que sugiere que la fórmula específica produce una menor concentración de glucosa en sangre y una disminución más rápida de los niveles de glucosa durante las primeras 3 horas de administración de este preparado. Por otra parte el análisis de los parámetros cinéticos de la concentración de insulina, muestran como los pacientes tratados con la fórmula específica presentan significativamente menores medias de AUC0-t y Cmax, pero no de Tmax. Lo que sugiere que la fórmula específica produce una menor concentración de insulina en sangre. Estas diferencias están presumiblemente producidas por el aporte de fibra por parte de la fórmula específica, ya que el aporte y calidad de los carbohidratos, asi como el de las grasas es muy similar en ambas fórmulas. Con respecto al aporte y calidad de proteínas tampoco existen diferencias. Debemos tener en cuenta que el tipo de proteínas puede influir en la respuesta glucémica e insulinémica. Por ejemplo, estudios realizados en personas sanas, han informado niveles de insulina plasmática ligeramente más altos, después de la infusión nasogástrica continua de una fórmula con aminoácidos, comparado con dietas isonitrogenadas e isocalóricas que contienen oligopéptidos o proteína entera20. Calbet y MacLean21 observaron que la administración oral combinada de péptidos hidrolizados y glucosa, en sujetos sanos, aumentó las concentraciones de insulina plasmática. Estos autores proponen que esta respuesta de insulina está determinada por la absorción más rápida del péptido hidrolizado a nivel de intestino delgado, comparado con proteínas de leche entera entregadas como una solución láctea21. En la revisión de M. Elias et al.10, se demuestra que en los ensayos clínicos que han utilizado fórmulas especificas para diabéticos, el area debajo de la curva de glucemia y de insulinemia, asi como el pico de hiperglucemia postpandrial fue menor, utilizándose en todos ellos formulas con fibra, además de otras modificaciones en la composición de la fórmula como fue su enriquecimiento en acidos grasos monoinsaturados frente a la fórmula control. La presencia de fibra en estas fórmulas modularía el vaciamiento gástrico, asi como su acción con posibles efectos incretinicos.
La importancia del buen control de la glucemia postprandial se ha demostrado en algunos estudios, existiendo una correlación de este parámetro con complicaciones macrovasculares22-25. Esto sugeriría que la utilización de estas formulas específicas enteralaes a largo plazo en pacientes con diabetes mellitus podría reducir las complicaciones macrovascualres en estos pacientes. No obstante son necesarios más estudios para evaluar estos efectos crónicos en una población tan heterogenea como es el paciente con diabetes mellitus y desnutrición26-28.
En resumen, los pacientes diabéticos que han recibido Novasource Diabet® presentaron significativamente menores medias de AUC0-t, Cmax y Tmx en las curvas de glucemia, también presentaron menores medias de AUC0-t y Cmax en las curvas de insulina. Son necesarios más estudios y más prolongados con el fin de demostrar que este efecto previene complicaciones crónicas en este tipo de pacientes.
Referencias
1. Soriguer F, Goday A. Prevalence of diabetes mellitus and impaired glucose regulation in Spain: the Di@bet.es Study UK Prospective Diabetologia 2012;55:88-93UK Prospective Diabetes Study (UKPDS) Group: Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet 1998; 352: 837-53. [ Links ]
2. Jones BM, Stratton RJ, Holden C, Russell C, Glencorse G, Micklewright A. Trends in Artificial Nutritional support in the UK 2000-2003: Annual report of the British Artificial Nutrition Survey (BANS). Redditch, UK, BAPEN, 2005. [ Links ]
3. de Luis DA, Aller R, Izaola O, Terroba MC, Cabezas G, Cuellar LA. Experience of 6 years with HEN in an area of Spain. Eur J Clin Nutr 2006; 60: 553-7. [ Links ]
4. Cashmere KA, Costil DL, Cataland S, Hecker AL. Serum endocrine and glucose response elicited from ingestion of enteral feedings. Fed Proc 1981; 40: 440A. [ Links ]
5. Coulston AM. Clinical experience with modified enteral formulas for patients with diabetes. Clin Nutr 1998; 17 (Suppl. 2): 46-56. [ Links ]
6. Garg A. High-monounsaturated-fat diets for patients with diabetes mellitus: a meta-analysis. Am J Clin Nutr 1998; 67 (Suppl. 3): 577S-582S. [ Links ]
7. Druetzler A, Bowen P, Cashmere K, Horwitz A. Acute and chronic response of glucose tolerance to a soy polysaccharide enriched liquid formula diet. Fed Proc 1985; 44: 1499. [ Links ]
8. Koivisto VA, Yki-Jarvinen H. Fructose and insulin sensitivity in patients with type 2 diabetes. J Intern Ned 1993; 223: 145-53. [ Links ]
9. Elia M, Ceriell A, Laube H, Sinclair AJ, Engfer M, Stratton RJ. Enteral nutritional support and use of diabetes.secific formulas for patients with diabetes. A Systematic review and metaanalysis. Diabetes Care 2005; 28: 2267-79. [ Links ]
10. American Diabetes Association Position Statement. Nutrition Principles and Recommendations in Diabetes. Diabetes Care 2004; 27: S36. [ Links ]
11. Mayr P, Mertle-Roetzer M, Lauster F, Pohl M, Haslbeck M, Eriksen J, et al. Metabolic control in type 2 diabetes tube fed patients after brain damage during long-term treatment with a new low carbohydrate, high monounsaturated fatty acid containing enteral formula versis a standard-like formula: a randomized, prospective controlled, double blind multi centre trial. Clin Nutr 2005; 23: 1497-8. [ Links ]
12. McCargar LJ, Innis SM, Bowron E, Leichter J, Dawson K, Toth E, Wall K. Effect of enteral nutritional products differing in carbohydrate and fat on indices of carbohydrate and lipid metabolism in patients with NIDDM. Mol Cell Biochem 1998; 188: 81-9. [ Links ]
13. Mesejo A, Acosta JA, Ortega C, Vila J, Fernandez M, Ferreres J, sanchis JC, Lopez F. Comparison of a high-protein disease specific enteral formula with a high-protein enteral formula in hyperglycemic critically ill patients. Clin Nutr 2003; 22: 295-305. [ Links ]
14. Wang W, Zhang YF, Zhou D, Liu Z, Hong X. Open-label, randomizedmultiple-center, parallel study comparing glycemic responses and safety profiles of glucerna versis Fresubin in subjects of type 2 diabetes mellitus. Endocr 2008; 33: 45-52. [ Links ]
15. Pohl M, Mayr P, Mertl-Roetzer M, Lauster F, Haslbeck M, Hipper B, Steube D. Gkycemic control in patients with type 2 diabetes mellitus with type 2 diabetes mellitus with a specific disease enteral formula: stage II of a randomized, controlled multicenter trial. J of Parenteral and Enteral Nutrition 2009; 33: 37-49. [ Links ]
16. Grahm TW, Harrington TR, Isaac RM. Low carbohydrate with fiber enteral formula impedes development of hyperglycaemia in patients with acute head injury (abstract). Clin Res 1989; 37:138A. [ Links ]
17. Alish CJ, Garvey WT, Maki KC, Sacks GS, Hustead DS, Hegazi RA, Mustad VA. A diabetes-specific enteral formula improves glycemic variability in patients with type 2 diabetes. Diabetes Technol Ther 2010; 12: 419-25. [ Links ]
18. de Luis DA, Izaola O, Aller R, Cuellr L, Terroba MC, Martin T, Canbezas G, Rojo S, Domingo M. A randomized clinical trial with two enteral diabetes specific supplements in patients with diabetes mellitus type 2: metabolic effects. Eur Rev Med Pharmacol Sci 2008; 12: 261-6. [ Links ]
19. Collin-Vidal C, Cayol M, Obled C, Ziegler F, Bommelaer G, Beaufrere B. Leucine kinetics aredifferent during feeding with whole protein or oligopeptides. Am J Physiol Endocrinol Metab1994; 267: E907-E914. [ Links ]
20. Calbet JA, Maclean DA. Plasma glucagon and insulin responses depend on the rate of appearance of amino acids after ingestion of different protein solutions in humans. J Nutr 2002; 132; 8: 2174-82. [ Links ]
21. Ceriello A, Hanefeld M, Leiter L, Monnier L, Moses A, Owens D, Tajima N, Tuomilehto J. Postprandial glucose regulation and diabetic complications. Arch Intern Med 2004; 164: 2090-5. [ Links ]
22. Fonseca V. Clinical significance of targeting postpranidal and fasting hyperglycemia in managing type 2 diabetes mellitus. Curr Med Research Opin 2003; 19: 635-41. [ Links ]
23. Heine RJ, Balkau B, Ceriello A, Del Prato S, Horton ES, Taskinen MR. What does postprandial hyperglycaemia mean? Diabet Med 2004; 21: 208-13. [ Links ]
24. Hanefeld M. STOP-NIDDM: a new paradigm for diabetes prevention? Nutr Metab Cardiovasc Dis 2002; 12: 253-8. [ Links ]
25. López Martínez J, Mesejo Arizmendi A, Montejo González JC. Artificial nutrition in hyperglycemia and diabetes mellitus in critically ill patients. Nutr Hosp 2005; 20 (Suppl. 2): 34-7. [ Links ]
26. Queiroz KC, Novato Silva I, de Cássia Goncalves Alfenas R. Influence of the glycemic index and glycemic load of the diet in the glycemic control of diabetic children and teenagers. Nutr Hosp 2012; 27: 510-5. [ Links ]
27. Castañeda-González LM, Bacardi Gascón M, Jiménez Cruz A. Effects of low carbohydrate diets on weight and glycemic control among type 2 diabetes individuals: a systemic review of RCT greater than 12 weeks. Nutr Hosp 2011; 26 (6): 1270-1723. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
D. A. de Luis.
Professor of Endocrinology and Nutrition.
Center of Investigation of Endocrinology and Nutrition.
Medicine School. Valladolid University.
Hospital Universitary Río Hortega.
C/ Los Perales, 16 (Urb. Las Aceñas).
47130 Simancas, Valladolid.
E-mail: dadluis@yahoo.es
Recibido: 18-I-2013.
Aceptado: 28-I-2013.