INTRODUCCIÓN
Apreciado Presidente de Honor, Presidenta, miembros de la Junta Directiva y del Comité Científico de la SENPE. Es para mí un honor poder disertar en la XIII Lección Jesús Culebras. ¡Muchas gracias por su confianza!
Al Dr. Culebras “lo descubrí” como organizador principal en el II Congreso de la SENPE en León (1985). En aquellos momentos, a los congresos nacionales asistía poca gente, con lo cual el cambio de información y la proximidad nos ayudó a aquellos jóvenes que queríamos aprender sobre nutrición clínica y más los que proveníamos del campo farmacéutico.
Con el Dr. Culebras siempre estuve en contacto a través de su querida revista “Nutrición Hospitalaria” (36 años), donde siempre encontré sus consejos para mejorar las publicaciones.
En nuestra Sociedad, creo que tiene un plus añadido: su multidisciplinariedad. Actualmente se habla con frecuencia de que el conocimiento es transversal y SENPE, desde sus inicios, creyó en esta filosofía.
Por último, un recuerdo para dos farmacéuticos que en los inicios de nuestra Sociedad nos marcaron el camino: el Dr. Domingo García y el Dr. Jiménez Torres.
LOS INICIOS (1976-1980)
Los farmacéuticos de hospitales fueron, desde un inicio, miembros activos de las nuevas Comisiones de Nutrición Parenteral creadas en los hospitales a finales de los setenta del siglo pasado. En nuestro centro, nos ayudó la filosofía del Dr. Bonal sobre el nuevo concepto de la “unidosis”, que para él era un medio, no una finalidad, ya que se trataba de conseguir que el farmacéutico conociera y se introdujera en la sala de los pacientes, pasando visita con los facultativos.
Los otros miembros de la Comisión eran: a) Cirugía General en el contexto de la inserción del catéter central para poder administrar la nutrición parenteral (NP) a causa de su alta osmolaridad (> 1000 mOsm/L) y, principalmente, para el cierre de las fístulas duodeno-yeyunales de alto débito; b) Unidad de Cuidados Intensivos (UCI), que en aquellos momentos atendía a los enfermos politraumatizados y los primeros íleos paralíticos secundarios a la sedación para poder controlar la ventilación mecánica; c) Neonatología, a causa de los prematuros de bajo peso. Debido al éxito de la NP, pocos meses después pidieron entrar en la Comisión: d) Oncología-Hematología, debido a los efectos adversos de la quimioterapia, como la mucositis de grado III-IV, la EICH intestinal y los primeros trasplantes de médula ósea; y e) Digestivo, en el apartado de dejar en reposo el aparato digestivo: pancreatitis aguda y enfermedades inflamatorias intestinales (colitis ulcerosa y enfermedad de Crohn).
La finalidad de Farmacia en la Comisión era la preparación estéril de la NP, pero también nos involucramos en las preparaciones, por ejemplo, de oligoelementos, no disponibles en el mercado nacional. Realizamos los primeros trabajos sobre la estabilidad de la insulina en la NP y diagnosticamos, conjuntamente con los clínicos, un déficit de zinc en una enferma con duodenostomía tras diferentes fallos de sutura en el postoperatorio de una neoplasia gástrica. En este caso todavía se administraban en la NP, a días alternos, las vitaminas y los oligoelementos en el contexto de una posible interacción cobre-vitamina C. Descubrimos en estos primeros estudios clínicos la importancia del estado nutricional preoperatorio, principalmente en los enfermos candidatos a cirugía mayor en las complicaciones quirúrgicas, mejorando la mortalidad y el número de complicaciones en los enfermos candidatos a esofaguectomía en la neoplasia de esófago, y en la gastrectomía total en la neoplasia gástrica.
UN SALTO DE CALIDAD FARMACÉUTICA EN LA NUTRICIÓN PARENTERAL: DE LA PREPARACIÓN EN FRASCOS INDIVIDUALES AL “TODO EN UNO” (1981-1985)
Los primeros trabajos galénicos en la preparación de las bolsas de NP fueron el paso de la administración de soluciones individuales en frasco de vidrio de glucosa más aminoácidos y lípidos (Intralipid©) en “Y” con la anterior, a la preparación “todo en uno” (1980-1981), según la filosofía de Solassol y Joyeux (1) en Montpellier.
Anteriormente a este paso de “todo en uno”, decidimos estudiar si la utilización de las bolsas de policloruro de vinilo (PVC) que en aquellos momentos estaban en el mercado podían ceder ftalatos a niveles superiores a los permitidos. Las 3 bolsas comercializadas estudiadas dieron los rangos permitidos pero, a pesar de ello, cambiamos a bolsas de etileno-vinil-acetato (EVA), que no contenían ftalatos.
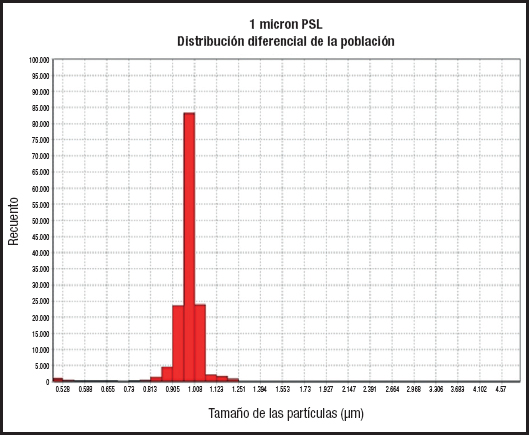
La nueva preparación en una misma bolsa de los aminoácidos, la glucosa y los lípidos (todo en uno) dignificó a los farmacéuticos de hospital debido a que este paso conllevaba la estabilidad de la emulsión, ya que las partículas ≥ 5 micras producidas en la ruptura de la emulsión provocaban embolia grasa pulmonar y la muerte (Fig. 1).
Estudiamos la concentración crítica de agregación (CCA) según la ley de estabilidades para coloides a partir de la suma de a cationes monovalentes + 64b cationes divalentes + 729c; para Hardy (2), una CCA de 690 mmol/L era estable durante 15 días a 4-8 °C (el 95 % de las partículas < 2 micras) utilizando un microscopio electrónico. La CCA era solo una guía para predecir posibles rupturas de la emulsión ya que la composición de los aminoácidos y el pH influyen en este valor.
Más tarde, Driscoll (3), utilizaría el contaje de partículas por “light obscuration”. Este método se apoya en el oscurecimiento de la luz cuando hacemos pasar un flujo diluido de partículas en una suspensión líquida entre una fuente de luz —un diodo láser— y un detector. El detector mide la reducción de la intensidad de la luz y, empleando una curva de calibración, procesa la señal para determinar el tamaño de las partículas. Puede medir entre 1 µm y 100 µm (Fig. 2). Driscoll no encuentra relación con el valor del CCA de ≥ 600 mmols/L con < 600 mmols/L y define la ruptura de la emulsión en: ≥ 0,4 % de las partículas con un diámetro de ≥ 5 µm.
En el 2008, la United States Pharmacopeia (USP), en el capítulo 729 (4), define la estabilidad por 2 métodos analíticos, el mencionado ligth obscuration y la espectrometría de correlación fotónica, que nos informa de porcentajes de partículas a partir de un haz de luz láser que incide directamente sobre la muestra de partículas en suspensión y nos determina la distribución a partir de los tamaños de las mismas. Con la primera se acepta que ≤ 0,05 % de las partículas pueden ser ≥ 5 micras, mientras que para la estabilidad, según la USP, por espectroscopia de correlación fotónica, el 100 % de las partículas deben ser ≤ 5 micras (Figs. 2 y 3).
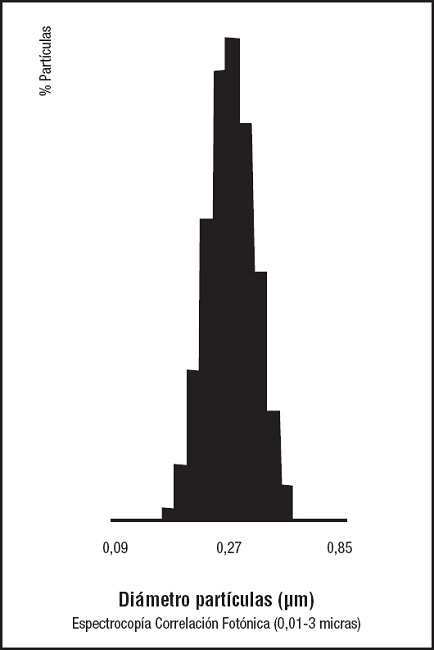
Figura 3. Espectroscopia de correlación fotónica. Detecta el porcentaje de partículas entre 0,01 y 3 micras.
Esta preparación “todo en uno” podía enmascarar la posible precipitación calcio-fosfato inorgánico, que podía producir una embolia pulmonar microvascular, con lo cual fueron los farmacéuticos de hospital Dr. Jiménez Torres y Dr. Roncheras (5) unos de los primeros en editar normogramas de posibles precipitaciones de fosfato tricálcico a partir del pH final de la NP y las concentraciones de calcio/fosfato inorgánico. En dicho trabajo, ambos firmantes nos avisaban de las causas directas, como que a mayor acidez, mayor solubilidad de calcio-fosfato, o indirectas: a) las fuentes de las sales de calcio, la disminución de la solubilidad cloruro > gluconato > glucobionato; b) si en la concentración final de la NP, Mg++/Ca++ < 2, mayor solubilidad; c) si la concentración final de aminoácidos ≤ 3 %, mayor posibilidad de precipitación; d) orden de la mezcla, añadir los fosfatos al final, y e) mayor temperatura, más posibilidades de precipitación.
Para el control microbiológico seguimos a Devaux-Goglin (6), que usan un método por filtración del 2,5-5 % del volumen de la NP utilizando Tween 80® y un filtraje por 0,45 µ utilizando el vacío, recogidos los filtros en placa de ágar para el control microbiológico. Este método fue validado por nosotros en 1999 (7). Introducimos un método estadístico de sumas acumuladas y, si daban negativo en los controles de una bolsa de cada 5, llegamos a analizar una bolsa cada 30 preparaciones.
Desde un inicio, la preparación de NP para neonatos se hizo como una solución “madre” sin lípidos, cuya dosificación es mL/kg de peso, siempre utilizando un filtro de 0,22 µ. Los lípidos se administran externamente y diariamente en 8-10 horas bajo filtros de 1,2 m en “Y” con la solución “madre”. En los últimos años se ha introducido una segunda fórmula para neonatos de muy bajo peso (≤ 1,5 kg).
En aquellos momentos se utilizaban, tanto en adultos como en pediatría, las bolsas EVA (etil-vinil-acetato), con una permeabilidad alta de oxígeno: 840 cc/m2. No será hasta el 2004, tras un estudio realizado por nosotros (8), que empleamos las bolsas multicapa (EVA + benzo-triazol -filtros UV-, adhesivo, EVA-alcohol etilvinílico, adhesivo, EVA) con una permeabilidad al oxígeno de ≤ 60 cc/m2,. El trabajo fue la evaluación de la formación de peróxidos en 4 tipos de NPT con emulsiones lipídicas diferentes (Intralipid 20 %; MCT/LCT 20 %; Clinoleico 20 % y Soyacal 20 %) y empleando bolsas EVA frente a multicapa. Como resultados, después de un almacenamiento de 6 días a 4 °C y 48 h a temperatura normal, encontramos que en las soluciones lipídicas ricas en poliinsaturados (Intralipid 20 %©, Soyacal 20 %©), la formación de peróxidos en las bolsas EVA fue tres veces mayor que en las multicapa. Mientras, las soluciones MCT/LCT 20 %© y Clinoleico 20 %© duplicaron el valor original en tiempo 0. En las bolsas multicapa, excepto en las NPT con Soyacal, donde aumentan los peróxidos un 20 %, las restantes fuentes lipídicas no se incrementaron más de un 5 %.
RACIONALIZAR LAS INDICACIONES DE NUTRICIÓN PARENTERAL Y SU APLICACIÓN EN LA CLÍNICA DIARIA: EL COSTE-EFICACIA Y EL BOOM DE LA NUTRICIÓN ENTERAL (1986-1992)
CLASIFICACIÓN Y RACIONALIZACIÓN DE LAS INDICACIONES EN LA NUTRICIÓN PARENTERAL
Se debían clasificar las indicaciones de la NP que, en un principio, seguían una vaga definición: “el/la que no puede comer”, “el/la que no quiere comer” y “el/la que no debe comer”; para ello, en la Comisión de NP del hospital escogimos la filosofía de Collin JP & Alley PG (9), que clasificaban las indicaciones de la nutrición parenteral total (NPT) de cirugía según la desnutrición, el tipo de cirugía (mayor, etc.) y las complicaciones (fallos de sutura, íleo paralítico, sepsis). La UCI se integraba en la sepsis de los enfermos quirúrgicos. Añadimos el grupo de “reposo del tubo digestivo” (enfermedad inflamatoria, pancreatitis aguda), las “obstrucciones del aparato digestivo” por bridas o neoplasias y un concepto de desnutrición severa que era la “hipoalbuminemia < 25 g/L”; finalizamos con las indicaciones de “politrauma” y una miscelánea de indicaciones heterogéneas en el contexto de la desnutrición. Para la nutrición parenteral periférica (NPP): < 550 mOsm/L, 10 g de N2 y 1000 kcal no proteicas, que clasificamos para el postoperatorio de la cirugía media e íleo paralítico de duración ≤ 5 días.
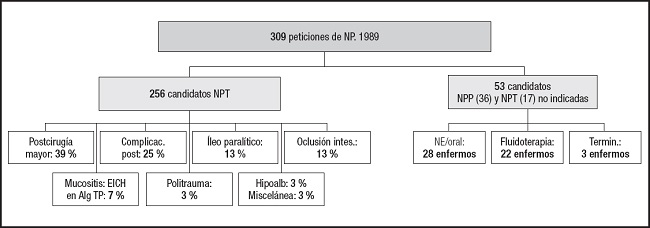
El “boom” de las indicaciones de la NPT en los principales hospitales de Barcelona y su área, entre 1987-1992, se refleja en la figura 4. Este incremento de la NPT llevó a racionalizar las indicaciones. Los cirujanos “para curarse en salud”, pedían NPP los viernes a todos los enfermos postoperados de cirugía media: hemicolectomía D por neo de colon, Bilroth I por neoplasia o úlcera gástrica y postaorto-bifemoral electiva en cirugía vascular, y la suspendían el lunes. Estudiamos el estado nutricional preoperatorio a partir del índice pronóstico nutricional (IPN) de Buzby y Mullen (10): %IPN = 158 - 16,6 (ALB) - 0,78 (TSF) - 0,20 (TFN) - 5,8 (RI) (Nota: Alb: albúmina (g/L); TSF: pliegue del tríceps (mm); TFN: transferrina (mg/dL); RI: respuesta intradérmica a 5 antígenos: PPD, candidina, Varidasa©, toxoplasmina y tricofitina; + si ø respuesta ≥ 5 mm.
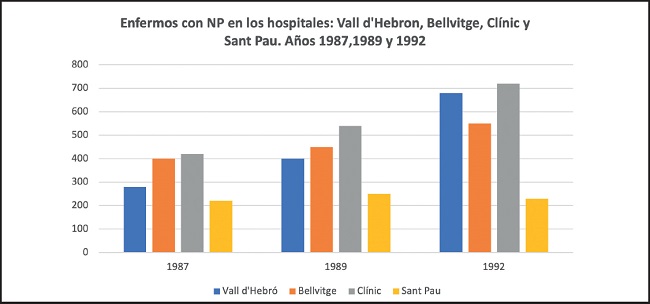
Figura 4. Seguimiento del número de enfermos candidatos a NP en los años 1987, 1989 y 1992 en los principales hospitales del área de Barcelona (Fuente: Cardona D. Veinticinco años de nutrición artificial en la farmacia hospitalaria. El Farmacéutico 2000;12(extra):112-21) (NP: nutrición parenteral).
Los autores predicen que si el valor era ≤ 50 %, observaban menos complicaciones en el postoperatorio. En estas 3 cirugías antes citadas, comparamos en grupos bien nutridos, preoperatoriamente ≤ 50 %, la administración de sueros frente a NPP, resultando que en la hemicolectomía D, como en el Bilroth I, no se observaron diferencias en las complicaciones y estancias hospitalarias; sí que en el postoperatorio de aorto-bifemoral, en cirugía vascular, la NPP postoperatoria disminuía las complicaciones y la estancia hospitalaria.
El mantenimiento del número de enfermos por año en nuestro hospital (Fig. 4) se debió a lo anteriormente expuesto y a la publicación de unos algoritmos de decisión en los que se decidía, frente a una consulta de NP como, por ejemplo, la gastroparesia, el íleo paralítico, etc., desviar a nutrición enteral y oral. A partir de aquí racionalizamos las indicaciones. Así, en el año 1989, en nuestro hospital, un 16 % de las peticiones de NP las trasladamos a nutrición enteral por sonda nasogástrica (SNG) o suplementación oral (o eran enfermos terminales), lo que conllevó un ahorro solo de dieta de NP de 15.665 $/año (11) (Fig. 5).
CATERING EN NUTRICIÓN PARENTERAL Y EL “ESTALLIDO” DE LA NUTRICIÓN ENTERAL
En 1986 ocurren dos fenómenos importantes en el soporte nutricional, el primero frente el auge de la NP: el laboratorio Braun inicia el catering, con lo cual en 24 horas cualquier hospital podía pedir una dieta de NP, en un primer momento según los protocolos del laboratorio y más tarde según las dietas parenterales del propio hospital: Nutriservice. El segundo, en el VIII Congreso de ESPEN en Paris, en 1986, donde los stands de nutrición enteral (NE) duplican los de NPT. Se dejan atrás las sondas de 14- 16 French (fr), aparecen las dietas túrmix con nuevas presentaciones líquidas, acompañadas de nuevas sondas y ostomías más fisiológicas. Se impone la filosofía de que la NE evita la translocación bacteriana y con ello hay menos infecciones; además es más barata. En un primer momento parecía que la NE acabaría con la NPT pero solo consiguió normalizar las indicaciones de soporte nutricional. Este crecimiento de las indicaciones de la NE produce un aumento de las consultas de enfermería a los servicios de farmacia de los hospitales sobre qué fármacos pueden administrarse por sonda nasogástrica (12). Al mismo tiempo se abre la necesidad de estudiar las interacciones fármaco-nutrientes a partir del trabajo de Krishnaswamy (13) sobre la influencia del estado nutricional en la cinética de los fármacos, y además revisamos el efecto de los fármacos en los macronutrientes, los electrolitos, las vitaminas y los oligoelementos (14).
PRIMEROS ESTUDIOS DE DESNUTRICIÓN HOSPITALARIA; LA IRRUPCIÓN DE LAS BOLSAS TRICAMERALES; NUEVOS SUBSTRATOS PROTEICOS Y DE LÍPIDOS EN LA NUTRICIÓN PARENTERAL Y LA ORDEN DE 2 DE JUNIO DE 1987 PARA REGULAR LA NUTRICIÓN ENTERAL DOMICILIARIA (1993-2000)
PRIMEROS ESTUDIOS DE DESNUTRICIÓN HOSPITALARIA
En la primera década de los noventa del siglo pasado, el farmacéutico de soporte nutricional continúa solicitado para las estabilidades de los fármacos con la NPT, sobre todo en “Y”, y se finalizan los estudios de estabilidad de las vitaminas en la mezcla “todo en uno” (15).
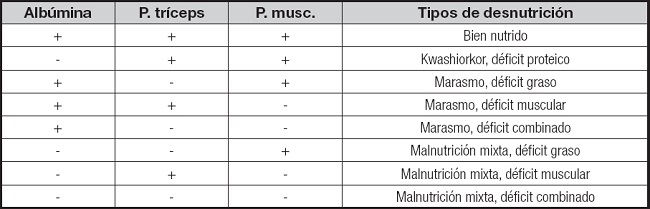
Se empieza a observar en nuestro hospital la relación entre desnutrición y complicaciones posquirúrgicas y médicas, acompañadas de aumentos de las estancias hospitalarias. En 1992 y 1994 se realiza una valoración del estado nutricional según Gassull (16) (Tabla I), en cortes de un día en diferentes servicios, y observamos el porcentaje de desnutrición en: oncología (52 %), cirugía (37 %) y traumatología (40 %), mientras que en 1994 disminuye en Oncología, pero aumenta en cirugía (60 %) y traumatología (62 %) (Fig. 6). En el 2004 repetimos el estudio y se mantenían los dos servicios de cirugía y traumatología con más enfermos desnutridos: un 58 % y 68 %, respectivamente. En 2014, ya con el screeening de la ESPEN, el NSR 2002 (17), continúan en Traumatología (45 %) los desnutridos al ingreso en la sala, seguidos de Medicina Interna y Respiratorio con un 33 %.
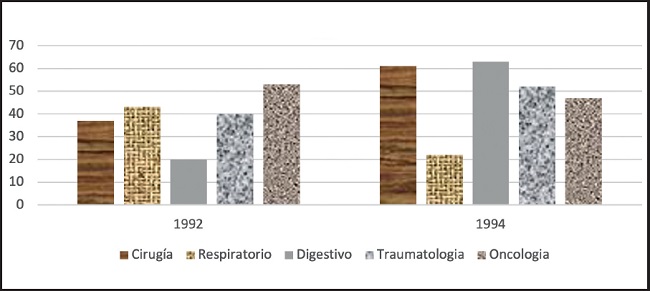
Figura 6. Porcentaje de desnutrición. Corte de un día por salas de cirugía, respiratorio, digestivo, traumatología y oncología. Años 1992 y 1994. Hospital S. Creu i S. Pau, BCN.
Irrupción de las bolsas tricamerales (TC) en las formulaciones de la nutrición parenteral
En 1995 se comercializan primero las bolsas bicamerales (glucosa, aminoácidos, electrolitos) para dejar paso en poco tiempo a las bolsas tricamerales (TC) con los lípidos incluidos. Las ventajas son: a) con el tiempo, mejores formulaciones: disminución del volumen, incremento del nitrógeno por bolsa y una relación aceptable de glucosa y lípidos; b) disminuyen los errores de preparación; c) utilizan glicerofosfato como fuente de fosfato orgánico, y d) menor tiempo de preparación frente a las preparaciones estándar de farmacia (Fig. 7).
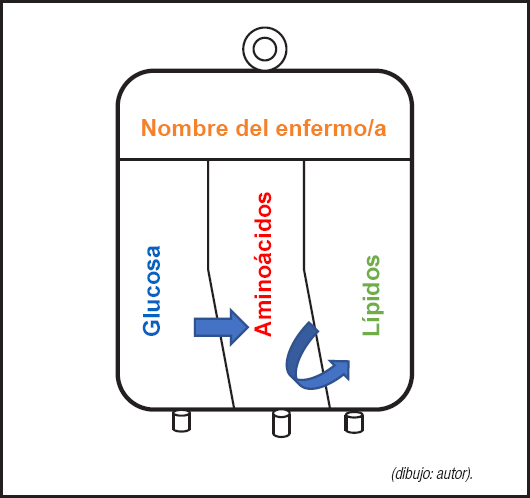
Figura 7. Bolsa tricameral. Orden de ruptura de los espacios individuales: glucosa + aminoácidos y final invasión mezcla anterior al espacio de los lípidos.
Las desventajas: a) necesidad de una cámara estéril para añadir en farmacia las vitaminas y oligoelementos; b) problema con la ruptura completa de los 3 compartimentos (aminoácidos, glucosa y lípidos); c) aumento casi al doble del tiempo de llenado si debemos añadir, p. ej., 250 mL de suero fisiológico; d) tendinitis en los técnicos en relación con la fuerza para romper los 3 compartimentos, y e) falta un estudio profundo de la contaminación por plásticos en el sellado de separación de los tres compartimentos (18). A partir de este trabajo se recomendó la utilización de filtros de 1,2 µ en la administración de la NP.
En la figura 8 podemos observar la evolución de las indicaciones de las TC, en 2005 y 2011 (19), entre 3 tipos de hospitales según el número de camas (< 300; 300-499 y > 500) en Cataluña, notificándose la utilización masiva de bolsas de TC en 2011 en los hospitales de < 300 camas y el aumento significativo en los grandes hospitales. La encuesta personal realizada en abril 2022, no publicada (20), a pesar de que solo hemos entrevistado a 3 hospitales de entre 300 y 499 camas, el incremento de la prescripción de TC es casi del 70 % de las formulaciones, mientras que en los grandes hospitales hay una disminución del 50 % al 42 % en el contexto de las nuevas máquinas de llenado: p. ej., Exactamix© y Baxter (Vall d'Hebron y Bellvitge). A pesar de ello, el Hospital de la Vall d'Hebron maneja un 83 % de sus formulaciones con las TC.
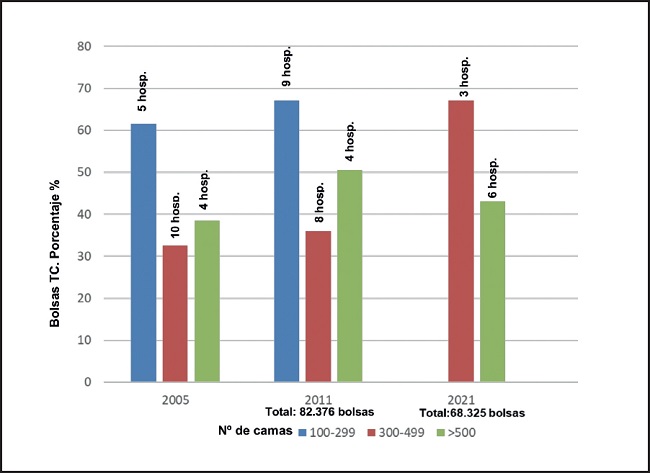
Figura 8. Evolución de la utilización de tricamerales en los hospitales catalanes de < 300 camas, de entre 300 y 499 camas y de > 500 camas. Años 2005, 2011 y 2021 (17,18).
El 4 de noviembre del 2014, el laboratorio Baxter y la Agencia Española de Medicamentos y Productos sanitarios (AEMPS) notifican los errores durante el uso de Olimel© y PeriOlimel©, relacionados con la falta de “activación” (mezclado posruptura de compartimentos) o una “activación incompleta” u otros tipos de errores de medicación, tales como la velocidad de infusión excesiva o la vía de administración. Antes, Sirvent (21) se había adelantado al problema al publicar 9 recomendaciones sobre las buenas prácticas en el uso seguro de los TC. Resumiendo, recuerda que la prescripción y la validación de las TC deberán ser igual que en las NPT preparadas en farmacia; no deberían existir en las dotaciones de medicamentos de las salas de hospitalización, y la adición de vitaminas y oligoelementos debe realizarse bajo condiciones estrictas de asepsia.
NUEVOS SUBSTRATOS DE AMINOÁCIDOS Y DE LÍPIDOS
Fürst (22) opina que la proteína de huevo es la que más refleja un alto valor biológico, pero comenta que algunos aminoácidos no esenciales, que pueden ser esenciales en algunas situaciones clínicas, están exentos de las soluciones comerciales, como la L-glutamina, la L-cisteína o la L-tirosina, a causa de su poca solubilidad (35 g/L; 0,4 g/L y 0,1 g/L, respectivamente), o que falta taurina, un aminoácido no esencial que se almacena en el espacio intracelular pero que puede ser esencial en situaciones catabólicas.
En el caso particular de la L- glutamina, en la farmacia de nuestro hospital fabricamos en 1995 este aminoácido (23) a partir de una solución salina al 0,2 % que contenía un 2 % de L-glutamina, preparándose mediante filtración esterilizante por 0,2 µ debido a la pérdida de estabilidad por calor. El estudio de estabilidad se realizó a -20 °C, 5 °C y a temperatura ambiente durante los días 0 (el mismo día de la preparación), 1, 3, 7 y 15. La solución de L-glutamina al 2 % fue estable 7 días a 5 °C. Su indicación princeps era evitar la translocación bacteriana intestinal y, con ello, disminuir las infecciones. Probamos en el Servicio de Hematología de nuestro hospital, en las mucositis de grado IV y en el EICH intestinal. No obtuvimos buenos resultados. Dos años más tarde, Fresenius comercializó 2 dipéptidos: Glamin (glicil-L-glutamina)© y Dipeptiven (L-alanina-L-glutamina)©.
En la utilización de las emulsiones lipídicas, después de un inicio de empleo de Intralipid© en la NP, iniciamos en 1985 el empleo de la mezcla MCT/LCT© con la finalidad de disminuir la cantidad de poliinsaturados ricos en α-linoleico (omega-6), principal causa en la producción de ecosanoides proinflamatorios; así, del 52 % con el Intralipid 20 %© pasamos al 22 %. En el 2000, la irrupción de la emulsión lipídica con aceite de oliva (Clinoleico©) disminuyó al 19 % los poliinsaturados y además aportó ácidos grasos monoinsaturados en cantidades importantes. No tuvieron éxito los lípidos estructurados. Su formulación era una emulsión grasa de ácidos grasos de cadena media (MCT) -aceite de coco- y ácidos grasos de cadena larga (LCT) -aceite de soja- esterificados en la misma molécula de glicerol. Mejoraron la disminución de la hipertrigliceridemia.
En 2003 se lanzan en el mercado dos marcas comerciales con aceite de omega-3, que sustituyen al suplemento de ácidos grasos omega-3 (Omegaven©): la primera, Lipoplus©, es una mezcla de aceite de soja y aceite de coco rica en omega-3 (5,4 %); la otra, Smof©, es similar a la anterior, pero con un 30 % de aceite de oliva y una cantidad menor, poco significativa, de omega-3, del 4,5 %.
LA ORDEN DE 2 DE JUNIO DE 1997 PARA REGULAR LA NUTRICIÓN ENTERAL DOMICILIARIA. LA CONTRIBUCIÓN DE LOS FARMACÉUTICOS DE HOSPITAL A LA PREPARACIÓN DE GUÍAS PARA LA ADMINISTRACIÓN DE FÁRMACOS POR SONDA NASOGÁSTRICA Y ENTEROSTOMÍA
En la Orden de 2 de junio de 1997 (24), para regular la NED en el Sistema Nacional de Salud, se ocasiona, excepto en las comunidades autónomas de Galicia y Cataluña, un retroceso en los conocimientos de NE de los farmacéuticos responsables de la nutrición artificial de los hospitales españoles ya que, en 1996, la Sociedad Española de Endocrinología consigue que las jefaturas de las unidades de nutrición recaigan en un endocrinólogo/a con la especialidad MIR, y serán estos los que pautaran las dietas enterales domiciliarias (NED). Mientras, en las dos comunidades mencionadas, la dispensación se realizará a partir de los servicios de farmacia de los hospitales de referencia. Este hecho implica que los farmacéuticos, excepto en las dos comunidades citadas, no conocerán la NE (tipo de dietas, tipos de sondas, etc.). Nosotros, en un primer momento, tuvimos que editar un vademécum de las dietas enterales comercializadas (25), donde los apartados más importantes eran: sabores, densidad calórica, fibra y tipos, viscosidad y carga renal de solutos. La indicación más importante, en un primer momento, de los 4 apartados de la Orden de 2 de junio fue la suplementación oral. Esta fue la primera indicación en el registro nacional de la nutrición enteral domiciliaria (NED), coordinado por el grupo NADYA (Nutrición Artificial Domiciliaria y Ambulatoria).
Esta orden ministerial relanza la figura de los dietistas después de un largo recorrido en busca de su identidad. En 1987, la figura del dietista en España todavía no estaba clara. En muchos hospitales ejercen como “dietistas” los administrativos que son responsables de las compras de las comidas para los enfermos de los hospitales. No se aprobará la Diplomatura en Dietética y Nutrición (3 años) hasta el Consejo de Ministros de marzo del 1998 como título universitario, a pesar de que las universidades del País Vasco, Navarra y Barcelona impartían la diplomatura desde 1987.
Los dietistas de los equipos multidisciplinarios de soporte nutricional nos piden a los farmacéuticos las interacciones de los fármacos con los alimentos. En 1999 publicamos dichas interacciones (26), intentando seguir la filosofía americana de la Joint Commission on Acreditation of Health Care Organization (JCAHO), que recomienda desde 1985 monitorizar las posibles interacciones entre fármacos y alimentos a partir del nivel farmacocinético (absorción, metabolización, etc.). Concluíamos que era difícil conocer cuáles eran las interacciones relevantes excepto las que habían producido problemas clínicos (interacciones de lácteos con algunos antibióticos), y avisamos que los fármacos con estrecho margen terapéutico, frente a un problema de absorción o metabolización, podían desajustar estos niveles. Finalizamos, a partir de una revisión de Delgado (27) de la administración de fármacos que se deberían tomar en ayunas, con las comidas para aumentar la absorción o disminuir las molestias gastrointestinales, y lo que se debe tomar 20 min. antes de las comidas o 1 hora después de las mismas.
Un año más tarde, tras la Orden de 1997, publicamos un estudio prospectivo de utilización de medicamentos por SNG o enterostomía. Se realizó durante 34 días en pacientes ingresados en nuestro hospital y portadores de SNG (62) o enterostomía (4) (28). Se recogió información de los 82 fármacos prescritos a 66 pacientes y la forma farmacéutica utilizada. En la metodología, cada presentación de fármaco, en comprimidos o cápsulas, se diluía en 50 mL de agua antes de su administración, mientras que los jarabes, soluciones o suspensiones se aplicaban directamente. Valoramos: la osmolaridad (≥ 1000 mOsm/kg), la posibilidad de diarreas y el pH, si ≤ 3,5 o ≥ 10, que aumentan las precipitaciones en la SNG; la viscosidad y la velocidad de caída del fármaco por la SNG se determinaron para conocer la posible dificultad de la administración según el diámetro de la sonda, y si contenían o no sorbitol en el contexto de las diarreas por este poliol utilizado como edulcorante.
Hidalgo y cols. (29) fueron de los primeros, en 1995, en publicar una guía de administración de fármacos por sonda nasogástrica; siguieron, entre otros, Piñeiro (1999) (30) y, en los inicios del 2000, sobresale Izco (31). Últimamente, Romero (2017) (32) revisa los fármacos con la NE en los pacientes crónicos complejos y Crespo (33), del Grupo de Farmacia de la SENPE y el Grupo de Nutrición Clínica de la SEFH (2022), edita unas recomendaciones para la administración de antineoplásicos e inmunomoduladores orales por sonda enteral.
EL PRIMER DECENIO DEL NUEVO MILENIO, LOS FARMACÉUTICOS DE HOSPITALES RESPONSABLES DE NUTRICIÓN EN BUSCA DE UNA NUEVA IDENTIDAD. PRIMEROS ENFERMOS CON INTESTINO CORTO CON NUTRICIÓN PARENTERAL DOMICILIARIA (2001-2010)
Como hemos mencionado, el auge de la NED deja fuera de contexto a la mayoría de los farmacéuticos responsables de la nutrición de su hospital, excepto en las dos comunidades autónomas antes citadas. Se pide, como en las especialidades médicas, que no son especialistas, un área de capacitación específica en nutrición clínica para los farmacéuticos especialistas en farmacia hospitalaria. La verdad, surgió la diferencia entre los farmacéuticos “preparadores” de la NP y los clínicos que podían pasar visita en el seguimiento de la NP.
En la farmacia del Hospital de la Santa Creu i Sant Pau, para reforzar los conocimientos sobre NP y NE, se realizaron 4 cursos (2000-2004) de una semana con el nombre de “Formación de formadores en nutrición artificial”. El curso era gratis pero los “formadores” debían comprometerse a realizar en su área nacional de farmacia hospitalaria el mismo curso. Se quería producir un efecto dominó. Durante la estancia se pasaba visita por las mañanas con el farmacéutico responsable de la nutrición en el Hospital Santa Creu i Sant Pau y, por las tardes, se comentaban los enfermos, revisando los temas teóricos por las preguntas recogidas de la mañana. Funcionó el efecto dominó durante dos años, después fue difícil su seguimiento. A pesar de todo, surgió un grupo de 20-25 personas con una nueva mentalidad en la nutrición hospitalaria y ayudó a que el Real Decreto 1277/2003 avalase al farmacéutico como facultativo sanitario para la dirección de la Unidad de Nutrición y Dietética (34). A pesar de ello, la mayoría de jefaturas de servicio de farmacia de nuestro país, quizás por falta de medios, no lideraron esta nueva situación.
En nuestro centro, en este decenio continuamos los estudios de estabilidad de fármacos en “Y” con la nutrición parenteral total, así como en la periférica: metamizol, paracetamol, micofenolato de mofetilo, dexketoprofeno y ciclosporina.
La responsabilidad de facilitar la NED nos abrió nuevos estudios con la NE: cómo la viscosidad de la dieta enteral podía influir en la velocidad y el tiempo de administración en las sondas de diámetro externo de 8 y 10 French (2,4 mm y 3 mm) (35) (Fig. 9).
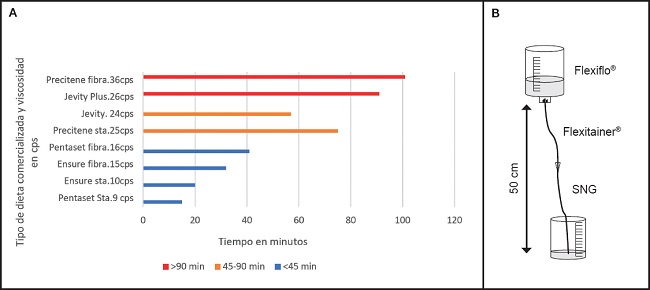
Figura 9. A. Tipos de dietas enterales. Relación entre la viscosidad y el tiempo de caída libre por sonda de 8 Fr (Fuente: Montejo O, et al. Nutr Hosp 2001;16:41-5). B. Método de ensayo. Tipo de dieta, diámetro de SNG y tiempo de caída libre.
Otra área de revisión de la NED fue la utilización de los suplementos orales. En el resumen anual de NADYA de 1999 (36), de los 2262 pacientes estudiados, un 50,7 % utilizaban la suplementación oral (500-600 kcal/d). En una revisión del 2002 editamos una posible guía de utilización (37), recordando que podíamos cambiar en algunos casos el suplemento por 250 ml de leche entera a media mañana y media tarde, acompañada de un suplemento polivitáminico: p. ej., Dayamineral© gotas, XX gotas en la toma de media mañana. Sí que eran recomendables los suplementos orales en los ancianos con sarcopenia u obstrucción crónica del flujo respiratorio y en los enfermos postoperados de cirugía gástrica con un IMC ≤ 20 kg/m2.
Sin duda, el trabajo que nos han citado más veces en la bibliografía general ha sido también una aplicación de una dieta enteral en la inmunosupresión, que se comercializó a los inicios del nuevo decenio: la dieta Impact©, una mezcla de nucleótidos, arginina y omega-3 con suplementación de zinc (38). Aleatorizamos a 66 pacientes candidatos a gastrectomía total en 2 grupos. En el acto quirúrgico se insertaba por vía s.c. en el brazo un catéter de politertrafluoetileno. Durante el postoperatotio inmediato (12-24 h) se administraban por yeyunostomía en infusión continua: en el grupo de control, Isosource protein© y en el grupo de estudio, IMPACT© (nuleótidos, arginina, omega-3, con suplementación de zinc en valores superiores a los normales). Ambos grupos recibían diariamente la misma cantidad de proteínas y calorías. Al 4.º día se llegaba al 100 % de las necesidades. La duración del estudio fue de 7 días. Este séptimo día se retiraba el catéter subcutáneo y se analizaba la cantidad de hidroxiprolina, un aminoácido semiesencial exclusivo de la formación de colágeno. Los ítems del estudio entre los 2 grupos eran: tiempo de cicatrización de la herida, fallos de sutura, infecciones y días de estancia hospitalaria. En el grupo de estudio, la cantidad de hidroxiprolina producida fue el doble que en el grupo de control y ello se tradujo en diferencias significativas: menor tiempo de cicatrización, menos fallos de sutura y directamente menor estancia hospitalaria.
En el 2007 tuvimos los primeros 2 enfermos con intestino corto (enfermedad de Crohn e isquemia intestinal masiva), candidatos a nutrición parenteral domiciliaria (NPD).
FINAL. ACONSEJAMOS EL MANEJO DE LAS ILEOSTOMÍAS TERMINALES, REVISAMOS CÓMO SE ABSORBEN LOS FÁRMACOS EN LAS CIRUGÍAS GÁSTRICAS, BARIÁTRICAS, ETC., Y LOS CENTROS DE SALUD NOS PREGUNTAN CÓMO ADMINISTRAR LOS FÁRMACOS CON LOS ESPESANTES (2010-2018)
Seguimos en el inicio de este decenio con las estabilidades de fármacos en “Y” con la NPT y la NPP: ciclosporina, fluconazol, ceftriaxona, heparina sódica, amiodarona y dexmedetomidina. En 2013 (39) publicamos una revisión de los fármacos que eran compatibles e incompatibles con la NPT, ídem con la NPP; de los fármacos estables en la NPT, de los fármacos con controversia respecto a su estabilidad en la administración en “Y” y en la NP. Se revisaban: su estabilidad química y si se observaba ruptura de la emulsión.
El tema que nos ha sorprendido últimamente son las complicaciones en una cirugía media como la hemicolectomía D por neo de colon ascendente y empleando la nueva filosofía ERAS (Enhanced Recovery After Surgery). En 2018, en la indicación de la NP en cirugía destacaban un 20 % de íleos paralíticos, especialmente en este tipo de cirugía, posiblemente por la insuflación de aire en la laparoscopia, y un número mucho menor de fallos en la sutura de la anastomosis ileón-colon transverso. En estos últimos tuvimos que aconsejar en la ileostomía terminal temporal (2-3 meses) el manejo nutricional y cómo resolver las pérdidas de líquido en los casos de > 2 L/día (> 7 veces/día el vaciamiento de bolsas de 300 mL).
Mejoramos esta situación: a) que el agua de bebidacontuviera sodio y bicarbonato; b) pautamos loperamida 4 mg/8 h como máximo; c) aportar fibra de Plantago ovata/8 h; d) mantener los niveles de magnesio a pesar de dosis elevadas de lactato de magnesio (4 mEq/comp): 2-2-2. Aprendimos que la absorción de magnesio en un tránsito intestinal rápido tiene un máximo de absorción, que si sobrepasamos este dintel se elimina por orina; e) iniciar omeprazol 40 mg/12 o 24 h en caso de líquido de ileostomía ácido (color amarillo) que daña la piel al sujetar la bolsa (Fig. 10).
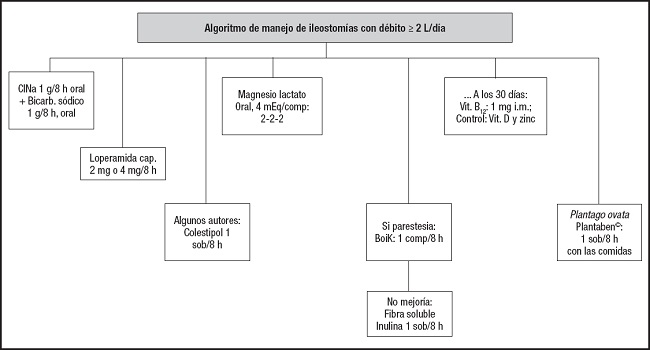
Figura 10. Medidas generales en el manejo de las ileostomías, en el contexto del alta hospitalaria, con débitos de ≥ 2 L/día, de consistencia líquida el 100 % y color amarillo o bilioso.
Las residencias y los centros de día nos pidieron cómo debían administrar los fármacos con los espesantes. Para ello realizamos un estudio sobre el cambio de viscosidad de algunos espesantes a la adición de fármaco más prescritos en geriatría. Observamos una disminución de la viscosidad en la galantamina, memantina y fosfomicina (40).
¿EL FUTURO...?
A pesar de todo ello, el farmacéutico clínico, el pase de visita diario con los clínicos, tienen un futuro no muy halagüeño según las respuestas a una encuesta realizada personalmente a 120 residentes R-2 y R-3 de 61 hospitales de nuestro país en el Curso de Farmacia Clínica de 2017, que organiza el Servicio de Farmacia del Hospital de la Sta. Creu i Sant Pau de Barcelona.
La primera pregunta era si todavía forman en NP en el Servicio de Farmacia (≤ 6 meses, suficiente tiempo para su conocimiento): 9 hospitales (31 %) confirmaron la formación, pero en 27 hospitales (45 %) la instrucción sobre NP y NE se hacía en el Servicio de Endocrinología (1-3 meses) y, en un 10 %, en la Unidad de Cuidados Intensivos; en el 13 % no se hacía ninguna formación.
La segunda era si conocían la NE: el 65,5 % tenían contacto a partir del Servicio de Endocrinología (1-3 meses) y un 15 % no se formaban nunca en NE. Sí que los residentes de las comunidades autónomas de Galicia y Cataluña conocían la NE a partir de sus hospitales.
El futuro es el de siempre: si un farmacéutico pasa visita con los cirujanos, endocrinos e intensivistas principalmente, surgirán preguntas de estos profesionales hacia nosotros sobre las posibles interacciones entre fármacos y los tipos de nutrición, como NP, NE u oral. No solamente sobre las interacciones farmacocinéticas sino también sobre la estabilidad físico-química de los fármacos administrados en “Y” con la NP y sobre cómo debemos manejar los medicamentos insertados por sondas nasogástricas y por ostomías.
La investigación en NP o NE en los servicios de farmacia de nuestro país es complicada. A nivel personal siempre he creído en la investigación clínica: “realizas un trabajo a partir de las preguntas que te haces o te hacen los clínicos en el pase de visita”. Hemos sobrevivido con algunas ayudas de la industria puntuales. Hemos de retornar a la relación de la farmacia de hospital con los servicios de galénica y de nutrición de nuestras facultades. Importante es este último departamento, donde deberíamos estar atentos a las tesis doctorales que se presentan y aprovechar algún método analítico para un futuro trabajo práctico clínico.