INTRODUCCIÓN
A pesar de los efectos benéficos del trasplante renal (TR), las alteraciones del metabolismo del calcio y el fósforo son frecuentes en los receptores de trasplante renal (RTR), condicionando un aumento en la morbimortalidad (1). La enfermedad metabólica ósea (EMO) en RTR se caracteriza por alteraciones en la formación y mineralización ósea, con reducción de la osteoblastogénesis y aumento de la apoptosis del osteoblasto. Dentro de los factores asociados a la EMO en RTR se encuentran: a) las alteraciones del eje FGF23 (factor de crecimiento fibroblástico 23)/PTH (hormona paratiroidea)/vitamina D; b) la terapia de inmunosupresión; c) la presencia de EMO pre-TR; d) las alteraciones de la función del injerto; y e) la hipofosfatemia. Dentro de estos factores, los más importantes son la hipovitaminosis D, el hiperparatiroidismo persistente y el uso de fármacos inmunosupresores (2).
La hipovitaminosis D, definida como la disminución de las concentraciones de 25-hidroxivitamina D [25(OH)D] por debajo de 30 ng/mL según la Endocrine Society (3), se encuentra hasta en el 97 % de los RTR antes del primer año, persistiendo en el 94 % después del primer año post-TR (4). Aproximadamente, el 30 % se encuentran en rangos de deficiencia y el 81-85 % en insuficiencia (5,6). La hipovitaminosis D se asocia con un aumento de la morbimortalidad (2,7) y una reducción de los efectos benéficos del TR (6). Dentro de los mecanismos propuestos en la etiopatogenia de la hipovitaminosis D en los RTR destacan: a) la deficiente suplementación de vitamina D antes y después del TR; b) el aumento del catabolismo de 25(OH)D inducido por los fármacos inmunosupresores (6); c) la conversión acelerada de la 25(OH)D en 1,25(OH)2D ante la hipofosfatemia y la elevación de la PTH (8,9); y d) la reducción de la exposición solar para la prevención del cáncer de piel (6).
Se ha reportado que las adecuadas concentraciones de 25(OH)D en los RTR tienen un efecto positivo sobre el metabolismo mineral óseo, la función cardiovascular, la función del injerto, la prevención de infecciones, la antiproteinuria, la disminución de la incidencia del cáncer de novo y la disminución de la mortalidad (10). El tratamiento con colecalciferol es eficaz para la normalización de las concentraciones de 25(OH)D, demostrándose un efecto benéfico sobre el eje PTH/vitamina D/calcio en individuos aparentemente sanos y en pacientes con diálisis peritoneal o hemodiálisis, caracterizado principalmente por la disminución de las concentraciones de PTH (11-17); sin embargo, los estudios acerca del efecto del colecalciferol sobre el eje PTH/vitamina D/calcio y FGF23/klotho/fósforo en los RTR, sobre todo al lograr el efecto terapéutico de normalización de las concentraciones de 25(OH)D, son escasos.
El objetivo principal de este estudio fue evaluar el efecto de la normalización de las concentraciones séricas de 25(OH)D sobre el eje PTH/vitamina D/calcio y FGF23/klotho/fósforo en RTR tratados con colecalciferol. El objetivo secundario fue evaluar las asociaciones entre los componentes del eje PTH/vitamina D/calcio y FGF23/klotho/fósforo a la normalización de las concentraciones de 25(OH)D.
MÉTODO
PACIENTES
Se realizó un estudio prospectivo en RTR con hipovitaminosis D atendidos en la clínica de metabolismo mineral óseo del departamento de endocrinología de un hospital de tercer nivel de atención. Se incluyeron hombres y mujeres mayores de 18 años de edad, con evolución de más de un mes pero menos de 1 año post-TR, con una tasa estimada de filtrado glomerular (TFGe) > 60 mL/min/1,73 m2, sin datos de disfunción o rechazo del injerto y con antecedente de enfermedad primaria como causa de enfermedad renal crónica (ERC). Se excluyeron los pacientes con datos de disfunción o rechazo del injerto, TFGe < 60 mL/min/1,73 m2, hipercalcemia, hipersensibilidad conocida al fármaco y enfermedades crónico-degenerativas como diabetes, hipertensión arterial, hepatopatía, obesidad, enfermedades autoinmunes, infecciosas o neoplasias, esto con el propósito de disminuir los sesgos generados por el efecto deletéreo directo de dichos factores sobre el metabolismo mineral.
Se definió la hipovitaminosis D como una concentración de 25(OH)D en sangre inferior a 30 ng/mL (3). Se consideró que había deficiencia de vitamina D cuando la concentración de 25(OH)D era < 20 ng/mL e insuficiencia cuando se encontraron entre 21 y 29 ng/mL (3). Se realizó la evaluación clínica y bioquímica del eje PTH/vitamina D/calcio y FGF23/klotho/fósforo antes del inicio del colecalciferol y al lograr la normalización de las concentraciones de 25(OH)D.
TRATAMIENTO CON COLECALCIFEROL
El tratamiento de la hipovitaminosis D consistió en la administración de colecalciferol a dosis de 4000 unidades internacionales por día (UI/d), con medición de la 25(OH)D sérica mensualmente, hasta lograr la normalización (> 30 ng/mL). Se indicó un aumento de 2000 UI/d cada mes cuando el paciente continuaba con 25(OH)D por debajo de 30 ng/dL. La dosis máxima de colecalciferol fue de 10,000 UI/d (3). Una vez lograda la normalización de la 25(OH)D, la dosis de mantenimiento fue de 2000-4000 UI/d [2000 UI/d si las concentraciones de 25(OH)D eran > 40 ng/mL y 4000 UI/d si las concentraciones de 25(OH)D estaban entre 30 y 39 ng/mL]. Se cuantificó en semanas el tiempo en que se logró la normalización de la 25(OH)D. Solo se incluyeron en el análisis los pacientes que lograron la normalización de las concentraciones de 25(OH)D. Las reacciones adversas medicamentosas (RAM) investigadas fueron: hipercalcemia, hiperfosfatemia, hipercalciuria, litiasis renoureteral e hipersensibilidad. Se utilizó el método de recuento de píldoras para evaluar la adherencia terapéutica. Esta medida indirecta y objetiva contó el número de píldoras que se habían tomado entre dos visitas a la clínica en comparación con el número total de píldoras recibidas por el paciente (número de píldoras dispensadas - número de píldoras restantes) / (número prescrito de píldoras por día × número de días entre 2 visitas); el resultado se multiplicó por 100 para obtener el porcentaje de adherencia. La adherencia exitosa se definió como la toma del 90-100 % de las píldoras durante el seguimiento. La función renal se evaluó midiendo las concentraciones de urea y creatinina, así como la tasa de filtración glomerular estimada (TFGe) por CKD-EPI.
EVALUACIÓN BIOQUÍMICA
Se realizó la toma de una muestra de 5 mL de sangre a través de venopunción después de 8 horas de ayuno. Se utilizaron métodos automatizados basados en ensayos colorimétricos y espectrofotométricos (COBAS, Roche, EE. UU.) para la medición del calcio (suero y orina), el magnesio (suero), el fósforo (suero y orina), la albúmina (suero), la urea (suero), la creatinina (suero) y la fosfatasa alcalina (suero). El rango normal (RN) de cada una de estas fue: calcio sérico: 8,4-10,2 mg/dL; calcio urinario de 24 horas < 300 mg/día; fósforo sérico: 2,7-4,5 mg/dL; fósforo urinario de 24 horas: 400-1300 mg/día; magnesio: 1,6-2,6 mg/dL; urea: 10-50 mg/dL; creatinina: 0,40-1,2 mg/dL; albúmina: 3,5-5,2 g/dL; y fosfatasa alcalina: varones: 40-129 U/L; mujeres: 35-104 U/L. Las concentraciones de calcio sérico corregido (mmol/L) se obtuvieron mediante la siguiente fórmula: 4 g/dL - concentración de albumina sérica (g/dL)) × 0,8 + calcio sérico total medido (mg/dL). La relación calcio urinario/peso corporal fue el cociente de la división entre el calcio urinario de 24 horas y el peso en kg (RN < 4 mg/kg de peso corporal por día). Se utilizó un ensayo quimioluminiscente específico para medir la PTH (DiaSorin Inc, EE. UU.), con una sensibilidad de 1 pg/mL y un coeficiente de variación (CV) inter e intraensayo del 5,3 % y 3,5 %, respectivamente, con RN de 15-65 pg/mL. Las concentraciones séricas de 25(OH)D se midieron por quimioluminiscencia (DiaSorin Inc., EE. UU.) con una sensibilidad de 4 ng/mL y unos CV inter e intraensayo del 5,1 % y 8,6 %, respectivamente. Para las mediciones de las concentraciones séricas de FGF23 y klotho se empleó un ensayo inmunoenzimático (ELISA). Para el FGF23 se utilizó el kit "Human FGF23 ELISA" (Aviva Systems Biology, Corp. San Diego, CA, EE. UU.), con RN de 15,6-1000 pg/mL y sensibilidad de 10 pg/mL, con CV intraensayo del 4 % e interensayo del 6,4 %. Para la klotho se utilizó el kit de ELISA "Human KL" (Aviva Systems Biology, Corp. San Diego, CA, EE. UU.), con un RN de 7,8-500 pg/mL y una sensibilidad de 2,4 pg/mL, y un CV intra e interensayo del 4,7 % y 7,1 %, respectivamente.
INMUNOSUPRESIÓN
Todos los pacientes recibieron tratamiento inmunosupresor con prednisona, micofenolato mofetilo y tacrolimus, los cuales fueron reportados como dosis en mg/día.
ANÁLISIS ESTADÍSTICO
Las variables categóricas se informaron como frecuencias absolutas y porcentajes. Las variables cuantitativas se describieron como media ± desviación estándar (DE) o mediana y rango intercuartílico (RIC), según su distribución. La relación entre las variables categóricas se evaluó mediante la prueba del χ2; las variables cuantitativas se analizaron mediante las pruebas T, de Wilcoxon o U de Mann-Whitney, según su distribución. Las correlaciones de las variables cuantitativas se realizaron con el coeficiente de correlación de Spearman. La regresión lineal se utilizó para explicar la relación entre una variable dependiente y una o más variables independientes. Se utilizó la transformación logarítmica en los datos no paramétricos para incluirlos en el modelo de regresión lineal. Todas las pruebas estadísticas se calcularon a dos colas; el valor p < 0,05 se consideró estadísticamente significativo. El tamaño de la muestra tuvo un valor α = 0,05, un b = 0,1 y una potencia estadística 1 - β = 0,9 (G*Power). Se utilizaron los programas estadísticos IBM SPSS Statistics v.25.0 (IBM SPSS, EE. UU.) y STATA v.13 (StataCorp, EE. UU.) para el análisis.
ASPECTOS ÉTICOS
Este protocolo fue desarrollado de acuerdo a las recomendaciones nacionales e internacionales en materia de investigación y fue aprobado por el Comité Local de Ética e Investigación. Se obtuvo del consentimiento informado de todos los pacientes previamente a su inclusión en el estudio.
RESULTADOS
CARACTERÍSTICAS BASALES DE LA POBLACIÓN
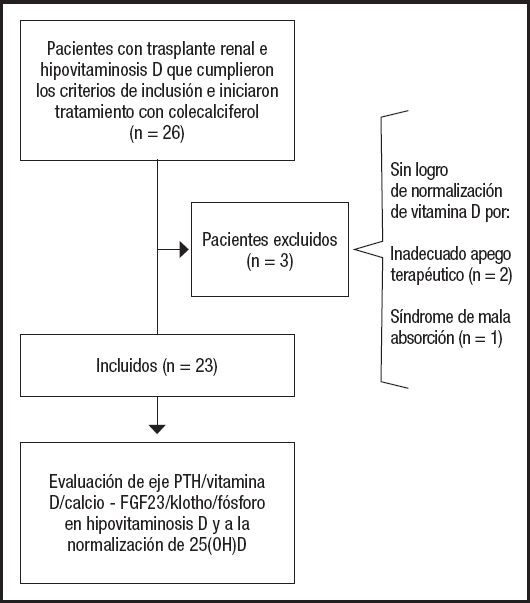
De un total de 26 RTR con hipovitaminosis D tratados con colecalciferol se incluyeron en el análisis 23 pacientes que lograron la normalización de las concentraciones séricas de 25(OH)D. De los 3 pacientes que no lograron normalizar la 25(OH)D, dos tuvieron un inadecuado apego terapéutico y en un paciente se diagnosticó síndrome de malabsorción intestinal (Fig. 1). El 52,2 % (n = 12) fueron hombres, con una mediana de edad de 28 años (RIC: 25-33,5). Todos los pacientes eran latinos. Las características basales de los pacientes se resumen en la tabla I.
Tabla I. Características basales de los receptores de trasplante renal incluidos en el estudio (n = 23).
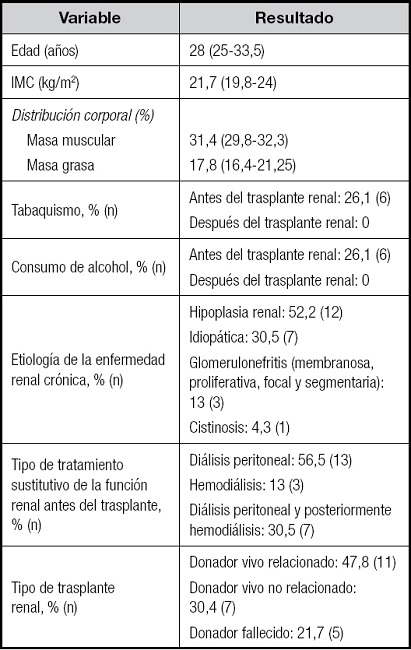
IMC: índice de masa corporal.
Variables cualitativas reportadas en porcentajes y frecuencia. Variables cuantitativas reportadas en mediana y rango intercuartílico.
Después del inicio del colecalciferol, el tiempo para lograr la normalización de las concentraciones séricas de 25(OH)D fue de 12 semanas (RIC: 4-12). La dosis de colecalciferol requerida para lograr la normalización de la 25(OH)D fue de 5000 UI/día (RIC: 4000-6000). Durante el tratamiento con colecalciferol no se evidenciaron reacciones adversas medicamentosas o sospecha de las mismas.
EFECTO DE LA NORMALIZACIÓN DE LAS CONCENTRACIONES SÉRICAS DE 25(OH)D SOBRE EL EJE PTH/VITAMINA D/CALCIO EN RECEPTORES DE TRASPLANTE RENAL TRATADOS CON COLECALCIFEROL
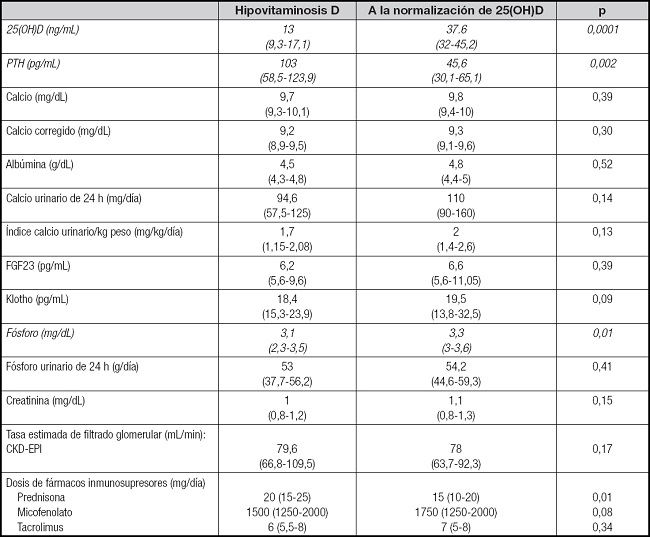
Cuando se logró la normalización de la 25(OH)D se evidenció el aumento de las concentraciones de 25(OH)D [13 (9,3-17,1) vs. 37,6 (32-45,2) ng/mL; p = 0,000] y la reducción de la PTH [103 (58,5-123,9) vs. 45,6 (30,1-65,1) pg/mL; p = 0,002] con respecto al estado de hipovitaminosis D. Se evidenció una reducción del 56 % en las concentraciones de PTH. No se encontraron diferencias estadísticamente significativas en las concentraciones de calcio, calcio urinario de 24 h e índice CaU/kg (Tabla II). En el 96 % (n = 22) de los pacientes, las concentraciones de PTH se normalizaron.
EFECTO DE LA NORMALIZACIÓN DE LAS CONCENTRACIONES SÉRICAS DE 25(OH)D SOBRE EL EJE FGF23/KLOTHO/FÓSFORO EN RECEPTORES DE TRASPLANTE RENAL TRATADOS CON COLECALCIFEROL
Al evaluarse las características del eje FGF23/klotho/fósforo se observó un aumento de las concentraciones de fósforo sérico [3,1 (2,3-3,5) vs. 3,3 (3-3,6) mg/dL; p = 0,01]. No se evidenciaron diferencias estadísticamente significativas en las concentraciones de FGF23, klotho y fósforo urinario de 24 h al compararlas durante la hipovitaminosis D y a la normalización de las concentraciones de 25(OH)D (material suplementario).
No se evidenciaron diferencias en las concentraciones de magnesio [1,7 (1,5-1,9) vs. 1,7 (1,5-1,8) mg/dL; p = 0,37], fosfatasa alcalina [82 (71-92) vs. 75 (68-82,5) U/L; p = 0,22], creatinina [1 (0,8-1,2) vs. 1,1 (0,8-1,3) mg/dL; p = 0,15] ni en la TFGe [79,6 (66,8-109,5) vs. 78 (63,7-92,3) mg/dL; p = 0,17] con la normalización de las concentraciones de 25(OH)D.
ASOCIACIONES ENTRE LOS COMPONENTES DEL EJE PTH/VITAMINA D/CALCIO Y FGF23/KLOTHO/FÓSFORO A LA NORMALIZACIÓN DE LAS CONCENTRACIONES SÉRICAS DE 25(OH)D
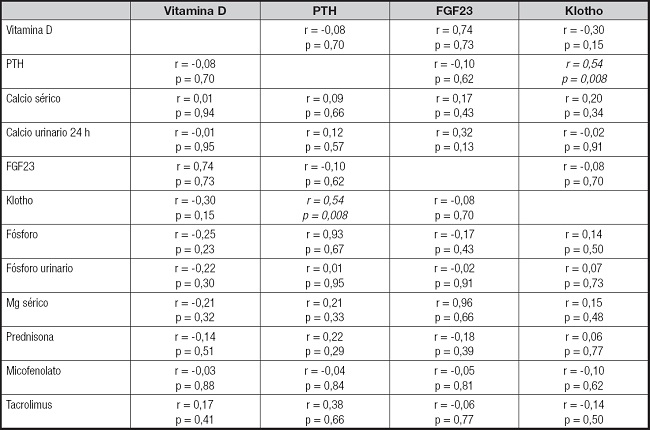
El análisis de las asociaciones entre los diferentes componentes del eje PTH/vitamina D/calcio y FGF23/klotho/fósforo cuando se logró la normalización de las concentraciones de 25(OH)D corroboró una asociación positiva entre klotho y PTH (r = 0,54; p = 0,008; regresión lineal, β = 0,421; B = 0,004; IC 95 %, 0,003 a 0,007; p = 0,045). No se observaron asociaciones entre el resto de las variables y tampoco se evidenció asociación con la dosis de los fármacos incluidos en el esquema inmunosupresor (Tabla III).
DISCUSIÓN
En este estudio se evaluó el efecto de la normalización de las concentraciones séricas de 25(OH)D sobre el eje PTH/vitamina D/calcio y FGF23/klotho/fósforo en RTR tratados con colecalciferol, evidenciándose una reducción de la PTH (incluso la normalización de esta hormona en la mayoría de los pacientes) y la optimización de las concentraciones de fósforo con respecto al estado de hipovitaminosis D, sin evidencia de hipercalcemia, hiperfosfatemia, hipercalciuria o modificaciones de la función renal durante el tratamiento. Por otra parte, se encontró como hallazgo relevante la asociación positiva entre klotho y PTH, no descrita previamente en RTR.
El trasplante renal exitoso mejora las alteraciones del metabolismo mineral óseo, principalmente a lo largo del primer año post-TR (18). Como se comentó previamente, a pesar del efecto benéfico del TR, las alteraciones del metabolismo del calcio y fósforo son frecuentes en los pacientes RTR. La hipovitaminosis D, al igual que en la población general, es frecuente en los RTR, condicionando un aumento de la morbimortalidad. La normalización de las concentraciones séricas de 25(OH)D en los RTR es posible con el tratamiento con colecalciferol, lo cual promueve efectos positivos sobre el metabolismo mineral óseo tal y como evidenciamos en este estudio. Algunos estudios han evaluado el efecto de colecalciferol sobre el eje PTH/vitamina D/calcio y FGF23/klotho/fósforo en poblaciones diferentes a la incluida en este estudio.
En individuos aparentemente sanos con hipovitaminosis D, el tratamiento con colecalciferol ha mostrado una reducción de las concentraciones de PTH y, sin embargo, un aumento significativo de 1,25(OH)2D y FGF23 (11); en este estudio controlado con placebo, el tratamiento con colecalciferol condicionó un incremento de las concentraciones de FGF23, el cual se asoció de manera directa con el aumento en las concentraciones de 1,25(OH)2D (11). En los pacientes con obesidad/sobrepeso e hipovitaminosis D, la administración de colecalciferol normalizó las concentraciones de 25(OH)D y disminuyó las concentraciones de PTH (12).
En los pacientes en diálisis peritoneal, el tratamiento con colecalciferol condicionó un aumento exponencial del FGF23 con niveles elevados (> 30.000 pg/mL) en el 74 % de los casos y con reducción hasta valores basales a las 32 semanas de su suspensión (13). En dicho estudio, la elevación de los valores de FGF23 se asoció también al incremento de los valores de 1,25(OH)2D (13). Por otra parte, en una población con ERC y TGFe > 30 mL/min/1,73 m2 no se evidenciaron modificaciones de las concentraciones de FGF23 y klotho después del tratamiento con colecalciferol (14).
En los pacientes en hemodiálisis, el tratamiento con colecalciferol logró la normalización de la 25(OH)D dentro de los primeros 3 meses de tratamiento, sin modificaciones de las concentraciones de PTH a lo largo de su seguimiento; sin embargo, al compararlos contra un grupo con placebo, se observaron menores concentraciones de PTH (15). Otro estudio de pacientes en hemodiálisis demostró una reducción de las concentraciones de klotho durante el tratamiento con colecalciferol, sin modificaciones de FGF23 (16).
Específicamente en los RTR se ha observado una reducción de la PTH (12 %) a los 12 meses de tratamiento con colecalciferol (17), independientemente de si se logró la normalización de la 25(OH)D; sin embargo, su efecto sobre otros parámetros del eje FGF23/klotho/fósforo no se había descrito hasta este momento. Cabe destacar que, en cada uno de los estudios previamente comentados, los componentes del eje PTH/vitamina D/calcio y FGF23/klotho/fósforo no se evaluaron de manera simultánea, a diferencia de nuestro estudio.
En nuestro estudio corroboramos la disminución de las concentraciones de PTH con un porcentaje mayor al reportado (56 % vs. 12 %), observando incluso que la mayoría de los pacientes normalizaron la PTH (96 %); en el paciente en que no se normalizó esta hormona, se evidenció una reducción mayor del 50 % con respecto a su valor pretratamiento. Aunado a lo anterior, evidenciamos una optimización de las concentraciones de fósforo, sin condicionar hiperfosfatemia, aunado al mantenimiento de normocalcemia y, a diferencia de lo evidenciado en otras poblaciones, no se corroboraron diferencias significativas en las concentraciones de FGF23 o klotho.
Por otra parte, resultan interesantes la dosis y el tiempo requeridos para normalizar las concentraciones de 25(OH)D en nuestro estudio. En la población general se recomienda el tratamiento con colecalciferol a una dosis 1500-2000 UI/día para los adultos de entre 19 y 50 años con hipovitaminosis D, con un tiempo aproximado de 4 a 6 semanas para la normalización de las concentraciones séricas de 25(OH)D (3). En nuestro estudio observamos que la dosis de colecalciferol requerida para normalizar la 25(OH)D en los pacientes RTR fue de 5000 UI/día, con un tiempo de 12 semanas, ambos mayores a lo establecido, lo cual puede guardar relación con alteraciones en parámetros farmacocinéticos como la absorción de colecalciferol, las alteraciones en su distribución o el aumento del catabolismo de vitamina D mediado por otros fármacos (glucocorticoides u otros inmunosupresores). En un estudio previo realizado en una población semejante a la de este estudio se mostró un requerimiento de 4000 UI/día para el mantenimiento de concentraciones séricas de 25(OH)D > 30 ng/dL durante el primer año de seguimiento post-TR (18). Este dato puede ser importante para normar la dosis de colecalciferol a largo plazo dentro de los protocolos para la atención y el tratamiento integral de los RTR.
Durante el tratamiento con colecalciferol no evidenciamos RAM ni sospecha de las mismas; sin embargo, es importante mencionar que, debido al diseño y al objetivo de nuestro estudio, el seguimiento fue relativamente corto. Un estudio previo en nuestra población informó que el tratamiento con colecalciferol no produjo RAM como hipercalcemia o hiperfosfatemia a los 12 meses, detectándose solo un caso de hipercalciuria entre los 74 pacientes incluidos (18). En otra cohorte de RTR tratados con colecalciferol se informó una frecuencia de hipercalcemia del 3,2 % sin observarse hiperfosfatemia, litiasis, hipercalciuria, rechazo del injerto, alteraciones de la función renal, ni fracturas (17). Consideramos que, durante el tratamiento con colecalciferol, los estudios de farmacovigilancia a largo plazo para la detección de RAM o sospecha de las mismas son indispensables para evaluar la seguridad del fármaco y la relación riesgo/beneficio en los pacientes con TR; además, los datos proporcionados por dichos estudios podrían servir para sugerir modificaciones de las dosis de mantenimiento de colecalciferol de manera dinámica y personalizada a cada población.
Otro hallazgo relevante en nuestro estudio es la asociación positiva de klotho y PTH. Klotho tiene un papel importante en la regulación del metabolismo del calcio tanto a corto como a medio plazo, en un sistema regulador de "varios pasos". Klotho se une a la Na+,K+-ATPasa y regula su reclutamiento en la superficie celular; en respuesta a concentraciones reducidas de calcio extracelular, controla la reabsorción de calcio en las células del túbulo contorneado distal y la secreción de PTH en las glándulas paratiroides. En la "regulación de segundos a minutos", klotho promueve el transporte transepitelial de Ca2+ y la secreción de PTH. En la "regulación de minutos a horas" y "de horas a días" regula la homeostasis del calcio a través de la acción de la PTH y de la producción de 1,25(OH)2D mediada por PTH (19). La asociación entre klotho y PTH observada en nuestro estudio puede ser explicada por este mecanismo fisiológico. En la población general con función renal conservada, se ha evidenciado una asociación entre klotho y PTH dependiente del sexo: en hombres se ha visto una asociación positiva entre estas dos variables mientras que en mujeres la asociación es negativa (20). En RTR se ha encontrado una asociación de klotho con la DMO y los niveles de osteocalcina (21); sin embargo, la asociación de klotho y PTH en pacientes RTR no se ha publicado aún, por lo que el hallazgo en nuestro estudio resulta novedoso y original. Cabe destacar que, si bien se demostró una disminución estadísticamente significativa de la dosis de prednisona a la normalización de la 25(OH)D con respecto al estado de hipovitaminosis D, no evidenciamos una asociación de la dosis de este fármaco con alguno de los componentes del eje calcio-fosfotrópico, por lo que las modificaciones de PTH o fósforo no se pueden atribuir a las modificaciones de las dosis de prednisona.
Dentro de las fortalezas de nuestro estudio destacamos la originalidad y relevancia al realizarlo en una población en la cual el efecto del colecalciferol sobre el eje calciotrópico y fosfotrópico aún no se ha estudiado, así como la intervención terapéutica con fines de normalización de las concentraciones de 25(OH)D y no solo de substitución con colecalciferol. Dentro de las limitaciones se encuentra el tamaño de muestra aparentemente reducido derivado de los criterios de inclusión y exclusión establecidos; sin embargo, es importante destacar que con el número de pacientes incluidos se cumplió con un adecuado poder estadístico. Proponemos la realización de estudios futuros para evaluar los efectos de la normalización de las concentraciones de 25(OH)D con colecalciferol sobre el eje calcio-fosfotrópico a largo plazo, su farmacovigilancia y su efecto sobre otras variables a nivel cardiovascular, renal e inmunológico, así como el efecto sobre el pronóstico y la sobrevida.
CONCLUSIONES
El tratamiento con colecalciferol dentro del primer año post-TR es eficaz para la normalización de las concentraciones de 25(OH)D, con un efecto benéfico sobre el metabolismo calcio-fosfotrópico caracterizado por una reducción de PTH y un incremento de la fosfatemia, sin condicionar hipercalcemia, hipercalciuria, hiperfosfatemia, ni modificaciones de FGF23 o klotho. Aunado a lo anterior, se observa una asociación directa entre klotho y PTH al normalizar la 25(OH)D. El presente estudio demuestra que la normalización de las concentraciones de 25(OH)D en pacientes RTR tratados con colecalciferol conduce al control del hiperparatiroidismo secundario sin inducir elevación de FGF23, siendo aquel un fármaco seguro.