INTRODUCCIÓN
La leche materna es el alimento ideal para neonatos e infantes que de manera segura provee la energía y los nutrientes necesarios para su crecimiento y desarrollo; en consideración a esto, la Organización Mundial de la Salud (OMS) recomienda la lactancia materna exclusiva desde el nacimiento y hasta el sexto mes, y la continuación de la lactancia de manera complementaria hasta el segundo año de vida (1). No obstante, existen factores socioculturales, económicos e individuales que pueden afectar de manera negativa a la práctica de la lactancia, bien sea por la separación inevitable del binomio madre-hijo o la presencia de barreras en el contexto de la madre, o porque la práctica misma se encuentra contraindicada; en estos casos, el niño y la madre quedan expuestos a los riesgos de no lactar y sus consecuencias potenciales a corto y largo plazo (2).
En el mundo, según cifras de la OMS para el año 2021, solo el 44 % de los niños recibían lactancia materna exclusiva los primeros 6 meses (3); en Colombia, según datos de la ENSIN 2015, la situación fue similar con solo el 32 % (4). Como estrategia para mejorar la cobertura de la lactancia materna, en el año 2011, en Colombia se inauguran los dos primeros bancos de leche humana (BLH) (5); desde entonces se ha avanzado en la implementación de estos centros, habiendo hasta el momento, según la Sociedad Colombiana de Pediatría, un total de 15 en el país (6). A la fecha, existe un vacío en el reporte de la cantidad y/o calidad del aporte de los biocomponentes que modulan la respuesta inmune y que pueden verse afectados por las técnicas de pasteurización de la leche humana donada que se recibe y procesa en los BLH en Colombia (7).
La composición de la leche humana varía entre las madres, con la etapa de lactancia y de acuerdo con el tiempo de gestación; algunos de sus nutrientes se sintetizan en el lactocito mientras otros provienen de la dieta o de las reservas maternas (8). Además de su aporte significativo de macro y micronutrientes (9,10), la leche materna contiene compuestos bioactivos que impactan la función, condición y/o salud del cuerpo (11); entre estos, hay factores de crecimiento y factores inmunológicos fundamentales para el desarrollo y bienestar del infante (12). En medio de los factores inmunológicos encontrados en mayor concentración están la lactoferrina (LF), proteína multifuncional que se encuentra en una concentración de 1,17-2,11 mg/ml en la leche materna fresca (13) y que está involucrada en la homeostasis del hierro (14); se le reconocen propiedades antimicrobianas, antinflamatorias, anticancerígenas (14,15) e inmunomoduladoras (16) que a su vez favorece la proliferación y diferenciación celular (14,17), y la inmunoglobulina A (IgA) secretora, la inmunoglobulina más abundante en la leche humana (18) y una proteína de respuesta a los patógenos que, si bien no cuenta con actividad antimicrobiana de manera aislada, se ha evidenciado que potencia las propiedades de la LF en este aspecto (19).
En Colombia, los BLH, conforme a los lineamientos del Ministerio de Salud y Protección Social de Colombia (5), someten la leche donada, en miras de garantizar su inocuidad, al proceso de pasteurización Holder; durante este, la leche experimenta cambios de temperatura desde la congelación (-14 °C) hasta los 62,5 °C. Diversos estudios han descrito que la pasteurización Holder conlleva una disminución de los biocomponentes LF e IgA con variaciones considerables; es así como, en cuanto a la LF, los estudios han evidenciado porcentajes de retención del 9 % (19) y el 22 % (20), con pérdidas reportadas en estudios recientes del 87,5 % (21) mientras que, respecto a la IgA, los estudios han mostrado niveles de retención del 49 % (19) y el 72 % (20), con pérdidas reportadas del 20 al 64 % (22).
Conforme a lo anterior, el objetivo de este estudio es hacer una revisión de la literatura disponible en torno a la variación en el contenido de LF e IgA secretora en la leche humana sometida a pasteurización Holder en los BLH.
MATERIALES Y MÉTODOS
Con el propósito de desarrollar este objetivo se llevó a cabo una búsqueda de artículos de investigación relacionados al tema de interés en las bases de datos PubMed y ScienceDirect y en otros motores de búsqueda, como Google Academic, en función de los siguientes descriptores: leche materna, bancos de leche, biocomponentes, pasteurización Holder, inmunoglobulina-A y lactoferrina. Estos descriptores luego fueron organizados en ecuaciones booleanas en español e inglés para facilitar el proceso de búsqueda, como se muestra a continuación: ((banco de leche humana) AND (pasteurización holder) AND (inmunoglobulina A)) OR ((banco de leche humana) AND (pasteurización Holder) AND (lactoferrina)), ((human milk banks) AND (holder pasteurization) AND (immunoglobulin a)) OR ((human milk banks) AND (holder pasteurization) AND (lactoferrin)). Como criterios de inclusión durante la búsqueda, se incorporaron a la revisión artículos de investigación en inglés y español y del año 2009 en adelante; así mismo, se incluyeron artículos publicados o en proceso de publicación en revistas indexadas con un índice H superior a 20 y mínimamente ubicadas en el cuartil dos (Q2) del área correspondiente al estudio, siendo esta información obtenida a partir de los indicadores de ScimagoJR.
En cuanto a criterios de exclusión, no se tuvieron en consideración los artículos de revisión ni aquellos estudios que en su metodología no incluyeran el procesamiento y análisis de muestras de leche humana sometidas a pasteurización Holder o que, por el contrario, no incluyeran en sus resultados la evaluación de los biocomponentes de interés. Con esta ecuación de búsqueda, en la base de datos PubMed se encontraron 15 artículos, en Science Direct 128 artículos y en Google Academic 57 artículos.
A partir de este proceso se seleccionaron 20 artículos que cumplieron con los criterios de inclusión y exclusión; de estos se descartaron 5, dos de los cuales corresponden a estudios sobre el calostro humano, otros dos dedicados a la medición de la actividad antirrotaviral remanente sin cuantificar la reducción en biocomponentes, y un último sobre los efectos del enfriamiento sobre la leche pasteurizada. Al finalizar el proceso de selección bibliográfica, los investigadores hicieron revisión y extracción de la información relevante para su posterior síntesis.
RESULTADOS
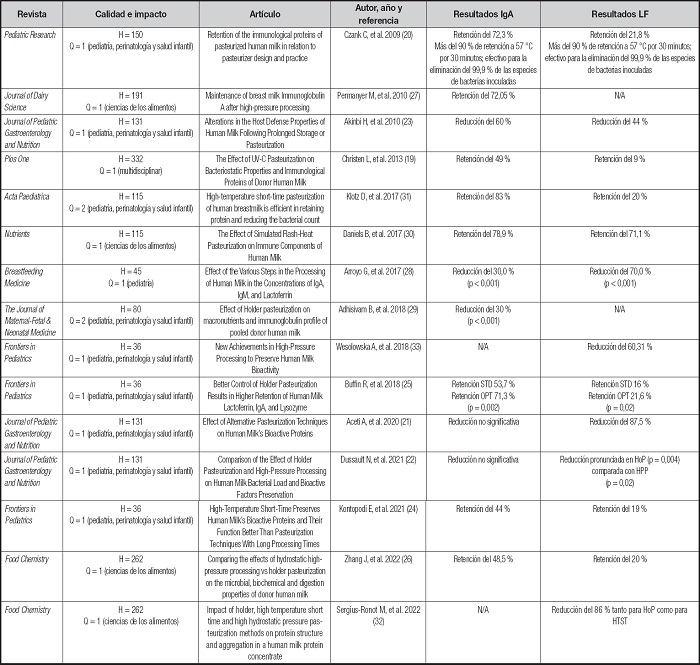
La literatura académica en torno al tema demuestra que el impacto de la pasteurización Holder sobre los niveles de IgA y LF en muestras de leche humana donada es diversa y variable. A continuación se hará una exposición de los hallazgos más importantes encontrados durante la investigación para cada uno de estos biocomponentes. En la tabla I se describen los estudios incluidos en la revisión, sus características y resultados.
INMUNOGLOBULINA-A
Algunos estudios demuestran pérdidas cercanas o superiores al 50 % cuando la leche humana es sometida a pasteurización Holder; al comparar la concentración de esta proteína entre muestras de leche humana pasteurizada y recién extraída, se han evidenciado pérdidas promedio de hasta el 60 % (23). Por otro lado, se ha observado el nivel de retención de IgA es inferior en la pasteurización Holder cuando se la compara con un método de pasteurización mediante radiación ultravioleta (UV-C), siendo este del 49 % y el 89 %, respectivamente (19). También se ha visto que, al ser comparado con un método de pasteurización de alta temperatura y corto lapso (HTST), el protocolo Holder no muestra diferencias significativas en cuanto al nivel de retención de IgA, el cual fue del 44 % (24). Otros investigadores han propuesto la optimización del método Holder mediante la disminución de la temperatura y el tiempo de calentamiento, con lo cual, comparado con el protocolo tradicional, el porcentaje de retención de IgA fue superior en un 17,6 % (25). Adicionalmente, al comparar la pasteurización Holder con un método de alta presión hidrostática (HHP) a 400 MPa, la primera mostró de nuevo menor capacidad de retención de IgA (48,5 %) en relación con el protocolo alternativo (97,8 %) (26).
En contraste con los hallazgos anteriores, otros investigadores reportan que la retención de IgA en la leche humana sometida a pasteurización Holder puede superar el 70 %. Respecto a esto, se ha observado una retención del 72,3 % de esta proteína en la leche humana pasteurizada, pudiendo alcanzar hasta un 90 % con una disminución de la temperatura a 57 °C durante el tiempo estandarizado de 30 minutos (20). Así mismo, una retención del 72 % se evidenció en un estudio que comparó el método Holder con un protocolo de pasteurización hiperbárica (HPP) (27). Por su parte, en los BLH pertenecientes a hospitales de Guatemala e India se ha descrito una reducción del 30 % en las concentraciones de IgA posterior a la pasteurización Holder (28,29). Ahora bien, investigaciones que comparan el método Holder con el protocolo HTST también han generado controversia, ya que algunas demuestran mayor retención de este biocomponente con el método tradicional; en este orden de ideas, un estudio comparó la pasteurización Holder con el método HTST (72 °C durante 15 segundos) y determinó que la primera fue superior al momento de mantener las concentraciones de IgA (30); no obstante, una investigación del 2017 contradice estos resultados, encontrándose un porcentaje de retención del 83 % para la pasteurización Holder y del 95 % para el método HTST (31).
LACTOFERRINA
Con relación a la LF, la literatura indica que el efecto de la pasteurización Holder sobre esta proteína en la leche humana es más pronunciado cuando se lo compara con el impacto sobre la IgA. El porcentaje de retención de la LF se ha visto que puede llegar a ser de apenas el 9 % en muestras sometidas a pasteurización Holder, contrastando el 87 % alcanzado por un método de irradiación mediante UV-C (19). Así mismo, un estudio demostró que tanto la pasteurización Holder como el método HTST generan disminuciones promedio del 87,5 % y el 83,5 %, respectivamente (21). Por otra parte, investigadores observaron que para ambos protocolos, la pérdida correspondió al 86 % (32). Los resultados indican que la pasteurización Holder genera una reducción pronunciada y estadísticamente significativa de esta proteína (p = 0,004) (22).
Los estudios con resultados más prometedores mostraron una retención cercana o superior al 20 %. De esta forma, se ha reportado que la pasteurización Holder retuvo el 19 % del contenido de LF en muestras de leche humana, pudiendo este incrementarse al 26 % mediante la incorporación de un sistema de calentamiento rápido (24). Por su parte, otros estudios encontraron un 20 % de retención de LF posterior a la pasteurización Holder; adicionalmente, no hallaron diferencias significativas en la conservación de esta proteína entre los protocolos Holder y HTST (p = 0,18), y observaron que el tratamiento mediante HHP alcanzó una retención del 86,8 % (26,31). Seguidamente, la evidencia indica que se puede pasar de una conservación promedio de LF del 21,8 % a más del 90 % mediante la disminución de la temperatura a 57 °C (20) o del 16 % al 21,6 % mediante una optimización del control de temperatura y tiempo (25).
Los resultados demuestran que, si bien hay un impacto sobre las concentraciones de LF, este pudiera no ser tan pronunciado. Algunos investigadores han reportado una reducción correspondiente al 70 % (28), mientras que otros observaron una disminución del 60,31 %, demostrando a su vez un mejor porcentaje de retención a partir del tratamiento mediante HPP (33). Otros estudios han encontrado porcentajes de reducción del 44 % en comparación a muestras de leche fresca (23), y niveles de retención de LF de hasta el 71,1 % después de la pasteurización Holder (30).
DISCUSIÓN
A partir de los resultados, es posible afirmar que, para ambos biocomponentes, los porcentajes de reducción como retención son variables; una de las posibles causas puede ser la variedad de protocolos aplicados en centros de investigación y BLH (19), sumado a otros factores como el origen de las muestras, las cuales poseen una carga de factores inmunológicos que son individuales (7). Igualmente, las condiciones de almacenamiento y la diversidad de estuches comerciales y métodos de análisis favorecen dicha variabilidad (34). Durante la revisión de los artículos solo se evidencia el reporte de la temperatura y el tiempo de mantenimiento, mas no un protocolo completo de temperatura con los periodos de calentamiento y enfriamiento, que a su vez dependen del volumen de la muestra, la densidad y la composición de la leche humana, así como del material y grosor del envase (19). Dicho lo anterior, resulta innegable que, en todos los estudios, el método Holder disminuyó de forma significativa las concentraciones de estas proteínas en la leche humana.
El efecto de la pasteurización Holder sobre los biocomponentes revisados puede explicarse a partir del proceso de desnaturalización que se produce, entre otras causas, por la exposición a altas temperaturas (35). De esta forma, la temperatura y el tiempo de la pasteurización Holder, y los procesos previos de congelación y descongelación, generan desnaturalización de las proteínas bioactivas de la leche humana, incluyendo la IgA y la LF, lo que de manera directa reduce la cantidad y la actividad biológica de estas (28,36). La preocupación respecto a la pérdida de las proteínas bioactivas y sus efectos protectores hace buscar alternativas que garanticen la calidad microbiológica de la leche humana donada sin afectar sus propiedades inmunomoduladoras (37). La Academia Americana de Pediatría atribuye a la presencia de estos biocomponentes en la leche un menor riesgo de enterocolitis necrotizante, sepsis y mortalidad, mayor tolerancia a la alimentación y mejor crecimiento y neurodesarrollo (38). En este sentido, el diseño de este protocolo de pasteurización en cuanto a temperatura y tiempo se propuso originalmente teniendo como referente el usado para el procesamiento comercial de la leche de vaca, con el objetivo de destruir microorganismos clave (M. tuberculosis y C. burnetti) (39); algunos autores consideran que este tratamiento pudiera ser excesivo para garantizar la inocuidad de la leche humana. Sobre esto, uno de los estudios incorporados en los resultados observó una reducción del 99,9 % de todas las especies bacterianas inoculadas a muestras de leche humana tratadas a 57 °C por 30 minutos o 62,5 °C por 20 minutos (20); así mismo, existe evidencia que indica que las bacterias patógenas comunes en la leche humana pueden ser eliminadas mediante procesamiento a 62,5 °C por 5 minutos o 56 °C por 15 minutos (39).
Por otro lado, existe un riesgo bien establecido de transmisión de partículas virales madre-hijo por medio de la leche materna para los casos del citomegalovirus (CMV), el virus de la inmunodeficiencia humana (VIH-1) y el virus linfotrópico humano de células T (VLHT tipos 1 y 2), además de otras enfermedades virales (40). Diversos estudios demostraron que la mayoría de los virus potencialmente presentes en la leche humana resultan destruidos a temperaturas entre los 50 y los 60 °C, a excepción del CMV, sobre el cual no existe evidencia de su completa eliminación a temperaturas inferiores a los 62,5 °C o en un tiempo inferior a 30 minutos (39).
Lo anterior explica por qué algunos investigadores proponen modificar el método Holder mediante una disminución de la temperatura o el tiempo, o un mejor control de estas variables a lo largo de todo el procedimiento (20,24,25); esto con el objetivo de mejorar la retención de varios compuestos bioactivos y garantizar la inocuidad del producto. No obstante, y a pesar de sus limitaciones, el método Holder sigue siendo el protocolo predilecto para el tratamiento de la leche humana de donante, que constituye la mejor alternativa para el infante que no tiene acceso a la leche de su propia madre (37,41).
El Comité de Nutrición de la Sociedad Europea de Gastroenterología, Hepatología y Nutrición Pediátrica insiste en la necesidad de continuar con la investigación enfocada a mejorar el procesamiento de la leche en los BLH, particularmente en lo concerniente a los tratamientos por calor (42). De esta forma, se han propuesto alternativas a la pasteurización Holder y se ha descrito su impacto sobre las concentraciones de IgA y LF. El HTST es una de ellas, donde el procesamiento se da a 72 °C por 15 segundos; algunos estudios que aplicaron este método comparándolo con la pasteurización Holder (21,24,30,31) hallaron resultados mixtos en cuanto a la conservación de los biocomponentes de interés, por lo que resulta difícil establecer la superioridad objetiva de un método sobre otro. Ahora bien, otros estudios defienden el hecho de que la pasteurización HTST conserva mejor el perfil proteico de la leche humana, tomando en consideración compuestos bioactivos distintos a la IgA y la LF (43,44); así mismo, es una alternativa que reduciría el tiempo de procesamiento y la fuerza laboral en los BLH, sin afectar la calidad microbiológica final del producto (44).
Otra alternativa es la pasteurización mediante HPP, un proceso en el cual la leche se somete a alta presión hidrostática (300 a 800 MPa) por períodos de hasta 10 minutos con el fin de inactivar los patógenos presentes (45). Los resultados de la revisión evidencian que, comparado con el método Holder, este tratamiento logra niveles de retención de IgA y LF muy superiores (26,27,32,33); por estas características, el método HPP se está aplicando con más frecuencia en la industria alimentaria como alternativa al tratamiento por calor (46); sumado a esto, investigaciones sugieren que esta tecnología pudiera ser más efectiva que la pasteurización para garantizar la inocuidad de los alimentos, y que presiones de 300 a 400 MPa son seguras para la mayoría de los componentes de la leche humana (47). A pesar de sus beneficios, los altos costos de equipo y operación impiden la implementación de este sistema a gran escala, pudiendo ser un 130 % más altos en comparación con la pasteurización Holder (45).
Otras investigaciones han reportado el uso de la pasteurización mediante UV-C, la cual aprovecha las propiedades germinicidas de la radiación UV (39). Para este método se han reportado niveles de retención superiores al 80 % tanto para la IgA como para la LF (19), conservando la actividad de compuestos bioactivos distintos a los mencionados y cumpliendo con los requerimientos de inocuidad de los bancos de leche (48). Específicamente, la irradiación a 254 nm se ha investigado como lternativa a la pasteurización Holder, demostrando una mejor conservación de la IgA, la LF y la lisozima, así como la inactivación del CMV, un patógeno común en la leche materna (49). Sin embargo, también se han reportado limitaciones para su implementación en la industria de alimentos, dada la escasa profundidad de penetración de este tipo de radiación en los alimentos líquidos con una alta absorbancia de rayos UV y gran cantidad de partículas suspendidas (50). Entonces, para que la luz UV-C se absorba de manera efectiva por la leche humana, debe ser presentada al sistema en una fina capa (39), y se requieren dosis más altas de irradiación dependiendo de los sólidos totales de la muestra de leche (48).
Por último, se ha estudiado el procesamiento ultrasónico de 20 a 100 kHz, el cual es una tecnología que se fundamenta en la generación de cavitación inercial; esta consiste en la formación de burbujas microscópicas que colapsan, produciendo ondas de choque y puntos de calor de aproximadamente 5000 °C y presiones de 50 MPa con una duración de microsegundos (51). Se ha evidenciado que el procesamiento ultrasónico es más efectivo en la eliminación de microorganismos patógenos cuando se combina con el tratamiento por calor; este método, conocido como pasteurización termoultrasónica, conduce a retenciones de IgA y LF del 91 % y 77 %, respectivamente (52), porcentajes superiores a los observados a partir de la pasteurización Holder en esta revisión.
CONCLUSIONES
La evidencia científica demuestra que el procesamiento de la leche humana donada mediante pasteurización Holder acarrea un impacto significativo sobre las concentraciones de IgA y LF, pero la magnitud de este fenómeno es difícil de cuantificar con precisión por la heterogeneidad de los protocolos de investigación entre los diferentes estudios. Por ello se han venido desarrollando otras alternativas, como HTST, HPP, radiación UV-C y termoultrasónica, cada una demostrando potenciales ventajas sobre el método Holder pero con un mayor costo para su implementación. En general, y teniendo en cuenta sus limitaciones, la pasteurización Holder es un método costo-efectivo que garantiza la calidad microbiológica de la leche humana donada, la cual, aun después de su procesamiento, demuestra propiedades beneficiosas para la salud del infante, razón por la que hoy día sigue siendo el principal método de tratamiento en los BLH.