Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Avances en Odontoestomatología
versión On-line ISSN 2340-3152versión impresa ISSN 0213-1285
Av Odontoestomatol vol.32 no.5 Madrid sep./oct. 2016
Implicaciones moleculares del Factor de crecimiento Transformante Beta (TGF-β) en el desarrollo de las fisuras labiopalatinas
Molecular implications of transforming growth factor beta (TGF-β) signaling pathway in the development of cleft lip and palate
Madera Anaya M.V.*, Moneriz Pretell C.E.** y Suárez Causado A.***
* Odontólogo. Magíster en Bioquímica. Universidad de Cartagena. Magíster en Epidemiología Clínica. Universidad de la Frontera.
** Químico Farmacéutico. Doctor en Bioquímica y Biología Molecular. Docente Universidad de Cartagena, Colombia.
*** Química Farmacéutica. Doctora en Bioquímica y Biología Molecular. Docente Universidad de Cartagena, Colombia.
Dirección para correspondencia
RESUMEN
Las fisuras labio palatinas se generan por la falta de fusión de los tejidos del labio o del paladar durante las primeras etapas del desarrollo fetal, estas se encuentran entre los defectos congénitos más comunes causados por el desarrollo facial anormal durante la gestación; su etiología no se encuentra totalmente aclarada, sin embargo se intenta explicar por medio del modelo de umbral multifactorial, planteándose que es producto de la interacción de factores endógenos y exógenos, entre los endógenos se han reportado alteraciones en la señalización del TGF-β, el cual está involucrado en el desarrollo embrionario, diferenciación celular y en la regulación del desarrollo del paladar. En esta revisión se muestran los recientes avances sobre las implicaciones moleculares de la vía de señalización TGF-β en el desarrollo de las fisuras labio palatinas.
Palabras clave: Desarrollo del paladar, fisuras labio palatinas, TGF-β, vías de señalización celular.
SUMMARY
Cleft lip and palate are generated by the lack of fusion of the tissues of the lip or palate during early fetal development, these are among the most common birth defects caused by abnormal facial development during gestation. The etiology of these cracks is not fully elucidated, however attempts to explain by means of multifactorial threshold model, considering that is the product of the interaction of endogenous and exogenous factors, endogenous alterations have been reported in TGF-β signaling, which is involved in embryonic development, cell differentiation and in the regulation of development of the palate. In this review, the recent advances implications of the molecular signaling pathway TGF-β in the development of cleft lip and palate shown.
Key words: Development palate, cleft lip and palate, TGF-β, cell signaling pathways.
Introducción
Las fisuras labio palatinas (FLP) se generan por la falta de fusión de los tejidos del labio o del paladar durante el desarrollo fetal, se encuentran entre las deformidades cráneo faciales más frecuentes y hacen parte de los defectos congénitos más comunes generados en el desarrollo facial (1-3); constituyéndose en uno de los principales problemas morfológicos, funcionales y estéticos; afectando la masticación, deglución, amamantamiento, digestión, habla, audición, la ventilación del oído medio y el desarrollo a nivel social (3-5); estos pacientes requieren cuidados desde su nacimiento hasta la adultez de muchas disciplinas incluyendo, cirugía plástica, cirugía maxilofacial, otorrinolaringología, fonoaudiología, enfermería, psicología, consejería genética y odontología (6-11).
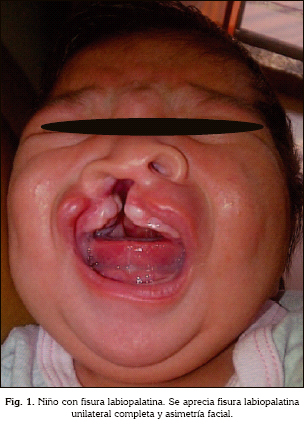
Clínicamente las fisuras se clasifican en labiales y del paladar; la fisura labial se considera una anormalidad congénita del paladar primario; esta puede ser: completa, incompleta, unilateral o bilateral, y puede implicar una fisura palatina (12,13) (Figura 1). Las fisuras palatinas, denominadas regularmente como paladar hendido, se clasifican en cuatro categorías:
- Completa con fisura de labio.
- Fisura del paladar primario, en el cual la hendidura está limitada a la fosa incisiva anterior y puede o no involucrar fisura de labio.
- Fisura del paladar secundario, en donde el defecto es limitado a la fosa incisiva posterior, y
- Fisura submucosa que puede incluir una úvula bífida (14).
Aproximadamente el 70% de todas las fisuras orofaciales son no sindrómicas, mientras que el 30% restante se presentan en compañía de síndromes, entre estos, los síndromes de Pai, Van der Woude y Smith-Lemli-Opitz (15,16).
La incidencia a nivel mundial de la fisuras orofaciales es aproximadamente 1 a 2 por 1.000 nacidos vivos, esta frecuencia cambia en relación al origen étnico, el área geografía y a la naturaleza propia de la fisura (17,18). En el contexto de las fisuras labiales extendidas a paladar, la incidencia es aproximadamente 0,3 por cada 1.000 nacidos en poblaciones afroamericanas, de 1,0 por cada 1.000 en poblaciones caucásicas y de 2,1 por cada 1.000 en poblaciones asiáticas; las fisuras unilaterales son nueve veces más comunes que las fisuras bilaterales y los hombres son en su mayoría más afectados por fisuras labiales en una relación de 2:1 respecto a las mujeres; mientras que estas son más afectadas por fisuras palatinas (19-21). En Colombia, este tipo de malformaciones se presenta con una frecuencia de 1 por 1.000 nacidos vivos y según el Tercer Estudio Nacional de Salud Bucal (ENSAB III) se reportó una prevalencia tanto de labio como de paladar fisurado de 0,2% (22,23).
La etiología de estas fisuras no se encuentra totalmente aclarada, sin embargo se intenta explicar por medio del modelo de umbral multifactorial, planteándose que es producto de la interacción de factores endógenos y ambientales; entre los cuales están la etnia, variaciones geográficas, desordenes genéticos, aberraciones cromosómicas y exposición a teratógenos como el alcohol, tabaco, anticonvulsivantes y metales pesados; lo que sugiere que múltiples genes y factores ambientales esta involucrados en su desarrollo (24-28).
En el presente trabajo de revisión, se muestran las principales implicaciones moleculares de la vía de señalización del Factor de Crecimiento Transformante Beta (TGF-β) en el desarrollo de las fisuras labio palatinas.
Vía de señalización TGF-β
Los miembros de la familia del TGF-β son codificados por 33 genes que traducen polipéptidos estructuralmente relacionados que corresponden a los precursores de los ligandos, estos están compuesto por un propéptido de gran tamaño y un polipéptido maduro C-terminal que se produce por clivado de su precursor (29,30). Los ligandos de la familia del TGF-β son homodímeros o heterodímeros del polipéptido C-terminal unidos por enlaces disulfuros, estos incluyen TGF-β, activinas, BMP (proteínas morfogenéticas óseas), Nodal y GDFs (factores de crecimiento y diferenciación) (31-33). El TGF-β es secretado en forma de complejo junto con otras proteínas que evitan la unión del ligando al receptor; este complejo de TGF-β latente es activado y liberado por clivaje proteolítico del propéptido (30). La vía TGF-β estimula varias redes de señalización involucradas en la determinación, crecimiento y diferenciación celular; además algunos de sus miembros pueden inhibir el crecimiento e inducir apoptosis en un gran número de tipos de células, especialmente células epiteliales (34-36).
La señalización mediada por los ligandos del TGF-β es traducida a través de un complejo de receptores celulares de superficie entre los que se destacan el TβRI (receptor beta tipo I) y el TβRII (receptor beta tipo II), que tienen actividad proteína quinasa en su dominio citoplasmático y forman heterodímeros para ser activos (37,38). Además se ha reportado la existencia del TβRIII (receptor beta tipo III), este contribuye a mejorar la afinidad del TβRII por los respectivos ligandos. En mamíferos, existen siete receptores tipo I (ALK-1-7) y cinco receptores tipo II, por lo tanto, una gran variedad de combinaciones heteroméricas han sido reportadas. La unión del ligando estabiliza la formación de un complejo receptor tetramérico, constituido por un par de receptores tipo I y un par de receptores tipo II, en el cual los receptores tipo II con su respectiva actividad quinasa fosforila a los tipo I. El receptor II tiene una actividad quinasa constitutiva. La unión del TGF-β al TβRII es reconocida por el receptor TβRI, uniéndose a él para formar un complejo. A continuación, el receptor TβRI es fosforilado por el TβRII, lo que estimula su actividad serina-treonina quinasa, con la subsiguiente fosforilación de distintas proteínas que actúan como efectores intracelulares; a partir de este punto existen dos vías por las cuales los miembros de la familia del TGF-β pueden desencadenar la respuesta celular, están son la vías de señalización dependiente de proteínas Smad y la independiente de proteínas Smad (Figura 2).
Vía de señalización TGF-β Dependiente de SMAD
Luego de la fosforilación del receptor TβRI, este fosforila a miembros de la familia de proteínas efectoras Smad, específicamente las Smad 2 y 3, estas proteínas fosforiladas se unen a otro miembro de la familia, el Smad 4 y como resultado, se produce su translocación al núcleo, donde interacciona de forma célula específica con otros factores de transcripción, para finalmente regular la expresión génica. Una de las principales consecuencias de la unión de TGF-β a sus receptores es su capacidad de inhibir el crecimiento y regular diferenciación y muerte celular. Se ha demostrado que el TGF-β inhibe las actividades de los complejos ciclina D-Cdk4/6 y ciclina E/Cdk2 (reguladores del ciclo celular), lo que conduce a la hipofosforilación de p-Retinoblastoma y a una disminución de la actividad transcripcional de E2Fs. En definitiva, se produce la detención del ciclo celular. Estos efectos inhibidores se han asociado con la capacidad del TGF-β de aumentar la expresión de los inhibidores de ciclinas (CKIs) p15Ink4B, p21Cip1 y p27Kip1.
Vía de señalización TGF-β Independiente de SMAD
El TGF-β también activa otras cascadas de señalización independiente de Smad, estas incluyen MAPK tales como ERK, JNK (c-Jun-N-terminal quinasa) y p38 (39), se ha sugerido que TGF-β es capaz de inducir apoptosis mediante la producción de especies reactivas de oxígeno o activando las rutas JNK o de DAP quinasa (DAPK: Proteína quinasa asociada a muerte), así como interfiriendo con algunas rutas de supervivencia (como la fosfatidilinositol-3-quinasa, PI3-K), activando finalmente la ruta mitocondrial de la apoptosis (40,41) (Figura 2).
Desarrollo del paladar
La formación completa del paladar logra la separación de la cavidad bucal y nasal. Este es un proceso complejo que incluye múltiples eventos, entre estos crecimiento, elevación y fusión del paladar. En humanos el desarrollo del paladar se realiza a partir de dos primordios, que luego forman el paladar primario y el secundario. El paladar primario representa únicamente una pequeña porción del paladar duro en adultos, el paladar secundario contribuye al desarrollo del paladar duro y partes del paladar blando. El paladar inicia su formación a partir de la sexta semana de vida intrauterina; inicialmente los procesos palatinos son posicionados verticalmente a cada lado de la lengua, luego como resultado del crecimiento de la mandíbula y el descenso de la lengua, el paladar se reorienta adoptando una posición horizontal, se expande y fusiona. En el paladar duro, las células mesenquimales son reemplazadas por formación de hueso intramembranoso; en contraste la parte posterior del paladar secundario, la cual constituye el paladar blando, no sufre el proceso de osificación. La fusión de paladar es marcada por el rafe palatino medio (42).
Las estructuras del paladar son formadas por células del ectomesénquima derivadas de las células de la cresta neural craneal, células derivadas del mesodermo y células epiteliales derivadas del ectodermo faríngeo (42). El epitelio que recubre el paladar está regionalmente dividido en oral, nasal y medial. El epitelio nasal es escamoso y el epitelio oral es seudoestratificado, mientras que el medial proviene de una fusión de linajes celulares como células apoptóticas, de migración y la transformación del epitelio mesénquima (43,44).
Las interacciones epitelio mesénquima involucradas en la formación de paladar son reguladas por dos grandes grupos de genes. El primero de ellos está conformado por factores de transcripción también llamados genes maestros entre estos los genes de la familia Homeobox son los más importantes. Estos genes se han conservado evolutivamente, lo que se evidencia en la similitud de sus secuencias y en la función que desempeñan en diferentes especies (29). En el ser humano y otros mamíferos, como el ratón, existen 38 genes dentro de cuatro clústeres, cada uno ubicado en distinto cromosoma. La mayoría de los genes involucrados en desarrollo craneofacial no se encuentran en estos clústeres, sin embargo poseen un homeodominio, que es la región que se une al promotor de los genes blanco para regular su transcripción ya sea activándola o inhibiéndola (32).
TGF-β en el desarrollo de las fisuras labiopalatinas
Para la etiología de las fisuras palatinas no sindrómicas diversos autores reportan que algunos genes como MSX1, IRF6, GABA, TGF-β, muestran gran susceptibilidad para riesgo de fisuras bucales (45-47).
Con relación a los genes de TGF-β, estos codifican para 3 isoformas de TGF-β altamente conservadas entre las especies, teniendo secuencias idénticas de pares de bases aproximadamente en un 75% y similares señales a través del factor de transcripción Smads; sin embargo los fenotipos resultantes de los knockout de estos mamíferos con las diferentes isoformas, son muy distintos, lo que indica que los ligandos tienen actividades específicas que no pueden ser compensados por otros miembros de la familia.
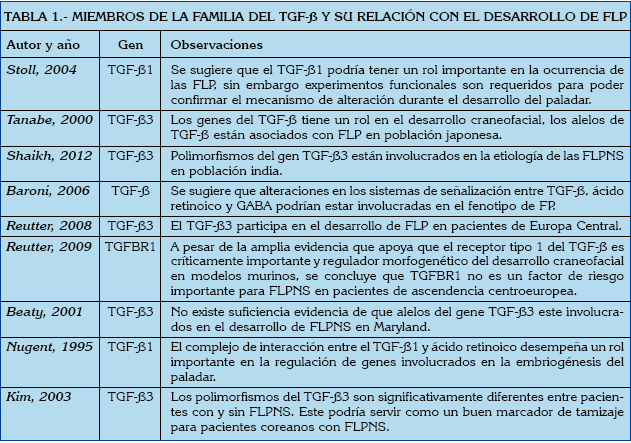
Se ha reportado que alteraciones en los miembros de la familia del TGF-β durante el desarrollo del paladar podrían estar asociadas con la etiología de las fisuras labio palatinas (Tabla 1). Asimismo, se ha sugerido que la inhibición del TGF-β1 y TGF-β2 no afectan la transformación epitelio mesénquima en el paladar de ratón; el ratón knockout para TGF-β1 muere antes de los 11 días de gestación y el del TGF-β2 tiene defectos en la mandíbula y el maxilar superior; de estos, sólo el 23% corresponden a fisuras palatinas. El TGF-β1 y 3 son epiteliales, este último puede ser detectado en el epitelio de los procesos palatinos desde los inicios y persiste hasta que el epitelio desaparece, por su parte el TGF-β2 se expresa en el mesénquima (19).
La presencia del TGF-β3 es fundamental para la fusión del paladar secundario en humanos; sin embargo, en algunos animales, como el pollo y el ratón, ningún TGF-β está presente en la lámina epitelial labial, ni es capaz de experimentar transformación epitelio mesénquima (41); posiblemente, en este caso, actúan otros factores presentes en el epitelio, como el factor de transcripción Shh, cuya función es regular el crecimiento de los procesos maxilares, nasales y su neutralización.
TGF-β3 tiene la función más importante en la fusión palatina y en la transformación epitelio mesénquima, mientras que TGF-β2 estimula la síntesis de ADN y la proliferación en el mesénquima, desde las etapas tempranas del desarrollo del paladar; por otro lado el TGF-β1 es un potente inductor de apoptosis. Asimismo, el TGF-β3 estimula la fosforilación del factor de transcripción Smad-2 a través de un receptor específico y una vez fosforilado, entra al núcleo para regular positivamente la síntesis y activación del factor de transcripción LEF-1, este factor es necesario para la activación de algunos genes involucrados en la transformación epitelio mesénquima, como Snail que reprime la expresión de caderina-E (20,34). Adicionalmente se ha reportado que el ratón knockout para TGF-β3 no desarrolla fisura labial y que sus alteraciones están relacionadas únicamente con fisuras del paladar secundario (24,43); por lo tanto, se podría pensar que la presencia de fisuras labiopalatinas completas no son generadas por alteraciones de un solo gen sino que involucra una serie compleja de eventos en donde intervienen factores genéticos y epigenéticos.
Conclusión
El desarrollo y formación del paladar primario y secundario es guiado por procesos de diferenciación, crecimiento y proliferación celular, en donde participan varios genes incluyendo al TGF-β; por lo cual se sugiere que alteraciones moleculares en la vía de señalización del TGF-β posiblemente están involucradas en el desarrollo de las fisuras labiopalatinas.
Bibliografía
1. Berbert-Campos C. Legal considerations in the management of cleft lip and palate. Cleft Palate Craniofac J 2007;44(2):223-5. [ Links ]
2. Chen JL, Messner AH, Curtin G. Newborn hearing screening in infants with cleft palates. Otol Neurotol 2008;29(6):812-5. [ Links ]
3. Cooper-Brown L, Copeland S, Dailey S, Downey D, Petersen MC, Stimson C, et al. Feeding and swallowing dysfunction in genetic syndromes. Dev Disabil Res Rev 2008;14(2):147-57. [ Links ]
4. Goudy S, Lott D, Canady J, Smith RJ. Conductive hearing loss and otopathology in cleft palate patients. Otolaryngol Head Neck Surg 2006;134(6):946-8. [ Links ]
5. Millar K, Bell A, Bowman A, Brown D, Lo TW, Siebert P, et al. Psychological status as a function of residual scarring and facial asymmetry after surgical repair of cleft lip and palate. Cleft Palate Craniofac J 2013;50 (2):150-7. [ Links ]
6. De Bodt M, Van Lierde K. Cleft palate speech and velopharyngeal dysfunction: the approach of the speech therapist. B-ENT 2006;2 Suppl 4:63-70. [ Links ]
7. Prahl-Andersen B, Ju Q. Quality improvement of cleft lip and palate treatment. Angle Orthod 2006;76(2): 265-8. [ Links ]
8. Arosarena OA. Cleft lip and palate. Otolaryngol Clin North Am 2007;40(1):27-60, vi. [ Links ]
9. Aminpour S, Tollefson TT. Recent advances in presurgical molding in cleft lip and palate. Curr Opin Otolaryngol Head Neck Surg 2008;16(4): 339-46. [ Links ]
10. Costello BJ, Ruiz RL. Unilateral cleft lip and nasal repair: the rotation-advancement flap technique. Atlas Oral Maxillofac Surg Clin North Am 2009;17(2):103-16. [ Links ]
11. Costello BJ, Edwards SP, Clemens M. Fetal diagnosis and treatment of craniomaxillofacial anomalies. J Oral Maxillofac Surg 2008;66(10):1985-95. [ Links ]
12. Doucet JC, Delestan C, Montoya P, Matei L, Bigorre M, Herlin C, et al. New Neonatal Classification of Unilateral Cleft Lip and Palate Part 2: To Predict Permanent Lateral Incisor Agenesis and Maxillary Growth. Cleft Palate Craniofac J 2013. [ Links ]
13. Rossell-Perry P, Gavino-Gutierrez AM. Asymmetric bilateral cleft lip: classification and a surgical technique. J Craniofac Surg 2012;23(5):1367-72. [ Links ]
14. Chai Y, Maxson RE, Jr. Recent advances in craniofacial morphogenesis. Dev Dyn 2006;235(9):2353-75. [ Links ]
15. Ocak Z, Yazicioglu HF, Aygun M, Ilter MK, Ozlu T. Prenatal detection of Pai syndrome without cleft lip and palate: a case report. Genet Couns 2013;24(1):1-5. [ Links ]
16. Jugessur A, Farlie PG, Kilpatrick N. The genetics of isolated orofacial clefts: from genotypes to subphenotypes. Oral Dis 2009;15(7):437-53. [ Links ]
17. Mossey PA, Little J, Munger RG, Dixon MJ, Shaw WC. Cleft lip and palate. Lancet 2009;374(9703):1773-85. [ Links ]
18. Wong FK, Hagg U. An update on the aetiology of orofacial clefts. Hong Kong Med J 2004;10(5):331-6. [ Links ]
19. Hussein EA, Borno HT, Dudin A, van Aalst JA. Incidence of Cleft Lip and Palate in the Palestinian Territories: A Retrospective Study From the Makassed Hospital Neonatal Unit. Cleft Palate Craniofac J 2013. [ Links ]
20. Ajike SO, Adebola RA, Efunkoya A, Adeoye J, Akitoye O, Veror N. Epidemiology of adult cleft patients in North-western Nigeria: our experience. Ann Afr Med 2013;12(1):11-5. [ Links ]
21. Bell JC, Raynes-Greenow C, Bower C, Turner RM, Roberts CL, Nassar N. Descriptive epidemiology of cleft lip and cleft palate in Western Australia. Birth Defects Res A Clin Mol Teratol 2013;97 (2):101-8. [ Links ]
22. Chavarriaga J, González M, Rocha A, Posada A, A A. Factores relacionados con la prevalencia de Labio y Paladar Hendido en la población atendida en el Hospital Infantil "Los Ángeles". Municipio de Pasto (Colombia), 2003-2008. Revista CES Odontología 2011; 24(2):33-41. [ Links ]
23. Colombia Rd. Tercer Estudio Nacional de Salud Bucal (ENSAB III) In; 1998. [ Links ]
24. Cobourne MT. The complex genetics of cleft lip and palate. Eur J Orthod 2004;26(1):7-16. [ Links ]
25. Little J, Cardy A, Munger RG. Tobacco smoking and oral clefts: a meta-analysis. Bull World Health Organ 2004;82(3):213-8. [ Links ]
26. Lidral AC, Moreno LM, Bullard SA. Genetic Factors and Orofacial Clefting. Semin Orthod 2008;14(2):103-114. [ Links ]
27. Scapoli L, Martinelli M, Arlotti M, Palmieri A, Masiero E, Pezzetti F, et al. Genes causing clefting syndromes as candidates for non-syndromic cleft lip with or without cleft palate: a family-based association study. Eur J Oral Sci 2008;116(6): 507-11. [ Links ]
28. Meng L, Bian Z, Torensma R, Von den Hoff JW. Biological mechanisms in palatogenesis and cleft palate. J Dent Res 2009;88(1):22-33. [ Links ]
29. Mazzieri R, Jurukovski V, Obata H, Sung J, Platt A, Annes E, et al. Expression of truncated latent TGF-beta-binding protein modulates TGF-beta signaling. J Cell Sci 2005;118(Pt 10):2177-87. [ Links ]
30. Annes JP, Chen Y, Munger JS, Rifkin DB. Integrin alphaVbeta6-mediated activation of latent TGF-beta requires the latent TGF-beta binding protein-1. J Cell Biol 2004;165(5):723-34. [ Links ]
31. Derynck R, Zhang YE. Smad-dependent and Smad-independent pathways in TGF-beta family signalling. Nature 2003;425(6958):577-84. [ Links ]
32. Chen Y, Dabovic B, Annes JP, Rifkin DB. Latent TGF-beta binding protein-3 (LTBP-3) requires binding to TGF-beta for secretion. FEBS Lett 2002;517(1-3): 277-80. [ Links ]
33. Sakaki-Yumoto M, Katsuno Y, Derynck R. TGF-beta family signaling in stem cells. Biochim Biophys Acta 2013;1830(2):2280-96. [ Links ]
34. Massague J, Wotton D. Transcriptional control by the TGF-beta/Smad signaling system. EMBO J 2000; 19(8):1745-54. [ Links ]
35. Shen MM. Nodal signaling: developmental roles and regulation. Development 2007;134(6):1023-34. [ Links ]
36. Kruithof-de Julio M, Alvarez MJ, Galli A, Chu J, Price SM, Califano A, et al. Regulation of extra-embryonic endoderm stem cell differentiation by Nodal and Cripto signaling. Development 2011;138(18):3885-95. [ Links ]
37. Tsai VW, Macia L, Johnen H, Kuffner T, Manadhar R, Jorgensen SB, et al. TGF-b superfamily cytokine MIC-1/GDF15 is a physiological appetite and body weight regulator. PLoS One 2013;8(2): e55174. [ Links ]
38. Andrieux G, Fattet L, Le Borgne M, Rimokh R, Theret N. Dynamic regulation of Tgf-B signaling by Tif1gamma: a computational approach. PLoS One 2012;7(3):e33761. [ Links ]
39. Kang JS, Liu C, Derynck R. New regulatory mechanisms of TGF-beta receptor function. Trends Cell Biol 2009;19(8):385-94. [ Links ]
40. Qian X, Jin L, Lloyd RV. TGF-B and Estrogen Regulate P27 (Kip1) and Cyclin D (1) in Normal and Neoplastic Rat Pituitary Cells. Endocr Pathol 1997;8(3):241-50. [ Links ]
41. Yang G, Yang X. Roles of TGF-b superfamily in the genesis, development and maintenance of cartilage. Yi Chuan 2008;30(8):953-9. [ Links ]
42. Ito Y, Yeo JY, Chytil A, Han J, Bringas P, Jr., Nakajima A, et al. Conditional inactivation of Tgfbr2 in cranial neural crest causes cleft palate and calvaria defects. Development 2003;130 (21):5269-80. [ Links ]
43. Martínez-Álvarez C, Tudela C, Pérez-Miguelsanz J, O'Kane S, Puerta J, Ferguson MW. Medial edge epithelial cell fate during palatal fusion. Dev Biol 2000; 220(2):343-57. [ Links ]
44. Shuler CF, Halpern DE, Guo Y, Sank AC. Medial edge epithelium fate traced by cell lineage analysis during epithelial-mesenchymal transformation in vivo. Dev Biol 1992;154(2): 318-30. [ Links ]
45. Lidral AC, Murray JC, Buetow KH, Basart AM, Schearer H, Shiang R, et al. Studies of the candidate genes TGFB2, MSX1, TGFA, and TGFB3 in the etiology of cleft lip and palate in the Philippines. Cleft Palate Craniofac J 1997;34(1):1-6. [ Links ]
46. Zucchero TM, Cooper ME, Maher BS, Daack-Hirsch S, Nepomuceno B, Ribeiro L, et al. Interferon regulatory factor 6 (IRF6) gene variants and the risk of isolated cleft lip or palate. N Engl J Med 2004; 351(8):769-80. [ Links ]
47. Filezio MR, Bagordakis E, de Aquino SN, Pereira Messetti AC, Martelli-Junior H, Swerts MS, et al. Polymorphisms in GABRB3 and oral clefting in the Brazilian population. DNA Cell Biol 2013;32(3): 125-9. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Amileth Suárez Causado
Universidad de Cartagena
Campus de la Salud. Zaragocilla
Facultad de Medicina
Departamento de Ciencias Básicas
Unidad de bioquímica
Correo electrónico: asuarezc1@unicartagena.edu.co
Fecha de recepción: 27 de abril de 2015
Aceptado para publicación: 1 de mayo de 2016