Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO  Similares em Google
Similares em Google
Compartilhar
Archivos de la Sociedad Española de Oftalmología
versão impressa ISSN 0365-6691
Arch Soc Esp Oftalmol vol.78 no.11 Nov. 2003
ARTÍCULO ORIGINAL
INTERFERÓN-ALFA Y HEMANGIOMAS ORBITARIOS INFANTILES
INTERFERON ALPHA AND INFANTILE ORBITAL HEMANGIOMA
DAMAS MATEACHE B1, MENÉNDEZ SUSO JJ2, ABELAIRAS GÓMEZ JM3,
ALBAJARA VELASCO L2, PERALTA CALVO J3, VERDÚ SÁNCHEZ C2, ROYO OREJAS A4
| RESUMEN Objetivo: Estudiar la eficacia y seguridad de la terapia con interferón-alfa en el tratamiento de los hemangiomas infantiles con afectación orbitopalpebral y compromiso visual. Palabras clave: Interferón alfa, hemangioma, hemangioma orbitario, hemangiomas infancia, diplejia espástica. | SUMMARY Objective: To determine the efficacy and safety of interferon alpha therapy for the treatment of infantile periorbital hemangiomas associated with visual impairment. Key words: Interferon alpha, hemangioma, orbital hemangioma, infantile hemangioma, spastic diplegia. |
Recibido:28/1/03. Aceptado: 15/10/03.
Servicios de Oftalmología y Pediatria General del Hospital Universitario La Paz. Madrid. España.
1 Licenciada en Medicina. Servicio de Oftalmología.
2 Licenciado en Medicina. Servicio de Pediatría.
3 Doctor en Medicina. Servicio de Oftalmología.
4 Licenciada en Medicina. Servicio de Radiología.
Los autores no han recibido apoyo económico alguno para la realización de este trabajo y no tienen ningún interés comercial en el producto.
Correspondencia:
B. Damas Mateache
Ctra. del Plantio, 98, 1.º B
28220 Majadahonda (Madrid)
España
INTRODUCCIÓN
El hemangioma es un tumor benigno del endotelio vascular. Se trata del tumor de partes blandas más frecuente en la infancia, con una incidencia de 5-10% al año de edad (1). Es más frecuente en la raza caucasiana, en el sexo femenino (3:1) (2), y en los prematuros (22%) (1).
Aproximadamente el 55% está presente al nacimiento, y el resto aparece a las 4-8 semanas (3). Son más frecuentes en el área de cabeza y cuello (60%) (3).
En general, durante los 6-12 primeros meses de vida, acontece una fase proliferativa, en la que la lesión aumenta de tamaño. Posteriormente, y tras un período variable de estabilización, sucede una segunda fase de involución, en la que disminuye progresivamente de tamaño (el 70% han desaparecido a los 7 años) (4). Por ello, en muchos, no es necesario el tratamiento. Aunque se decida no intervenir en la historia natural del tumor, sí es importante, en todos los casos el tratamiento de las alteraciones de la refracción con lentes correctoras y, de la ambliopía, mediante parches.
Con la inyección intralesional de corticoides se obtienen buenos resultados (2). Cuando ésta no se puede realizar, fundamentalmente porque el hemangioma sea de difícil acceso, los corticoides sistémicos constituyen una opción, ya que, hasta en un 30%, consiguen alterar la evolución natural, reduciendo significativamente el tamaño de la lesión (5,6).
La cirugía suele reservarse para casos refractarios al tratamiento médico. La radioterapia y embolización son opciones actualmente en desuso.
Con el objetivo de conseguir mejores resultados y, de evitar los efectos secundarios de la terapia corticoidea, nuevas alternativas terapéuticas se han desarrollado en los últimos años. De todas ellas, es el interferón alfa-2, una molécula con propiedades antiangiogénicas, sobre el que recaen las mayores esperanzas.
Desde que en 1989 se usara por primera vez con éxito, muchos han sido los artículos que se han publicado describiendo su eficacia en el tratamiento de los hemangiomas infantiles (7-10). Sin embargo, apenas existen artículos en los que específicamente se describan los efectos sobre los hemangiomas con componente orbitario (11-14). En este estudio, se recoge nuestra experiencia con interferón alfa en el tratamiento de los hemangiomas orbitarios infantiles. Se estudia la eficacia del mismo y, la aparición de efectos secundarios atribuibles al tratamiento.
SUJETOS, MATERIAL Y MÉTODO
Estudio retrospectivo de 4 pacientes con hemangioma orbitario. El diagnóstico se realizó entre los años 2000 y 2002, en nuestro Centro, mediante la exploración física y pruebas de imagen. Se definió el grado de afectación orbitaria con ecografía, eco-Doppler, TC y RM. La respuesta al tratamiento se evaluó mediante la medición de la lesión por métodos de imagen (ecografía, TC y RM) en determinaciones sucesivas.
Los 4 pacientes estudiados eran niñas, nacidas a término y de raza blanca. La edad media en el momento del diagnóstico, y al comienzo del tratamiento con interferón alfa fue de 2,6 meses (0,6-4 meses) y, 5,6 meses (2,5-12 meses), respectivamente. El tiempo durante el cual estuvieron recibiendo inyecciones diarias subcutáneas de interferón fue de 5,5 meses (3,5-8 meses). Actualmente, todos los pacientes descritos en este artículo, han acabado el tratamiento. Una de las niñas había recibido corticoides sistémicos (2 mg/kg/día) previamente, durante un período de 5 meses, sin objetivar una respuesta significativa.

Fig. 1. Uno de los pacientes del estudio en el que se aprecia
proptosis del globo ocular izquierdo secundaria a
hemangioma orbitario.

Fig. 2. El mismo paciente de la figura 1 tras finalizar el
tratamiento con interferón alfa.
La evaluación inicial previa al tratamiento, además de una anamnesis y examen físico incluyó un análisis con hemograma y bioquímica completa (con urea y creatinina) y, pruebas de función hepática con transaminasas.
A cada paciente se le administró interferón alfa-2b a dosis de 3 millones de unidades por metro cuadrado de superficie corporal, desde el principio del tratamiento, en una inyección diaria subcutánea, durante un período de tiempo variable (mínimo 4 meses). La dosis acumulativa media fue de 190,5 millones de unidades.
El tratamiento se consideró eficaz cuando se objetivaron reducciones mayores del 50% con respecto al tamaño inicial de la lesión. Se definió como respuesta completa, la reducción mayor del 90% y, parcial entre el 50 y 90%.
Se decidió intervenir en la evolución natural en aquellas que presentaban una o más de las siguientes complicaciones posibles en los hemangiomas orbitarios: obstrucción total o parcial del eje visual, lagoftalmos, anisometropía mayor de 3 dioptrías y neuropatía óptica por compresión. Indicaciones relativas de tratamiento serían: estrabismo, anisometropía menor de 3 dioptrías y cosmética.
Una vez iniciado el tratamiento, las revisiones fueron mensuales durante los 2 primeros meses. En cada una de ellas se realizaron nuevos controles químicos, analíticos y radiológicos, y si en éstas no se detectaron alteraciones, las posteriores fueron cada 3-4 meses. Tras finalizar el tratamiento, todos los pacientes siguieron revisiones periódicas con el fin de descartar el rebrote de las lesiones y la aparición de efectos secundarios tardíos de la medicación.
RESULTADOS
Las características clínicas y terapéuticas junto con la evolución de cada paciente se resumen en la tabla I.
En los 4 pacientes de nuestro estudio el tratamiento con el interferón alfa 2b fue eficaz. Se observaron respuestas completas en 3 casos y respuesta parcial en el restante.
Sólo en uno de los pacientes se detectó astigmatismo atribuible al hemangioma que se resolvió con el tratamiento.
En todos los pacientes se detectó fiebre moderada (38-38,5ºC) durante los primeros días de la administración del fármaco, que fue controlada satisfactoriamente con paracetamol. En todos los casos se detectó un incremento de los niveles de transaminasas en las primeras semanas de la administración del fármaco, sin repercusión clínica, que no requirieron la suspensión del tratamiento. En todos ellos dichos niveles se normalizaron pocas semanas después.
En un paciente se detectó una elevación significativa de los niveles de colesterol (248 mg/dl) y, especialmente, de triglicéridos (539 mg/dl, 2 veces por encima del límite superior de la normalidad) a los 1,5 meses del inicio del tratamiento. Desde entonces, y hasta cumplir los 4 meses de tratamiento, se observó una disminución progresiva de estos valores. Actualmente, un mes después de suspender el interferón persiste una hipertrigliceridemia (377 mg/dl) a expensas de la fracción VLDL (34%) con una disminución llamativa de la fracción HDL (16%).
No se detectaron otras alteraciones significativas, ni bioquímicas, ni en el hemograma.
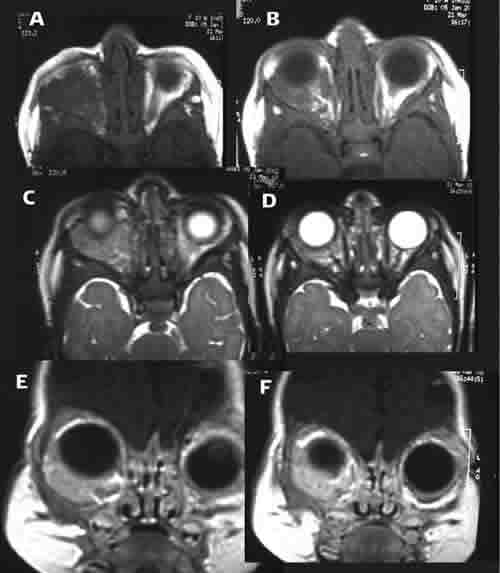
Fig. 3. Reconstrucciones axiales potenciadas en T1 (a,b) y T2 (c,d) y coronales potenciales en T1
congadolinio intravenoso (e,f). Lesión con componente intra y extraconal, de bordes mal definidos,
hipointenso en T1 e hiperintenso en T2, que capta Gadolinio correspondiente al hemangioma.
Se trata del paciente de la figura 1.

Fig. 4. Reconstrucciones axiales potenciadas en T1 (g,h) y T1 con Gadolinio y
saturación grasa (k,l). Ausencia de la masa, quedando únicamente algunos
tractos fibrosos y, borramiento de grasa correspondiente a restos fibrosos.
Se trata del paciente de la figura 2.
En uno de nuestros pacientes se detectó, a los 7,5 meses de vida (5 meses tras el inicio del tratamiento), alteraciones en la exploración neurológica compatibles con un cuadro de diplejia espástica. Al suspender el tratamiento, progresivamente fueron desapareciendo los signos de hiperexcitabilidad e hipertonía en los miembros inferiores, alcanzando la paciente un desarrollo psicomotor normal, si bien con un ligero retraso en la deambulación autónoma. Actualmente, 12 meses después de finalizar el tratamiento, no presenta ninguna secuela neurológica.
Hasta el momento los pacientes han seguido revisiones periódicas, objetivándose un desarrollo psicomotor normal, una función visual adecuada y la ausencia de recidiva de las lesiones.
DISCUSIÓN
La incidencia de complicaciones de los hemangiomas periorbitarios es muy alta. Haik y Jakobiec encuentran que sólo un 20% de individuos con hemangiomas periorbitarios tienen una visión normal en el ojo afectado, en un seguimiento de 5 años (15). Así, el manejo de estas complicaciones (ambliopía fundamentalmente), es muy importante.
La mayoría de los hemangiomas periorbitarios que afectan a la órbita lo hacen en la parte anterior de la misma, de manera que existe un fácil acceso para la inyección intralesional de corticoides. Sin embargo, aproximadamente un 7% (3) producen únicamente proptosis; en éstos, es más arriesgada la inyección intralesional. Es en este último caso, y cuando los corticoides intralesionales no solucionen el problema, cuando proponemos el uso del interferón.
Aunque el mecanismo de acción del interferón alfa no se conoce con exactitud, se sabe que ejerce un efecto supresor sobre el endotelio vascular, inhibiendo la proliferación de las células endoteliales y, la producción de sustancias estimulantes de la angiogénesis, como el factor de crecimiento fibroblástico beta (bFGF) (16,17).
Según diferentes autores, el interferón alfa, consigue una reducción de más del 50% del tamaño del hemangioma en un 58% de los casos, y en el 26% una reducción entre el 20 y el 40% (4). En aproximadamente un 15% de los casos, no existe respuesta al tratamiento. Pocos son los autores que han descrito específicamente el efecto del interferón sobre los hemangiomas con participación orbitaria. Fledelius (11) estudió 9 niños con hemangiomas faciales que comprometían la visión, 3 de los cuales además afectaban la cavidad orbitaria, observando una reducción significativa en el 100% de los casos tras el tratamiento con este fármaco.
Aunque actualmente no se han definido marcadores que determinen la respuesta al interferón. Estudios recientes sugieren que niveles elevados en orina de FGF al inicio del tratamiento, parecen predecir una mejor respuesta al mismo (18).
En la mayoría de los casos el interferón alfa es una medicación bien tolerada por el paciente pediátrico. Es frecuente la aparición de efectos secundarios leves, en su gran mayoría pasajeros. Entre ellos destacan por su frecuencia la fiebre durante los primeros días de su administración, la hipoorexia, cambios en el carácter, un discreto incremento en las enzimas hepáticas y neutropenia transitoria. Sin embargo, son los efectos secundarios sobre el sistema nervioso los que más preocupan por su posible irreversibilidad. En aproximadamente un 25% de los pacientes tratados con interferón aparecen alteraciones neurológicas. En los lactantes, lo más frecuente son alteraciones motoras menores y, generalmente transitorias como retraso o inestabilidad en la marcha y retraso en la adquisición de los movimientos finos de las manos. Pero el efecto adverso más grave descrito, y por el cual recientemente se pone en tela de juicio su uso en lactantes, es la diplejia espástica. El primer autor en describirla fue Vesikari en 1988 en un niño de 2 años que recibió interferón alfa-2a como tratamiento de una papilomatosis laríngea (19). Barlow, en 1998 describió 5 casos en un grupo de 26 lactantes con hemangiomas tratados con interferón alfa; 3 de ellos quedaron con secuelas permanentes relacionadas con la deambulación, de diferente severidad (20). Posteriormente, otros autores han descrito el mismo cuadro aunque con menor incidencia (11), siendo muy puntuales los casos en los que se describen secuelas permanentes (16).
Existen 2 tipos de interferón alfa: alfa-2ª (Roferon A) y alfa-2b (Intron A). Con ambos se ha descrito neurotoxicidad (17). El efecto parece ser dependiente de la dosis. Se habla de una dosis acumulativa máxima, que si no se sobrepasa, no se produciría este efecto adverso tan temido. Se ha descrito diplejia espástica con una dosis acumulativa media de 627 millones de U (rango 253-1946) (11,20). Asimismo, parece ser dependiente de la duración del tratamiento (17), por lo que los niños requieren un seguimiento neurológico cercano. También se relaciona con la instauración precoz del mismo. Algunos dicen que el efecto neurotóxico se debería al conservante, alcohol, y que no aparecería si se utilizara solución salina (21).
En nuestra serie una de las 4 pacientes desarrolló un cuadro compatible con diplejia espástica a los 4 meses de iniciado el tratamiento, 7,5 meses de edad. Tras la supresión del fármaco, y con el apoyo de medidas de rehabilitación, desaparecieron progresivamente los signos propios de esta complicación, si bien se objetivó un retraso de la marcha autónoma. Actualmente, el desarrollo psicomotor de la niña es el adecuado para su edad. A diferencia de las otras alteraciones motoras, la diplejia espástica se presenta mas tardíamente (de 8 meses a 3 años tras el inicio del tratamiento), incluso después de haber terminado el mismo, y suele ir precedida de alteraciones motoras groseras como retraso o inestabilidad en la marcha o en la adquisición del lenguaje.
El hecho de que en niños mayores con hepatitis B crónica, en tratamiento prolongado con interferón, no se haya descrito esta complicación, refuerza la idea de que la inmadurez de un sistema nervioso todavía en periodo de desarrollo, como es el del lactante, es un factor esencial que predispone al desarrollo de ésta (21).
Con el objetivo de evitar la aparición de diplejia espástica algunos autores sugieren un régimen de dosis bajas de interferón, para el tratamiento de los hemangiomas infantiles, a razón de 1 millón U/día 3 días a la semana durante 2 semanas seguidas, de 3 millones U/m2/día 3 días a la semana hasta el final del tratamiento. Parece que la eficacia es la misma reduciéndose el coste del tratamiento y postulan que también la aparición de efectos secundarios (22). El efecto real de esta opción no está estudiado.
En nuestro artículo describimos la importante alteración del perfil lipídico encontrado en una de las pacientes. Aunque tanto las cifras de colesterol como las de triglicéridos se elevaron por enzima del rango de la normalidad, son las de estos últimos las que más se vieron alteradas a expensas principalmente de la fraccion VLDL. Estos hallazgos no impidieron que se completara el tratamiento. A las pocas semanas de la suspensión del mismo, las cifras de colesterol se normalizaron, pero las de triglicéridos aún permanecen elevadas 1 mes después de la misma.
Como conclusión, el interferón alfa es un tratamiento que ha demostrado ser eficaz en el manejo de los hemangiomas infantiles con afectación orbitaria. A pesar que la eficacia es superior a la de los tratamientos clásicos y, que en general, es un tratamiento muy bien tolerado por el lactante, se ha descrito la asociación a diplejia espástica. Si bien la incidencia de la misma y, la probabilidad de que no se resuelva o deje secuelas en la deambulación no está del todo definida, es necesario instaurar un programa de seguimiento adecuado siempre que se administre, para detectar su aparición precozmente. Son necesarios más estudios para precisar el posible efecto beneficioso de los programas de dosis bajas y, sobre todo, para determinar factores predictores de la respuesta al interferón, como pueden llegar a ser los títulos elevados de bFGF en orina. Proponemos su uso fundamentalmente en aquellos hemangiomas en que no se pueda inyectar corticoides intralesionalmente o esto falle. La superioridad beneficio-riesgo del interferón intravenoso sobre los corticoides sistémicos queda por demostrar.
BIBLIOGRAFÍA
1. Drolet BA, Esterly NB, Frieden IJ. Hemangiomas in children. N Engl J Med 1999; 341: 173-179. [ Links ]
2. Kushner BJ. Hemangiomas. Arch Ophthalmol 2000; 118: 835-836. [ Links ]
3. Goldberg NS, Rosanova MA. Periorbital hemangiomas. Dermatol Clin 1992; 10: 653-661. [ Links ]
4. Greinwald JH Jr, Burke DK, Bonthius DJ, Bauman NM, Smith RJ. An update on the treatment of hemangiomas in children with interferon alfa-2a. Arch Otolaryngol Head Neck Surg 1999; 125: 21-27. [ Links ]
5. Enjorlas O, Riche MC, Merland JJ, Escande JP. Management of alarming hemangiomas in infancy: a review of 25 cases. Pediatrics 1990; 85: 491-498. [ Links ]
6. Bartoshesky LE, Bull M, Feingold M. Corticosteroid treatment of cutaneus hemangiomas: how effective? A report of 24 children. Clin Pediatr 1978; 17: 625-638. [ Links ]
7. White CW, Sondheimer HM, Crouch EC, Wilson H, Fan LL. Treatment of pulmonary hemangiomatosis with recombinant interferon alfa-2a. N Engl J Med 1989; 320: 1197-200. [ Links ]
8. Orchad PJ, Smith CM 3rd, Woods WG, Day DL, Dehner LP, Shapiro R. Treatment of hemangioendotheliomas with alfa interferon. Lancet 1989; 2: 565-567. [ Links ]
9. Ezekowitz RA, Mulliken JB, Folkman J. Interferon alfa-2a therapy for life-threatening hemangiomas of infancy. N Engl J Med 1992; 326: 1456-1463. [ Links ]
10. McArthur CJ, Senders CW, Katz J. The use of interferon alfa-2a for life-threatening hemangiomas. Arch Otolaryngol Head Neck Surg 1995; 121: 690-693. [ Links ]
11. Fledelius HC, Illum N, Jensen H, Prause JU. Interferon-alfa treatment of facial infantile haemangiomas: with emphasison the sight-treatening varietes. A clinical series. Acta Ophthalmol Scand 2001; 79: 370-373. [ Links ]
12. Ricketts RR, Hatley RM, Corden BJ, Sabio H, Howell CG. Interferon-alfa-2a for the treatment of complex hemangiomas of infancy and childhood. Ann Surg 1994; 219: 605-612. [ Links ]
13. Tamayo L, Ortiz DM, Orozco-Covarrubias L, Duran-McKinster C, Mora MA, Avila E et al. Therapeutic efficacy of interferon alfa-2b in infants with life-threatening giant hemangiomas. Arch Dermatol 1997; 133: 1567-1571. [ Links ]
14. Loughnan MS, Elder J, Kemp A. Treatment of a masive orbital-capillary hemangioma with interferon alfa-2b: short-term results. Arch Ophthalmol 1992; 110: 366-367. [ Links ]
15. Haik BG, Jakobiec FA et al. Capillary hemangioma of the lids and orbit: an analysis of the clinical features and therapeutic results in 101 cases. Ophthalmology 1979; 86: 760-792. [ Links ]
16. Grimal I, Duveau E, Enjolras O, Verret JL, Ginies JL. Effectiveness and dangers of interferon-alpha in the treatment of severe hemangiomas in infants. Arch Pediatr 2000; 7: 163-167. [ Links ]
17. Metry DW,Hebert AA. Benign cutaneus vascular tumors of infancy: when to worry, what to do. Arch Dermatol 2000; 136: 905-914. [ Links ]
18. Chang E, Boid A, Nelson CC. Crowley D, Law T, Keough KM et al. Succesful treatment of infantile hemangiomas with interferon-alfa 2b. J Pediatr Hematol Oncol 1997; 19: 237-244. [ Links ]
19. Vesikari T, Nuutila A, Cantell K. Neurologic sequelae following interferon therapy of juvenile laryngeal papilloma. Acta Paediatr Scand 1988; 77: 619-622. [ Links ]
20. Barlow CF, Priebe CJ, Mulliken JB, Barnes PD, Mac Donald D, Folkman J et al. Spastic diplegia as a complication of interferon alfa-2a treatment of hemangiomas of infancy. J Pediatr 1998; 132: 527-530. [ Links ]
21. Deb G, Jenker A et al. Spastic diplegia and interferon. J Pediatr 1999; 134: 382. [ Links ]
22. Rampini E, Rampini P. Interferon alpha 2b for treatment of complex cutaneous haemangiomas of infancy: a reduce dosage schedule. Br J Derm 2000; 142: 189-191. [ Links ]















