Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos de la Sociedad Española de Oftalmología
versión impresa ISSN 0365-6691
Arch Soc Esp Oftalmol vol.79 no.7 jul. 2004
ARTÍCULO ORIGINAL
GRANULOCITO-AFERESIS EN BEHÇET OCULAR
REFRACTARIO AL TRATAMIENTO MÉDICO
GRANULOCYTE-APHERESIS IN OCULAR BEHÇETS DISEASE
RESISTANT TO MEDICAL TREATMENT
GARCÍA GARCÍA O1, VIDALLER PALACÍN A2, MUÑOZ SÁNCHEZ J1, ROCA LINARES G1
| RESUMEN Objetivo: El objetivo del estudio fue evaluar la viabilidad de la granulocitoaferesis (GCAP) en pacientes con enfermedad de Behçet (EB) ocular resistente al tratamiento con inmunosupresores (prednisona, ciclosporina, azatioprina o micofenolato mofetilo). Palabras clave: Granulocitoaféresis, enfermedad de Behçet, inmunosupresores. | SUMMARY Objective: To assess the feasibility of granulocyte apheresis (GCAP) in patients with Ocular Behçets Disease (BD) resistant to immunosuppressive therapy (prednisone, cyclosporin, azathyoprine or mycophenolate mofetil). Key words: Granulocyte-apheresis, Behçets disease, immunosuppressants. |
Recibido: 9/3/04. Aceptado: 24/6/04.
Ciutat Sanitaria i Universitaria de Bellvitge.
1 Licenciado en Medicina.
2 Doctor en Medicina.
Correspondencia:
Olga García García
Ciutat Sanitaria i Universitaria de Bellvitge
C/ Feixa Llarga, s/n
08907 L'Hospitalet de Llobregat. Barcelona. España
E-mail: 23221ogg@comb.es
INTRODUCCIÓN
La enfermedad de Behçet (EB) es una vasculitis multisistémica de etiología desconocida que afecta principalmente a los sistemas ocular, mucocutáneo, vascular, articular y nervioso central. En la inmunopatogenia de esta enfermedad, se ha demostrado la existencia de hiperactividad de la función granulocítica, incremento en el número de granulocitos, concentración elevada de células inflamatorias en la pared vascular y los tejidos adyacentes y apoptosis (2).
La afección oftalmológica más característica es una vasculitis retiniana oclusiva, crónica y recidivante, de mal pronóstico visual.
El tratamiento actual se basa en la inmunosupresión. La gravedad de esta vasculitis obliga a utilizar corticosteroides y dos o más fármacos inmunosupresores sistémicos (ciclosporina, azathioprina o micofenolato mofetilo) para evitar recidivas (2).
La granulocitoaféresis (GCAP) con acetato de celulosa es una nueva técnica que ha tenido resultados esperanzadores en el tratamiento de otras enfermedades autoinmunes, tales como la colitis ulcerosa (3), la enfermedad de Crohn (grupo GETECCU, datos no publicados, octubre 2003) y la artritis reumatoide (4). El mecanismo de acción implicado es una disminución selectiva del número de granulocitos y monocitos y una inmunomodulación de diversas citocinas (IL-1, IL-8, IL-4, IL-10 y TNF-alfa); la acción conjunta de estos factores reduce la inflamación en los órganos afectados (5).
Se administró tratamiento coadyuvante compasivo con GCAP en cinco casos de EB, definida según los criterios internacionales (6), con inflamación ocular grave resistente a la terapia estándar. El objetivo era usar el efecto antiinflamatorio de la GCAP, basándonos en la efectividad y seguridad del tratamiento descritas en otras enfermedades autoinmunitarias (7-9), con el fin de reducir los requerimientos de prednisona a dosis más tolerables, sin que ello provocara una recidiva de la inflamación intraocular.
SUJETOS, MATERIAL Y MÉTODOS
Estudio prospectivo de cinco pacientes, cuatro presentaban resistencia al tratamiento médico y uno no había padecido recidivas durante los últimos 6 años, pero al tratarse de un paciente joven con ojo único con baja visión era arriesgado reducirle el tratamiento médico.
Las sesiones de GCAP, técnica de aféresis extracorporea, fueron realizadas por personal formado y especializado en el procedimiento. El acceso venoso se realizó a través de las venas antecubitales del paciente; la velocidad de flujo del circuito fue de 30 ml/min y el tiempo empleado en cada aféresis fue de 60 minutos. Las sesiones se realizaron a intervalos de una semana durante un periodo de 5 semanas. Esta pauta terapéutica se seleccionó basándonos en experiencias anteriores con otras enfermedades autoinmunitarias (10). Después de las 5 sesiones de aféresis, que constituyen el tratamiento de inducción, el paciente 1 recibió 5 sesiones de aféresis adicionales (a intervalos de dos semanas) por tratarse de un caso más avanzado. En cada sesión se controló la AV según la escala de Snellen, el grado de inflamación intraocular mediante biomicroscopia y funduscopia y se reguló la dosis de prednisona en función de la respuesta a la GCAP.
Para las variables continuas se utilizó la prueba t de Student para datos apareados.
Antes de iniciar la GCAP, se obtuvo el consentimiento informado de todos los pacientes y el Ministerio de Sanidad español lo autorizó como tratamiento de uso compasivo en los cinco casos.
Caso 1
Mujer de 24 años con diagnóstico de EB en 1996 tras un brote de vasculitis retiniana bilateral, eritema nodoso en extremidades inferiores y antecedentes de aftas orales recidivantes. Se inició el tratamiento con prednisona a 1 mg/kg/día y ciclosporina a 5 mg/kg/día, con buena respuesta inicial. Tras varias recidivas de vasculitis retiniana se añadió azatioprina y se realizó una fotocoagulación panretiniana en ambos ojos debido a una importante isquemia retiniana periférica. A pesar del triple tratamiento, corticoides subtenonianos e intravitreos, la paciente presentó una media de cuatro recidivas anuales de uveítis posterior (tabla I).
En el momento de iniciar el tratamiento con GCAP, la AV era de 0,25 en el ojo derecho (OD) y 0,15 en el ojo izquierdo (OI) ( AV máxima que se consiguió en cada ojo desde la aparición de la enfermedad, la paciente estaba sin brote); con un tratamiento de 25 mg/día de prednisona, 300 mg/día de ciclosporina y 2000 mg/día de micofenolato mofetilo (tabla II).
Caso 2
Mujer de 28 años con diagnóstico de EB en marzo de 2002 por vasculitis retiniana en ambos ojos, aftas orales, eritema nodoso en extremidades inferiores y tromboflebitis superficial en la pierna izquierda. Se inició el tratamiento con 1 mg/kg/día de prednisona.
A pesar del tratamiento con 1 mg/kg/día de prednisona, no fue posible reducir la dosis de prednisona a menos de 25 mg/día. La paciente rechazó el tratamiento con ciclosporina y azatioprina y presentó ocho recidivas de uveítis posterior en ambos ojos durante el 2002 (una recidiva mensual) (tabla I).
Ante la falta de control del cuadro clínico, se decidió iniciar el tratamiento con GCAP con una AV de 0,5 en el OD y 0,9 en el OI, y 50 mg/día de prednisona (tabla II).
Caso 3
Hombre de 22 años diagnosticado de EB en 1997 tras padecer panuveítis en ambos ojos y aftas genitales y orales recidivantes. Se inicia el tratamiento con 1 mg/kg/día de prednisona y 5 mg/kg/día de ciclosporina. Un edema macular en el ojo izquierdo requirió triamcinolona subtenoniana que produjo un glaucoma, el cual sólo se controló con una trabeculectomía. En 1999 tuvo que añadirse azatioprina al tratamiento, pero las recidivas continuaron a pesar del tratamiento con 30 mg/día de prednisona, 200 mg/día de ciclosporina y 150 mg/día de azatioprina (tabla I).
En el momento de iniciarse el tratamiento con GCAP, la AV era de 0,9 en el OD y contar dedos a 3 metros en el OI (tabla II).
Caso 4
Hombre de 38 años con diagnóstico de EB en 1986, con antecedentes de uveítis anterior con hipopión en el OD, aftas orales recidivantes y tromboflebitis en la extremidad inferior izquierda. El paciente fue tratado con prednisona y ciclosporina, pero tuvo una media de 3 recidivas de uveítis anuales hasta 1997 (tabla I).
En 1999 fue preciso cambiar la ciclosporina por micofenolato mofetilo debido a nefrotoxicidad con insuficiencia renal e hipertensión arterial. Fue necesario también administrar tratamiento para la osteopenia inducida por corticosteroides.
El paciente no había sufrido una recidiva desde 1997 pero se inició la GCAP en un esfuerzo por reducir las dosis de mantenimiento de fármacos inmunosupresores. La AV era de percepción luminosa en dos cuadrantes en el OD y de 0,6 en el OI (tabla II).
Caso 5
Hombre de 23 años con diagnóstico de EB en febrero de 2003 tras padecer vasculitis retiniana y vitritis en ambos ojos, trombosis de rama temporal en el OD y aftas orales recidivantes. Mala respuesta a 1 mg/kg/día de prednisona y a triamcinolona subtenoniana en el OD (tabla I).
Debido al rechazo del paciente a otro tratamiento inmunosupresor, se inició GCAP como tratamiento coadyuvante, la AV era de 0,6 en el OD y de 0,9 en el OI (tabla II).
RESULTADOS
La agudeza visual mejoró en todos los pacientes tras 5 semanas de tratamiento. La inflamación intraocular se controló (figs. 1 y 2) y no se produjeron recidivas durante el tratamiento con GCAP. La dosis media de prednisona al final del tratamiento descendió en más de la mitad comparada con la dosis al inicio del tratamiento. (Reducción media de 52,7%; DE 14) (tablas 2 y 3). El tratamiento con microfenolato mofetilo también se redujo de 2000 mg/día a 1.500 mg/día en el caso 4.
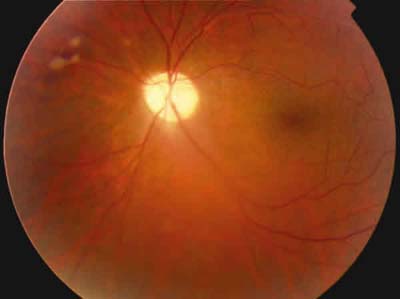
Fig. 1. Retinografía ojo izquierdo del caso 4 al inicio del tratamiento.
Se aprecia vasculitis arcada temporal superior y vitritis escasa.
Papila pálida secundaria a los múltiples brotes de inflamaciones previas.
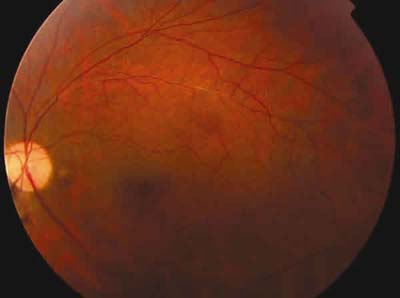
Fig. 2. Retinografía del mismo ojo al finalizar el tratamiento.
Persiste manguito vascular residual pero sin vitritis.
No se observaron efectos secundarios y el proceso de aféresis fue bien tolerado en todos los casos.
DISCUSIÓN
Los neutrófilos de pacientes diagnosticados de EB tienen incrementada la producción de superóxidos y reactivada la quimiotaxis, lo cual da lugar a lesiones tisulares (11).
Además, unos niveles elevados de citocinas inflamatorias pueden estar relacionados con la activación de neutrófilos así como de otras moléculas de adhesión en la EB (12,13). Algunos autores han descrito un descenso en las citocinas (TNF-, IL-1, IL-6, IL-8) (5) y las moléculas de adhesión (L-Selectina) (14) y la generación de antagonistas de los receptores de la interleucina 1 y receptores solubles I y II del TNFa tras la GCAP (Hanai H, documento inédito, 2003). Se ha presentado esta deplección de citocinas como el mecanismo de acción de la GCAP en otras enfermedades autoinmunitarias como la colitis ulcerosa y la enfermedad de Crohn, en las cuales se ha administrado este tratamiento y se ha demostrado su eficacia clínica (15).
Nuestros resultados muestran la eficacia clínica de la GCAP en la EB en un grupo de pacientes especialmente difíciles de tratar. Se ha medido dicha eficacia en cuanto a la mejoría de la agudeza visual y la disminución de la dosis total de fármacos inmunosupresores, sin la aparición de nuevas recidivas.
Es muy conocida la toxicidad relacionada con el uso de corticosteroides o de inmunosupresores. La GCAP es un proceso de filtración sanguínea extracorpóreo caracterizado por su alto nivel de seguridad. No hay constancia de efectos adversos ni de muerte alguna en las publicaciones que hacen referencia a la utilización de la GCAP (16).
Además de conseguir disminuir las dosis de prednisona sin recidivas, la agudeza visual mejoró hasta situarse en niveles que no se habían alcanzado desde el comienzo de la enfermedad; lo cual puede ser consecuencia de una reducción en la infiltración del tejido de células inflamatorias debido al efecto inmunomodulador de la GCAP.
La GCAP puede constituir una alternativa terapéutica válida que facilite la reducción del tratamiento con inmunosupresores, así como la disminución del número de recidivas.
Se sugiere que el tratamiento con GCAP puede convertirse en un nuevo tratamiento alternativo eficaz para las manifestaciones oculares de EB resistente a corticosteroides e inmunosupresores.
No obstante, para definir la pauta terapéutica adecuada de la GCAP como alternativa para el tratamiento de la EB grave, se requieren más casos, un seguimiento más prolongado y ensayos clínicos controlados.
BIBLIOGRAFÍA
1. Sakane T, Takeno M, Suzuki N, Inaba G. Behcet´s disease. N Engl J Med 1999; 341: 1284-1291. [ Links ]
2. Dick A D, Azim M, Forrester JV. Immunosuppresive therapy for chronic uveitis: optimising therapy with steroids and cyclosporin A. Br J Ophthalmol 1997; 81: 1107-1112. [ Links ]
3. Hanai H, Watanabe F, Takeuchi K, Iida T, Iwaoka Y, Saniabadi A, et. al. Leukocyte adsorptive apheresis for the treatment of active ulcerative colitis: a prospective, uncontrolled, pilot study. Clin Gastroenterol Hepatol 2003; 1: 28-35. [ Links ]
4. Kashiwagi N, Hirata I, Kasukawa R. A role of granulocyte and monocyte apheresis in the treatment of rheumatoid arthritis. Ther Apher 1998; 2: 134-141. [ Links ]
5. Kashiwagi N, Sugimura K, Koiwai H, Yamamoto H, Yoshikawa T, Saniabadi AR, et al. Immunomodulatory effects of granulocyte and monocyte adsorption apheresis as a treatment for patients with ulcerative colitis. Dig Dis Sci 2002; 47: 1334-1341. [ Links ]
6. Criteria for the diagnosis of Behcet´s disease. International Study Group for Behcets Disease. Lancet 1990; 335: 1078-1080. [ Links ]
7. Shimoyama T, Sawada K, Hiwatashi N, Sawada T, Matsueda K, Munakata A, et al. Safety and efficacy of granulocyte and monocyte adsorption apheresis in patients with active ulcerative colitis: a multicenter study. J Clin Apheresis 2001; 16: 1-9. [ Links ]
8. Hanai H, Watanabe F, Saniabadi AR, Matsushitai I, Takeuchi K, Iida T. Therapeutic efficacy of granulocyte and monocyte adsorption apheresis in severe active ulcerative colitis. Dig Dis Sci 2002; 47: 2349-2353. [ Links ]
9. Matsui T, Nishimura T, Matake H, Ohta T, Sakurai T, Yao T. Granulocytapheresis for Crohn´s disease: a report on seven refractory patients. Am J Gastroenterol 2003; 98: 511-512. [ Links ]
10. Hanai H, Watanabe F, Takeuchi K, Iida T, Yamada M, Iwaoka Y, et al. Leukocite adsorptive apheresis for the treatment of active ulcerative colitis: a prospective uncontrolled pilot study. Clin Gastroenterol Hepatol 2003; 1: 28-35. [ Links ]
11. Sakane T, Takeno M, Suzuki N, Inaba G. Behcets disease. N Engl J Med 1999; 341: 1284-1291. [ Links ]
12. Boyd SR, Young S, Lightman S. Immunopathology of the non-infectious posterior and intermediate uveitides. Surv Ophthalmol 2001; 46: 209-233. [ Links ]
13. Benezra D, Maftzir G, Barak V. Blood serum interleukin-1 receptor antagonist in pars planitis and ocular Behcet disease. Am J Ophthalmol 1997; 123: 593-598. [ Links ]
14. Rembacken BJ, Newbould HE, Richards SJ, Misbah SA, Dixon ME, Chalmers DM, et al. Granulocyte apheresis in inflammatory bowel disease: possible mechanisms of effect. Ther Apher 1998; 2: 93-96. [ Links ]
15. Tsukada Y, Nakamura T, Iimura M, Iizuka BE, Mayashi N. Cytokine profile in colonic mucosa of ulcerative colitis correlates with disease activity and response to granulocytapheresis. Am J Gastroenterol. 2002; 97: 2820-2828. [ Links ]
16. Yamaji K, Tsuda H, Hashimoto H. Current topics on cytapheresis technologies. Ther Apher 2001; 5: 287-292. [ Links ]