Introducción
Según estadísticas publicadas por entidades científicas desde el año 2015 hasta la fecha, la mamoplastia de aumento es el procedimiento quirúrgico más realizado en la especialidad de Cirugía Plástica en muchos países del mundo, y principalmente aquellos en los que se realiza un mayor número de cirugías estéticas, como EE.UU. y Brasil.(1)
La presencia de ondulación en el polo superior de los senos,(2)conocida generalmente por su nombre en inglés como rippling,es una queja cada vez más frecuente en nuestro consultorio en pacientes portadoras de implantes mamarios retroglandulares que perdieron mucho peso o que fueron sometidas a mastectomía y posterior reconstrucción del seno con colocación de implantes mamarios en un plano prepectoral.(3)
En los últimos años, hemos visto publicados diversos estudios científicos que constatan como en pacientes sometidas a aumento mamario con prótesis en un plano submuscular, el diagnóstico de patologías mamarias en los exámenes rutinarios es más precoz que en aquellas en las que los implantes están colocados en un plano prepectoral o subglandular.(3)Esos mismos estudios hacen mención a que en las pacientes que tenían que someterse a mastectomía como tratamiento a su patología, las prótesis que estaban en un plano submuscular no necesitaban por lo general ser manipuladas y podían permanecer en posición sin interferir con la cirugía oncológica.(3)Todos estos aspectos influyen claramente en nuestra predilección por la colocación de los implantes mamarios en el plano submuscular.
Cuando se realiza una mamoplastia de aumento con colocación de la prótesis en plano submuscular, lo habitual es utilizar anestesia general.(4)Existen métodos anestésicos alternativos a la anestesia general como: bloqueos de nervios intercostales,(5)bloqueo paravertebral torácico,(6)bloqueo epidural torácico alto,(7)infiltración de soluciones anestésicas locales y sedación,(8)o el bloqueo de ramos del plexo braquial por inyección percutánea del anestésico asistida por ecografía.(9)
Por otro lado, hemos de señalar que la cirugía ambulatoria se ha incrementado hasta tasas sin precedentes a nivel mundial(10)y que cada vez se realizan bajo esta modalidad procedimientos más complejos, entre los que están los propios de la cirugía reconstructiva mamaria y la colocación de implantes mamarios con fines de aumento estético.(10)Para que esto se tornara posible, fue necesario modificar el método anestésico utilizando bloqueos locorregionales que sustituyeran o complementaran a la tradicional anestesia general. Esto ha permitido que las pacientes, una vez finalizada la cirugía y después de unas horas de cuidados postoperatorios en la clínica, continúen la recuperación en su domicilio.
Existen además grandes ventajas de la anestesia regional en comparación con la anestesia general, entre las cuales podemos citar la disminución de los costos, un mejor manejo del dolor, la colaboración del paciente en cuanto a su posición y movilización precoz, y en conjunto, una más rápida recuperación postoperatoria.(10)
El presente trabajo pretende mostrar, como alternativa a la anestesia general, un método anestésico que bloquea ramas nerviosas del plexo braquial por medio de infiltración de bolos de preparado anestésico de forma directa en el área donde anatómicamente se encuentran los nervios a bloquear. Si bien este tipo de bloqueos están presentes en anteriores publicaciones,(9)suelen ser realizados mediante punción transcutánea auxiliada con ecografía.
Presentamos nuestra metodología indicada para mamoplastias con colocación de implantes por distintas indicaciones en plano submuscular, empleando inyección anestésica directa intraoperatoria a cielo abierto y mediante el uso de cánula, a la vez que hacemos una recogida de casuística personal.
Material y método
Técnica anestésica y quirúrgica
Con la paciente en posición de decúbito supino en la mesa quirúrgica, diseñamos con bolígrafo marcador de tinta indeleble en el área media infraclavicular lo que sería la proyección anatómica en la piel de los nervios pectoral lateral y pectoral medial y hacemos una tercera marca siguiendo la línea axilar anterior hasta llegar al área donde se proyectaría el nervio torácico largo (Fig. 1).

Figura 1. Proyección del trayecto de las ramas nerviosas diseñada sobre la piel: pectoral medial, pectoral lateral y torácico largo, que inervan respectivamente los músculos pectoral menor, pectoral mayor y serrato anterior.
El anestesiólogo realiza sedación con midazolan y fentanyl, y una vez que la paciente alcanza un nivel de sedación adecuado, con jeringa de 20 ml y aguja hipodérmica desechable de 21G y 40 mm inyectamos una solución anestésica compuesta por 40 ml de lidocaína al 2% más una ampolla de 1 ml de adrenalina en 1000 ml de solución salina en la piel del área periareolar inferior y en el tejido celular subcutáneo (TCS), profundizando en el parénquima mamario y llegando hasta el plano aponeurótico supramuscular.
Tras unos minutos, iniciamos la cirugía con incisión semicircular en el contorno periareolar inferior de más o menos 5 cm de longitud, profundizando la divulsión en TCS y transglandularmente hasta llegar al plano muscular. Exponemos una franja de la aponeurosis muscular de aproximadamente 7 x 3 cm siguiendo la anatomía aparente de las fibras musculares y en dirección hacia la axila. En esa franja muscular expuesta infiltramos 10 ml de la misma solución anestésica con aguja hipodérmica. Incidimos la aponeurosis muscular, con una apertura de 5 cm de longitud y el músculo con lámina de bisturí, en forma paralela a la dirección de las fibras musculares. A partir de la porción inferior del músculo y en dirección al hueco axilar (Fig. 2), practicamos divulsión del músculo con tijera de Metzenbaum de punta roma, separando las fibras musculares en profundidad hasta llegar al plano areolar que separa el músculo pectoral mayor del pectoral menor. Una vez en ese plano, colocamos un separador de Farebeuf y elevamos el pectoral mayor para exponer un túnel virtual submuscular dirigido sagitalmente en sentido cefálico hacia las marcas realizadas en la piel. Introducimos en ese túnel una cánula de infiltración multiperforada (cánula de Klein) de 20 cm de longitud y 2 mm de diámetro, hasta unos 2 cm por debajo de la clavícula (Fig. 3), donde inyectamos 120 ml de la solución anestésica preparada; esta infiltración tiene por objetivo bloquear la inervación del músculo pectoral mayor (nervio pectoral lateral), del pectoral menor (nervio pectoral medial) y del músculo serrato anterior (nervio torácico largo). Para asegurar el bloqueo de la inervación del músculo serrato anterior inyectamos 60 ml de la misma solución anestésica en la línea media axilar y en el mismo plano submuscular anterior (Fig. 4).
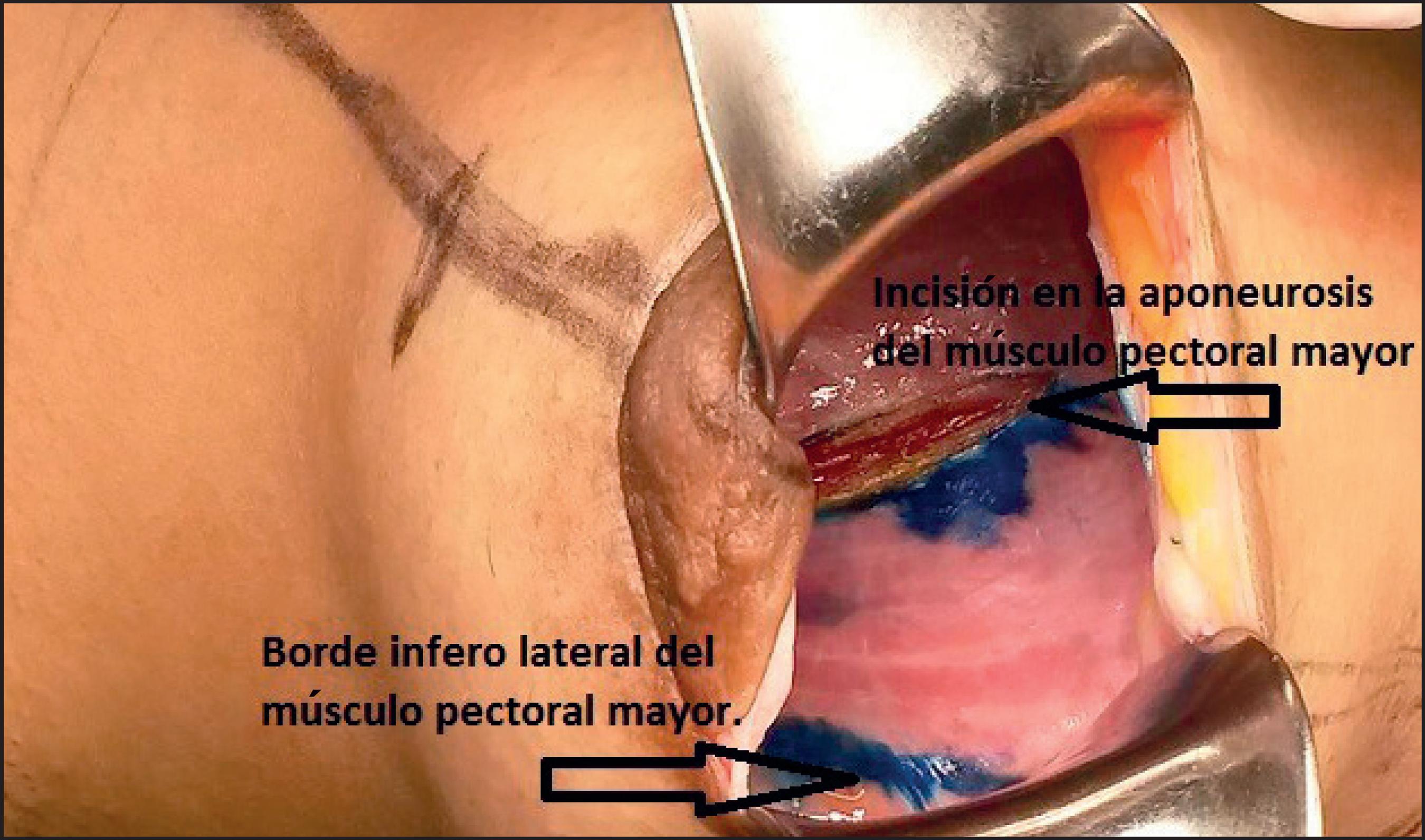
Figura 2. Incisión en la aponeurosis del músculo pectoral mayor paralela al sentido de las líneas musculares a partir de la porción inferior, en dirección al hueco axilar de 5 cm de largo.

Figura 3. Introducción de la cánula de Klein en dirección a la región infraclavicular media lateral (2 cm por debajo de la clavícula), donde se inyecta la solución anestésica para bloquear los nervios pectoral medial y pectoral lateral que inervan respectivamente a los músculos pectoral menor y mayor.

Figura 4. Cánula de Klein introducida en el mismo plano submuscular en dirección a la línea axilar media para bloquear el nervio torácico largo que inerva al músculo serrato.
Una vez concluidas estas maniobras, iniciamos la creación del bolsillo submuscular que alojará la prótesis. Realizamos la divulsión de forma digital, iniciando desde el cuadrante látero-superior del músculo pectoral mayor y en dirección al cuadrante lateral inferior, llegando hasta el músculo serrato anterior y haciendo que la aponeurosis y la porción anterior del músculo formen parte del bolsillo submuscular que está siendo creado y que abrazará la prótesis. Continuamos con la divulsión en el cuadrante inferior y medio-esternal del músculo pectoral mayor y finalizamos en el cuadrante superior medio-esternal. Revisamos todo el bolsillo creado y en las áreas donde no fue posible la divulsión digital, complementamos el procedimiento con electrobisturí. De igual manera realizamos hemostasia cuidadosa cauterizando los vasos sangrantes.
Una vez creado el bolsillo adecuado al volumen de la prótesis que vamos a utilizar, colocamos un drenaje de succión por contraabertura a través de incisión de 4 mm en la línea submamaria. Introducimos la prótesis de silicona en el bolsillo submuscular creado (Fig. 5) y realizamos la sutura de la abertura muscular con hilo reabsorbible 2-0 (Fig. 6). Suturamos por planos el tejido mamario y el TCS con puntos simples empleando el mismo hilo y la piel con sutura continua intradérmica de hilo mononylon 3-0. Finalizamos colocando un curativo microporoso y fijando el tubo de drenaje.

Figura 6. Sutura de la abertura realizada en el musculo pectoral mayor. Prótesis cubierta en su totalidad por la musculatura torácica.
No indicamos el uso de fajas compresivas en el postoperatorio
Serie de casos
Llevamos a cabo un estudio retrospectivo de una serie de pacientes operadas entre enero del 2014 y abril del 2018, incluyendo de forma consecutiva todas aquellas pacientes sometidas a mamoplastia con utilización de implantes, ya fuera para resolver hipomastias, corregir ondulaciones de la piel producidas por las prótesis (rippling), cambio de prótesis y cambio de plano (del subglandular al submuscular), suspensiones mamarias asociadas a cambio de implantes, mastectomías con reconstrucción de mama con prótesis y por último, mamoplastias de aumento con suspensión mamaria. En todos los casos la colocación de los implantes se hizo en el plano submuscular.
Todas las pacientes provenían de consultas particulares y fueron operadas en clínica privada. Todas realizaron los estudios preoperatorios rutinarios para este tipo de procedimiento y fueron informadas sobre el método anestésico a emplear (sedación más bloqueo de nervios del plexo braquial), con una explicación breve acerca de que el bloqueo es una variante de la anestesia local. Las pacientes firmaron los correspondientes documentos de consentimiento informado. Las intervenciones se realizaron en el mismo centro quirúrgico, siguiendo todos los protocolos de asepsia, antisepsia y de seguridad normales para este tipo de procedimiento. Todos los procedimientos fueron inicialmente programados como ambulatorios, sin ingreso hospitalario.
Los parámetros estudiados para la valoración de la técnica anestésica empleada fueron: la consecución objetiva del bloqueo de las ramas nerviosas y la presencia o no de complicaciones inherentes al procedimiento anestésico.
Para el control postoperatorio y de resultados, el seguimiento postoperatorio mínimo fue de 12 meses. Las curaciones se hicieron 2 veces por semana durante las primeras 3 semanas, 1 vez cada 15 días hasta los 3 meses y las pacientes retornaron a consulta cada 3 meses hasta finalizar el año de postoperatorio.
Realizamos fotos de frente, oblicuas y perfil en el preoperatorio y después de los 3, 6 meses y 1 año en el postoperatorio.
Resultados
Recogimos un total de 172 pacientes con edades comprendidas entre los 18 y los 63 años (media de 35 años), de las que el mayor número estuvo entre los 26 y los 35 años de edad (58 pacientes, 33.72%), con 55 pacientes entre los 46 y los 63 años (31.97%) y 37 pacientes entre 36 a 45 años (21.51%); por último, el menor número de paciente estuvo entre los 18 y los 25 años (22 pacientes, 12.8%) (Tabla I).
Tabla I. Demografía de las pacientes del grupo de estudio
| EDAD | ||
|---|---|---|
| Años | Nº de pacientes | % |
| 18 a 25 | 22 | 12.8 |
| 26 a 35 | 58 | 33.72 |
| 36 a 45 | 37 | 21.51 |
| 46 a 63 | 55 | 31.97 |
| TOTAL | 172 | 100 |
De las 172 pacientes incluidas en el estudio, en 161 (93%) utilizamos prótesis redondas texturizadas de perfil alto y en 11 casos (6.3%) prótesis anatómicas. El volumen de los implantes osciló entre 150 a 480 cc (media de 281 cc) (Tabla II).
Tabla II. Medidas de los implantes empleados en las pacientes del grupo de estudio
| TAMAÑO DE PRÓTESIS | ||
|---|---|---|
| Volumenen (cc) | Nº de pacientes | % |
| 150-225 | 45 | 26.17 |
| 250-275 | 42 | 24.41 |
| 300-325 | 45 | 26.17 |
| 350-480 | 40 | 23.25 |
| TOTAL | 172 | 100 |
*Prótesis redondas 161, anatómicas 11
La utilización de la técnica anestésica para colocación de implantes en plano submuscular se hizo tanto en hipomastias (61 pacientes: 35.47%), como en recambio de prótesis (52 pacientes: 30.23%), cambio de prótesis más suspensión (25 pacientes: 14.53%), suspensión mamaria más prótesis (19 pacientes: 11.05%), corrección de ondulaciones en polo superior mamario (rippling) (11 pacientes: 6.40%) y por último en casos de reconstrucción mamaria postmastectomía (4 casos: 2.32%) (Tabla III).
Tabla III. Indicaciones de la cirugía practicada en las pacientes del grupo de estudio
| INDICACIONES | Nº | % |
|---|---|---|
| AUMENTO DE SENOS | 61 | 35.47 |
| RECONSTRUCCIÓN DE SENOS | 4 | 2.32 |
| CAMBIO DE PRÓTESIS | 52 | 30.23 |
| CAMBIO DE PRÓTESIS + SUSPENSIÓN | 25 | 14.53 |
| SUSPENSIÓN + PRÓTESIS | 19 | 11.05 |
|
ONDULACIONES EN POLO SUPERIOR (rippling) |
11 | 6.40 |
| TOTAL | 172 | 100 |
En todas las pacientes el procedimiento se realizó en régimen ambulatorio.
El tiempo quirúrgico varió entre los 60 y los 90 minutos en cirugías primarias sin suspensión (media de 75 minutos) y entre 2 y 3 horas en las mamosplastias de aumento con suspensión (media de 2 horas y 30 minutos).
En ningún caso hubo complicaciones intraoperatorias como: punción pleural, arterio-venosa o técnica fallida, ni tampoco en el postoperatorio como: hematomas, seromas o infección.
Tabla IV. Complicaciones en nuestro grupo de estudio
| Tipos de complicaciones | Nº y/o % | Cómo fueron controladas |
|---|---|---|
| Dolor postoperatorio hasta 3 horas (leve) | 17 (10%) | Con inyectables de rutina |
| Dolor después de 3 horas de postoperatorio (elevado) | 5 ( 2.9 % ) | Con internación + analgésicos de mayor potencia |
| Dolor transoperatório en el cuadrante ínfero-medial del bolsillo submuscular | 12 ( 6.9 % ) | Complementación con anestesia local |
Si bien en todos los casos el procedimiento anestésico fue exitoso y la cirugía culminó sin necesidad de recurrir a anestesia general, en 12 casos (6.97 %), durante la divulsión de los músculos serratos anteriores y en la porción inferior del bolsillo que vendría a abrigar la prótesis (ya en contacto con la aponeurosis y con el músculo recto abdominal en su tercio superior), las pacientes refirieron dolor, por lo que fue necesario complementar el bloqueo anestésico con reinfiltración del preparado anestésico bajo visión directa con la misma metodología descrita, en las aéreas mencionadas, para así culminar el procedimiento quirúrgico sin mayores requerimientos de anestesia general.
Una vez pasado el efecto anestésico del bloqueo realizado, todas las pacientes relataron dolor de diferentes intensidades en el postoperatorio mediato. De rutina realizamos un esquema de inyección endovenosa de 200 mg de ketoprofeno diluido en 500 ml de suero fisiológico a goteo lento apenas terminó el procedimiento quirúrgico y en el caso de que persistiera alguna queja dolorosa después de 90 minutos de postoperatorio, aplicamos ketorolaco a dosis de 60 mg directo intravenoso; si pasadas las 3 horas de postoperatorio aún persistían quejas dolorosas intensas, la conducta fue la internación para realizar analgesia con goteo continuo.
Del total del grupo de estudio, 167pacientes (97.09%) recibieron el alta de la clínica a las 3 horas de la intervención. En 5 casos (2.9 %) hubo necesidad de internación de las pacientes durante 24 horas porque el dolor en la región pectoral no pudo ser controlado con el esquema de analgesia endovenosa rutineramente utilizado por nuestro equipo médico para este tipo de procedimiento quirúrgico. A las pacientes internadas se les administró analgesia a base de 3 ampollas de tramadol de 100 mg más 4 g de terapirol diluidos en 1000 ml de suero fisiológico, a ritmo de 14 gotas por minuto, con la que se pudieron controlar las quejas por dolor, permitiendo el alta hospitalaria a las 24 horas.
En todos los casos, una vez de alta hospitalaria, las pacientes continuaron con tratamiento medicamentoso domiciliario a base de diclofenaco relax 50 mg y pridinol 4 mg cada 12 horas durante 1 semana y paracetamol 325 mg asociado a tramadol 37.5 mg cada 8 horas durante 5 días.
Discusión
En párrafos superiores mostramos en detalle nuestra técnica anestésica con infiltración directa de los ramos del plexo braquial en cirugía de mamoplastia con implantes en plano submuscular, infiltrando el preparado anestésico con cánula multiperforada en el área anatómica donde emergen las ramas nerviosas que inervan la musculatura torácica; hacemos la identificación de esta área anatómica mediante los puntos de referencia anatómicos de superficie.
Podemos afirmar que la técnica anestésica objeto de este estudio es la aportación principal del presente artículo porque si bien hay publicaciones de técnicas anestésicas que realizan bloqueos selectivos de los ramos nerviosos que inervan la musculatura torácica para cirugías de reconstrucción mamaria,(9,11)estas publicaciones describen una técnica que precisa acompañarse del empleo de sofisticados aparatos de ultrasonido y del apoyo de un profesional que manipule estos aparatos. Consideramos que la no necesidad de emplear ultrasonidos, marca una gran diferencia por parte de la técnica que describimos en esta publicación, ya que permite disminuir tiempo y costos, y por la ausencia de complicaciones descritas en otros métodos de bloqueo de nervios que utilizan una vía de acceso percutánea, sin visualización directa.(9,11)
La mamoplastia de aumento con prótesis es actualmente el procedimiento quirúrgico más realizado mundialmente en Cirugía Plástica.(1)El tipo de anestesia más empleado en este tipo de intervención es la general.(4,7)A pesar de ello, es válido también admitir que la comunidad científica se encuentra siempre en la búsqueda de métodos menos invasivos que permitan que la mayoría de los procedimientos quirúrgicos en Cirugía Plástica, Estética y Reconstructiva sean catalogados como ambulatorios(10,12,13)y tengan el alta médico-hospitalaria horas después de finalizado el acto quirúrgico para proseguir con la recuperación postoperatoria en su domicilio lo antes posible.
La cirugía ambulatoria aporta grandes ventajas cuando se realiza dentro las normas de seguridad oportunas e imprescindibles; entre esas ventajas podemos citar: disminución de costos, mayor colaboración del paciente e incluso mejor respuesta al estrés quirúrgico ya que la mayoría de los pacientes refieren tener temor a la anestesia general.
La anestesia local con sedación(4,5)ya es un modelo anestésico frecuentemente utilizado en mamoplastia de aumento con colocación de prótesis en plano subglandular, así como en mamoplastias de reducción y suspensión; pero cuando la prótesis se coloca en un plano submuscular, la anestesia de preferencia suele ser la general.(4,7)
Existen publicaciones científicas que, en la búsqueda de métodos alternativos a la anestesia general incursionan en la anestesia por bloqueo de ramas del plexo braquial,(9,11)inyectando la solución anestésica mediante punción transcutánea con agujas hipodérmicas para mamoplastia de aumento con colocación de prótesis en plano submuscular; pero este acto solo es posible de realizar de forma segura si es asistido durante el procedimiento por sofisticados aparatos de ultrasonografía, lo cual si bien lo torna más seguro, también lo encarece y dificulta su utilización de forma más amplia; igualmente este procedimiento anestésico no está exento de posibles complicaciones, como: punción arterio-venosa, punción pleural, técnica fallida o dolor durante la punción y después de ella en el mismo sitio de la punción.(9,11)En esta misma línea de estudio, nosotros incursionamos en un método anestésico mediante bloqueo de las ramas nerviosas del músculo pectoral mayor, pectoral menor y músculo serrato anterior. La técnica que describimos con detalles metodológicos y de la que presentamos resultados en base a una amplia experiencia propia, consigue que la anestesia para el tipo de procedimiento quirúrgico analizado se torne menos onerosa, menos invasiva y más segura. En todos nuestros casos fue posible alcanzar el objetivo de finalizar la intervención sin tener que recurrir a la anestesia general.
Durante la confección del bolsillo que abrigaría la prótesis en el plano submuscular, en 12 casos de nuestra serie hubo la necesidad de complementar el bloqueo de las ramos del plexo braquial con anestesia local realizada de forma directa en el área del cuadrante ínfero-medial, donde se encuentra la porción superior del músculo recto abdominal que no se inerva por los ramos provenientes del plexo braquial. Esta maniobra fue realizada en pacientes a las cuales les colocamos prótesis mayores de 400 cc, en las que fue necesario ampliar el área de divulsión para formar el bolsillo que abrigaría la prótesis.
Siguiendo la técnica descrita, desde nuestro punto de vista y en base a nuestra amplia experiencia personal, consideramos que el procedimiento descrito constituye una alternativa viable para realizar mamoplastia con colocación de implantes en plano submuscular, ya sea con fines estéticos o reconstructivos. La introducción de la solución anestesia con cánula multiperforada en el área donde anatómicamente se encuentran los ramos que inervan los músculos del tórax, bajo visualización y control directo, desde nuestro punto de vista torna segura la utilización de la técnica.
Conclusiones
Los resultados de la técnica anestésica que presentamos, mediante bloqueo de ramas del plexo braquial que inervan la musculatura torácica realizando la infiltración de la solución anestésica a cielo abierto durante el acto quirúrgico y utilizada en 172 pacientes, muestran que en todos los casos fue exitosa, consiguiendo realizar un procedimiento quirúrgico de bajo costo, evitando el uso de aparatología de imagen para localizar los plexos nerviosos, pero igualmente bajo parámetros de seguridad y anestesia adecuados, sin complicaciones ni técnica fallida.
Consideramos por ello que se trata de una alternativa segura a la anestesia general que puede usarse en mamoplastias de todo tipo con colocación de implantes en plano submuscular, tanto estéticas como reconstructivas.
















