Introducción
Las quemaduras se encuentran entre los traumatismos más graves y con mayor repercusión tanto estética como funcional. Desde los años 70 el tratamiento estándar de las quemaduras dérmico-profundas y de espesor completo se basa en el desbridamiento tangencial temprano seguido de la cobertura con autoinjertos,1,2 lo que ha permitido reducir estancia, mortalidad e incidencia de complicaciones infecciosas.3 Sin embargo, este tratamiento implica una gran invasividad sobre el paciente, con gran pérdida hemática, numerosos tiempos quirúrgicos y la necesidad de gran cantidad de recursos para su realización. Además, el análisis histológico de las sucesivas láminas de escara desbridada de forma tangencial revela que el tejido necrótico se acompaña de parte de tejido sano.4
La aparición del desbridamiento enzimático basado en bromelaína y otras enzimas proteolíticas ha mostrado en numerosos estudios que permite reducir la pérdida hemática durante el tratamiento, así como la pérdida de tejido sano, demostrando ser un tratamiento más específico y reduciendo la necesidad del uso de injertos.5 La reducción en la tasa de injerto gracias a la preservación de dermis sana ha sido demostrada por los estudios sobre desbridamiento enzimático, mostrando disminuciones en el uso de injertos sobre quemaduras intermedias y dérmico-profundas de un 64% y tasas de epitelización de 25 días, con tasas bajas de cicatrización hipertrófica.6 De hecho, Schulz demostró que el aumento del tiempo hasta epitelización completa por encima del paradigma de los 21 días clásicos, que ya había sido reportado por otros autores,7 no mostraba un aumento de la cicatrización hipertrófica y encontraba sólo un aumento del eritema de la cicatriz resultante en los meses iniciales, para obtener mejores resultados al año de seguimiento en pigmentación, grosor, pliabilidad, rigidez e irregularidad. No obstante, no había diferencias respecto al tratamiento estándar al evaluar eritema, viscoelasticidad, perdida de humedad y discromía.8
La mayor parte de los estudios centran sus resultados en pacientes con quemaduras desbridadas enzimáticamente por debajo del 15% de superficie corporal quemada total (SCQ), bien en pacientes con superficies quemadas menores de ese porcentaje, o en aquellos en los que al ser mayores, se realizaban desbridamientos enzimáticos en superficies menores del 15% mientras que el resto era tratado mediante tratamiento estándar. El consenso europeo publicado en 2017 por Hirche recogía, entre sus recomendaciones, la limitación del uso de forma general a superficies menores del 15%. Sin embargo, varios autores miembros del consenso reportaban experiencia con superficies mayores, tanto en una única aplicación como en aplicaciones sucesivas.9 La guía clínica de consenso española publicada el mismo año recogía la aplicación en tiempos sucesivos cuando se trata a pacientes grandes quemados, con superficies por encima del 15%, recomendando la monitorización del paciente y realizando los desbridamientos sucesivos en áreas no mayores del 30% cada vez y según la estabilidad clínica del paciente.10
Ojeda analizó el número de intervenciones quirúrgicas y la necesidad de transfusiones en función del tipo de desbridamiento utilizado, mostrando resultados consistentes con la literatura previa en el caso de quemaduras pequeñas. En el grupo de grandes quemados, el desbridamiento se realizaba en tiempos sucesivos de 15-20% SCQ en áreas diferentes mediante el uso de bromelaína, hasta completar el desbridamiento completo. Encontró que el grupo desbridado enzimáticamente, con 16 casos, frente al grupo control de 21, tenía menor cantidad de cirugías, menor necesidad de transfusiones durante el ingreso y tiempos más cortos hasta lograr el desbridamiento completo. En el grupo de mayores del 15% SCQ se encontró una reducción de la necesidad de escarotomías durante el ingreso, con significación estadística.11
En esa línea, otros autores analizaron la eficacia del desbridamiento enzimático para la prevención de la aparición del síndrome compartimental en quemaduras circulares de segundo grado profundo y tercer grado, reduciendo la necesidad de realizar escarotomías en los miembros afectados.12
Algunos estudios muestran como la principal variable del gasto hospitalario en el tratamiento del gran quemado es la estancia. El impacto económico de la estancia en el tratamiento del paciente gran quemado supone el 65.8% del gasto total, repartido en un 55.6% la estancia en la Unidad de Cuidados Intensivos y un 10.2% en la planta convencional.13,14 Ojeda no observó diferencias en cuanto a estancia hospitalaria entre el grupo de desbridamiento enzimático y el grupo de tratamiento estándar, lo que se atribuyó al bajo número de pacientes y a la diferencia en superficie corporal quemada entre ambos grupos.
Con el fin de ampliar el conocimiento, específicamente en los pacientes grandes quemados, realizamos un estudio para comparar los resultados obtenidos en el tratamiento de pacientes con afectación del 20%-50% de SCQ, separados en un grupo tratado con desbridamiento enzimático y otro mediante tratamiento estándar.
Material y método
Diseñamos un estudio de cohortes retrospectivas con todos los pacientes grandes quemados del 20 al 50% de SCQ, que ingresaron en la Unidad de Quemados del Hospital Universitario La Paz en Madrid, España, entre enero de 2012 y diciembre de 2017. Incluimos 197 pacientes cuyos criterios de inclusión fueron, además de la SCQ, edad mayor de 18 años, de cualquier sexo, que presentaran quemaduras por mecanismo térmico (escaldadura, llama o contacto) y cuya profundidad fuera mayor de dérmica-intermedia; descartamos pacientes con quemaduras dérmico-superficiales.
Dividimos 2 grupos en función del tipo de desbridamiento inicial: desbridamiento tangencial como tratamiento estándar o desbridamiento enzimático utilizando Nexobrid® (Mediwound Ltd., Alemania). Determinamos el criterio de selección de los pacientes para un grupo u otro de forma temporal para evitar un sesgo de selección: para el grupo control no seleccionamos ningún paciente posterior a 2015, puesto que a partir de esa fecha se introdujo Nexobrid® en el Hospital y se podrían haber elegido pacientes descartados para tratamiento enzimático. Los grupos quedaron distribuidos en 32 pacientes en el grupo de desbridamiento enzimático y 165 en el grupo control. Todos los pacientes recibieron consentimiento informado, siendo firmado por el propio paciente si se encontraba consciente o por su familiar más directo en el caso de encontrarse bajo sedación o intubado. Obtuvimos la base de datos de forma confidencial, evitando la recogida de datos que permitiera la identificación del paciente y siendo estos anonimizados en la base. Recogimos solo los datos estrictamente necesarios para el estudio, siendo este aceptado por el Comité de Ética de nuestro hospital.
Los datos fueron obtenidos de forma retrospectiva, revisando las historias clínicas de los pacientes de la unidad, recogiendo los datos demográficos del paciente y de la quemadura: edad, sexo, índice de comorbilidad de Charlson, SCQ, mecanismo, profundidad, SCQ profunda, índice de gravedad de BAUX, así como los datos del curso clínico desde el punto de vista quirúrgico que incluían tiempo de estancia total, tiempo de estancia en Cuidados Críticos, número de intervenciones en quirófano, número de transfusiones sanguíneas (hematíes) durante el desbridamiento y durante el ingreso.
Protocolo de tratamiento quirúrgico de cada grupo
Los pacientes con SCQ por encima del 20% reciben tratamiento tras ingreso en la Unidad de Quemados Críticos en todos los casos. Una vez ingresados se inicia el tratamiento de desbridamiento quirúrgico de acuerdo a su estabilidad clínica y a la profundidad de sus quemaduras, de acuerdo a los estándares reconocidos internacionalmente, iniciándose tan pronto como es posible.
En el caso del desbridamiento tangencial convencional se realiza en quirófano de acuerdo al protocolo del hospital, en tiempos quirúrgicos sucesivos en función de la estabilidad clínica del paciente. Tras el desbridamiento el lecho se cubre de forma temporal mediante piel alogénica en forma de aloinjertos de piel parcial laminar fijada con grapas.
En el caso del grupo de desbridamiento enzimático, este se realiza en la habitación o box de la Unidad de Quemados Críticos. El protocolo de desbridamiento enzimático se realiza de acuerdo al publicado por la Guía de Consenso Europea, en tiempos quirúrgicos sucesivos de 15-20% hasta el desbridamiento completo. El protocolo de aplicación consistió en 4 fases: preparación del lecho mediante cura húmeda al menos 2 horas antes del inicio. Posteriormente se aplica Nexobrid® en un 15-20% de SCQ en proporción de 5 g por cada 3% de SCQ bajo un apósito transparente e impermeable, durante 4 horas. Se retira tras ese periodo y se aplica una nueva cura húmeda al menos otras 2 horas. Posteriormente se aplican curas cada 24-48 horas con polihexanida en gel (Prontosan® Wound Gel, B Braun Melsungen AG, Alemania). Tras 2-4 días el paciente se traslada a quirófano donde se retiran los apósitos y se cubren las heridas con aloinjertos laminares de piel criopreservada de banco fijados con grapas. El lecho se prepara mediante cepillado.
Tras la estabilización clínica del paciente en la Unidad de Quemados Críticos, se realiza de forma sucesiva la retirada de la cobertura temporal de los aloinjertos para iniciar el recambio con autoinjertos mallados con ratio 3:1 de las zonas que no pueden epitelizar de forma espontánea. Esta fase es común a ambos grupos, que son homogéneos en la cobertura temporal y definitiva elegida para el tratamiento.
Para el uso de hemoderivados se siguen las guías de recomendaciones publicadas y aceptadas en nuestro hospital para politraumatizados y quemados críticos, que implican evitar la transfusión en situaciones de estabilidad clínica y hemoglobina por encima de 8 gr/dl, salvo que se prevea sangrado activo intraoperatorio en ese momento y en pacientes con patología coronaria. Este protocolo fue aplicado a ambos grupos terapéuticos.
Las intervenciones quirúrgicas fueron programadas por el equipo de Cirugía Plástica asociado a la Unidad de Quemados para ambos grupos. Todas las intervenciones de desbridamiento tangencial se programaron en quirófano, así como las coberturas en ambos grupos. Sin embargo, el procedimiento de desbridamiento enzimático se llevaba a cabo en el box del paciente dentro de la Unidad de Quemados Críticos, no siendo necesario su traslado a quirófano para el mismo.
Por último, el alta del paciente desde la Unidad de Quemados Críticos a la planta convencional se realizó por criterios clínicos: ante la estabilidad hemodinámica del paciente, la buena tolerancia a las curas y/o la rehabilitación, con buen manejo del dolor durante las mismas.
Estadística
Recogimos todos los datos en formato Microsoft® Excel Office 365. La base fue importada y tratada mediante un software estadístico (SPSS Statistics 21.0, IBM®). Las variables cualitativas fueron medidas mediante frecuencias absolutas y relativas en forma de porcentaje y comparadas mediante test x2 de Pearson o test exacto de Fisher (si n<20 o si algún valor de la tabla de valores esperados era menor de 5). Las variables cuantitativas continuas fueron descritas como media y desviación estándar. Los análisis de comparación de medias se llevaron a cabo mediante el test no paramétrico U de Mann Whitney. Se consideraron las diferencias estadísticamente significativas con una probabilidad de error menor del 5% (p<0.05).
Resultados
Incluimos en el estudio 197 pacientes, la mayoría varones en proporción 2.7:1 y con una edad media en torno a los 50 años. El mecanismo etiológico más frecuentemente implicado en la quemadura fue la llama, seguido por la escaldadura y, de forma anecdótica, el contacto con sólido caliente. La SCQ media fue cercana al 30% (24% en el caso de la superficie con quemadura profunda entendida como mayor o igual que dérmica-profunda) y el valor del índice de gravedad ABSI (Abbreviate Burn Severity Index) medio próximo a 7 puntos. En la Tabla I pueden observarse los detalles demográficos y las características de las quemaduras de los pacientes de ambos grupos. No se encontraron diferencias estadísticamente significativas en edad, SCQ, SCQ profunda, mecanismo lesional de la quemadura ni en los diferentes índices de gravedad, aunque el análisis del índice de comorbilidad de Charlson mostraba una tendencia a mayores valores en el grupo de desbridamiento enzimático.
El análisis de los resultados clínicos en ambos grupos (Tabla II) mostró una reducción muy importante del tiempo desde el ingreso hasta la cirugía de casi 5 veces, con medias de 5.1±4.9 días en el grupo de desbridamiento convencional frente a 0.8±0.9 en el caso de desbridamiento enzimático. Los datos mostraron una clara reducción en el número de intervenciones (tiempos de cirugía llevados a cabo en quirófano) en el grupo de desbridamiento enzimático (2.6±2.1 frente a 1.9±2.0). Igualmente se observó una reducción del sangrado que se vio reflejada en una reducción estadísticamente significativa de las transfusiones de concentrados de hematíes durante el ingreso así como durante la fase de desbridamiento. En este caso observamos una reducción de casi 20 veces los valores encontrados con el desbridamiento convencional (4.7±4.4 frente a 0.2±0.7). En la figura 1 mostramos los resultados obtenidos en un paciente del grupo experimental, observando la ausencia de sangrado tras la retirada de Nexobrid®. Vimos también estos resultados en el reemplazo hemático con plasma y plaquetas, con reducciones de entre 10 y 20 veces (Grafíco 1).

Figura 1. Paciente de 92 años con quemaduras de 24% de SCQ por llama, dérmico-profundas con áreas subdérmicas, circulares en piernas que precisó de escarotomías. Se realizó desbridamiento tangencial y cobertura con autoinjertos. Se muestra el aspecto al ingreso a la izquierda tras escarotomías y a los 6 meses del tratamiento
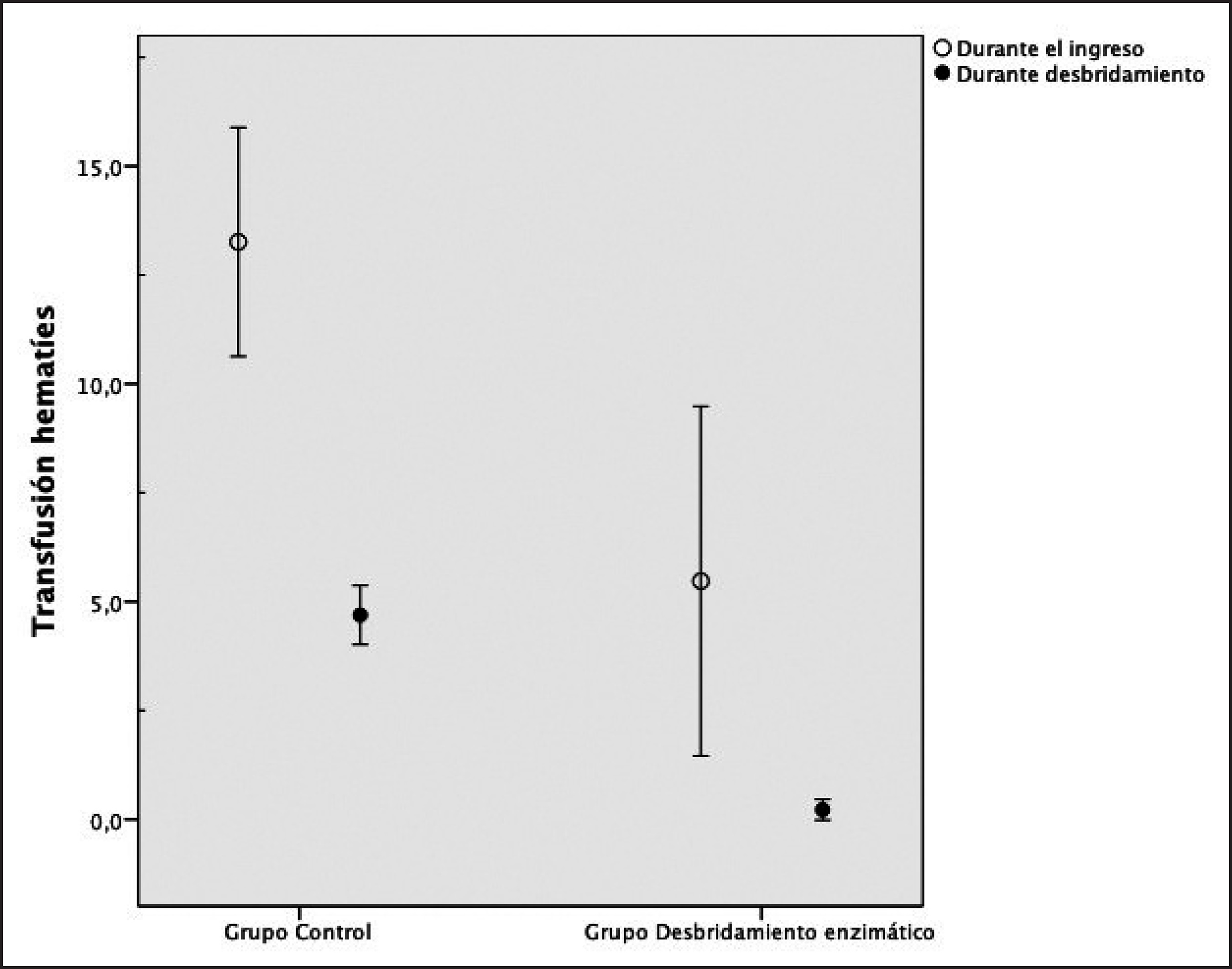
Grafíco 1. Representación de las transfusiones de hematíes. Se representa la media y el intervalo al 95% de las transfusiones realizadas durante el tiempo hasta desbridamiento completo, o bien durante todo el ingreso en ambos grupos. La diferencia es estadísticamente significativa con p<0.05 para ambas variables
En el estudio comprobamos también una reducción del 60% de la necesidad de escarotomías, con 48 casos en el grupo convencional (29.1%) frente a 3 casos en el grupo de desbridamiento enzimático (9.4%), con diferencias estadísticamente significativas entre ambos. En la figura 2 mostramos 1 paciente del grupo control con escarotomías en miembros inferiores.
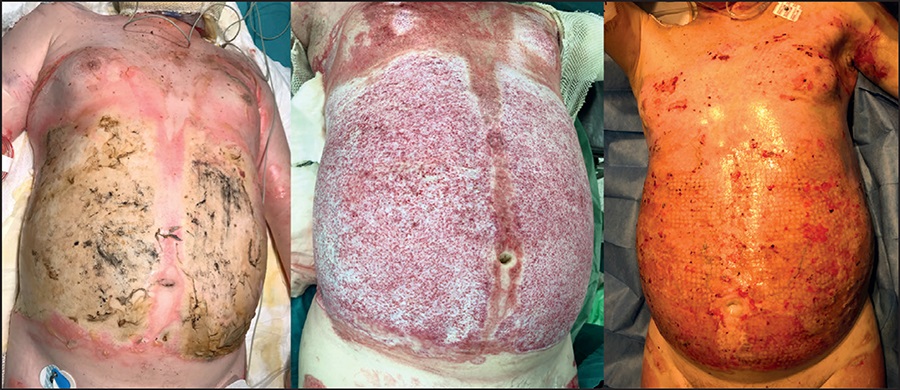
Figura 2. Paciente de 64 años con quemaduras por llama del 47% SCQ, dérmico-profundas. Se muestra la imagen al ingreso a la izquierda; tras la retirada de Nexobrid® que fue aplicado a las 24 horas del ingreso (centro) y el resultado a los 30 días, tras cobertura con injertos tipo Meek 6:1
La evaluación de la agresividad quirúrgica, el sangrado, el número de intervenciones, así como el de reemplazo hemático mostraba una mejora estadísticamente significativa respecto al grupo control. Observamos una reducción de los días de ingreso de los pacientes en el grupo de desbridamiento enzimático, con reducciones de la estancia en UCI de 31.4±38.6 días a 20.2±19.2 días, también con significación estadística (Gráfico 2).
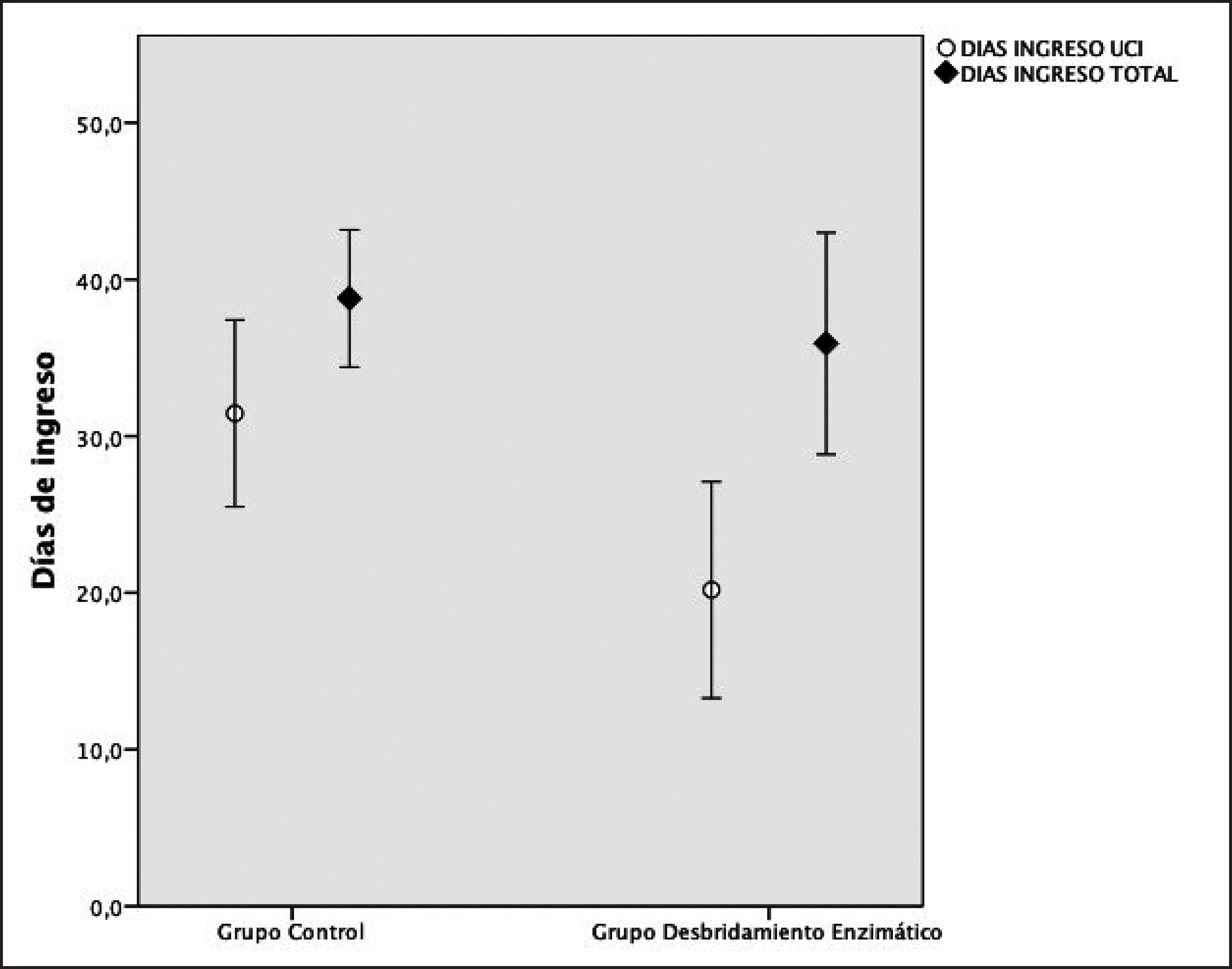
Grafíco 2. Días de ingreso por grupos. Se compara los días de ingreso en Unidad de Cuidados Críticos así como los días de ingreso totales en el hospital. Se observan diferencias estadísticamente significativas en el número de días de ingreso en Unidad de Críticos (p<0.05) aunque no en la estancia global
Finalmente, a pesar de encontrar mejoras en la precocidad del desbridamiento, con menores tiempos quirúrgicos, menos escarotomías, menos días de ingreso en Unidad de Cuidados Críticos, así como menor número de transfusiones tanto en el procedimiento de desbridamiento como en el ingreso total, no encontramos diferencias en las tasas de mortalidad, con 41 fallecimientos en el grupo control (24.8%) frente a 5 en el grupo experimental (15.6%). Si bien existe una aparente tendencia a la reducción de las tasas de mortalidad, no pudimos demostrar esta diferencia de forma estadística (p=0.19).
Discusión
Desde la década de los 70, el tratamiento estándar del paciente quemado ha consistido en el desbridamiento tangencial hasta alcanzar tejido sano sobre el cual poder injertar piel autóloga para conseguir cobertura. Sin embargo, como se ha demostrado en estudios histológicos, este desbridamiento implica la retirada de tejido sano en muchas ocasiones, reduciendo la posibilidad de epitelización espontánea. Con la aparición de Nexobrid® para desbridamiento enzimático se encontró que, conservando mayor cantidad de dermis viable, se mantenía un mayor potencial de epitelización espontánea, especialmente en pacientes con dermis gruesa y con mayor cantidad de anejos cutáneos. Esta circunstancia se daba especialmente en pacientes con quemaduras dérmico-intermedias y dérmico-profundas.15
Los ensayos clínicos con desbridamiento enzimático en pacientes con quemaduras inferiores al 15% de SCQ han demostrado que su uso reduce la cantidad de tiempos quirúrgicos así como el sangrado y la necesidad de injertos, acortando el tiempo hasta desbridamiento completo respecto al tratamiento estándar. Más específicamente se consigue una disminución en el tiempo hasta alcanzar la retirada de toda la escara por quemadura de 8.7 a 2.2 días, lo que trae consigo la reducción de la carga de tejido necrótico en el paciente. Esta precocidad en el desbridamiento ha constituido el eje central del desbridamiento estándar, que debe ser lo más precoz posible y que tal y como se demostró en los trabajos de Barret, supone una reducción de la estancia y de las complicaciones infecciosas.16 Sin embargo, este desbridamiento está condicionado por la estabilidad clínica del paciente para poder afrontar un tratamiento tan agresivo.
La mayor parte de las publicaciones hasta el momento actual se han centrado en el tratamiento de pacientes con quemaduras inferiores al 15% de SCQ, aunque existen comunicaciones de series pequeñas con superficies mayores. Los resultados en pequeños quemados son excelentes en cuanto a sangrado y necesidad de injertos, por lo que la necesidad de extender el tratamiento a pacientes con superficies quemadas mayores parece más que razonable. Los resultados preliminares de nuestra serie, publicados por Ojeda en 2017, mostraron una eficacia por encima del 95% en cuanto a desbridamiento completo de las quemaduras, permitiendo el inicio muy precoz del mismo y la reducción del tiempo medio hasta cirugía de 4.76 a 0.93 días.11
En el estudio actual hemos recogido sólo los pacientes grandes quemados de 20%-50% de SCQ para poder compararlos con el grupo control de tratamiento estándar. Y, si bien las cifras varían al aumentar el número de pacientes respecto a los trabajos previos, hemos encontrado que se reduce de 5.3±5.0 a 0.9±1.0 días, con diferencias estadísticamente significativas. Este resultado está en la línea de todas las publicaciones con Nexobrid® hasta el momento, lo que pone de manifiesto la facilidad de uso de forma precoz para poder comenzar el desbridamiento desde las primeras 24 horas. A su vez, esto hace posible que podamos afirmar que permite mejorar los tiempos con respecto al tratamiento estándar.
La precocidad en su aplicación, así como la eficacia mostrada en los estudios experimentales y clínicos, ha permitido la posibilidad de expandir la indicación a situaciones muy precoces, en las que el riesgo de desarrollo de síndrome compartimental en pacientes con quemaduras circulares es alto. De hecho, algunas publicaciones muestran cómo la indicación de uso del desbridamiento enzimático puede incluir estas situaciones precoces al ingreso del paciente. A pesar de que las recomendaciones para el uso de Nexobrid® incluyen una cura húmeda precoz de 2 horas o más, en aquellos casos en los que existe riesgo de síndrome compartimental las guías clínicas publicadas hasta el momento recomiendan su aplicación sin esperar ese tiempo, siempre y cuando las condiciones clínicas lo permitan. El riesgo de desarrollo de un aumento de la presión compartimental, especialmente en grandes quemados, se produce por dos mecanismos: la disminución del continente por la contractura de la quemadura circular y el aumento del contenido por la elevación de la presión debido al edema secundario.17 Como ya hemos mencionado, existen algunos trabajos que analizan la eficacia del desbridamiento enzimático para la prevención de la aparición del síndrome compartimental en quemaduras circulares. Sin embargo, algunos de ellos no hacen distinción entre quemados por debajo o por encima del 20% de SCQ en los que se puede sumar el riesgo de síndrome compartimental por edema tras la reposición hídrica y resucitación del paciente.12 Fisher y col. publicaron su estudio sobre 20 extremidades superiores en 13 pacientes con riesgo de síndrome compartimental, con una SCQ media del 21%. Encontraron liberación del compartimento en todos los casos sin necesidad de realizar escarotomías quirúrgicas secundarias. El seguimiento se realizó solamente en 9 pacientes por pérdida del resto, con resultados funcionales cercanos a la recuperación completa. Los autores concluyeron que, respetando los criterios de exclusión (traumatismo eléctrico, aplastamiento o escaras muy secas), el desbridamiento enzimático es eficaz en la prevención del síndrome compartimental, sin necesidad de convertir el tratamiento a una escarotomía quirúrgica.18 Sin embargo, en esta serie no se hacía comparación con respecto al tratamiento estándar. En la serie actual mostramos que el uso precoz del desbridamiento enzimático contribuye a disminuir la incidencia de escarotomías del 29.1% al 9.4% de manera estadísticamente significativa.
La indicación de escarotomía no desaparece totalmente en el grupo de desbridamiento enzimático por dos razones: la primera es que en muchos casos la escarotomía se realiza antes del traslado a nuestro hospital; la segunda es que en aquellos casos en los que se eleva la presión compartimental por encima de los 40 mmHg durante el traslado y la resucitación inicial, existe indicación de descompresión quirúrgica, por lo que la aplicación del desbridamiento enzimático se hace con posterioridad a la descompresión. Hasta el momento no existen estudios específicos del uso de Nexobrid® como tratamiento del síndrome compartimental, por lo que no está contemplado como primera línea de tratamiento en estos casos. Todas las publicaciones muestran la eficacia como profilaxis en el desarrollo del cuadro en casos de quemaduras circulares. Por tanto, sería deseable el diseño de estudios prospectivos que permitan comparar la efectividad de la liberación de la presión compartimental entre la escarotomía quirúrgica y la escarectomía enzimática.
Desde el ensayo clínico publicado por Rosemberg se ha comprobado que el uso de Nexobrid® reduce la necesidad de injertos debido a la conservación de la dermis sana no quemada, que preserva parte del potencial para la reepitelización desde los remanentes de dermis. Esta capacidad está también en clara relación con la extensión de zona quemada, puesto que una parte de la epitelización ocurre desde el lecho y otra desde los bordes de la herida. Este potencial de epitelización se ve también en grandes quemados. En el estudio actual observamos cómo se reduce la necesidad de tiempos quirúrgicos para alcanzar cobertura completa de 2.6± 2.1 en el grupo de tratamiento estándar a 1.9± 2.0 en el grupo de desbridamiento enzimático. Aunque existe una reducción estadísticamente significativa en el número de intervenciones, esta diferencia no es tan grande si la comparamos con los resultados publicados por otros grupos en quemados de menor superficie corporal. Este resultado parece estar en relación con una superficie cruenta mayor, que necesita tiempos demasiado prolongados para su reepitelización, por lo que se requieren injertos en un mayor número de ocasiones. Además, en grandes quemados la necesidad de injertos es mayor en cualquiera de los dos grupos, por lo que las diferencias en cuanto a tiempos quirúrgicos quedan reducidas.
El desbridamiento tangencial supone el tratamiento estándar del paciente quemado. El comienzo precoz del mismo es la piedra angular del tratamiento quirúrgico del paciente quemado desde los trabajos de Herndon, ya que la precocidad se relaciona con la disminución del sangrado que se estima como 0.5 ml por cada cm2 de piel desbridada.19 Los resultados con Nexobrid® muestran una reducción del sangrado en los ensayos clínicos respecto al tratamiento estándar que también se observó en la serie publicada por Ojeda. En el trabajo actual los resultados demuestran cómo la necesidad de derivados hemáticos se reduce durante toda la estancia del paciente de 13.3±17.1 concentrados en el grupo control a 5.5±11.13 en el grupo de desbridamiento enzimático, lo que sugiere que el desbridamiento precoz y la reducción de la cantidad de cirugías trae consigo una disminución de las necesidades de transfusión. Si se analiza sólo el tiempo hasta desbridamiento completo, observamos cómo el procedimiento con Nexobrid® tiene una menor tasa de transfusiones que se reducen de 4.7±4.4 concentrados en el grupo control a 0.2±0.65. La reducción de las transfusiones a lo largo del ingreso no se explica sólo por la ausencia de sangrado en el momento del desbridamiento y, aunque pueden existir más factores implicados, la precocidad, la reducción de la agresividad en el desbridamiento y la disminución del número de intervenciones tendrían un papel relevante en la estabilidad clínica y en la reducción del uso de hemoderivados durante el ingreso.
Por último, cabría pensar que todas estas diferencias encontradas hasta el momento podrían tener alguna influencia sobre la estancia hospitalaria. De hecho, esta variable es la más importante relacionada con el gasto en el tratamiento del paciente quemado. Estudios previos han mostrado cómo el costo de la atención sanitaria que precisa un paciente quemado es muy elevado. En concreto, la estancia hospitalaria supone el factor más determinante en el gasto total empleado en esa asistencia.20 Nuestro grupo analizó el coste de los pacientes quemados tratados con Nexobrid® y observó que la estancia en UCI constituía el 55.6% del gasto total por cada paciente.13 Al analizar los resultados del trabajo actual observamos que, si bien la estancia hospitalaria global es similar en ambos grupos, el tiempo de estancia en la Unidad de Quemados Críticos se redujo de forma estadísticamente significativa de 31.5±38.6 días a 20.2±19.2 días, lo que supone una reducción del 36%. Existen numerosos factores implicados en la duración de la estancia en la Unidad de Quemados Críticos que no han sido analizados en este estudio, aunque parece que los efectos beneficiosos relacionados con la menor agresividad en el grupo Nexobrid® respecto al grupo control podrían tener un papel protagonista en este hallazgo. En esta misma línea observamos una tendencia a la disminución de la mortalidad, aunque las diferencias no fueron estadísticamente significativas.
Este trabajo presenta algunas limitaciones a pesar de las diferencias estadísticamente significativas encontradas entre ambos grupos. En primer lugar, se trata de un estudio retrospectivo, por lo que sus hallazgos deben tratarse con cautela a la hora de extraer conclusiones extrapolables a otras Unidades de Quemados. A pesar de la homogeneidad en cuanto a las características de ambos grupos, se trata de dos cohortes evaluadas de forma retrospectiva consecutiva (de años diferentes), por lo que podría existir un sesgo de tratamiento en cuanto a la diferencia en la experiencia técnica del equipo sanitario que atiende al paciente. Por último, la estancia tanto global como en la Unidad de Quemados Críticos viene determinada por multitud de factores relacionados con la evolución clínica del paciente quemado, por lo que las diferencias encontradas tras analizar 197 pacientes podrían estar influenciadas por diferentes condicionantes propios de este tipo de patología (complicaciones infecciosas, comorbilidades, etc…) que no han sido tenidos en cuenta en este análisis.
Conclusiones
La aplicación precoz del desbridamiento enzimático en grandes quemados, con superficies quemadas de entre el 20 y el 50%, favorece la escarectomía completa del paciente de forma más rápida y precoz que en el caso del tratamiento estándar de desbridamiento tangencial, con una disminución clara de las necesidades de hemoderivados. Su aplicación puede reducir significativamente los tiempos quirúrgicos y la necesidad de escarotomías.
Por último, la menor agresividad quirúrgica parece disminuir la estancia en la Unidad de Quemados Críticos, aunque no encontramos diferencias en cuanto a mortalidad o estancia hospitalaria global.

















