Introducción
La viabilidad del complejo areola pezón (CAP) es un aspecto de vital importancia en cirugía mamaria.(1) Las diferentes técnicas quirúrgicas descritas para mastopexia se clasifican según el tamaño de la cicatriz resultante en: circumareolar, circumvertical, en J y en T invertida y además, según el pedículo que contiene el CAP en: técnicas de pedículo superior, súpero-medial, súpero-lateral, bipedículado, central e inferior.(2) La principal fuente de aporte sanguíneo del CAP viene dada por arterias ramas de la mamaria interna en un 60% y ramas de la torácica lateral en un 30%.(3,4) Sin embargo, sabemos que existen variantes anatómicas que no siguen esta distribución porcentual y por el contrario, se pueden presentar patrones erráticos de vasculazión.(4,5)
En los años 60 se aseveraba que la vascularización del CAP. se restituía totalmente al pasar al menos 10 años de una cirugía mamaria y describían que era seguro plantear nuevas cirugías confiando en cualquiera de los pedículos vasculares pasado ese tiempo. En un estudio previo,(6) publicado en esta misma revista, presentamos, mediante el uso de mamografía 3D, cómo la revascularización de los CAP después de una mastopexia no siempre es ad-integrum y que en efecto, existen patrones vasculares distintos en algunas pacientes después de someterse a cirugía mamaria, posiblemente debido al propio evento de cicatrización de los tejidos y a factores individuales. Siendo de vital importancia conocer previamente el pedículo dominante y el calibre de sus vasos cuando vamos a planificar una mastopexia, más aún cuando existen antecedentes de cirugías mamarias previas, se han intentado otros estudios con esta finalidad como el ecodoppler(7) y la resonancia magnética.(5)
En nuestra Unidad de Cirugía Plástica y Postbariátrica de Caracas, Venezuela, estructuramos protocolos estrictos en cirugía mamaria, incluyendo el estudio previo de las mamas con mamografía 3D (tomomamografía), terapia de oxígeno hiperbárico, hemoglobina por encima de 12 gr/dl y elegimos el pedículo vascular a preservar basándonos en 3 variables: el grado de ptosis, la flacidez del polo inferior y el patrón vascular visualizado en la tomomamografía(6) Como parte de una línea de investigación en nuestra Unidad, empleamos el uso de pentoxifilina intradérmica, un medicamento con funciones hemorreológicas, para mejorar las condiciones de los tejidos y de los CAP al detectar signos clínicos de compromiso vascular en el intra o postoperatorio. Aun así, la complicación de la necrosis del CAP. existe, entre un 1.1%. de necrosis parcial y un 1.1% de necrosis total, dando un total en nuestra experiencia de un 2.2%.
Existen métodos para evaluar la circulación de los tejidos ya no solo de forma previa a la cirugía, sino durante el transoperatorio, como son: la colorimetría,(8) método no invasivo que utiliza un patrón de color para evaluar los cambios de perfusión tisular a través de una tabla; la indocianina verde,(9) medio de contraste que se administra para evaluar la penetración en el tejido; y la termografía.(10) Las cámaras térmicas miden la longitud de onda de la radiación infrarroja emitida desde un objeto o sitio y calculan su temperatura. Evaluando la temperatura, se evalúa indirectamente la vascularización subyacente, pudiendo de esa manera detectar el compromiso vascular en los colgajos y permitiendo tomar decisiones que mejoren la viabilidad de los mismos.(11)
El interés del estudio que presentamos es evaluar la utilidad de la fotografía térmica en el monitoreo de la temperatura de los CAP en un grupo de pacientes sometidas a cirugía mamaria y la posibilidad de agregar esta tecnología como una nueva herramienta que nos aporte mayor seguridad y complemente nuestros protocolos como predictor del compromiso vascular de los CAP durante la cirugía de mastopexia.
Material y método
Estudio prospectivo observacional en 37 pacientes (74 mamas) sometidas a mastopexia con Técnica Reglada(12) en la Unidad de Cirugía Plástica y Postbariátrica de Caracas,Venezuela.
Realizamos mediciones de temperatura utilizando la cámara térmica portátil para teléfono inteligente Flirone pro®, modelo 435-0004-03m y el teléfono de marca Apple®, Iphone 12, versión 16.1.1
Las fotografías fueron realizadas por el mismo operador, a 20 cm de distancia de la mama, centradas en el CAP con la ayuda de un instrumento de manera referencial sobre el pezón para su correcta localización y centrado de la foto. Esperamos entre 30 y 40 segundos a la calibración estable del registro de temperatura y realizamos 3 fotografías térmicas en cada mama en cada una de las 37 pacientes (74 registros): una foto térmica antes de comenzar la cirugía con la paciente ya anestesiada, otra a la mitad de la cirugía (en el momento de cuadrar la vertical o mástil) y una tercera al terminar la cirugía. Cada foto térmica se acompañó de una fotografía del momento quirúrgico. Registramos también la temperatura de quirófano en cada caso.
Evaluamos los signos clínicos de compromiso vascular: palidez del CAP. y disminución del llenado capilar. Al momento de aparecer signos clínicos de posible compromiso vascular, procedimos a la aplicación del esquema de pentoxifilina intradérmica a una dilución de 1 cc en 0.5 cc de cifarcaína al 1%, esperamos aproximadamente 2 minutos y evaluamos nuevamente los signos clínicos de posible compromiso vascular y realizamos nueva foto térmica.
Archivamos todas las fotos en el en el teléfono inteligente. Los datos fueron registrados en fichas de recolección (Tabla I) y posteriormente diagramados en Excel® y enviados a análisis por un estadístico de la Universidad Central de Venezuela.
Tabla I. Ficha empleada para registro de las fotos térmicas.
|
Nombre: Edad: Tipo de cirugía: Pedículo utilizado: Con o sin implantes: Tamaño del implante: Temperatura de quirófano: | |
| Mama derecha | Mama izquierda |
| Temperatura previa: | Temperatura previa: |
| Temperatura punto mástil/intermedia: | Temperatura punto mástil/intermedia: |
| Temperatura final: | Temperatura final: |
| Evolución transoperatoria: | Evolución transoperatoria: |
| Colocación de pentoxifilina: | Colocación de pentoxifilina: |
| Evolución postoperatoria: | Evolución postoperatoria: |
Resultados
La edad media de las pacientes del grupo de estudio fue de 43 años (rango de 23 a 60 años). A todas se le realizó mastopexia: 30 con implantes mamarios y 7 sin implantes, y en todas ellas se empleó la Técnica Reglada.(12)
La temperatura promedio de quirófano fue de 16.6 ºC (rango de 14.7 a 18.3). Las temperaturas registradas con la cámara térmica en cada mama al inicio, durante (cierre del mástil o cicatriz vertical) y al final de la cirugía, fueron las siguientes: en mama derecha, la temperatura inicial fue 26.3±2.5 ºC, al momento mástil 22.9 ± 1.9 ºC y al momento de la finalización de la cirugía 23.2 ± 1.9 ºC. En la mama izquierda, la temperatura inicial fue 26.5 ± 2.7ºC, al momento mástil 23.2 ± 2.1 ºC y al momento de la finalización de la cirugía 23.4 ± 2.1 º (Tabla II).
Tabla II. Distribución de pacientes según estadísticos descriptivos de temperatura del CAP.
| Temperatura | Mínimo | Máximo | Media | Desviación estándar |
|---|---|---|---|---|
| De quirófano | 14.7 | 18.3 | 16.6 | 1.0 |
| Mama derecha | ||||
| Inicial | 21.0 | 31.9 | 26.3 | 2.5 |
| Mástil | 19.7 | 27.7 | 22.9 | 1.9 |
| Final | 19,9 | 27,6 | 23,2 | 1,9 |
| Mama izquierda | ||||
| Inicial | 22.3 | 32.5 | 26.5 | 2.7 |
| Mástil | 18.8 | 27.1 | 23.2 | 2.1 |
| Final | 19.0 | 28.6 | 23.4 | 2.1 |
Observamos una diferencia de temperatura promedio de <3.1 grados entre el inicio y el final de la cirugía, relacionando ambas mamas. En la Fig. 1 se pueden apreciar los cambios de temperatura al inicio, intermedio y final de la cirugía de ambas mamas y la fotografía normal que acompaña a cada etapa, donde no se aprecian cambios clínicos del CAP.
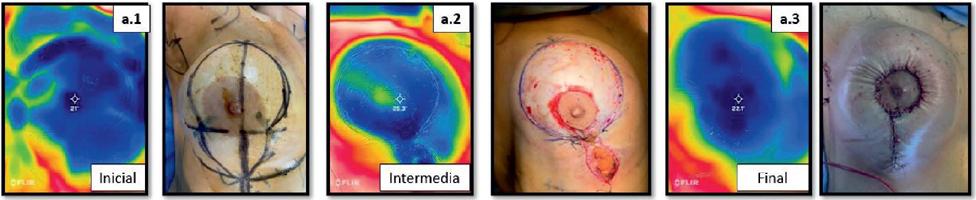
Figura 1 A. Mama derecha, foto térmica y foto normal: (a1) Inicial, (a2) intermedia, (a3) final de cirugía. Mastopexia según Técnica Reglada, recambio de implantes de 450 cc a 440 cc, plano submuscular modificado y cicatriz circumvertical.
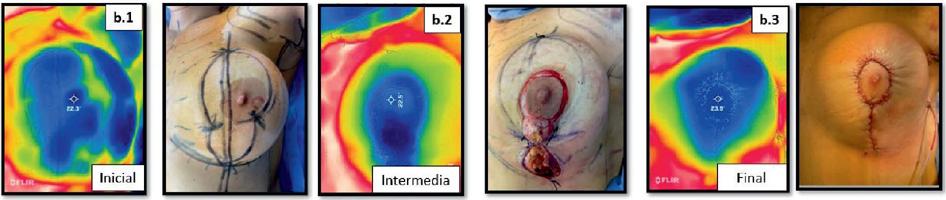
Figura 1 B. La misma paciente, mama izquierda, foto térmica y foto normal: (b1) inicial, (b2) intermedia, (b3) final de cirugía.
En 3 pacientes se presentó en el postoperatorio inmediato signos clínicos de compromiso vascular: palidez, cambio de color en comparación con el CAP contralateral y retardo en llenado vascular. Describimos estas pacientes a continuación.
Caso 1. Paciente sometida a mastopexia por Técnica Reglada con resultante de cicatriz en T invertida, recambio de implantes de 485 cc a 475 cc. El CAP derecho mostró signos clínicos de compromiso vascular, temperatura inicial de 25.6 ºC, intermedia/mástil de 20 ºC y final de 20.4 ºC, con una diferencia de 5.2 ºC entre la inicial y la final. Aplicamos tratamiento con pentoxifilina según pauta y esperamos aproximadamente 3 minutos; retomamos foto térmica con una lectura de 23.3 ºC. Evidenciamos una recuperación de 2.9 ºC después del tratamiento y una mejoría de los signos clínicos (Fig. 2 A y B).
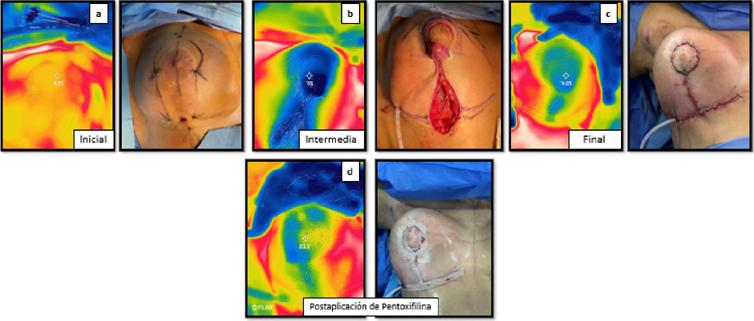
Figura 2 A. Caso 1, mama derecha: CAP con signos clínicos de compromiso vascular, (a) temperatura inicial 25.6ºC; (b) intermedia/mástil 20ºC y (c) final 20.4ºC: diferencia de 5.2ºC entre la inicial y la final. Tratamiento con pentoxifilina; tras 3 minutos, foto térmica (d) con lectura de 23.3ºC, recuperación de 2.9ºC y mejoría de los signos clínicos
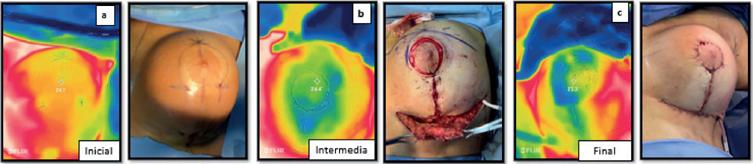
Figura 2 B. Caso 1, mama izquierda: foto térmica y foto normal:(a) inicial, (b) intermedia, (c) final de cirugía.
Caso 2. Paciente sometida a mastopexia por Técnica Reglada con resultante de cicatriz circumvertical, recambio de implantes de 375 cc a 335 cc. C.A.P izquierdo con signos clínicos de compromiso vascular. Temperatura inicial de 24.1 ºC, intermedia/mástil de 24.9 ºC y final de 20.9 ºC. Aplicamos tratamiento con pentoxifilina según pauta, esperamos aproximadamente 3 minutos y retomamos foto térmica con una nueva lectura de 22.2 ºC Una recuperación de 1.3 ºC, aunque los signos clínicos mejoraron levemente. La diferencia de temperatura entre el inicio y el final fue de 3.2 ºC, recuperándose el CAP posterior al tratamiento con evolución sin inconvenientes (Fig. 3 A y B).
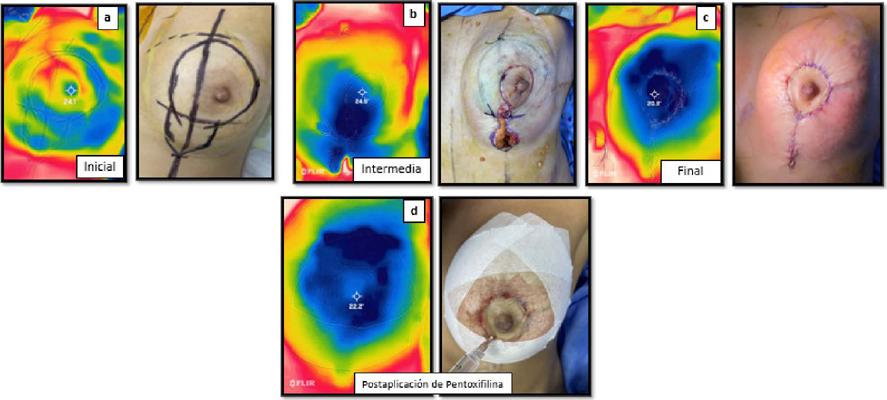
Figura 3 A. Caso 2, mama izquierda: (a) preoperatorio, (b) tras realización del mástil, (c) signos clínicos de palidez del CAP, (d) tras aplicación de pentoxifilina (3 minutos), foto térmica (d) con nueva lectura de 22.2ºC, recuperación de 1.3ºC, aunque los signos clínicos mejoraron levemente.
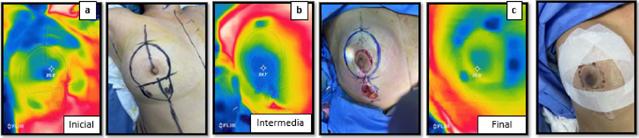
Figura 3 B. Caso 2, mama derecha, foto térmica y foto normal:(a) inicial, (b) intermedia, (d) final de cirugía.
Caso 3. Paciente postbariátrica sometida a mastopexia con Técnica Reglada con implantes de 380 cc con resultante de cicatriz circumvertical. CAP. derecho con signos clínicos de compromiso vascular. Temperatura inicial de 25.1 ºC, intermedia/mástil de 22.7 ºC y final de 21.3 ºC. Aplicamos tratamiento con pentoxifilina según pauta, esperamos aproximadamente 3 minutos y retomamos foto térmica con una nueva lectura de 23.1 ºC. Una recuperación de 1.8 ºC; aunque los signos clínicos mejoraron levemente, la paciente evolucionó satisfactoriamente en el postoperatorio. La diferencia de temperatura entre el inicio y el final fue de 3.8 ºC, recuperándose tras el tratamiento con nueva foto térmica a las 24 horas en la que se registraron 27.1ºC (Fig. 4).
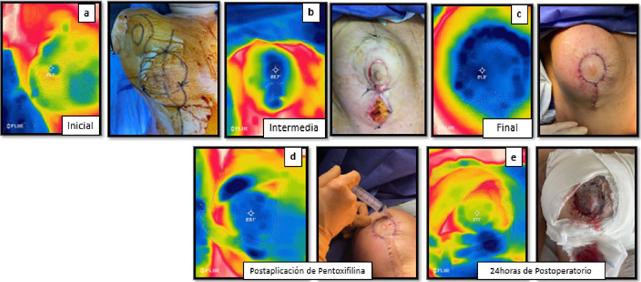
Figura 4 A. Caso clínico 3, mama derecha: (a) preoperatorio, (b) a la realización del mástil, (c) final con signos clínicos de palidez del CAP (d) Aplicación de pentoxifilina, y a los 3 minutos, nueva foto térmica con recuperación de 1.8ºC. A las 24 horas, nueva foto térmica (e) con recuperación clínica.
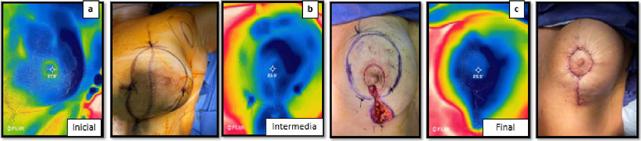
Figura 4 B. Caso clínico 3, mama izquierda: foto térmica y foto normal: (a) inicial (b) intermedia, (c) final de cirugía.
El promedio de diferencial de temperatura entre inicial y final de estas 3 pacientes con evidencia clínica de cambios de perfusión de los CAP, fue de 5.2 ºC en el caso 1, en el caso 2 de 3.2 ºC y en el caso 3 de 3.8 ºC, es decir, en promedio superior a 4 ºC de diferencial. En el resto de las pacientes, en las que los CAP no presentaron signos clínicos de cambios de flujo sanguíneo encontramos un diferencial entre la temperatura inicial y la final < 3.1 ºC (Gráficos 1 y 2).

Gráfico 1. Diferencia media de temperatura de acuerdo a la evolución del CAP en las 3 pacientes con evidencia clínica de cambios de perfusión (mama derecha).
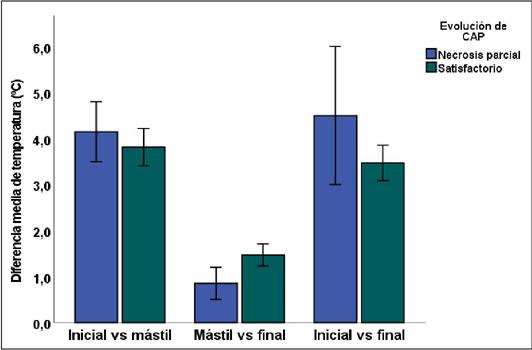
Gráfico 2. Diferencia media de temperatura de acuerdo a la evolución del CAP en las 3 pacientes con evidencia clínica de cambios de perfusión (mama izquierda).
Evaluamos el tamaño del efecto del diferencial de temperatura entre el momento inicial y final en las 3 pacientes que presentaron cambios clínicos que respondieron a tratamiento; para un cambio medio de temperatura mayor de 4 ºC, el estadístico de tamaño de efecto de Cohen fue 1.10 (IC-95%: 0.68 – 1.50) que de acuerdo a la interpretación de Sawilosky fue un efecto grande, clínicamente por la respuesta experimentada en el ascenso de temperatura posterior a tratamiento y en la mejoría de los signos clínicos y evolución satisfactoria.
Discusión
La necrosis parcial o total del CAP es una complicación muy temida en la cirugía de reducción y pexia mamaria que puede provocar una deformidad estética importante y una afectación psicológica para las pacientes.
En nuestra experiencia, todo aquello que ayude a prevenirla se suma para la seguridad de los resultados. Los métodos descritos para determinación de flujo en los tejidos y viabilidad de los colgajos, como la colorimetría, método no invasivo que mide una escala de color para determinar la viabilidad tisular, el uso de la indocianina verde y la termografía, ofrecen parámetros que tienen utilidad en la práctica diaria. Sin embargo, no aportan la relación entre temperatura y flujo vascular de los tejidos, siendo, en nuestra opinión, métodos poco fidedignos si queremos evaluar el riesgo de necrosis en tiempo real.
La termografía es un método sencillo y práctico que se ha utilizado para medir temperatura y flujo sanguíneo en los colgajos; a mayor temperatura mayor flujo sanguíneo y a menor flujo sanguíneo menor temperatura. Weerd Mercer y col.(11) determinaron zonas calientes de mayor flujo en colgajos viables y zonas frías en colgajos comprometidos. Aunque lo describen como un método subjetivo al no poder cuantificar la variación de temperatura relacionada al diferencial de flujo, sirvió de guía en la supervivencia de los tejidos en los casos estudiados. Souza y col.(13) describen que el uso de la termografía para medir temperatura en mamas determinó que existen varios factores que influyen en la temperatura en cada individuo, encontrando variaciones de entre 16 y 26 grados en las salas operatorias que influyeron en variaciones de temperatura corporal de los pacientes y no lograron establecer un método matemático para confirmar la temperatura ideal de la mama.
En nuestro estudio logramos estandarizar la temperatura de quirófano entre 16 y 18 ºC; para estabilizar esa variable en la monitorización del flujo vascular del CAP, realizamos mediciones iniciales, durante y al término de la cirugía mamaria, logrando determinar un promedio de variación de 3.1 ºC de temperatura entre el comienzo y el final de la cirugía en todas aquellas pacientes con signos clínicos de estabilidad de flujo sanguíneo del CAP, no así en las pacientes que presentaron signos clínicos de déficit de flujo (palidez y retardo en el llenado capilar) que tuvieron un diferencial de más de 4 ºC. Aunque por motivos éticos, no quisimos dejar evolucionar espontáneamente los 3 casos mencionados para comprobar si en efecto irían a presentar necrosis, es evidente y consideramos un efecto importante el hecho de que el diferencial > 4 ºC estuviese relacionado con los cambios clínicos observados.
Según describe Espinoza,(9) un tejido con compromiso de flujo vascular presentará consecuencias en un período no superior a 16 horas y pierde la posibilidad de supervivencia, por lo cual es importante diagnosticar a través de un método simple, seguro y sencillo como es la termografía durante el acto quirúrgico, y de una manera más objetiva podremos predecir un posible compromiso vascular y actuar inmediatamente para restaurar el flujo sanguíneo del CAP.
Conclusiones
Mantenerse a la vanguardia en la seguridad de la especialidad es un hecho que nos compromete, y día a día hay que intentar todo lo que esté a nuestro alcance para ofrecer a nuestros pacientes procedimientos seguros y no dejar al azar lo que podamos predecir.
En nuestro estudio logramos estandarizar la temperatura de quirófano y realizamos mediciones iniciales de temperatura mamaria con cámara térmica antes, durante y al termino de la cirugía de mastopexia según Técnica Reglada, logrando medir un promedio de variación de 3.1 ºC de temperatura entre el comienzo y el final de la cirugía en todas aquellas pacientes con signos clínicos de estabilidad de flujo sanguíneo del CAP, y un diferencial de más de 4 ºC en pacientes que presentaron signos clínicos de déficit de flujo (palidez y retardo en el llenado capilar).
En nuestra experiencia, agregar en nuestro arsenal de opciones la cámara térmica nos permite dar un criterio menos subjetivo a los parámetros clínicos que pueden ser predictivos de compromiso vascular o déficit de flujo sanguíneo del CAP en cirugía mamaria, favoreciendo su tratamiento de manera oportuna y eficaz.















