Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO  Similares em Google
Similares em Google
Compartilhar
Revista Española de Enfermedades Digestivas
versão impressa ISSN 1130-0108
Rev. esp. enferm. dig. vol.97 no.3 Madrid Mar. 2005
|
TRABAJOS ORIGINALES |
Una estrategia para mejorar la detección de hepatotoxicidad por medicamentos
A. Ruiz Montero, J. A. Durán Quintana, M. Jiménez Sáenz1 y J. A. Abadín Delgado
Servicios de Farmacología Clínica y 1Aparato Digestivo. Hospital Universitario Virgen Macarena. Sevilla
RESUMEN
Objetivos: comunicar una nueva estrategia para la detección de reacciones hepatotóxicas por medicamentos que mejora los resultados obtenidos con otros métodos utilizados.
Diseño: el modelo se basa en la identificación de una señal de alerta simple en los pacientes de varios servicios diana, durante 12 meses. Cada paciente fue posteriormente entrevistado siguiendo un protocolo específico. Se analizaron: los fármacos sospechosos de producir hepatotoxicidad, la relación de causalidad entre el fármaco sospechoso y la hepatotoxicidad, la gravedad y la incidencia de hepatotoxicidad medicamentosa/100.000 habitantes.
Pacientes: la población del área de influencia de nuestro hospital (519.381 habitantes).
Resultados: se encontraron 80 sospechas de reacciones hepatotóxicas a medicamentos. La relación de reacciones confirmadas/sospechadas fue de 35/80. El fármaco imputado con mayor frecuencia fue amoxicilina/clavulánico (4 casos). En relación al grado de imputabilidad, 2 sospechas fueron calificadas como definitivas y 14 como probables. Según la gravedad, se encontraron 6 reacciones graves y 29 leves. La incidencia de reacciones hepatotóxicas por medicamentos/100.000 habitantes (6,74) fue mucho mayor que las obtenidas con otros métodos.
Conclusiones: la aplicación de este método mejora la detección de reacciones hepatotóxicas por medicamentos y podría ser empleado en otros tipos de reacciones adversas.
Palabras clave: Hepatotoxicidad medicamentosa. Farmacovigilancia.
INTRODUCCIÓN
La hepatotoxicidad es una de las reacciones adversas a medicamentos (RAM) más frecuente y grave (1). Existe en los últimos años un interés creciente por su detección y conocimiento (2-5). Dicha detección suele realizarse en pacientes hospitalizados (mediante registros intensivos) y en la población general (a través del sistema de notificación voluntaria). Ambos métodos presentan unas series de limitaciones que explican las deficiencias en el conocimiento epidemiológico de la hepatotoxicidad por medicamentos (6).
El objetivo de este trabajo es comunicar una estrategia que mejora los resultados de la detección de RAM hepatotóxicas con los métodos antes citados.
MÉTODOS
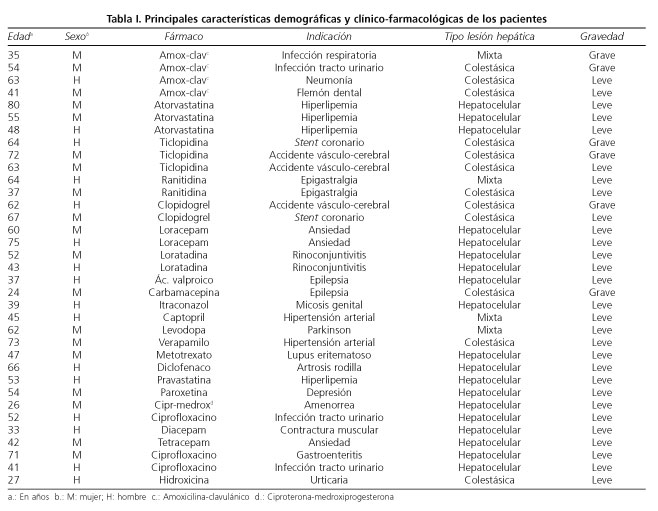
Se realizó un estudio piloto, promovido y coordinado por el Servicio de Farmacología Clínica del Hospital Universitario Virgen Macarena (Sevilla, España), para probar un modelo de detección de RAM hepatotóxicas. Las principales características demográficas y clínico-terapéuticas de los pacientes que las presentaron se recogen en las tabla I.
El modelo, que se aplicó entre junio del 2002 y julio del 2003, está basado en la identificación de una
señal de alerta simple en una serie de servicios diana del propio hospital.
La señal de alerta que hacía sospechar toxicidad hepática medicamentosa, podía ser una de las siguientes (7): a) > 76 U/L de GPT; b) > 0,6 mg/dL de bilirrubina conjugada; c) > 80 U/L de GOT, > 2 mg/dL de bilirrubina total y 516 U/L de fosfatasa alcalina (simultáneamente).
Bastaba la existencia de una de ellas para generar la sospecha.
Los servicios diana se seleccionaron basándose en el número de consultas por sospecha de hepatotoxicidad medicamentosa que recibían en la Unidad de Hepatología (Servicio de Aparato Digestivo). Fueron los siguientes: Medicina Interna (Unidad de Lípidos), Neurología, Dermatología, Oncología y la propia Unidad de Hepatología.
Cuando los médicos de dichos servicios detectaban una o varias de las señales de alerta, identificaban con una marca preestablecida la primera página de la historia clínica del paciente. Semanalmente, personal entrenado (médicos residentes) del Servicio de Farmacología Clínica acudía a los servicios diana; recogían los datos de la historia clínica del paciente y lo citaban para una entrevista posterior en la que se seguía un protocolo específico para el análisis y valoración de este tipo de RAM. Cuando alguno de los servicios no dianas comunicaba espontáneamente alguna sospecha de RAM hepatotóxica, lo hacía a través de la Unidad de Hepatología y el caso seguía la dinámica antes comentada. Excepcionalmente, algunas sospechas de estos servicios no dianas fueron comunicadas directamente al Servicio de Farmacología Clínica. El esquema de este flujo de información aparece en la figura 1.
Del conjunto de la información obtenida se analizaron:
-Los fármacos sospechosos de RAM (identificación y número).
-La relación de causalidad entre el fármaco sospechoso y la RAM, siguiendo la escala de María & Vitorino; según el resultado, la relación se clasificaba como definitiva, probable, posible, poco probable y excluida (8).
-La gravedad de la RAM (severa, moderada y leve) (9).
-La incidencia de la RAM hepatotóxica/100.000 habitantes.
-La relación obtenida en cada Servicio entre el número de sospechas confirmadas/número de sospechas comunicadas.
RESULTADOS
En el periodo de estudio se recogieron 80 sospechas de RAM hepatotóxicas, de las que se descartaron 45 al comprobarse una etiología no farmacológica. De las 35 restantes, el 57,1% de los pacientes eran hombres y la edad media de aparición fue de 54,5 ± 17,8 años.
Los fármacos imputados fueron: amoxicilina-clavulánico (4 casos); ticlopidina, atorvastatina y ciprofloxacino (3 casos cada uno); ranitidina, clopidogrel, loracepam y loratadina (2 casos cada uno); diacepam, tetracepam, ácido valproico, carbamacepina, hidroxicina, itraconazol, captopril, levodopa, verapamilo, metotrexato, diclofenaco, pravastatina, paroxetina y ciproterona-meproxiprogesterona (1 caso cada uno).
En cuanto a la causalidad: 2 sospechas se clasificaron como definitivas, 14 como probables y 19 como posibles.
La distribución según la gravedad de la hepatotoxicidad fue: 6 casos graves y 29 leves.
En el mismo periodo, la incidencia de RAM hepatotóxica/100.00 habitantes obtenida fue de 6,74 (35 en una población de 519.381 habitantes) (10).
La distribución de la relación RAM confirmadas/RAM comunicadas por los distintos servicios fue: Digestivo (20/30), Medicina Interna (9/21), Neurología (4/15), Dermatología (2/10) y Oncología (0/4).
DISCUSIÓN
Los resultados confirman la correcta selección de los Servicios diana, con excepción del de Oncología, en el que los efectos adversos por la medicación son muy frecuentes; por esa razón, sólo se han considerado aquellos de grado de toxicidad III y IV según la clasificación de la OMS de fármacos antineoplásicos. Por otro lado, la proporción global de RAM confirmadas/sospechadas ha sido alta (35/80) y ello refuerza la aplicabilidad del método.
El método de registro intensivo de RAM medicamentosa es de organización fácil y tiene una sensibilidad elevada; presenta, sin embargo, algunas limitaciones: poca representatividad de la población general, escasa eficiencia, sensibilidad reducida para RAM nuevas o inesperadas, y dificultad para mantenerlo de forma permanente (6). El método seguido en este estudio, que podría calificarse de registro intensivo selectivo, supera algunas de ellas: facilita la notificación de la sospechas de este tipo de RAM, puede mantenerse de forma permanente al no sobrecargar el trabajo diario de los médicos, y permite aproximar el número de RAM hepatotóxicas detectadas a su incidencia real.
Por otra parte, el método de la notificación voluntaria tiene la ventaja de su simplicidad; se acompaña, no obstante, de dos inconvenientes: infranotificación de RAM y abundancia de sesgos, que lo llevan a una escasa eficiencia. En relación a esta, la incidencia de RAM hepatotóxicas/100.000 habitantes fue más alta con nuestro método que con el de notificación voluntaria Así, en el mismo periodo de tiempo, obtuvimos en nuestro estudio un valor de 6,74 (35 en una población de 519.381 habitantes), mientras que el sistema de notificación voluntaria obtuvo 1,79 (262 en una población de 40.202.160 habitantes) (11,12). Pese a ello, para no interpretar erróneamente los resultados, conviene recordar que ambos métodos persiguen objetivos diferentes: el del presente estudio es conocer la incidencia real aproximada de las RAM hepatotóxicas en el área de influencia de nuestro hospital, mientras que la notificación voluntaria pretende detectar las RAM graves e infrecuentes en la población general.
La principal limitación de nuestro método es que no detecta las RAM hepáticas poco significativas clínicamente en los Servicios no diana y en la asistencia extrahopitalaria. Por el contrario, detecta todas las RAM hepatotóxicas de carácter grave-moderado que se producen en el medio que se implante y todas las generadas en los servicios diana sea cual sea su gravedad.
En conclusión, el método aplicado ha demostrado su validez para mejorar y aumentar la detección de RAM hepatotóxicas y podría generalizarse a otros tipos de RAM.
BIBLIOGRAFÍA
1. Zimmerman HJ. Hepatotoxicity. The adverse effects of drugs and other chemicals on the liver. 2nd ed. Philadelphia: Lippincott Williams & Wilkins, 1999. [ Links ]
2. Andrade RJ, Lucena MI. Is drug-induced hepatotoxicity unavoidable? Rev Esp Enferm Dig 2001; 93: 51-3. [ Links ]
3. Vargas E. Drug-induced liver toxicity? Rev Esp Enferm Dig 2001: 93: 421-2. [ Links ]
4. García M, Andrade RJ, Lucena MI, Sánchez H, Ferrer T, Martín R, et al. Flutamide-induced hepatotoxicity: a case-report series. Rev Esp Enferm Dig 2001; 93: 428-32. [ Links ]
5. Camargo R, Andrade RJ, Lucena MI, Alcántara R, Carvajal A. Antidepressant-induced hepatotoxicity. Rev Esp Enferm Dig 2002; 94; 766-71. [ Links ]
6. MNG, ed. Meyler's side effects of drugs, 12th ed. Amsterdam: Excerpta Medica, 1992. [ Links ]
7. Standardization of definitions and criteria of causality assessment of adverse drug reactions. Drug-induced liver disorders: report of an international consensus meeting. Int J Clin Pharmacol Ther Toxicol 1990; 28: 317-22. [ Links ]
8. Maria VAJ, Vitorino RMM. Development and validation of a clinical scale for the diagnosis of drug-induced hepatitis. Hepatology 1997; 26: 664-9. [ Links ]
9. Capellá D, Avila P, Cabeza L, Moreno V, Vidal X, Laporte JR. Cuatro años de experiencia en farmacovigilancia. Med Clin (Barc) 1988; 91: 93-6. [ Links ]
10. Memoria anual del Área Hospitalaria Virgen Macarena (Sevilla). Consejería de Salud, Junta de Andalucía, Seville, Spain, 2002. [ Links ]
11. www.agemed.es December 2002. (In order to maintain confidentiality, the URL requires authorization to access the data.) [ Links ]
12. www.INE.es June 2002. [ Links ]











 texto em
texto em