My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Española de Enfermedades Digestivas
Print version ISSN 1130-0108
Rev. esp. enferm. dig. vol.101 n.10 Madrid Oct. 2009
Cinética viral durante el primer mes de tratamiento en pacientes con hepatitis crónica C genotipo 1
Viral kinetics during the first month of treatment in patients with genotype 1 chronic hepatitis C
A. Hernández, F. Domper, A. León1, R. Lorente, B. López, E. de la Santa, M. Cabanillas, R. Patón, J. Olmedo, M. D. Galván y E. Rodríguez
Unidades de Aparato Digestivo y 1de Apoyo a la Investigación. Hospital General de Ciudad Real
Dirección para correspondencia
RESUMEN
Objetivo: identificar qué factores predicen la respuesta al interferón pegilado alfa-2b y ribavirina en pacientes con hepatitis crónica C genotipo 1. Se estudió la cinética viral en la semana 2 y 4.
Métodos: se evaluaron de forma prospectiva y consecutiva a los pacientes con hepatitis crónica C genotipo 1 remitidos a nuestra consulta de hepatología entre enero de 2004 y octubre de 2006, para tratamiento antiviral. Se recogieron datos basales y la viremia se determinó horas antes de la dosis semanal de interferón pegilado por PCR cualitativa y cuantitativa.
Resultados: cincuenta y siete pacientes fueron incluidos aunque 3 fueron excluidos durante el seguimiento. Un 65% fueron varones (n = 35) con edad media de 42 (26-65) años. La viremia basal fue > 800.000 UI/ml en 67% (n = 36). Se realizó biopsia hepática en 86% (n = 46), 22% (n = 12) tenían fibrosis avanzada. 40 fueron naïves, 4 recidivantes y 10 no respondedores. La dosis de ribavirina se modificó por efecto secundario sólo en un paciente. La RFT y la RVS fueron de 59 y 41%, respectivamente. El análisis univariante mostró asociación estadísticamente significativa con RVS de la viremia basal (p = 0,006), GGT basal (p = 0,025) y el descenso en la viremia ≥ 2 logaritmos a las 2, 4 y 12 semanas (p = 0,001). El descenso de la viremia en la semana 2 se asoció con 100% de RVS y a las 4 semanas el VPP fue 84% y el VPN 96,5%. Se realizó un subanálisis en el grupo de pacientes naïves con resultados superponibles.
Conclusiones: en nuestro estudio el descenso de la viremia ≥ 2 logaritmos a las 2 semanas de tratamiento aseguró la RVS. A las 4 semanas, identificamos a la gran mayoría de los pacientes no respondedores.
Palabras clave: Hepatitis C. Tratamiento. Interferón pegilado. Viremia. Factores predictores.
ABSTRACT
Objective: to identify predictive factors of response to pegylated interferon alpha-2b and ribavirin in patients with genotype 1 chronic hepatitis C. Viral kinetics were studied in weeks 2 and 4.
Methods: a prospective and consecutive study of patients with genotype 1 chronic hepatitis C referred to our Hepatology Clinic between January 2004 and October 2006 for antiviral treatment. Baseline data were recorded and viremia levels were determined hours before the weekly dose of pegylated interferon by qualitative and quantitative PCR.
Results: 57 patients were included in the study, although 3 of these were excluded during follow up; 65% were male (n = 35), with a mean age of 42 (26-65) years. Baseline viremia levels were > 800,000 IU/mL in 67% (n = 36). Liver biopsy was performed in 86% (n = 46), 22% (n = 12) had advanced fibrosis. Forty were naïve, 4 relapsing and 10 non-responders. Ribavirin dose was modified in one patient alone due to adverse effects. End treatment response and sustained virological response (SVR) were 59 and 41%, respectively. A univariate analysis revealed a statistically significant association of SVR with baseline viremia (p = 0.006), baseline GGT (p = 0.025), and a reduction in viremia ≥ 2 logs at 2, 4 and 12 weeks (p = 0.001). The extent of viremia reduction at week 2 was associated with 100% SVR, and at 4 weeks the positive predictive values was 84% and the negative predictive values was 96.5%. A subanalysis of the naïve group yielded analogous results.
Conclusions: in our study, a reduction in viremia ≥ 2 logs 2 weeks after treatment could ensure SVR. At 4 weeks, most non-responders could be identified.
Key words: Hepatitis C. Treatment. Pegylated interferon. Viremia. Predictive factors.
Introducción
La hepatitis crónica por el virus de la hepatitis C (VHC) supone una enfermedad infecciosa de gran impacto en nuestro medio y la causa más frecuente de hepatitis crónica, cirrosis y hepatocarcinoma en el mundo occidental (1). En la actualidad la prevalencia de la infección por VHC es de 1-2% en los países desarrollados y es la primera indicación de trasplante hepático en Europa y Estados Unidos (2). El 20% de los infectados de forma crónica desarrollarán una cirrosis hepática, con un riesgo anual de degenerar en hepatocarcinoma del 1-4%.
La terapia actual basada en el empleo de interferón pegilado (pegIFN) y ribavirina (RBV) consigue una tasa global de respuesta viral sostenida (RVS) entre 54-56% mejorando el pronóstico de esta enfermedad (3,4).
Existen ciertas características del paciente, del virus y del tipo de tratamiento empleado que influyen en la respuesta terapéutica. Estas variables nos ayudarían a identificar la mayor o menor probabilidad de respuesta, lo que puede evitar gastos y efectos secundarios innecesarios, favorecen la adhesión del paciente al tratamiento e identifican a aquellos pacientes que se podrían beneficiar de tratamientos más intensivos o prolongados.
La cinética viral (variaciones en la carga viral) durante el tratamiento es el factor predictivo de respuesta más significativo y permite tomar decisiones terapéuticas. La respuesta virológica precoz (RVP) se define como el descenso de al menos 2 logaritmos de la carga viral basal en la semana 12 de tratamiento. Si no se alcanza esta RVP, la probabilidad de RVS es muy baja, con un valor predictivo negativo (VPN) que se acerca al 100%, por lo que en la actualidad las guías clínicas aconsejan la suspensión del tratamiento (5,6). La respuesta viral rápida (RVR) definida como la obtención de carga viral negativa en la semana 4, es un buen factor pronóstico de la RVS, con un valor predictivo positivo (VPP) del 91% (7-13). En varios estudios define la duración del tratamiento. Sin embargo, faltan estudios que evalúen el valor de la cinética viral más precozmente.
El objetivo de nuestro estudio ha sido identificar qué factores predicen la respuesta al pegIFN alfa-2b y RBV en pacientes con hepatitis crónica C genotipo 1, valorando los factores basales del virus y el huésped, pero sobre todo los factores dinámicos de la cinética viral en la segunda y cuarta semanas de tratamiento.
Pacientes y métodos
Se evaluaron de forma prospectiva y consecutiva a los pacientes con hepatitis crónica C genotipo 1 remitidos a la consulta de hepatología de nuestro hospital, entre enero de 2004 y octubre de 2006, que iniciaron tratamiento antiviral con pegIFN alfa-2b y RBV.
Los criterios de inclusión fueron: edad entre 18 y 70 años, PCR VHC en suero positiva, niveles de ALT superiores al valor normal de nuestro laboratorio (≤ 40 UI/l) en el último año. Los criterios de exclusión fueron: coinfección con VIH, serología HBsAg o ADN del virus de la hepatitis B positivos, contraindicación para el uso de pegIFN o RBV, cirrosis descompensada, ADVP activos y pacientes recluidos en centros penitenciarios.
Los pacientes recibieron pegIFN alfa-2b (PegIntron; Schering Plough) a dosis de 1,5 microgramos/kg de peso, una vez por semana, por vía subcutánea y RBV (Rebetol; Schering Plough) por vía oral, ajustando la dosis según peso (< 65 kg: 800 mg/día; 65-85 kg: 1.000 mg/día; > 85 kg: 1.200 mg/día) en dosis fraccionada mañana y tarde durante 48 semanas.
Se recogieron datos clínicos y analíticos basales, durante el tratamiento en las semanas 2, 4, 8, 12, 16, 20, 24, 36 y 48, y tras finalizar el tratamiento en la semana 72. La viremia se valoró unas horas antes de la dosis semanal de pegIFN, en las semanas 2, 4, 12, 24, 48, 60 y 72.
Hasta octubre de 2005 la carga viral se midió mediante la técnica Cobas Amplicor HCV Monitor 2.0 (límite de detección de 600 UI/ml). Las muestras negativas se sometieron a la determinación cualitativa del ARN en Cobas Amplicor HCV Test, versión 2.0 (sensibilidad de 50 UI/ml). A partir de esa fecha la técnica utilizada fue el COBAS Taqman HCV (sensibilidad 15 UI/ml, con determinación cuantitativa hasta 43 UI/ml). Se consideró carga basal baja ≤ 800.000 UI/ml (12,13).
El genotipo del VHC se determinó mediante la técnica Inno-lipa II (Innogenetics).
En los pacientes que presentaban anemia por el uso de la RBV se les administró eritropoyetina recombinante humana 40.000 UI/semana por vía subcutánea, con intención de evitar disminuir la dosis de RBV, tal y como han descrito algunos estudios (14,15).
La respuesta viral sostenida (RVS) se definió como negatividad del ARN VHC tras 6 meses de finalizado el tratamiento. La respuesta al final del tratamiento (RFT) como la negatividad del ARN VHC en la semana 48. La respuesta virológica precoz (RVP) como el descenso de al menos 2 logaritmos de la carga viral basal en la semana 12 de tratamiento. La respuesta viral a la semana 4 (RV4) se estableció como el descenso de al menos 2 logaritmos de la carga viral en la semana 4. La respuesta viral rápida (RVR) como la negatividad del ARN VHC a las 4 semanas. La respuesta de la carga viral a la semana 2 (RV2) se definió como el descenso de al menos 2 logaritmos de la carga viral basal en la semana 2.
Análisis estadístico
Estudio longitudinal de seguimiento de una cohorte. La estadística descriptiva para variables cualitativas se definió mediante tablas de distribución de frecuencias y gráficos de sectores. Las variables cuantitativas se definieron mediante estadísticos de tendencia central, de dispersión y representación gráfica de histogramas. En la estadística inferencial, la variable principal del estudio (RVS) se analizó utilizando el test de χ2 y exacto de Fisher para variables cualitativas y el test de Mann-Whitney y Kruskal-Wallis para variables cuantitativas.
Resultados
Se incluyeron 57 pacientes con hepatitis crónica C genotipo 1, aunque tres pacientes no finalizaron el estudio, dos por no acudir a las revisiones y uno por intervención quirúrgica urgente de una hernia abdominal complicada. Por tanto, concluyeron el seguimiento 54 pacientes.
La adherencia al tratamiento fue muy buena (> 80% de la dosis) en el 94,4% de los pacientes, sólo en un paciente se modificó la dosis de la RBV por anemia con respuesta parcial a la eritropoyetina.
Características basales de los pacientes
De los 54 pacientes que concluyeron el estudio, 35 eran varones (64,8%). La edad media al inicio de tratamiento fue de 42,7 años (26-65 años). Cuarenta pacientes eran naïve (74,1%), 4 con recidiva a tratamiento previo (7,4%) y 10 eran no respondedores previos (18,5%).
Se realizó biopsia hepática en 46 (85%). Doce tenían fibrosis grado III-IV. La carga viral basal fue > 800.000 UI/ml en 36 (66,7%). El índice de masa corporal (IMC) fue > 30 en 16 pacientes (30%). Presentaban crioglobulinemia asociada 13 pacientes (24%).
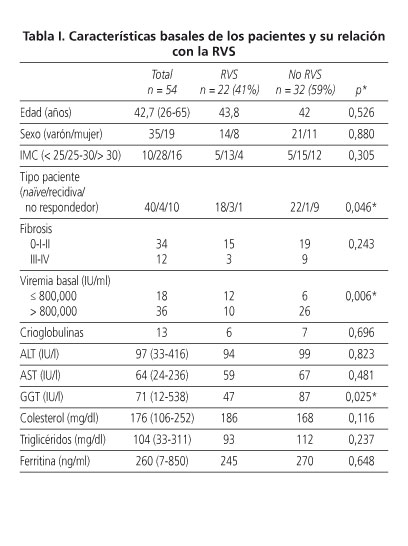
Las características analíticas se desglosan en la tabla I.
Respuesta al final del tratamiento y respuesta viral sostenida
Por protocolo la RFT fue del 59,3% (32/54) y la RVS de 41% (22/54). Por subgrupos la RVS fue del 45% (18/40) en los naïve, del 75% (3/4) en los recidivas y sólo del 10% (1/10) en los no respondedores a tratamientos previos (IFN o IFN con RBV).
Factores predictores de respuesta
El objetivo principal del estudio fue la predicción de la RVS estudiando características basales y la cinética viral durante el tratamiento. Las características basales y su relación con la RVS se desglosan en la tabla I. En el análisis comparativo alcanzaron significación estadística la carga viral basal (p = 0,006), la GGT basal (p = 0,025) y el tipo de paciente: naïve, recidiva, no respondedor (p = 0,046).
En el estudio alcanzaron mayor significación estadística (p = 0,001) los factores dinámicos de cinética viral como el descenso de la carga viral ≥ 2 logaritmos en la semana 2 (RV2), semana 4 (RV4) y semana 12 de tratamiento (RVP), al igual que la RVR (Tabla II). La RV2 tuvo un VPP del 100%, que fue disminuyendo conforme se continuaba con el tratamiento. De forma inversa el VPN fue progresivamente mayor hasta alcanzar el 100% en la semana 12 (RVP). Una respuesta rápida pronostica la curación mientras que la falta de respuesta tras 12 semanas indica que el paciente no va a responder. En nuestro estudio el VPN del descenso ≥ 2 log de la carga viral basal en la semana 4 (RV4) fue de 96,5%.
Estudio en el subgrupo de pacientes naïve
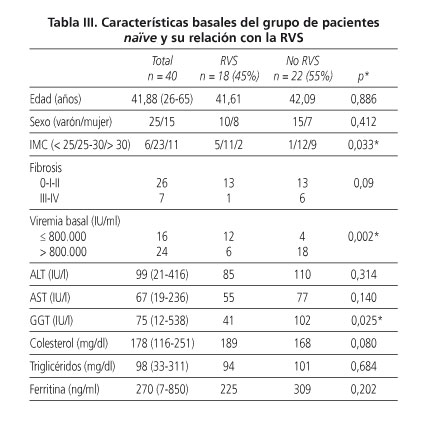
Se realizó también el mismo estudio comparativo en el subgrupo de pacientes naïve (n = 40) alcanzando significación estadística los factores basales como la carga viral (p = 0,002), la GGT (p = 0,025) y el IMC (p = 0,033). La fibrosis hepática avanzada se asoció con peor respuesta al tratamiento sin alcanzar significación estadística (p = 0,09) aunque probablemente la obtuviera al aumentar el número de pacientes (Tabla III).
También presentaron significación estadística (p = 0,001) los factores de la cinética viral RV2, RV4, RVR y RVP de forma paralela a lo comentado anteriormente con el global de los pacientes (Tabla II).
Efectos adversos del tratamiento
Ninguno de los pacientes incluidos suspendió el tratamiento por efectos adversos, que fueron frecuentes, aunque en la mayoría de los casos fueron leves. Se pautó eritropoyetina subcutánea en los pacientes con descenso de la hemoglobina por debajo de 10 g/dl. Sólo en un paciente se disminuyó la dosis de RBV por respuesta parcial a la eritropoyetina. La neutropenia y la plaquetopenia no requirieron ajuste de dosis. Se observó alteración significativa en las cifras de TSH en un 3,8%. Estos pacientes fueron remitidos a la consulta de endocrinología. Presentaron alteración en el estado de ánimo un 53%, un pequeño porcentaje de estos fueron remitidos a la consulta de psiquiatría e iniciaron tratamiento con antidepresivos.
Discusión
La tasa de RVS para pacientes naïve con hepatitis crónica C genotipo 1, con la combinación de pegIFN y RBV durante 48 semanas, es del 42-51% (3,4). En nuestra serie la RVS fue del 41% para la totalidad de los pacientes y en los pacientes naïve fue del 45%. En los no respondedores la RVS fue del 10%, semejante a los resultados de los estudios HALT-C y EPIC3, en pacientes no respondedores previos a tratamiento combinado con IFN estándar que refieren tasas de RVS entre 12-14% y aumenta hasta 53% si es recidivante (16,17).
En nuestro estudio la adherencia al tratamiento fue muy alta (94,4%), en posible relación al estrecho seguimiento mensual durante los primeros 6 meses y al uso de eritropoyetina cuando los pacientes presentaron anemia para evitar reducir dosis en los primeros 6 meses, tal y como está descrito en estudios previos (14,15). Esto hace pensar que la tasa de RVS de nuestro estudio debería haber sido algo mayor, pero también hay que tener en cuenta que incluimos un porcentaje importante de pacientes con fibrosis severa (22%), carga viral basal alta (66,7%), IMC > 30 (30%) y crioglobulinas (24%), factores que se han asociado a una peor respuesta al tratamiento.
En los últimos años se han descrito factores basales y durante el tratamiento que se relacionan con la RVS (18). En nuestro estudio, tanto en la totalidad de los pacientes como en el subgrupo de pacientes naïve alcanzaron significación estadística la carga viral basal y la GGT. En los pacientes naïve fue también estadísticamente significativo el IMC, mientras no fue significativo al incluir la totalidad de los pacientes posiblemente debido a la mayor heterogenicidad del grupo al incluir los pacientes no respondedores. La fibrosis, en los pacientes naïve, se acercaba a la significación estadística sin llegar a alcanzarla, esa tendencia posiblemente pudiera conseguir significación de ampliarse la muestra.
Los factores predictores de respuesta con mayor significación estadística fueron aquellos relacionados con la cinética viral. El descenso de la viremia ≥ 2 logaritmos a las 2 semanas de iniciado el tratamiento aseguró la RVS. Por tanto, la monitorización a la semana 2 estaría justificada dado que permite estimular a los pacientes para continuar con el tratamiento. A las 4 semanas identificamos a la gran mayoría de los no respondedores y a un elevado porcentaje de los pacientes con RVS. Los pacientes con descenso ≥ 2 logaritmos en la semana 4 tienen en nuestro estudio un VPP de 84%, y un VPN de 96,5%, por lo que solo un pequeño porcentaje de pacientes que continúen con el tratamiento estándar va a responder. Esto convendría confirmarlo con estudios con mayor número de pacientes.
Parece que el no descenso de la carga viral y el descenso de ≥ 2 logaritmos podrían marcar dos subgrupos con comportamiento diferente y nos indica la importancia de la rapidez en la supresión viral en la semana 4.
Las posibilidades de conseguir una RVS está relacionada con dos factores de la cinética viral: la rapidez de supresión del ARN VHC y el tiempo de duración de la supresión durante el tratamiento como demostraron Ferenci y cols. (6). En el genotipo 1 demostraron el valor de la determinación de la carga viral en la semana 4: si se conseguía una RVR, la RVS era del 91%, comparable a la RVS de genotipos más favorables (genotipos 2 y 3). Cuando no existía RVR pero sí RVP completa, con negativización del virus en la semana 12, la RVS descendía dependiendo si la carga a la semana 4 había disminuido ≥ 2 logaritmos (RVS: 70%) o < 2 logaritmos (RVS: 60%). En los pacientes con RVP parcial, con bajada en la semana 12 de al menos 2 logaritmos pero sin llegar a negativizar el virus, la RVS baja a 43%, lo que demostraba también la importancia del periodo tiempo total durante el cual permanece indetectable el ARN VHC en la predicción de la RVS. Todo ello, permite definir subgrupos de pacientes que podrían recibir pautas de tratamientos diferentes según su cinética viral. Independientemente de la RVP, cuanto más tarda el paciente en negativizar el ARN VHC menor probabilidad tiene de RVS.
La monitorización de la carga viral en el tratamiento de la hepatitis crónica C genotipo 1 aporta beneficios para el paciente. Si existen factores predictivos favorables el paciente intentará una mayor adhesión al tratamiento. Según nuestros resultados parece que sería de ayuda ampliar la monitorización de la carga viral a la semana 2 y corrobora la importancia de la respuesta en la semana 4, teniendo en cuenta no solamente la RVR sino la RV4, definida como el descenso de al menos 2 logaritmos de la carga viral basal, con un VPP similar a la RVR, pero un VPN mayor.
![]() Dirección para correspondencia:
Dirección para correspondencia:
Francisco Domper Bardají.
C/ Hospital de la Misericordia, 9, 5º D.
13003 Ciudad Real,
España.
e-mail: franciscodomper@telefonica.net
Recibido: 24-03-09.
Aceptado: 26-05-09.
Bibliografía
1. Shepard CW, Finelli L, Alter MJ. Global epidemiology of hepatitis C virus infection. Lancet Infect Dis 2005; 5: 55. [ Links ]
2. Di Bisciglie A. Hepatitis C. Lancet 1998; 351: 351-5. [ Links ]
3. Manns MP, McHutchinson JG, Gordon SC, Rustgi VK, Shiffman M, Reindollar R, et al. Peginterferon alfa-2b plus ribavirin compared with interferon alfa-2b plus ribavirin for initial treatment of chronic hepatitis C: a randomized trial. Lancet 2001; 358: 958-65. [ Links ]
4. Fried MW, Shiffman ML, Reddy KR, Smith C, Marinos G, Goncales FL Jr, et al. Combination peginterferon alfa-2a plus ribavirin for chronic hepatitis C virus infection. N Engl J Med 2002; 347: 975-82. [ Links ]
5. Davis G, Wong J, McHutchison J, Manns M, Harvey J, Albrecht J. Early virologic response to treatment with peginterferon alfa-2b plus ribavirin in patients with chronic hepatitis C. Hepatology 2003; 3839: 645-52. [ Links ]
6. Ferenci P, Fried MW, Shiffman ML, Smith CI, Marinos G, Goncales FL Jr, et al. Predicting sustained virological responses in chronic hepatitis C patients treated with peginterferon alfa-2a (40KD)/ribavirin. J Hepatol 2005; 43: 425-33. [ Links ]
7. Fried MW, Hadziyannis SJ, Shiffman M, Messinger D, Zeuzem S. Rapid virological response is a more important predictor of sustained virological response (SVR) than genotype in patients with chronic hepatitis C virus infection. J Hepatol 2008; 48: S5. [ Links ]
8. Dalgard O, Bjoro K, Hellum KB, Myrvang B, Ritland S, Skaug K, et al. Treatment with pegylated interferon and ribavarin in HCV infection with genotype 2 or 3 for 14 weeks: a pilot study. Hepatology 2004; 4: 1260-5. [ Links ]
9. Von Wagner M, Huber M, Brg T, Hinrichsen H, Rasenack J, Heintges T, et al. Peginterferon-alpha-2a (40kD) and ribavirin fop 16 or 24 weeks in patients with genotype 2 or 3 chronic hepatitis C. Gastroenterology 2005; 129: 5-7. [ Links ]
10. Mangia A, Santoro R, Minerva N, Ricci GL, Carretta V, Persico M, et al. Peginterferon alfa-2b and ribavirin for 12 vs 24 weeks in HCV genotype 2 or 3. N Egl J Med 2005; 352: 2609-17. [ Links ]
11. Zeuzem S, Buti M, Ferenci P, Sperl J, Horsman Y, Cianciara J, et al. Efficacy of 24 weeks treatment with peginterferon alfa-2b plus ribavirinin patients with chronic hepatitis C infected with genotype 1 and low pre-treatment viremia. J Hepatol 2006; 44: 97-103. [ Links ]
12. Zeuzem S, Awlotsky JM, Lukasiewicz E, Von Wagner M, Goulies I, Lurie Y, et al. International, multicenter, randomized, controlled study comparing dynamically individualized versus standard treatment in patients with chronic hepatitis C. J Hepatol 2005; 43: 250-7. [ Links ]
13. Sánchez-Tapias JM, Diago M, Escartín P, Enriquez J, Romero-Gómez M, Bárcena R, et al. Peginterferon alfa-2a (40KD) plus ribavirin for 48 versus 72 weeks in patients with detectable HCV-RNA at week 4 of treatment. Gastroenterology 2006; 131: 451-60. [ Links ]
14. Pockros PJ, Shiffman ML, Schiff ER, Sulkowski MS, Younossi Z, Dieterich DT, et al., Proactive Study Group. Epoeitin alfa improves quality of life in anemic HCV-infected patients receiving combination therapy. Hepatology 2004; 40: 1450-8. [ Links ]
15. Afdhal N, Dieterich DT, Pockros PJ, Schiff ER, Shiffman ML, Sulkowski MS, et al., Proactive Study Group. Epoetin alfa maintains ribavirin dose in HCV-infected patients: a prospective double-blind randomized, controlled study. Gastroenterology 2004; 126: 1302-11. [ Links ]
16. Shiffman M, Di Bisciegle A, Lindsay K, Morishima C, Wright E, Everson G, et al. Peginterferon alfa 2a and ribavirin in patients with chronic hepatitis C who have failed prior treatment. Gastroenterology 2004; 126: 1015-23. [ Links ]
17. Poynard T, Schiff E, Terg R, Moreno Otero R, Flamm S, Schmidt W, et al. Sustained viral response is dependent on baseline characteristic in the retreatment of previous alfa interferon/ribavirin no responders: final results from the EPIC program. J Hepatol 2008; 48(Supl. 2): S369. [ Links ]
18. Alberti A, Chemello L, Benbegnu L. Natural history of hepatitis C. J Hepatol 1999; 31(Supl. 1): 17-24. [ Links ]











 text in
text in