My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Farmacia Hospitalaria
On-line version ISSN 2171-8695Print version ISSN 1130-6343
Farm Hosp. vol.37 n.3 Toledo May./Jun. 2013
https://dx.doi.org/10.7399/FH.2013.37.3.581
ORIGINALES
Análisis del impacto presupuestario de adalimumab y etanercept en artritis reumatoide y espondiloartropatías
Analisis of the budget impact of adalimumab and etanercept in rheumatoid arthritis and spondyloarthropathies
A. González Álvarez1, M. Gómez Barrera2, J. Borrás Blasco3 y E. J. Giner Serret4
1Servicio de Farmacia, Hospital Obispo Polanco, Teruel, España.
2Grupo de Investigación GIMACES, Facultad de Ciencias de la Salud, Universidad San Jorge, Villanueva de Gállego, Zaragoza, España.
3Servicio de Farmacia, Hospital de Sagunto, Valencia, España.
4Servicio de Reumatología, Hospital Obispo Polanco, Teruel, España.
Dirección para correspondencia
RESUMEN
Objetivo: Evaluar el impacto económico derivado de la ampliación de los intervalos de administración de adalimumab (ADA) y etanercept (ETN), en el tratamiento de la artritis reumatoide (AR) y espondiloartropatias (EAP) en nuestro ámbito de trabajo.
Material y método: Se desarrolló un modelo de impacto presupuestario (MIP) para estimar la repercusión económica que tendría la ampliación en los intervalos habituales de administración de ADA 40 mg cada dos semanas y ETN 50 mg semanal (escenario A), por ADA 40 mg cada tres semanas y ETN 50 mg cada dos semanas (escenario B) de acuerdo a las guías y recomendaciones que se aplican a estos estudios, especificando la población diana, la perspectiva del estudio, el horizonte temporal y analizando la robustez del estudio a través de un análisis de sensibilidad univariante de tipo umbral.
Resultados: Se incluyeron un total de 71 pacientes en el estudio. La aplicación del MIP mostró unos ahorros anuales para ADA y ETN de 19.784€ y 38.271 € respectivamente. El coste neto, es decir, el ahorro que esto supuso en el horizonte temporal considerado (dos años) ascendió a 116.110 €. El análisis de sensibilidad realizado mostró que el MIP estimado para el periodo de estudio fue muy robusto ya que el resultado neto en diferentes escenarios apenas variaba, manteniéndose negativo en los nuevos escenarios.
Conclusiones: La ampliación de los intervalos de administración de ADA y ETN cada tres semanas y dos semanas respectivamente, sería una estrategia que permitiría generar ahorros en el presupuesto hospitalario cercanos a los 116.110 € en el horizonte temporal considerado, consiguiendo así una optimización del tratamiento con estos fármacos.
Palabras clave: Artritis reumatoide; Espondiloartropatías; Análisis de impacto presupuestario; Adalimumab; Etanercept; Inhibidores del factor de necrosis tumoral.
ABSTRACT
Purpose: To assess the economic impact derived from the widening of the administration intervals of adalimumab (ADA) and etanercept (ETN) for the treatment of rheumatoid arthritis (RA) and spondyloarthropathies (SAP) at our working environment.
Material and methods: A budget impact model (BIM) was developed to estimate the economic impact that would have widening the usual administration intervals of ADA, 40 mg every 2 weeks and ETN, 50 mg weekly (scenario A), to ADA, 40 mg every 3 weeks, and ETN, 50 mg every 2 weeks (scenario B) according to the guidelines and recommendations applied to these studies, specifying the target population, the study perspective, the temporal horizon, and analysing the study robustness by a threshold univariate sensitivity analysis.
Results: 71 patients were included in the study. The application of the BIM showed yearly savings for ADA and ETN of 19.784 € and 38.271 €, respectively. The net cost, that is to say the saving that this would imply within the temporal horizon considered (2 years), was 116.110 €. The sensitivity analysis showed that the estimated BIM for the study period was very robust since the net result in the different scenarios varied very little, being negative in the new scenarios.
Conclusions: widening the administration intervals of ADA and ETN to every 3 weeks and 2 weeks respectively, would be a strategy that would allow generating savings in the hospital budget close to 116.110 € for the temporal horizon considered, achieving this way optimization of the treatment with these two drugs.
Key words: Rheumatoid arthritis; Spondyloarthropathies; Budget impact analysis; Adalimumab; Etanercept; Tumour necrosis factor inhibitors.
Introducción
La artritis reumatoide (AR) es una enfermedad crónica que tiene un gran impacto en la calidad de vida del paciente y origina un coste social y económico importante. Desde sus fases iniciales, afecta a las actividades diarias de las personas que la padecen, no sólo en sus aspectos físicos, sino también en los aspectos sociales, psicológicos y económicos. Se trata de una enfermedad frecuente y su prevalencia varía poco entre países, oscilando entre el 0,5 y 1%1
Por otro lado, el término espondiloartropatías (EAP) o espondiloartritis designa genéricamente a enfermedades como la espondilitis anquilosante (EA) y la artritis psoríasica (APs) entre otras2, donde su prevalencia (0,1-2,5%) varía en función de la etnia, localización geográfica, y sobre todo, de la frecuencia del HLA-B27 en la población general3.
El tratamiento de estas patologías comprende en sus primeras etapas el uso de AINEs, fármacos modificadores de la enfermedad (FAMEs) tradicionales o combinación de los mismos y fisioterapia, sin embargo, ante la no respuesta a estos tratamientos, disponemos de fármacos como los inhibidores del factor de necrosis tumoral alfa (anti-TNF) tales como adalimumab y etanercept.
Adalimumab (ADA), es un anticuerpo monoclonal totalmente humanizado cuya posología recomendada es 40 mg administrados en semanas alternas4, mientras que etanercept (ETN), proteína de fusión IgG1 con el receptor de TNF de 75 kDa, se administra a razón de 50 mg semanales5.
Hoy día existe una considerable cantidad de datos clínicos en relación con la eficacia de estos fármacos y, sin embargo, todavía hay cierta incertidumbre sobre como optimizar su uso en la práctica clínica. Por ello, algunos estudios6-9 plantean que en determinados casos es posible la modificación del régimen de tratamiento (como reducciones de dosis o ampliación del intervalo de administración), como medida para su optimización.
Desde el punto de vista socioeconómico, los costes anuales derivados de la AR en España se han estimado en 2.250 millones de euros y el coste promedio anual por paciente en los 5.900 €10,11. Para la EA, el coste total medio (incluyendo costes directos e indirectos) se sitúa en los 7.920 € por paciente al año y 75.000 € en los casos de mala evolución o de enfermedad grave12.
El uso generalizado de FAMEs, la incorporación de nuevos agentes biológicos al mercado, la comorbilidad asociada y la incapacidad laboral derivada de estas patologías, junto con el análisis de estos datos, resumen el importante impacto económico que este grupo de enfermedades suponen para el Sistema Nacional de Salud.
Los análisis de impacto presupuestario son estudios cuyo propósito no es otro que estimar las consecuencias financieras de la adopción, utilización y difusión de una nueva intervención sanitaria (medicamento, producto sanitario, tecnología sanitaria) en un determinado entorno y ámbito (Sistema Nacional de Salud)13 y al mismo tiempo son análisis complementarios a diferentes evaluaciones económicas, tales como estudios coste-efectividad y coste-utilidad14,15.
Así pues, el conocimiento del impacto económico generado por los diferentes problemas de salud resulta de gran importancia. Esto es debido a que los recursos disponibles para hacer frente al gasto sanitario y social resultan limitados y es necesario diseñar estrategias para un uso eficiente de los mismos.
Por ello, el objetivo del presente estudio consiste en evaluar el impacto económico derivado de la ampliación de los intervalos de administración de ADA y ETN a cada tres semanas y dos semanas respectivamente, en el tratamiento de la AR y EAP en nuestro ámbito de trabajo.
Material y método
Se ha desarrollado un modelo de impacto presupuestario (MIP) para estimar la repercusión económica que tendría la ampliación en los intervalos habituales de administración de ADA 40 mg cada dos semanas y ETN 50 mg semanal (escenario A) en el tratamiento de patologías como la AR y EAP por ADA 40 mg cada tres semanas y ETN 50 mg cada dos semanas (escenario B).
Este modelo se ha llevado a cabo de acuerdo a las guías y recomendaciones que se aplican a estos estudios16,17, especificando la población diana, la perspectiva del estudio, el horizonte temporal, analizando la robustez del estudio a través de un análisis de sensibilidad univariante de tipo umbral y asumiendo que ambos fármacos son terapéuticamente equivalentes en el tratamiento de dichas patologías.
Población diana
Para determinar el número de pacientes candidatos a formar parte del estudio se tuvieron en cuenta los pacientes diagnosticados de AR y espondiloartropatías como EA o APs, atendidos en las consultas externas del Servicio de Reumatología del Sector Sanitario de Teruel. Los criterios de inclusión fueron: pacientes de ambos sexos, mayores de 18 años, en tratamiento activo con fármacos anti-TNFs como ADA y ETN. Los criterios de exclusión incluyeron: diagnóstico de patologías autoinmunes como enfermedad de Crohn y colitis ulcerosa, cambio de tratamiento a otro anti-TNF diferente a ADA o ETN, administración de abatacept o rituximab y discontinuación de tratamiento por efecto adverso a la terapia anti-TNF.
De los pacientes incluidos en el estudio, se recogieron las variables demográficas: edad, sexo, diagnóstico principal y años de tratamiento con terapia anti-TNF. Aquellos pacientes que se mantuvieron en remisión clínica entendiéndose por esta, valores de DAS28<2,6 para AR y APs de afectación periférica y BASDAI<4 para EA, y sin riesgo de progresión radiológica durante el último año de tratamiento, se modificaría su pauta posológica ampliando el intervalo de administración de los fármacos anti-TNF (ADA 40 mg cada tres semanas y ETN 50 mg cada dos semanas).
Perspectiva del estudio y horizonte temporal
Dado que se trata de un MIP la perspectiva elegida fue la del financiador, en este caso la propia Institución (Hospital) y el Servicio Aragonés de Salud. Sólo se incluyeron aquellos recursos sanitarios financiados públicamente, es decir costes directos generados por cada rama en estudio, no incluyendo por tanto, los costes financiados por el paciente o las pérdidas de productividad laboral u otros costes indirectos. El horizonte temporal considerado fue de dos años (2011-2013).
Análisis de sensibilidad
Dado que todo modelo económico lleva asociado cierto nivel de incertidumbre debido a las asunciones realizadas, se realizó un análisis de sensibilidad univariante y de tipo umbral con aquellas variables en las que se estimó tenían incertidumbre asociada, variando los valores adoptados en el escenario base dentro de un rango que osciló entre ± 50%. Las variables utilizadas fueron: el coste del tratamiento con ADA y ETN, el porcentaje de pacientes en tratamiento con ADA y el porcentaje de pacientes en tratamiento con ETN candidatos a la ampliación de su intervalo posológico.
Descripción del Modelo de Impacto Presupuestario (MIP)
Finalmente, se calculó el ahorro potencial observado tras la modificación del intervalo de administración. Dicho MIP se calculó para ambos fármacos mediante la siguiente fórmula15:
Impacto presupuestario = [CMa*(Na- Nnt)]+(CMni*Nni) -(CMa*Na)
donde CMe1 y CMa2 eran el coste medio mensual de los pacientes tratados con ETN 50 mg semanal o ADA 40 mg semanas alternas y Ne1 y Na2 el número de pacientes con esta pauta posológica. CMe2, CMa3y Ne2, Na3 eran los costes medios mensuales de los pacientes y el número de pacientes que se estimaba adoptarían la nueva intervención (ADA 40 mg cada 3 semanas, ETN 50 mg cada 2 semanas).
También se obtuvieron los ahorros proporcionales en función del porcentaje de pacientes de la población usuarios de la nueva intervención (ampliación del intervalo terapéutico), teniendo en cuenta una introducción progresiva de la misma.
Además las variables económicas por patología incluyeron el coste medio por paciente y coste medio mensual. Los costes de los medicamentos considerados se expresaron en euros (€), referidos a PVL+ IVA (4%) y al periodo de 2012. En el cómputo de estos costes se tuvo en cuenta la deducción del 7,5% estipulada por el Real Decreto-ley 8/2010, de 20 de mayo, para la compra de medicamentos con cargo a fondos públicos del Sistema Nacional de Salud.
Análisis estadístico
Se analizaron las frecuencias expresadas en porcentajes de pacientes para variables cualitativas, y para las variables cuantitativas se calculó la media y desviación estándar (DE).
Se comprobó la normalidad de la distribución con la prueba Shapiro-Wilk y la homogeneidad de varianzas mediante la prueba de Levene. Al no cumplir el supuesto de normalidad se aplicaron pruebas no paramétricas. Así para comparar variables cuantitativas independientes se utilizó el test U de Mann-Whitney y para variables cualitativas se empleó el test χ2.
El análisis estadístico fue realizado mediante el programa informático PASW Statistics 18.0 (IBM® SPSS software) donde se fijó un umbral de p = 0,05 para aceptar o rechazar la hipótesis nula.
Resultados
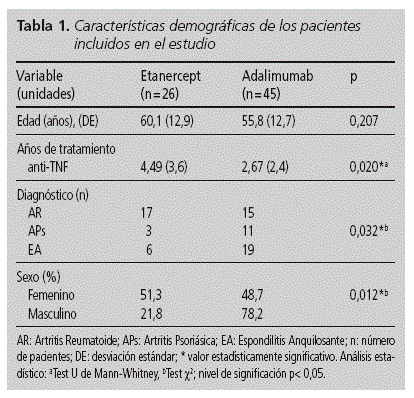
El número total de pacientes que formaron parte del estudio fue 71. El resumen de las características demográficas se observa en la tabla 1.
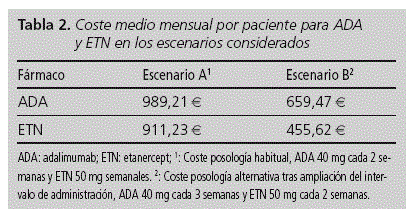
En cuanto a las variables económicas, el coste medio mensual teniendo en cuenta la patología fue de 30.329 € para AR, 13.615 € para APs y 24.262 € en el caso de EA. El coste total para las tres indicaciones ascendió a 68.206 €. El coste medio mensual por paciente para ADA y ETN antes y tras la ampliación del intervalo de administración se muestra en la tabla 2.
Por otro lado, el número de pacientes que cumplieron criterios de remisión clínica y candidatos a la aplicación del escenario B fueron en el grupo de ADA, cinco pacientes, y en el grupo de ETN, siete pacientes. La aplicación del MIP mostró unos ahorros anuales para ADA y ETN de 19.784 € y 38.271 € respectivamente. El coste neto, es decir, el ahorro que esto supuso en el horizonte temporal considerado (dos años) ascendió a 116.110 €.
Por otra parte, la figura 1 muestra el ahorro total en euros en función de la introducción progresiva de la terapia anti-TNF en la población de estudio. Los ahorros potenciales corresponden a la diferencia entre los resultados del coste actual de los pacientes con las pautas posológicas habituales y los costes futuros teniendo en cuenta una introducción progresiva de la nueva intervención.
Análisis de sensibilidad
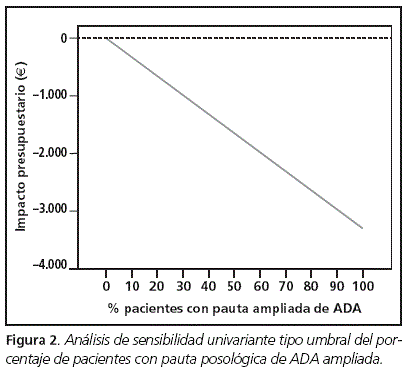
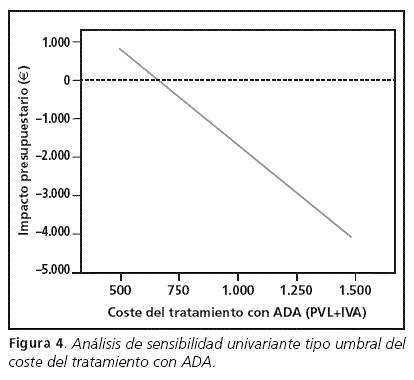
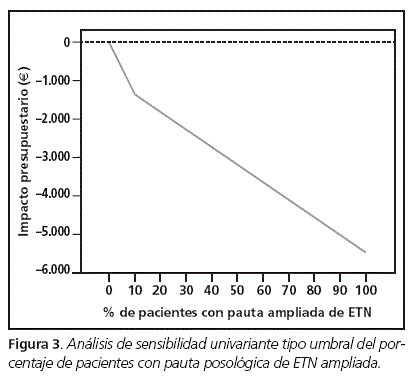
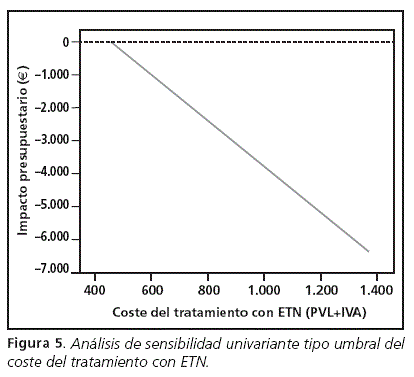
El análisis de sensibilidad realizado (figuras 2-5) muestra que el MIP estimado para el periodo 2011-2013 es robusto ya que el resultado neto en diferentes escenarios apenas varía, manteniéndose negativo en los nuevos escenarios. Sólo la figura 4, para costes de tratamiento con ADA inferiores a 600 €, muestra valores positivos, no consiguiéndose en este supuesto ahorros económicos para el modelo.
Discusión
De acuerdo con los estudios publicados hasta la fecha18-22, para la realización de este estudio y el desarrollo del MIP se ha asumido que ambos fármacos son terapéuticamente equivalentes en el tratamiento de dichas patologías. No obstante, es evidente que esta asunción no estará plenamente validada hasta que se disponga de ensayos clínicos que comparen directamente ambas alternativas.
En primer lugar, el análisis de las variables demográficas de la población mostró diferencias significativas salvo para la edad de los individuos (p=0,207). La distribución de sexos y la edad promedio en la muestra de estudio son equiparables a los obtenidos en otros trabajos23-25, siendo la patología más prevalente la AR (p = 0,032).
En segundo lugar, centrándonos en la perspectiva económica, observamos que ambos fármacos suponen una parte importante del gasto farmacéutico del hospital, cercano a los 68.000 € mensuales para las tres indicaciones, lo cual hace suponer que pequeñas intervenciones para el control del gasto en este campo podrían conseguir importantes ahorros económicos.
En el MIP diseñado en este trabajo, la aplicación del escenario B frente al escenario A, supondría ahorros económicos del orden de 120.000 € en el periodo de estudio, lo cual permitiría derivar estos recursos hacia el tratamiento de nuevos pacientes diagnosticados de AR o EAP y candidatos a recibir terapia anti-TNF.
Particularmente este ahorro aumenta de forma importante cuando se incrementa el número de pacientes candidatos a adoptar la pauta de intervalo ampliado. Así un porcentaje de introducción en la población de la pauta de administración ampliada (escenario B) cercano al 70% puede conseguir reducciones del gasto próximos a los 8.000 € y 11.000 € mensuales para ETN y ADA respectivamente (figura 1), es decir, teniendo en cuenta el horizonte temporal considerado (dos años) supondría ahorros de entre 192.000 € a 264.000 €.
Con relación a estos datos y a pesar de la falta de estudios al respecto, en nuestro país el estudio PRAXIS26 describió como la sustitución de ADA por ETN generaba un impacto económico de entre 22.600 € y 362.600 € para un hospital de 200 camas, reflejando así la importancia de incidir sobre estas terapias.
Sin embargo, dado que el sistema de información en salud no es perfecto, los resultados obtenidos en el MIP no están exentos de cierto grado de incertidumbre en las estimaciones realizadas. Así pues, el análisis de sensibilidad realizado nos ha permitido minimizar los posibles errores y comprobar la robustez del modelo.
Tal como muestran las figuras 2-5, la modificación de las variables sometidas a incertidumbre tales como el porcentaje de pacientes con pauta ampliada y coste del tratamiento tanto para ADA como ETN, muestran valores negativos o ahorros en la mayoría de los casos. Únicamente en el caso particular de un coste inferior a los 600 € para ADA ha mostrado ser sensible a este análisis, no obteniendo ahorros en el modelo (figura 4).
Este modelo, como todos los MIP presenta ciertas limitaciones. Entre ellas el limitado número de pacientes incluidos en el estudio, posiblemente debido a la dificultad en nuestro Hospital para recabar una muestra mayor, consecuencia de una gran dispersión y densidad poblacional pequeña. Por otro lado, se trata de un modelo de proyección futura en el uso de un grupo determinado de medicamentos, basado en algunas asunciones y en la actitud esperada de los clínicos ante la introducción de la nueva intervención o escenario. Tampoco se recogen datos del número de pacientes que recaen o empeoran tras la modificación del tratamiento, lo que complementaría los datos económicos obtenidos a lo largo del trabajo.
A pesar de las limitaciones expuestas en el estudio, la ampliación de los intervalos de administración de ADA y ETN cada tres semanas y dos semanas respectivamente, sería una estrategia que permitiría generar ahorros en el presupuesto hospitalario cercanos a los 116.110 € en el horizonte temporal considerado, consiguiendo así una optimización del tratamiento con estos fármacos y una gestión adecuada de los recursos disponibles.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
1. Griffith J, Carr A. What is the impact of early rheumatoid arthritis on the individual? Best Practice & Research in Clin Rheumatol. 2001;15(1):77-90. [ Links ]
2. Khan MA. Update on spondyloarthropathies. Ann Intern Med. 2002;136(12):896-907. [ Links ]
3. Onen F, Akar S, Birlik M, Sari I, Gurler O, Ergor A, et al. Prevalence of ankylosing spondylitis and related spondyloarthritis in an urban area of Izmir, Turkey. Ann Rheum Dis. 2006;65:541-2. [ Links ]
4. Lab. Abbvie Ltd. Ficha técnica de Humira® (adalimumab) (actualizado 9/2008). Disponible en: http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/000481/WC500050870.pdf. [ Links ]
5. Lab. Pfizer Limited. Ficha técnica de Enbrel® (etanercept) (actualizado 2/2010). Disponible en: http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/000262/WC500027361.pdf. [ Links ]
6. Moghimi J, Sheikhvatan M, Semnani V. The use of low-dose etanercept as an alternative therapy for treatment of ankylosing spondylitis: a case series. Rheumatol Int. 2012;32(8):2271-4. [ Links ]
7. Berthelot JM, Varin S, Cormier G, Tortellier L, Guillot P, Glemarec J, et al. 25 mg etanercept once weekly in rheumatoid arthritis and spondylarthropathy. Joint Bone, Spine. 2007;74(2):144-7. [ Links ]
8. Lee J, Noh JW, Hwang JW, Oh JM, Kim H, Ahn JK, et al. Extended dosing of etanercept 25 mg can be effective in patients with ankylosing spondylitis: a retrospective analysis. Clin Rheumatol. 2010;29(10):1149-54. [ Links ]
9. Castro Villegas Mdel C, Escudero Contreras A, Miranda Garcia MD, Collantes Estevez E. How to optimize the antiTNF alpha therapy in spondylitis? Reumatol Clin. 2012;8 Suppl 1:S26-31. [ Links ]
10. Lajas C, Abasólo L, Bellajdel B, Hernandez-Garcia C, Carmona L, Vargas E, et al. Costs and predictors of costs in rheumatoid arthritis: A prevalence-based study. Arthritis Rheum. 2003;49(1):64-70. [ Links ]
11. Ruiz-Montesinos MD, Hernandez-Cruz B, Ariza-Ariza R, Carmona L, Ballina J, Navarro-Sarabia F, et al. Cost analysis in a cohort of rheumatoid arthritis patients managed in rheumatology units in Spain. Reumatol Clin. 2005;1(4):193-9. [ Links ]
12. Kobelt G, Sobocki P, Mulero J, Gratacos J, Pocovi A, Collantes-Estevez E. The burden of ankylosing spondylitis in Spain. Value Health. 2008;11(3):408-15. [ Links ]
13. Mauskopf JA, Earnshaw S, Mullins CD. Budget impact analysis: review of the state of the art. Expert Rev Pharmacoecon Outcomes Res. 2005;5(1):65-79. [ Links ]
14. Hilden J. Budget impact analysis and its rational basis. Med Decis Making. 2008;28(4):460-1. [ Links ]
15. Brosa M, Gisbert R, Rodríguez JM, Soto J. Principios, métodos y aplicaciones del análisis de impacto presupuestario en el sector sanitario. Pharmacoeconomics Spa Res Articl. 2005 (2):65-78. [ Links ]
16. Trueman P, Drummond M, Hutton J. Developing guidance for budget impact analysis. Pharmacoeconomics. 2001;19(6):609-21. [ Links ]
17. Orlewska E, Mierzejewski P. Proposal of polish guidelines for conducting financial analysis and their comparison to existing guidance on budget impact in other countries. Value Health. 2004;7(1):1-10. [ Links ]
18. Salliot C. Indirect comparisons of the efficacy of biological antirheumatic agents in rheumatoid arthritis in patients with an inadequate response to conventional disease-modifying antirheumatic drugs or to an antitumour necrosis factor agent: a meta-analysis. Ann Rheum Dis. 2011;70(3):660-5. [ Links ]
19. Schmitz S, Adams R, Walsh CD, Barry M, FitzGerald O. A mixed treatment comparison of the efficacy of anti-TNF agents in rheumatoid arthritis for methotrexate non-responders demonstrates differences between treatments: a Bayesian approach. Ann Rheum Dis. 2012;71(2):225-30. [ Links ]
20. Mandema JW, Salinger DH, Baumgartner SW, Gibbs MA. A Dose Response Meta-Analysis for Quantifying Relative Efficacy of Biologics in Rheumatoid Arthritis. Clin Pharmacol Ther. 2011;90(6):828-35. [ Links ]
21. Kirchhoff TD, Mittendorf T, Schmidt RE, Jablonka A, Merkesdal S. Cost-effectiveness of TNF-alpha inhibition in active ankylosing spondylitis: a systematic appraisal of the literature. Expert Rev Pharmacoecon Outcomes Res. 2012;12(3):307-17. [ Links ]
22. Cortesi PA, Scalone L, D'Angiolella L, Belisari A, Fusco F, Olivieri I, et al. Systematic literature review on economic implications and pharmacoeconomic issues of psoriatic arthritis. Clin Exp Rheumatol. 2012;30(4):126-31. [ Links ]
23. Carter CT, Changolkar AK, Scott McKenzie R. Adalimumab, etanercept, and infliximab utilization patterns and drug costs among rheumatoid arthritis patients. J Med Econ. 2012;15(2):332-9. [ Links ]
24. Bullano MF, McNeeley BJ, Yu YF, Quimbo R, Burawski LP, Yu EB, et al. Comparison of costs associated with the use of etanercept, infliximab, and adalimumab for the treatment of rheumatoid arthritis. Manag Care Interface. 2006;19(9):47-53. [ Links ]
25. Wu E, Chen L, Birnbaum H, Yang E, Cifaldi M. Cost of care for patients with rheumatoid arthritis receiving TNF-antagonist therapy using claims data. Curr Med Res Opin. 2007;23(8):1749-59. [ Links ]
26. Rubio-Terres C, Ordovas Baines JP, Pla Poblador R, Martinez Nieto C, Sánchez Garre MJ, Rosado Souviron MA, et al. Use and cost of biological disease-modifying antirheumatic drugs in Spain (PRAXIS study). Farm Hosp. 2007;31(2):78-92. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico: agonzalezal@salud.aragon.es
(Alejandro González Álvarez)
Correo postal: Servicio de Farmacia.
Hospital Obispo Polanco.
Avenida Ruiz Jarabo, s/n.
44002 Teruel
Recibido: 20 de marzo de 2013.
Aceptado: 15 de abril de 2013.