Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Farmacia Hospitalaria
versión On-line ISSN 2171-8695versión impresa ISSN 1130-6343
Farm Hosp. vol.40 no.1 Toledo ene./feb. 2016
https://dx.doi.org/10.7399/fh.2016.40.1.10220
CARTAS AL DIRECTOR
Neumonitis intersticial por mesalazina en paciente con colitis ulcerosa
Mesalazine-induced intersticial pneumonitis in patients with ulcerative colitis
Dirección para correspondencia
Introducción
La mesalazina (5-ASA) y la sulfasalazina (sulfapiridina más 5-ASA) son aminosalicilatos ampliamente utilizados en el tratamiento de la enfermedad inflamatoria intestinal (EII). La mayoría de los efectos secundarios en el caso de la sulfasalazina han sido atribuidos a uno de sus metabolitos, la sulfapiridina, y no a la mesalazina. Sin embargo, existen algunos casos publicados que asocian la toxicidad pulmonar a la administración de mesalazina1. Las enfermedades pulmonares intersticiales difusas (EPID) constituyen un grupo de afecciones con manifestaciones clínicas, radiológicas y funcionales respiratorias similares; la etiología de las EPID es muy variada, solo en un 35% de los casos suele identificarse el agente causal. Las EPID por fármacos son relativamente frecuentes2.
Las manifestaciones clínicas más frecuentes son la disnea de esfuerzo y la tos; generalmente la disnea es progresiva, por lo que el paciente no es consciente de su estado hasta las 2 o 3 semanas, desde el inicio de la sintomatología. Hasta en un 15% de los casos la primera pista para el diagnóstico de patología intersticial es la alteración de la función pulmonar3. Habitualmente, la sospecha de que sea un fármaco el que puede estar provocando la situación clínica de neumonitis intersticial se produce cuando se descartan otras causas más frecuentes y otros procesos, como los neoplásicos.
Caso
Varón de 63 años, exfumador de menos de 5 cigarros al día con abandono del hábito tabáquico hace más de 10 años. Diagnosticado de colitis ulcerosa dos meses antes, había iniciado tratamiento con mesalazina oral (2 g cada 12 h durante el primer mes), siendo esta dosis reducida a 1 g cada 12 h tras estabilización de la patologia digestiva. Acude a la puerta de Urgencias con un cuadro de tos y disnea tras haber realizado durante 10 días tratamiento antibiótico con moxifloxacino (400 mg cada 24 h), y claritromicina (500 mg cada 12 h), por diagnóstico previo de neumonía incipiente y empeoramiento del cuadro. Se le realiza una auscultación, con presencia de crepitantes secos, y una placa de tórax, en la que aparecen infiltrados intersticiales con un patrón difuso bilateral. Se observa en la analítica una leve leucocitosis (11.100 leucocitos con 6% cayados) y una PCR en 18 mg/L. Se le realiza un TAC (tomografía axial computarizada) de urgencias en la que se observa la presencia de lesiones pulmonares compatibles con Enfermedad Intersticial Difusa Crónica (EPID); se habla con el Servicio de Neumología y se decide su ingreso para estudio.
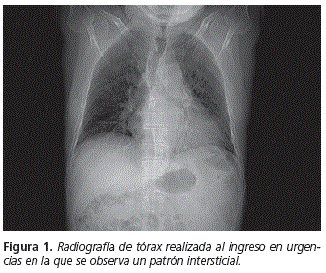

Durante el ingreso se le realiza una broncoscopia con toma de varias muestras (biopsia endobronquial, biopsia aspirado bronquial, biopsia cepillado bronquial) para análisis anatomopatológico, cuyos resultados ponen de manifiesto la ausencia de células neoplásicas y la presencia en la biopsia transbronquial de fibrosis leve y edema, con resto de biopsias sin hallazgos de interés. Se le realiza un estudio espirométrico, dando como resultado un patrón restrictivo con una FEV1 del 75% y una relación FEV1/FVC del 84% (FVC: 65%). Para descartar la patología infecciosa se solicita un cultivo microbiológico del aspirado bronquial, dando como resultado una flora normal y negativo para micobacterias. Se le realiza también un Mantoux que sale negativo, descartándose por tanto la infección por Mycobacterium tuberculosis. Tras descartar enfermedades de origen infeccioso y neoplásico, se realiza una búsqueda bibliográfica en Pubmed con el objetivo de poder encontrar otros factores relacionados con el paciente que pudiesen estar implicados en el desarrollo de la neumopatía, utilizando como criterio de búsqueda, "Pulmonary injury" and "Mesalazine", encontrando en la literatura científica varios casos que relacionan la mesalazina con la aparición de neumopatías intersticiales. Ante tales hallazgos, y tras consultar con el Servicio de Digestivo, se decide la retirada de la mesalazina y el alta del paciente por su estabilidad clínica respiratoria con seguimiento ambulatorio.
Tras un mes de la retirada del fármaco, se revisa al paciente en consulta, observando mejoría clínica de la disnea, desaparición auscultatoria de crepitantes y evolución positiva del patrón espirométrico, solicitando TAC de control a los seis meses posteriores a la retirada del fármaco, el cual da como resultado la desaparición de áreas de panalización y signos de fibrosis pulmonar.
Discusión
El uso de aminosalicilatos en la EII está basado en ensayos clínicos controlados, desarrollados en la década de los años setenta. En el caso de los aminosalicilatos tópicos u orales son los fármacos de elección en el tratamiento de la colitis ulcerosa leve a moderada4. La incidencia de enfermedad pulmonar intersticial en pacientes que sufren EII no se conoce sin embargo, se sabe que más del 50% de los pacientes que padecen EII tienen alteraciones de la función pulmonar sin hallazgos clínicos ni radiológicos. Los pacientes en tratamiento con sulfasalazina o mesalazina pueden desarrollar enfermedad pulmonar intersticial como reacción a la medicación5. Las alteraciones pulmonares, como la neumonitis por fibrosis, solo están recogidas como reacciones "muy raras" en la ficha técnica de algunas de las presentaciones de mesalazina disponibles en el mercado, complicando la identificación de los posibles casos6. Existen en la bibliografía varios artículos publicados en los que se relaciona el desarrollo de alteraciones pulmonares en pacientes con EII, como nuestro caso, y la administración de mesalazina; sin embargo, un factor que puede condicionar la identificación del cuadro como una reacción adversa a la mesalazina es el comienzo de los síntomas tras el inicio del tratamiento, ya que aunque en algunos casos existe una secuencia temporal razonable, como el caso publicado por Alskaf en 20137, en el que el paciente desarrolla un cuadro respiratorio a los diez días de iniciar el tratamiento, existen por el contrario otros casos reportados en los que el inicio del compromiso respiratorio se da a los tres meses8, como el nuestro o incluso después de siete años de tratamiento9.
En nuestro caso, aplicamos el algoritmo de Karch-Lasagna10 para establecer la relación entre la fibrosis pulmonar y la mesalazina, estableciéndose como "probable", ya que debido al riesgo que suponía reintroducir el fármaco de nuevo, no pudimos comprobar si los efectos reaparecían al reiniciar el tratamiento.
Concluimos por tanto que la mesalazina es un fármaco que produce neumopatías, por lo que es fundamental el conocimiento de esta reacción adversa por parte de los profesionales sanitarios, para poder detectarla a tiempo y no exponer al paciente a demasiadas pruebas invasivas en busca de otras etiologías.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Elena Prado Mel1 y Maria Gil López2
1Farmacéutica Especialista en Farmacia Hospitalaria. Servicio de Farmacia.
Hospital Universitario Virgen del Rocío. Sevilla.
2Médica Especialista en Medicina Familiar y Comunitaria.
Servicio de Urgencias. Hospital Comarcal Nuestra Señora de la Merced.
Osuna, Sevilla. España.
Bibliografía
1. Tanikawa K, Sugiyama K, Matsuyama H, Nakao H, Kohno K, Komuro Y, et al. Mesalazine-Induce Eosinophilic Pneumonía. Respiration. 1999;66(1):69-72. [ Links ]
2. Demetds M, Wells AM, Antó JM, Costobel U, Hubbard R, Cullinon P, et al. Interstitial lung disease: an epidemiological over-view. Eur Respir J. 2001;18(Suppl 32): 2S-16S. [ Links ]
3. Bollo de Miguel E, García Romero de Tejada JA, Juárez Morales C, Muñíz González F. Neumonías intersticiales idiopáticas. Arch Bronconeumol. 2011;47(Supl 8):15-19. [ Links ]
4. Gomollón F, García-López S, Sicilia B, Gisbert JP, Hinojosa. Guía clínica GETECCU del tratamiento de la colitis ulcerosa elaborada con la metodología GRADE. Gastroenterol Hepatol. (revista en internet) 2012 (citado 01/09/2015); 38(8): e1-e47. Disponible en: http://dx.doi.org/10.1016/j.gastrohep.2012.11.001. [ Links ]
5. Vennera MC, Picado C. Manifestaciones pulmonares de las enfermedades inflamatorias intestinales. Arch Bronconeumol. 2005;41(2): 93-8. [ Links ]
6. AEMPS: Centro de Información online de Medicamentos de la AEMPS - CIMA (Internet). Madrid: Agencia Española del Medicamento y Productos Sanitarios; (citado 9/09/2015). Disponible en: http://www.aemps.gob.es/cima/fichasTecnicas.do?metodo=detalleForm. [ Links ]
7. Alskaf E, Aljoudeh A, Edenboroug F. Mesalazine-induced lung fibrosis. BMJ Case Rep. (revista en internet) 2013 (citado 15/10/2015). Disponible en: http://doi:10.1136/bcr-2013-008724. [ Links ]
8. Sossai P, Cappellato MG, Stefani S. Can a drug-induced pulmonary hypersensibility reaction be dose-dependent?. A case with mesalamine. Mt Sinai J Med. 2001;68(6):389-95. [ Links ]
9. Shindoh Y, Horaguchi R, Hayashi K, Suda Y, lijima H, Shindoh C. A case of lung injury induced by long-term administration of mesalazine. Nihon Kokyuki Gakkai Zasshi. 2011; 49(11): 861-6. [ Links ]
10. Naranjo CA, Busto U, Sellers EM, Sandor P, Ruiz I, Roberts EA, et al. A method for estimating the probability of adverse drug reactions. Clin Pharmacol Ther. 1981;30(2): 239-45. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico: elenapradomel@gmail.com
(Elena Prado Mel).
Recibido: el 12 de noviembre de 2015;
Aceptado: el 23 de diciembre de 2015.














