Sra. Directora:
El índigo carmín o indigotina (E-132) es un colorante sintético de color azul empleado en la industria alimentaria y como excipiente farmacéutico. Se encuentra habitualmente en formas farmacéuticas orales. Además, es utilizado en cromoendoscopia para diagnóstico de pólipos -neoplasias colorrectales1, así como para otras aplicaciones diagnósticas2. Aunque el efecto adverso más común tras la administración parenteral es de tipo cardiovascular, se han descrito casos de decoloración cutánea tras extravasación, resolviéndose tras 24 horas aproximadamente2.
Se presenta el caso de un paciente de 10 años con decoloración dental en relación con la toma de metilfenidato (Medikinet® 30 mg). Tenía dificultad para ingerir la cápsula, por lo que se le indicó la posibilidad de abrirla para tomar su contenido con alimento, tal y como se refleja en el apartado 4.2 de la ficha técnica (FT)3. Desde el inicio de la toma del contenido capsular, el paciente presentó una “coloración considerablemente oscura del esmalte dental”. El caso se notificó de manera espontánea en junio de 2018 al Centro Regional de Farmacovigilancia del Principado de Asturias, como reacción adversa (RAM) de tipo “dientes manchados” según el Lowest Level Term (LLT) del Medical Dictionary for Medical Activities (MedDRA). El desenlace se calificó como recuperado/resuelto al revertirse la RAM ingiriendo las cápsulas enteras.
Esta RAM no está descrita en FT, a pesar de las referencias publicadas de tinción cutánea con el uso por vía parenteral y de los casos de coloración dental con el uso por vía oral. Tras revisar las FT de todas las presentaciones de Medikinet ®, encontramos que la indigotina está presente en el contenido capsular en todos los casos. Sin embargo, solo se encuentra en la envoltura en las presentaciones de 30 y 40 mg. En las cápsulas de 10 y 20 mg, el excipiente que forma parte de la envoltura es el azul patentado V (E-131). En otras presentaciones de metilfenidato comercializadas no se encontró indigotina como excipiente.
No se encontraron casos similares en la base de datos de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS): Farmacovigilancia Española, Datos de Reacciones Adversas (FEDRA®). Se analizó la base de datos de la Organización Mundial de la Salud, VigiBase™, encontrándose descritas 37.747 RAM para metilfenidato; 123 para el High-Level Group Term (HLGT) “alteraciones dentales y gingivales”, de las cuales 39 correspondían a niños de entre 2 y 11 años (31,7%). De los 123 casos, 21 (17,1%) se correspondían con el Preferred Term (PT) “decoloración dental”, siendo 14 (35,9%) en el grupo de niños de 2-11 años. El número total de casos de tinción dental podría estar infraestimado debido a la gran cantidad de PT existentes que engloban RAM dentales inespecíficas; como “trastorno dental” con 21 casos (17,1%) en población general y 6 casos (15,4%) en el segundo grupo, entre otros. En la Tabla 1 se pueden ver los diferentes PT de alteraciones dentales y gingivales recogidos para metilfenidato. Se ha descrito algún caso aislado de coloración amarillenta, pudiendo estar en relación con el cambio de color del E-132 en función del pH (azul a pH 11,4 y amarillo a pH 13)4.
Tabla 1. Reacciones adversas registradas en VigiBase™ con el HLGT “alteraciones dentales y gingivales” para metilfenidato, a fecha de 15 de julio de 2018.
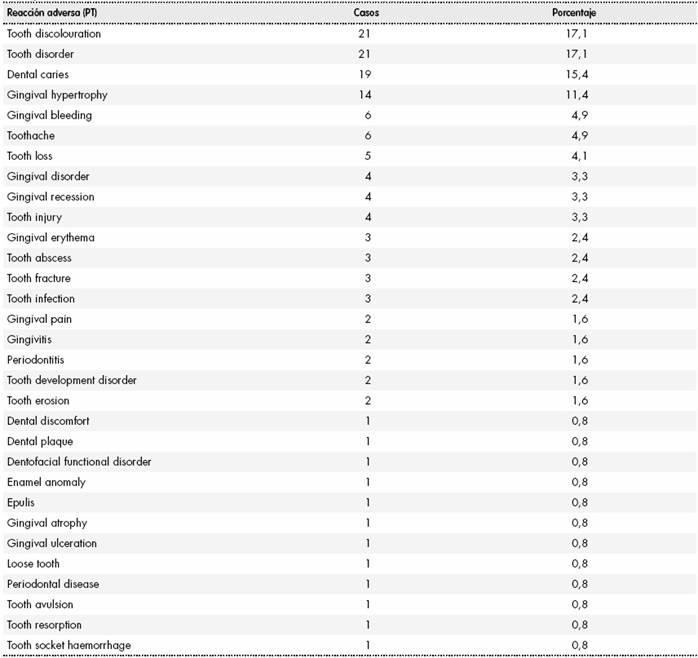
HLGT: High-Level Group Term; Preferred Term. The information is extracted from VigiBase, the WHO global database of individual case safety reports (ICSRs).
De acuerdo con lo detallado anteriormente, se proponen como posibles medidas correctoras: 1) Modificación de la FT, introduciendo una advertencia sobre la posible RAM de coloración dental con la apertura de la cápsula en el apartado 4.4, así como introducir la RAM en el apartado 4.8. 2) Supresión de la posibilidad de tomar el fármaco fuera de la envoltura o bien el cambio de excipientes en las presentaciones correspondientes.
Se debería fomentar el conocimiento y manejo por parte de los profesionales sanitarios de los excipientes y sus posibles efectos adversos, dada la potencial repercusión en términos de adherencia. Asimismo, parece necesaria la reevaluación del listado de excipientes de declaración obligatoria según el Real Decreto 1345/20075.














