My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Farmacia Hospitalaria
On-line version ISSN 2171-8695Print version ISSN 1130-6343
Farm Hosp. vol.43 n.4 Toledo Jul./Aug. 2019 Epub Oct 14, 2019
https://dx.doi.org/10.7399/fh.11183
ORIGINALES
Adherencia a las terapias biológicas en pacientes con artropatías inflamatorias crónicas
1Servicio de Farmacia, Complejo Hospitalario Universitario de Vigo, Vigo. España.
2Servicio de Farmacia, Centro Sanitario Centro Penitenciario A Lama, Pontevedra. España.
3Servicio de Reumatología, Complejo Hospitalario Universitario de Vigo, Vigo. España.
Objetivo
Los objetivos del estudio fueron cuantificar la adherencia, determinar los factores predictivos y conocer las consecuencias de una menor adherencia, en la práctica clínica diaria, en pacientes con artropatías inflamatorias crónicas tratados con terapias biológicas.
Método
Estudio descriptivo, observacional y retrospectivo. Se incluyeron pacientes con artritis reumatoide, espondilitis anquilosante y artritis psoriásica que iniciaron una terapia biológica entre el 1 de enero de 2009 y el 31 de diciembre de 2016. Se recogieron variables sociodemográficas, relacionadas con la enfermedad, sobre las terapias biológicas y los recursos hospitalarios. La adherencia se calculó mediante la ratio media de posesión.
Resultados
Se incluyeron 362 pacientes y 423 líneas de terapia biológica. La media de edad ± desviación estándar fue de 50,3 ± 13,9 años; 228 (53,9%) fueron mujeres. El porcentaje de adherentes fue de 187 de 216 (87%) en artritis reumatoide, 91 de 107 (85%) en espondilitis anquilosante y 84 de 100 (84%) en artritis psoriásica. La adherencia se relacionó con acudir con más frecuencia a la consulta del servicio de farmacia (odds ratio de 1,2; intervalo de confianza 95%: 1,1-1,3 ( p < 0,001)) e inversamente con no acudir a las consultas de reumatología en la fecha prevista (odds ratio de 0,2; intervalo de confianza 95%: 0,1-0,9 (p = 0,030)).
No hubo diferencias en el número de recursos hospitalarios utilizados por pacientes adherentes y no adherentes.
Conclusiones
La adherencia a las terapias biológicas entre las artropatías inflamatorias crónicas es similar. Dicha adherencia se correlaciona con la frecuentación a consultas externas, pero no implica un aumento del consumo de recursos.
PALABRAS CLAVE: Artritis reumatoide; Artritis psoriásica; Espondilitis anquilosante; Terapias biológicas; Adherencia a la medicación; Factores de riesgo
Introducción
La introducción de las terapias biológicas (TB) en el tratamiento de las artropatías inflamatorias crónicas (AIC), como la artritis reumatoide (AR), la espondilitis anquilosante (EA) y la artritis psoriásica (APs), ha supuesto una revolución farmacoterapéutica que ha producido mejoras considerables en el pronóstico de las AIC y en la calidad de vida de los pacientes1. Sin embargo, el sistema sanitario soporta una elevada carga económica debido a que las AIC son enfermedades crónicas y el coste de las TB es muy elevado2 3 4-5. La falta de adherencia en los tratamientos crónicos es un problema universal y real que compromete su efectividad y se puede traducir en un empeoramiento de la enfermedad, muerte e incrementos de los costes sanitarios6,7.
Existen publicaciones sobre la adherencia en las AIC7 8 9-10, aunque la mayoría de ellas son en pacientes con AR. Existen pocos datos sobre los factores predictivos de adherencia a las TB en pacientes con AIC11 y las consecuencias que implican para el sistema sanitario una menor adherencia11,12.
Los objetivos de este estudio fueron:
Cuantificar la adherencia a las TB en una cohorte de pacientes diagnosticados de AIC en la práctica clínica diaria.
Determinar los factores que pueden predecir la adherencia a las TB.
Conocer las consecuencias a nivel de recursos hospitalarios de una menor adherencia a las TB.
Métodos
Se realizó un estudio retrospectivo, descriptivo y observacional. El estudio se desarrolló en un hospital de tercer nivel que proporciona cobertura sanitaria a 564.452 ciudadanos. El Servicio de Farmacia (SF) dispone de una consulta monográfica para la atención a pacientes con TB y AIC, con una carga de trabajo de 3.000 consultas anuales (7,5% del total de la actividad de consultas externas del SF). Todos los pacientes que acuden a dicha consulta son atendidos por un farmacéutico especialista en farmacia hospitalaria. Las TB por vía intravenosa son administradas en el Hospital de día del mismo hospital.
Se incluyeron aquellos pacientes adultos diagnosticados de AR, EA o APs en seguimiento por el Servicio de Reumatología, que cumplían los criterios de clasificación de AR de la American Rheumatism Association 198713, los criterios de clasificación de EA de Nueva York modificados14,15 y los criterios CASPAR de clasificación de APs16, que iniciaron una TB con abatacept, adalimumab, certolizumab, etanercept, golimumab, infliximab, tocilizumab o ustekinumab, a partir del 1 de enero de 2009 y hasta 6 meses antes de la fecha de fin del estudio (31 de diciembre de 2016), y con una duración mínima de la TB de 180 días.
Para la obtención de la información clínica se consultó la historia clínica electrónica de cada paciente. Los datos que se recopilaron sobre las enfermedades y la utilización de los medicamentos se correspondieron con el patrón de la práctica clínica habitual. Al inicio de la TB se recogieron variables demográficas (edad y sexo), socioculturales (situación laboral, nivel cultural, hábito tabáquico, tamaño de población de residencia y distancia entre el domicilio y el hospital), clínicas (años de evolución de la enfermedad y comorbilidades según el índice de Charlson17) y parámetros analíticos como proteína C reactiva, velocidad de sedimentación globular y hemoglobina al inicio de la TB.
Para la evaluación de las posibles consecuencias de la no adherencia se tuvieron en cuenta los recursos sanitarios consumidos por los pacientes en atención especializada durante el periodo de tiempo en el que se midió la adherencia: número de ingresos hospitalarios, visitas al servicio de urgencias hospitalarias, visitas a la consulta de reumatología, visitas a otras consultas, visitas a la consulta externa del SF y al Hospital de día y pruebas de imagen (radiografías, resonancia magnética y de medicina nuclear). Para poder realizar comparaciones adecuadamente se calculó el consumo medio por paciente y año de TB.
En relación con las TB, se registraron los tratamientos concomitantes al inicio de la TB (metotrexato, leflunomida y glucocorticoides), la pauta posológica, la vía de administración y el número de línea de TB. Se registró si el paciente tomaba simultáneamente algún fármaco psicoactivo de los grupos NO5B, N05C, N06A, N06B, N06C y N06D según el Sistema de clasificación Anatómica, Terapéutica, Química18, por la posible relación entre una falta de adherencia y la toma de tratamientos psicoactivos19.
Para el cálculo de la adherencia se empleó la ratio media de posesión (RMP), que se define como el número de días con tratamiento dispensado dividido entre el número total de días del periodo analizado. Los datos sobre el número de dispensaciones de TB recogidas por el paciente se obtuvieron de los registros electrónicos del programa Silicon®. En el caso de los tratamientos que se administraban en Hospital de día, se tuvieron en cuenta los días en los que el paciente acudió a dicha unidad, registrados en el programa Oncofarm®. Se descontaron los tiempos de parada temporal debidos a ingresos hospitalarios o embarazo. Para el cálculo del número de días del periodo analizado se tuvo en cuenta la posología prescrita por el reumatólogo, y no la de la ficha técnica, por ello se consideraron optimizaciones e intensificaciones de dosis.
Para la evaluación de los posibles factores que podían predecir una mejor adherencia a las TB y las consecuencias de una mala adherencia, se dividió la muestra en dos grupos, líneas de TB en las que los pacientes son adherentes (RMP ≥ 0,8) y aquellas líneas de TB donde los pacientes no son adherentes (RMP<0,8).
El análisis estadístico se realizó mediante el programa SPSS. Se llevó a cabo un análisis descriptivo de la muestra de estudio. Las variables cuantitativas se expresaron como media ± desviación estándar (DE) en el caso de que tuvieran una distribución normal, o como mediana y rango intercuartílico (RI) si no tenían distribución normal. Las variables categóricas se expresaron como valores absolutos y porcentajes. Para establecer diferencias entre las variables cuantitativas se utilizaron la prueba de la t de Student (para dos variables) o la de Mann Whitney y, en el caso de variables cualitativas, se empleó la prueba de la χ2. Se consideró un valor de p < 0,05 como estadísticamente significativo.
Para la evaluación de los factores que podrían afectar a la adherencia se realizó un estudio de regresión logística multivariante con aquellas variables que en el estudio univariante resultaron significativas.
El estudio cumplió la Ley 15/1999, de 13 de diciembre, sobre la Protección de Datos Personales. Los datos se han empleado exclusivamente para la investigación de este estudio, permaneciendo anónimos y confidenciales. El estudio fue aprobado por el Comité Ético de Investigación del área sanitaria con código 2014/187.
Resultados
La muestra la constituyeron 362 pacientes, que supusieron 423 líneas de TB. La mediana de tiempo de duración de las TB del grupo adherente (RMP ≥ 0,8) fue de 823 días (RI 419-1.459) y para el grupo de TB no adherentes (RMP < 0,8) fue de 891 días (RI 608-1.443), sin diferencias entre ambos grupos.
Las características clínicas, sociodemográficas y farmacológicas de la muestra inicial de pacientes se muestran en la Tabla 1.
Tabla 1. Características generales de los pacientes del estudio

DE: desviación estándar; n: número de líneas de terapia biológica; RI: rango intercuartílico; TB: terapia biológica.
El número total de líneas de TB analizadas fue de 423. Los valores que se presentan en esta tabla se refieren al número de líneas para las cuales existían datos sobre las variables analizadas.
1Fumador activo en el momento del inicio de la TB. 2Índice validado para medir la comorbilidad pronóstica en estudios clínicos. Se asignó un valor de 1 punto a aquellos pacientes con una puntuación entre 0 y 3, un valor de 2 a aquellos con una puntuación entre 4 y 9, y un valor de 3 a aquellos con una puntuación ≥ 10.
3Pacientes en tratamiento con algún fármaco psicoactivo.
La adherencia media ± DE medida según la RMP fue de 0,89 ± 0,16. No hubo diferencias entre las patologías: la media ± DE en AR fue de 0,90 ± 0,17, en EA 0,89 ± 0,16 y en APs 0,89 ± 0,15. El porcentaje de pacientes con una RMP ≥ 0,8 fue similar entre las enfermedades: 187 en AR (87%), 91 en EA (85%) y 84 en APs (84%).
En la Tabla 2 se muestran los datos de la RMP para cada una de las TB por separado. Dada la diferencia de número de líneas entre las diversas TB no se pudo realizar un análisis estadístico que demostrase diferencias estadísticamente significativas entre ellas.
Tabla 2. Adherencia medida según la ratio media de posesión de las líneas de terapia biológica
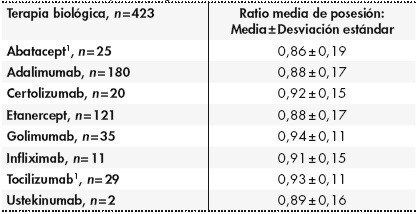
1Resultados conjuntos de terapia biológica con administración intravenosa y subcutánea.
Se dividió la muestra en dos grupos: pacientes adherentes (RMP ≥ 0,8; n = 362) y no adherentes (RMP < 0,8; n = 61). En la Tabla 3 se detallan los factores analizados en el estudio univariante.
Tabla 3. Factores que pueden influir en la no adherencia a las terapias biológicas. Estudio univariante
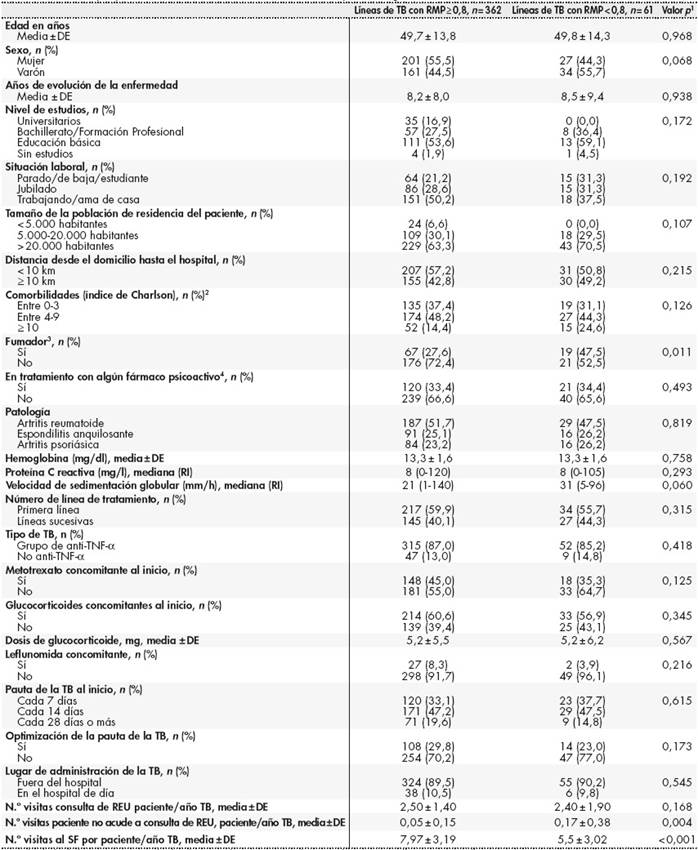
Para el cálculo de los porcentajes se dividió el número de eventos entre el número de pacientes adherentes o no adherentes.
Anti-TNF: antifactor de necrosis tumoral; DE: desviación estándar; n: número de pacientes; RI: Rango intercuartílico; REU: reumatología; RMP: ratio media de posesión; SF: Servicio de Farmacia; TB: terapia biológica.
1Se consideró estadísticamente significativo un valor de p < 0,05. 2Índice validado para medir la comorbilidad pronóstica en estudios clínicos.3Fumador activo en el momento de inicio del tratamiento biológico.4Pacientes en tratamiento con algún fármaco psicoactivo.
El análisis de regresión logística mostró correlación entre acudir con más frecuencia a la consulta del SF y una mejor adherencia a las TB, odds ratio (OR) 1,2 (intervalo de confianza (IC) 95%: 1,1-1,3; p < 0,001) y una correlación inversa con no acudir a las consultas de reumatología en la fecha prevista, OR 0,2 (IC 95%: 0,1-0,9, p < 0,001).
Con respecto a las consecuencias de una menor adherencia a las TB, no se encontró ninguna diferencia estadísticamente significativa entre el grupo de los adherentes frente a los no adherentes. Los resultados se detallan en la Tabla 4.
Tabla 4. Consecuencias de la no adherencia a las terapias biológicas
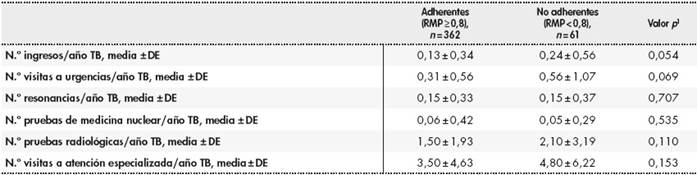
Para el cálculo de los porcentajes se dividió el número de eventos entre el número de adherentes o no adherentes.
DE: desviación estándar; RMP: ratio media de posesión; TB: terapia biológica.
1Se consideró significativo un valor de p < 0,05.
Discusión
Los datos obtenidos sobre el porcentaje de pacientes adherentes son similares a los publicados en estudios de pacientes con AR, oscilando entre el 85,7% y el 88,8%8,9. El porcentaje de pacientes adherentes en APs y EA (89% para ambas enfermedades) es similar al de los pacientes con AR. Dato similar al encontrado en la publicación de Arturi et al.10, en el que los pacientes con EA tenían un grado de adherencia similar a los de AR.
Con respecto al análisis de factores que podrían correlacionarse con una mayor adherencia a las TB fue acudir con más frecuencia a las consultas del SF. Además, el no acudir a las consultas de reumatología en la fecha prevista es un factor predictor de no adherencia. No hemos encontrado ningún estudio en pacientes con AIC y con TB que relacione estos aspectos, aunque sí se ha contemplado en otras enfermedades como el VIH20. Por tanto, resulta un hecho novedoso que indica que aquellos pacientes más ligados al sistema sanitario y con una mayor confianza en los profesionales sanitarios son más adherentes a las TB.
Al igual que en nuestros resultados, en los estudios publicados en población española no hubo diferencias en cuanto a la edad, sexo o número de línea de TB y la adherencia a las TB8,9. Sin embargo, Calip et al.11 presentaron en el año 2018 un estudio que relacionó la mayor edad, el sexo femenino y la pluripatología de los pacientes con una peor adherencia, aunque en concreto los datos sobre adherencia de este estudio realizado en Estados Unidos fueron muy diferentes a los nuestros, ya que solamente un 37% de los pacientes fueron considerados adherentes.
Con respecto a aspectos relacionados con las TB, el uso de una TB de administración subcutánea podría ser un factor predictor de no adherencia9 con respecto al uso de una vía intravenosa. Sin embargo, en nuestro estudio no hubo diferencias en cuanto a si la TB se administraba en el Hospital de día o en el domicilio (vía subcutánea). Esta diferencia con el dato publicado puede que se deba al bajo número de TB que en nuestro estudio se administraban por vía intravenosa. Tampoco encontramos diferencias en cuanto a los diferentes intervalos de dosificación, al contrario que otros estudios en AR, que encontraron como factores predictores de mala adherencia a TB la administración semanal versus mensual8. Esta discrepancia con los resultados del presente estudio puede deberse a que nuestro estudio realizó un análisis conjunto de los pacientes con AR, APs y EA. Tampoco se constataron diferencias en la adherencia entre pacientes con pauta de dosificación optimizada y no optimizada, lo cual podría apoyar la no influencia del tipo de intervalo posológico en la adherencia.
Nuestro trabajo presenta diferencias importantes entre el número de pacientes con adalimumab o etanercept respecto al resto de TB, lo que impide realizar un análisis comparativo entre las diferentes TB. Cuando se agruparon las TB según su mecanismo de acción (aquellas con mecanismo de acción antifactor de necrosis tumoral alfa frente a las de otro mecanismo de acción), no se encontraron diferencias entre ambos grupos, aunque en la publicación de Smolen et al. de 20197, el uso de fármacos antifactor de necrosis tumoral alfa sí fue un factor predictivo de adherencia pero no comparado frente a otras TB, sino frente al uso de fármacos modificadores de la enfermedad sintéticos.
Según nuestros resultados, una menor adherencia a las TB no se traduce en un mayor número de visitas a urgencias, consultas hospitalarias o ingresos. Sin embargo, estos datos no coinciden con los publicados en otros estudios en pacientes con AIC, en los que los pacientes no adherentes frente a los adherentes tenían un uso significativamente mayor de recursos11,12. Este hecho podría tener una explicación en base a que los pacientes no adherentes realizan una reducción de la dosis por su cuenta debido a que se encuentran bien, similar a las optimizaciones de TB que de forma reglada realizan los prescriptores cuando los pacientes están estables21.
Nuestro estudio tiene la limitación de ser de carácter retrospectivo, aunque en contraposición tiene la ventaja de haber podido realizar un seguimiento durante un periodo de 8 años. Otra limitación puede ser haber empleado un solo método para la evaluación de la adherencia. Sin embargo, la utilización de un test como el Morisky Green en este tipo de pacientes no parece tener tanta utilidad como en otras patologías8 y, además, al tratarse de un estudio retrospectivo la utilización de un cuestionario no sería válida para terapias previas.
Conclusión
Según los datos obtenidos, no existen diferencias en cuanto a la adherencia a las TB entre los pacientes con AR, EA y APs. No parece que los factores sociodemográficos o farmacológicos influyan en la adherencia a las TB. Sin embargo, sí parece haber una correlación entre las alianzas que el paciente tiene con el farmacéutico o el médico y la adherencia.
El uso de las TB en una dosis menor debido a falta de adherencia no se traduce en una disminución de la supervivencia de la TB ni en un aumento del consumo de recursos sanitarios.
REFERENCIAS
1. Madhok R, Kerr H, Capell HA. Recent advances: rheumatology. BMJ. 2000;321(7265):882-5. [ Links ]
2. Johansson K, Eriksson JK, van Vollenhoven R, Miller H, Askling J, Neovius M; ARTIS Study Group. Does disease activity at the start of biologic therapy influence health care costs in patients with RA? Rheumatology (Oxford). 2015;54(8):1472-7. DOI: 10.1093/rheumatology/kev021 [ Links ]
3. Ramírez-Herráiz E, Escudero-Vilaplana V, Alañón-Plaza E, Trovato-López N, Herranz-Alonso A, Morell-Baladrón A, et al. Efficiency of adalimumab, etanercept and infliximab in rheumatoid arthritis patients: dosing patterns and effectiveness in daily clinical practice. Clin Exp Rheumatol. 2013;31:559-65. [ Links ]
4. Strand V, Tundia N, Song Y, Macaulay D, Fuldeore M. Economic Burden of Patients with Inadequate Response to Targeted Immunomodulators for Rheumatoid Arthritis. J Manag Care Spec Pharm. 2018;24(4):344-52. DOI: 10.18553/jmcp.2018.24.4.344 [ Links ]
5. McDonnell PJ, Jacobs MR. Hospital admissions resulting from preventable adverse drug reactions. Ann Pharmacother. 2002;36(9):1331-6. [ Links ]
6. Schiff GD, Fung S, Speroff T, McNutt RA. Decompensated heart failure: symptoms, patterns of onset, and contributing factors. Am J Med. 2003;114(8):625-30. [ Links ]
7. Smolen JS, Gladman D, McNeil HP, Mease PJ, Sieper J, Hojnik M, et al. Predicting adherence to therapy in rheumatoid arthritis, psoriatic arthritis or ankylosing spondylitis: a large cross-sectional study. RMD Open. 2019;5(1):e000585. [ Links ]
8. Calvo-Alén J, Monteagudo I, Salvador G, Vázquez-Rodríguez TR, Tovar-Beltrán JV, Vela P, et al. Non-adherence to subcutaneous biological medication in patients with rheumatoid arthritis: a multicentre, non-interventional study. Clin Exp Rheumatol. 2017;35(3):423-30. [ Links ]
9. Mena-Vázquez N, Manrique-Arija S, Yunquera-Romero L, Urena-Garnica I, Rojas-Giménez M, Domic C, et al. Adherence of rheumatoid arthritis patients to biologic disease-modifying antirheumatic drugs: a cross-sectional study. Rheumatol Int. 2017;37(10):1709-18. DOI: 10.1007/s00296-017-3758-6 [ Links ]
10. Arturi P, Schneeberger EE, Sommerfleck F, Buschiazzo E, Ledesma C, Maldonado Cocco JA, et al. Adherence to treatment in patients with ankylosing spondylitis. Clin Rheumatol. 2013;32:1007-15. DOI: 10.1007/s10067-013-2221-7 [ Links ]
11. Calip GS, Adimadhyam S, Xing S, Rincon JC, Lee WJ, Anguiano RH. Medication adherence and persistence over time with self-administered TNF-alpha inhibitors among young adult, middle-aged, and older patients with rheumatologic conditions. Semin Arthritis Rheum. 2017;47(2):157-64. DOI: 10.1016/j.semarthrit.2017.03.010 [ Links ]
12. Lathia U, Ewara EM, Nantel F. Impact of adherence to biological agents on health care resource utilization for patients over the age of 65 years with rheumatoid arthritis. Patient Prefer Adherence. 2017;11:1133-42. DOI: 10.2147/PPA.S137206 [ Links ]
13. Arnett FC, Edworthy SM, Bloch DA, McShane DJ, Fries JF, Cooper NS, et al. The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis. Arthritis Rheum. 1988;31:315-24. [ Links ]
14. Rudwaleit M, Landewe R, van der Heijde D, Listing J, Brandt J, Braun J, et al. The Development of Assessment of Spondyloarthritis International Society (ASAS) Classification Criteria for Axial Spondyloarthritis (Part I): Classification of paper patients by expert opinion including uncertainty appraisal. Ann Rheum Dis. 2009;68:770-6. DOI: 10.1136/ard.2009.108217 [ Links ]
15. Rudwaleit M, van der Heijde D, Landewe R, Listing J, Akkoc N, Brandt J, et al. The Development of Assessment of Spondyloarthritis International Society (ASAS) Classification Criteria for Axial Spondyloarthritis (Part II): Validation and Final Selection. Ann Rheum Dis. 2009;68:777-83. DOI: 10.1136/ard.2009.108233 [ Links ]
16. Taylor W, Gladman D, Helliwell P, Marchesoni A, Mease P, Mielants H; CASPAR Study Group . Classification criteria for psoriatic arthritis: development of new criteria from a large international study. Arthritis Rheum. 2006;54(8):2665-73. [ Links ]
17. Charlson ME, Pompei P, Ales KL, McKenzie CR. A new method of classifying prognostic comorbidity in longitudinal studies: development and validation. J Chron Dis. 1987;40(5):373-83. [ Links ]
18. Real Decreto 1348/2003, de 31 de octubre, por el que se adapta la clasificación anatomica de medicamentos al sistema de clasificacion ATC. Boletin Oficial del Estado, no 264, (4 de noviembre de 2003) (accessed 10/3/2016). Available at:https://www.boe.es/boe/dias/2003/11/04/pdfs/A38970-39019.pdf [ Links ]
19. Kulkarni SP, Alexander KP, Lytle B, Heiss G, Peterson ED. Long-term adherence with cardiovascular drug regimens. Am Heart J. 2006;151(1):185-91. [ Links ]
20. Boeke CE, Nabitaka V, Rowan A, Guerra K, Kabbale A, Asire B, et al. Assessing linkage to and retention in care among HIV patients in Uganda and identifying opportunities for health systems strengthening: a descriptive study. BMC Infect Dis. 2018;18(1):138. DOI: 10.1186/s12879-018-3042-8 [ Links ]
21. Lau CS, Gibofsky A, Damjanov N, Lula S, Marshall L, Jones H, et al. Down-titration of biologics for the treatment of rheumatoid arthritis: a systematic literature review. Rheumatol Int. 2017;37(11):1789-98. DOI: 10.1007/s00296-017-3780-8 [ Links ]
Agradecimientos
Gracias a la Unidad de Estadística de nuestro Hospital, y en concreto a Cristina Martínez Reglero, por todo el apoyo estadístico realizado.
Anexo 1
Autores integrantes del Grupo de Trabajo IRIDIS (Inmunología, Reumatología y Enfermedades Inmunomediadas): María Rodríguez-Rodríguez1, Rafael Benito Melero-González2, Francisco José Maceiras-Pan2. 1Fundación biomédica de Pontevedra, Vigo y Orense. España. 2Servicio de Reumatología, Complejo Hospitalario Universitario de Vigo, Vigo, España.
Cómo citar este trabajo:Martínez-López de Castro N, Álvarez-Payero M, Samartín-Ucha M, Martín-Vila A, Piñeiro-Corrales G, Pego Reigosa JM, Working Group IRIDIS. Adherence to biological therapies in patients with chronic inflammatory arthropathies. Farm Hosp. 2019;43(4):134-139.
Presentación en Congresos:Congreso Nacional de la Sociedad Española de Farmacia Hospitalaria, Valencia, 15 de noviembre de 2015.
Aportación a la literatura científica:
En el caso de pacientes en tratamiento con terapias biológicas, no hay diferencias en cuanto a adherencia entre pacientes diagnosticados de artritis reumatoide, espondilitis anquilosante o artritis psoriásica.
No se ha encontrado que los factores sociodemográficos o relacionados con los medicamentos influyan en la adherencia. Sin embargo, aquellos pacientes con una mayor alianza con el sistema sanitario tienen una mayor probabilidad de ser adherentes a sus terapias biológicas.
Al contrario que en otras enfermedades, según nuestro estudio, una baja adherencia a las terapias biológicas, en el caso de las artropatías inflamatorias crónicas, no implica que el paciente consuma un mayor número de recursos hospitalarios.
Recibido: 04 de Diciembre de 2018; Aprobado: 15 de Abril de 2019











 text in
text in 


