Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Farmacia Hospitalaria
versión On-line ISSN 2171-8695versión impresa ISSN 1130-6343
Farm Hosp. vol.44 no.1 Toledo ene./feb. 2020 Epub 06-Jul-2020
https://dx.doi.org/10.7399/fh.11276
Originales
Administración intrapleural secuencial de agentes fibrinolíticos y dornasa alfa en el empiema. Protocolo de uso clínico en base a su estabilidad fisicoquímica
1Servicio de Farmacia, Área del Medicamento, Hospital Clínic, Barcelona. España.
2Servicio de Cirugía Torácica, Instituto Clínico Respiratorio, Hospital Clínic, Barcelona. España.
3Servicio de Neumología, Instituto Clínico Respiratorio, Hospital Clínic, Barcelona. España.
Objetivo:
La administración intrapleural de fibrinolíticos y dornasa alfa ha demostrado en estudios aleatorizados ser capaz de disminuir la necesidad de desbridamiento quirúrgico del empiema y los días de estancia media hospitalaria. Sin embargo, su aplicación en práctica clínica es limitada, probablemente debido a la falta de protocolos que simplifiquen su administración. El presente estudio tiene como objetivo analizar la estabilidad fisicoquímica de la administración simultánea de uroquinasa y dornasa alfa para el posterior desarrollo de un protocolo de uso en práctica clínica.
Método:
Ensayo de estabilidad in vitro de uroquinasa, dornasa alfa y la mezcla de ambos. Se evaluó su estabilidad como (i) ausencia de partículas, (ii) variación de color y (iii) cambios de pH a tiempos 0, 30 minutos, 1, 2 y 4 horas a 37 °C. Cada muestra se preparó y analizó por triplicado.
Resultados:
Las soluciones individuales de uroquinasa y dornasa alfa mostraron cambios ligeros del pH, sin cambios en su color ni presencia de partículas en suspensión. La mezcla de uroquinasa y dornasa alfa no fue estable transcurridas 2 horas, mostrando turbidez por la floculación y separación de fases con formación de precipitado a las 4 horas. Se desarrolló un protocolo de uso clínico basado en la administración secuencial de uroquinasa y dornasa alfa, ya que no fue posible garantizar la estabilidad fisicoquímica de la administración simultánea de ambos fármacos.
Conclusiones:
Los datos de estabilidad fisicoquímica no permiten asegurar la administración simultánea de ambos fármacos de manera segura y eficaz, por lo que se propone un protocolo de administración secuencial.
PALABRAS CLAVE: Dornasa; DNasa; Empiema; Protocolo; Tratamiento intrapleural; Uroquinasa
Introducción
El empiema es un derrame pleural (DP) parapneumónico complicado definido por la presencia de pus en la pleura y/o microorganismos. Se caracteriza por una mayor concentración de proteínas que el plasma (cociente proteínas DP/proteínas plasma > 0,5 g/l), lactato deshidrogenasa elevada (> 1.000 UI/l) y un pH ácido (< 7,2) como consecuencia de la presencia de pus en la pleura1-3. La base de su tratamiento consiste en la colocación de un drenaje pleural para la evacuación del pus junto con un tratamiento antibiótico sistémico1,3,4. Sin embargo, la falta de resolución del empiema con el tratamiento estándar se relaciona con la presencia de altas cantidades de fibrina en el espacio pleural infectado y de espacios tabicados de alta densidad que impiden el correcto drenaje del material purulento y la acción eficaz de la antibioterapia sistémica (se muestra un ejemplo en la Figura 1). De ahí surgió el interés en la terapia fibrinolítica intrapleural.

Figura 1. Imagen ecográfica correspondiente a empiema. D: diafragma; H: hígado; P: parénquima pulmonar. Las flechas indican los múltiples tabiques de fibrina en el seno del derrame pleural.
En los últimos 15 años, varios estudios han evaluado la eficacia y seguridad de la terapia fibrinolítica, aunque los resultados no son del todo concluyentes. Un primer estudio, el estudio MIST15, mostró que la administración intrapleural de estreptoquinasa no mejoró la mortalidad, la necesidad de cirugía ni la duración de la estancia hospitalaria. Posteriormente, basándose en la experiencia de uso de desoxirribonucleasa (DNasa) para reducir la viscosidad de las secreciones en pacientes con fibrosis quística, se postuló que el ácido desoxirribonucleico (ADN) era el principal causante del aumento de la viscosidad en el espacio pleural, lo que generó la hipótesis de que la administración intrapleural de la enzima DNasa mejora la eficacia del drenaje pleural. Fue en 2011 cuando Rahman et al.6 demostraron, en un estudio aleatorizado controlado amplio, una mejora en la respuesta al tratamiento del derrame pleural parapneumónico (DPPN) tipo empiema mediante la combinación de alteplasa y dornasa alfa, consiguiendo una reducción marcada y significativa de los días de estancia media hospitalaria, así como de la necesidad de desbridamiento quirúrgico del empiema comparado con placebo, y también respecto a dornasa alfa o alteplasa en monoterapia. Las dosis empleadas fueron escogidas empíricamente, basándose en estudios observacionales y series de casos previos6. Los fármacos fibrinolíticos usados difieren entre estudios, utilizando tanto fibrinolíticos no específicos como estreptoquinasa y uroquinasa, como fibrinolíticos específicos como alteplasa. Sin embargo, no existen estudios comparativos entre ellos.
Es necesario destacar que, hasta la fecha, las pautas de tratamiento fibrinolítico más comunes en nuestro entorno no han incorporado esta estrategia combinada. Es posible que ello se deba a la falta de protocolos de uso aplicables en la práctica clínica que corroboren la viabilidad de la administración de un tratamiento combinado intrapleural y reduzcan su complejidad. Estudios recientes7 han tratado de simplificar el tratamiento con la administración intrapleural concurrente de ambos fármacos, es decir, sin dejar un tiempo de actuación entre fármacos como anteriormente se realizó6. Aunque los autores concluyen que el régimen es relativamente seguro y efectivo, la estabilidad de la administración conjunta de ambos fármacos no ha sido nunca estudiada.
Por ese motivo, el objetivo de este estudio es analizar la estabilidad fisicoquímica de la administración conjunta de un agente fibrinolítico y dornasa alfa para el posterior desarrollo de un protocolo de uso en práctica clínica para pacientes con DPPN que requieran tratamiento intrapleural.
Métodos
Preparación de las muestras
Se preparó una solución madre de 500.000 UI de uroquinasa disuelta en 10 ml de suero fisiológico (SF) y una solución madre de 10 mg de dornasa alfa 2,5 mg/2,5 ml en 60 ml de agua para inyectables (API). Dado que en el tratamiento del empiema estos fármacos se emplean en una relación 1:6 (250.000 UI de uroquinasa en 5 ml de SF frente a 5 mg de dornasa alfa en 30 ml de API)6, utilizamos 1 ml de la disolución madre de uroquinasa y 6 ml de la disolución madre de dornasa alfa para formar tres alícuotas de la mezcla de los dos fármacos (7 ml) para llevar a cabo el estudio de estabilidad por triplicado.
Análisis de estabilidad in vitro
Se definió estabilidad como la ausencia de partículas, variación de color o cambios en el pH de la mezcla. Las muestras fueron sometidas a: (i) un examen visual para detectar precipitación, (ii) un proceso de centrifugación para la detección de precipitados no observados a simple vista, y (iii) una medición del pH (relacionado con la temperatura y la desnaturalización proteica).
En el examen visual intervinieron dos observadores diferentes para la evaluación del color, limpidez, así como la formación de burbujas y/o precipitado. La medición del pH fue realizada con un medidor PH BASIC 20 (CRISON, Barcelona) y la centrifugación se efectuó en una centrífuga digital Centromix II-BL (JPSELECTA, Barcelona). Los tubos de ensayo conteniendo la mezcla se mantuvieron a temperatura fisiológica (37 °C) en un baño termostático (LACOR, Bergara). Todos estos instrumentos fueron calibrados según el procedimiento normalizado de trabajo correspondiente del Laboratorio de Farmacotecnia del Servicio de Farmacia, de forma previa a las mediciones.
Las observaciones se llevaron a cabo a tiempo 0 (basal), 30 minutos, 1, 2 y 4 horas desde el proceso de mezcla.
Resultados
Los resultados del análisis fisicoquímico, expuestos en la Tabla 1, mostraron que la disolución madre de uroquinasa es ligeramente ácida (pH = 6,95 ± 0,04), mientras que la de dornasa alfa es neutra (pH = 7,32 ± 0,01). Sin embargo, la mezcla de ambos fármacos presentó un pH de 5,63 ± 0,02.
Tabla 1. Resultados obtenidos en el análisis in vitro de uroquinasa, dornasa alfa y la combinación de ambos fármacos
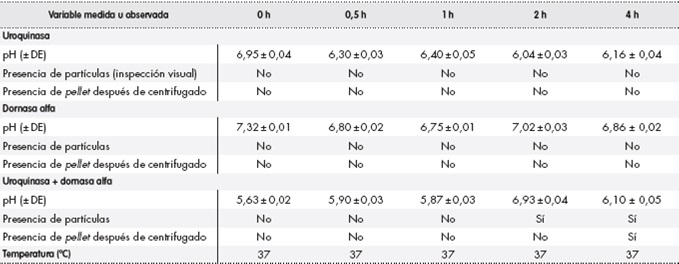
DE: desviación estándar; pellet: cada una de las porciones de material sedimentado.
Tabla 2. Propuesta de tratamiento secuencial con uroquinasa y dornasa alfa para el tratamiento intrapleural del empiema

* Uroquinasa 250.000 UI/8 h día 1 y uroquinasa 100.000 UI/8 h días 2 y 3. Disolver en 30 ml de suero fisiológico.
# Dornasa alfa 5 mg/12 h. Disolver en 30 ml de suero fisiológico.
En cuanto al tiempo de actuación conjunta de las enzimas estudiadas, se observó claramente un cambio en la estabilidad de las muestras. A tiempos 0, 30 minutos y 1 hora, las muestras no mostraron turbidez y su centrifugación no originó pellet (porciones de material sedimentado), mientras que a las 2 y 4 horas de contacto de ambas enzimas sí se observó la formación de flóculos (Figura 2). Transcurridas 4 horas en reposo, se produjo separación de la mezcla en dos fases, con la consiguiente formación de precipitado.

Figura 2. A) Se muestra la mezcla de dornasa alfa y uroquinasa a tiempo 0 (nítida) y a las 2 horas (turbia). B) Se muestra la formación de pellet (flecha) que se produce tras la centrifugación de los tubos de ensayo sometidos a 2 y 4 horas de contacto entre los fármacos estudiados.
A partir de los resultados obtenidos se elaboró un protocolo de actuación basado en una administración secuencial de los fármacos como se detalla en la Tabla 2. Éste consistiría primero en la administración de 100.000-250.000 UI de uroquinasa manteniendo un tiempo de pinzado de 2 horas. Tras este tiempo, se retiraría la uroquinasa y se administrarían 5 mg de dornasa alfa con un tiempo de pinzado de 2 horas más. La administración del tratamiento farmacológico intrapleural se mantendría durante 3 días con la administración de uroquinasa en una frecuencia de cada 8 horas y de dornasa alfa cada 12 horas.
Discusión
Los resultados de la evaluación in vitro indicaron que no es posible garantizar la estabilidad, y por tanto asegurar la actividad farmacológica, de uroquinasa y dornasa alfa transcurridas 2 horas desde la mezcla de ambos fármacos. Por ello, se descartó la posibilidad de la administración simultánea o concurrente de ambos fármacos en práctica clínica y se decidió elaborar un protocolo de actuación basado en la administración secuencial de uroquinasa y dornasa alfa.
Los datos referentes a la posibilidad del uso conjunto de uroquinasa y dornasa alfa resultan contradictorios, ya que en la ficha técnica de dornasa alfa se especifica que puede ser administrada con seguridad y eficacia junto con otros fármacos8. Sin embargo, para uroquinasa se desaconseja su uso conjunto con otros fármacos9. Además, estudios previos, a pesar de demostrar una eficacia in vivo comparable entre la administración de ambos fármacos de forma secuencial y simultánea7, no evalúan la estabilidad de la mezcla6,7, no permitiendo esclarecer dicha duda. Según nos consta, nuestro estudio es el primero en demostrar la inestabilidad fisicoquímica de la mezcla de los dos principios activos, clarificando las dudas existentes hasta el momento.
La determinación de pH inicial de la mezcla resultante de las dos enzimas fue inferior a lo esperado (5,63 ± 0,02), teniendo en cuenta que el valor mínimo de pH de los componentes individuales fue de 6,95 ± 0,04. Una posible explicación podría ser que se produjera una lisis de dornasa alfa por parte de la uroquinasa. Otra hipótesis planteada fue que la disminución del pH fuera debida a que la dornasa alfa sea menos estable en SF, medio en el que se diluyó la uroquinasa. Para comprobar dicha hipótesis, se midió el pH de la solución dornasa alfa en SF, siendo de 5,8 ± 0,04. De estos resultados concluimos que dornasa alfa parece perder estabilidad en SF, por lo que habría que vehiculizar la uroquinasa en API para analizar la estabilidad de la mezcla en un medio más favorable para la actividad de la dornasa alfa.
En nuestro ámbito, los protocolos de administración intrapleural de fibrinolíticos usados hasta la fecha incluían la administración de uroquinasa cada 8 horas, procediendo al cierre del drenaje durante un periodo de 4 horas para permitir la actuación del fármaco. Considerando que el tiempo de estabilidad de la uroquinasa tampoco garantiza una mayor eficacia en periodos más sostenidos de aplicación y que 2 horas de exposición son suficientes para conseguir el efecto fibrinolítico buscado9, se decidió reducir el tiempo de pinzado a 2 horas. Es de destacar que tiempos de pinzado inferiores hasta de solo 1 hora han demostrado la misma eficacia6. Por ello, nuestra propuesta debe ser considerada incluso conservadora. De forma práctica se adicionaría la dornasa alfa 5 mg a este tratamiento, de tal forma que se administraría 2 horas después de la administración de la uroquinasa y una vez retirada ésta, en un intervalo de 12 horas.
No existe un nivel de evidencia que justifique el uso intrapleural de agentes fibrinolíticos como tratamiento local único del empiema. Este hecho no deja de ser sorprendente si consideramos el empleo tradicional y regular de estos agentes y su elevado coste. En cambio, sí se dispone de evidencia científica de primer nivel a favor de incluir dornasa alfa en el tratamiento a pesar de no ser ésta la indicación aprobada en ficha técnica10. Parece muy adecuado incluir este segundo fármaco, pensando en el empleo de dos tratamientos enzimáticos con dianas distintas, en los protocolos de tratamiento intrapleural si tenemos en cuenta que el incremento de coste económico es mínimo. A título orientativo, y teniendo en cuenta el coste estimado promedio en el año en curso, la monoterapia con uroquinasa durante 3 días de tratamiento supone un coste directo (PVL) de 685 euros por paciente tratado, mientras que el tratamiento combinado con dornasa alfa supone un coste adicional (PVL) de 247 euros. Esta diferencia de coste es compensada ampliamente por la reducción esperada de días de estancia y, especialmente, por la disminución de las indicaciones de desbridamiento quirúrgico, ya que los pacientes sin tratamiento intrapleural tienen casi seis veces más probabilidad de requerir tratamiento quirúrgico que los pacientes en tratamiento intrapleural con fibrinolíticos y dornasa alfa6. Creemos que también es necesario remarcar que evitar la cirugía del tórax no sólo supone un beneficio en términos de costes, sino que implica menor morbilidad general, evita el dolor postoperatorio y otros aspectos poco valorados como el estrés asociado al paso por el quirófano. Por tanto, el beneficio potencial de la doble terapia enzimática es también significativo desde el punto de vista de la experiencia del paciente.
Por otra parte, este análisis presenta limitaciones que deben tenerse en cuenta. Una primera limitación surge de las condiciones en las que se ha llevado a cabo el análisis in vitro, que difieren de las del medio en que actuarán estos fármacos. La viscosidad aumenta la estabilidad al dificultar el movimiento de las partículas y, por tanto, su agregación. Así pues, cabe la posibilidad de que la mezcla sea marginalmente más estable en el lugar de acción que es rico en pus. Por último, este estudio se llevó a cabo con uroquinasa al ser éste el fibrinolítico de uso más común en esta indicación utilizado en nuestro centro, por lo que no será posible extrapolar los resultados obtenidos al resto de fibrinolíticos.
Son necesarios más estudios para esclarecer estos interrogantes. Aún con todo, este análisis supone una aproximación práctica al tratamiento intrapleural secuencial del empiema con ambos fármacos, apostando por garantizar la estabilidad fisicoquímica de los fármacos como paso necesario para tener los mejores resultados posibles en la práctica clínica.
En conclusión, creemos que hay evidencia muy sólida en la literatura para recurrir a la biterapia con fibrinolíticos y DNasa en el empiema. Los datos obtenidos en el estudio de estabilidad no permiten asegurar la administración simultánea de ambos fármacos de manera segura y eficaz, por lo que proponemos su administración de forma secuencial.
REFERENCIAS
Bedawi EO, Hassan M, Rahman NM. Recent developments in the management of pleural infection: A comprehensive review. Clin Respir J. 2018;12:2309-20. DOI: 10.1111/crj.12941 [ Links ]
Aboudara M, Maldonado F. Update in the Management of Pleural Effusions. Med Clin North Am. 2019;103:475-85. DOI: 10.1016/j.mcna.2018.12.007 [ Links ]
Villena Garrido V, Cases Viedma E, Fernández Villar A, de Pablo Gafas A, Pérez Rodríguez E, Porcel Pérez JM, et al. Recommendations of diagnosis and treatment of pleural effusion. Update. Arch Bronconeumol. 2014;50:235-49. DOI: 10.1016/j.arbres.2014.01.016 [ Links ]
Davies HE, Davies RJO, Davies CWH. BTS Pleural Disease Guideline Group. Management of pleural infection in adults: British Thoracic Society Pleural Disease Guideline 2010. Thorax. 2010;65 Suppl 2:ii41-53. DOI: 10.1136/thx.2010.137000 [ Links ]
Maskell NA, Davies CWH, Nunn AJ, Hedley EL, Gleeson FV, Miller R, et al. UK Controlled trial of intrapleural streptokinase for pleural infection. N Engl J Med. 2005;352:865-74. DOI: 10.1056/NEJMoa042473 [ Links ]
Rahman NM, Maskell NA, West A, Teoh R, Arnold A, Mackinlay C, et al. Intrapleural use of tissue plasminogen activator and DNase in pleural infection. N Engl J Med. 2011;365:518-26. DOI: 10.1056/NEJMoa1012740 [ Links ]
Kheir F, Cheng G, Rivera E, Folch A, Folch E, Fernandez-Bussy S, et al. Concurrent Versus Sequential Intrapleural Instillation of Tissue Plasminogen Activator and Deoxyribonuclease for Pleural Infection. J Bronchology Interv Pulmonol. 2018;25:125-31. DOI: 10.1097/LBR.0000000000000461 [ Links ]
Agencia Española de Medicamentos y Productos Sanitarios. Ficha técnica Pulmozyme 2.500 U/2,5 ml solución para inhalación por nebulizador (internet) Madrid. Centro de información de medicamentos (CIMA) (accessed 15/01/2019). Available at: https://cima.aemps.es/cima/dochtml/ft/60326/FT_60326.html [ Links ]
Agencia Española de Medicamentos y Productos Sanitarios. Ficha técnica Urokinase Vedim 250.000 UI polvo y disolvente para solución para perfusión (internet) Madrid. Centro de información de medicamentos (CIMA) (accessed 15/01/2019). Available at: https://cima.aemps.es/cima/dochtml/ft/52638/FT_52638.html [ Links ]
Chalmers JD, Singanayagam A, Murray MP, Scally C, Fawzi A, Hill AT. Risk factors for complicated parapneumonic effusion and empyema on presentation to hospital with community-acquired pneumonia. Thorax. 2009;64:592-7. DOI: 10.1136/thx.2008.105080 [ Links ]
Aportación a la literatura científica:
Recibido: 27 de Mayo de 2019; Aprobado: 29 de Septiembre de 2019











 texto en
texto en 


