Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Farmacia Hospitalaria
versión On-line ISSN 2171-8695versión impresa ISSN 1130-6343
Farm Hosp. vol.44 no.5 Toledo sep./oct. 2020 Epub 26-Jul-2021
https://dx.doi.org/10.7399/fh.11419
ORIGINALES
Comparación indirecta ajustada de anticuerpos monoclonales contra el péptido relacionado con el gen de la calcitonina en migraña crónica
1Unidad de Gestión Clínica de Farmacia, Hospital Universitario de Puerto Real, Puerto Real, Cádiz. Spain.
Introducción
La migraña es una cefalea primaria que se manifiesta en forma de episodios recurrentes de cefaleas de duración variable y de intensidad de moderada a severa. A menudo cursa como un dolor unilateral de carácter pulsátil, acompañado de náuseas, fotofobia y fonofobia. En un 30% de los casos, la migraña es precedida por síntomas neurológicos focalizados transitorios (visuales o sensoriales) denominados aura1. Dependiendo de la frecuencia de estos episodios, la migraña puede ser episódica (ME; con cefaleas durante menos de 15 días al mes) o crónica (MC; con cefaleas con frecuencia superior a los 15 días al mes durante más de 3 meses, y con síntomas claramente migrañosos durante al menos 8 de esos días).
El trastorno afecta a aproximadamente un 15% de la población, siendo de dos a tres veces más frecuente en mujeres. La prevalencia de la MC es del 2,4%1. Según el estudio de Carga Mundial de la Morbilidad2, la migraña es la sexta enfermedad de mayor prevalencia del mundo, con consecuencias que suponen un impacto considerable tanto a nivel individual como social. Esto significa que representa un grave problema sanitario que afecta de forma significativa la calidad de vida de las personas y entraña, además de costes directos para el sistema sanitario, costes indirectos relacionados con la pérdida de días de trabajo y de productividad3.
La migraña es provocada por la activación del tronco encefálico y del sistema trigémino vascular. Tras la activación, las terminaciones de dicho sistema dilatan los vasos craneales sensibles al dolor, liberando neuropéptidos algógenos, principalmente el péptido relacionado con el gen de la calcitonina (CGRP, por sus siglas en inglés) y el péptido intestinal vasoactivo, que inducen dilatación e inflamación. Ambos fenómenos vasculares son responsables del dolor causado por la migraña1. El tratamiento sintomático de la migraña consiste en el uso de fármacos de acción inespecífica (antiinflamatorios no esteroideos y analgésicos), fármacos de acción específica (triptanes y derivados ergotamínicos) y fármacos coadyuvantes (antieméticos y procinéticos). En cuanto al tratamiento preventivo, las guías recomiendan el uso de betabloqueantes (metoprolol, propranolol), antiepilépticos (ácido valproico, topiramato), antidepresivos (amitriptilina) o bloqueadores de los canales de calcio (flunarizina) en primera línea4. Para casos de MC, si el paciente no responde a estos tratamientos, o si estuvieran contraindicados, se recomienda el uso de toxina botulínica3.
Recientemente se han desarrollado nuevos anticuerpos monoclonales contra la vía del CGRP (anticuerpos anti-CGRP) para la prevención de ME y MC que se dirigen o bien al ligando de CGRP (fremanezumab, galcanezumab, eptinezumab) o a su receptor (erenumab)5-7. La eficacia de estos fármacos ha sido evaluada en ensayos clínicos aleatorizados (ECA)8-14. No obstante, la eficacia comparativa de los distintos anticuerpos anti-CGRP no ha sido dilucidada. Hasta el momento, la ausencia de comparación indirecta ajustada (CIA) ha dificultado la selección y el posicionamiento de dichas alternativas terapéuticas en el contexto de la MC. Dado el impacto social y económico de la MC, resulta esencial desarrollar estudios que den respuesta a los interrogantes existentes.
El objetivo del presente trabajo es doble. Por un lado, desarrollar una CIA entre los distintos fármacos anti-CGRP utilizados en MC en términos de eficacia, utilizando un comparador común. Por otro, utilizar una metodología previamente determinada para establecer si las distintas estrategias de tratamiento disponibles pueden considerarse alternativas terapéuticas equivalentes (ATE) para la MC15.
Métodos
Búsqueda en la bibliografía y criterios de inclusión
El 26 de diciembre de 2019 se realizó una búsqueda bibliográfica en la base de datos PubMed para identificar ECA de fase II o III que evaluaran el papel de los fármacos anti-CGRP en sujetos con MC. Se aplicaron filtros como clinical queries (preguntas clínicas) y narrow (estrecho) y se utilizaron los siguientes términos descriptivos: erenumab, fremanezumab, galcanezumab, eptinezumab y migraine (migraña).
Se incluyeron ECA que estudiaran poblaciones similares y utilizaran una misma definición de la MC (cefalea de cualquier duración o severidad que aparece 15 días o más al mes durante al menos 3 meses consecutivos, y que al menos durante 8 días presenta síntomas claramente migrañosos) con el mismo tiempo de seguimiento. El porcentaje de pacientes que experimentaron una reducción de al menos el 50% en el número de días de migraña sufridos cada mes se seleccionó como criterio para determinar la eficacia del tratamiento. Un día de migraña se definió como aquel durante el cual la cefalea persistía durante más de 4 horas consecutivas.
Análisis de los datos
Se llevó a cabo una CIA entre los distintos fármacos anti-CGRP utilizando el método de Bucher y la calculadora propuesta por la Agencia Canadiense de Medicamentos y Tecnologías en Salud16,17. Para determinar la eficacia relativa, se compararon los resultados con los del fármaco que produjo el mejor resultado numérico en la reducción de al menos el 50% de los días de migraña por mes.
Se utilizó la Guía ATE15, que proporciona pautas para el posicionamiento de dos o más fármacos como alternativas terapéuticas equivalentes, para determinar la posible equivalencia terapéutica de los fármacos anti-CGRP objeto de comparación. La Guía ATE ya había sido utilizada para la evaluación de medicamentos en la Guía farmacoterapéutica de hospitales de Andalucía. Según la Guía ATE, es preciso establecer un valor delta (Δ), definido como la máxima diferencia considerada como clínicamente irrelevante entre las distintas alternativas evaluadas. Al no existir para los fármacos evaluados un valor Δ reconocido por agencias evaluadoras, ni propuesto por paneles de expertos, ni utilizado en ECA de equivalencia o no inferioridad, ni empleado para el cálculo de muestra en ECA con comparador activo, se procedió a su determinación. Para ello, se desarrolló un metaanálisis de los estudios identificados utilizando la calculadora de Joaquín Primo18. Se tomó como valor Δ la mitad de la reducción absoluta de riesgo (RAR) obtenida en el metaanálisis para los fármacos anti-CGRP frente a placebo. La heterogeneidad y la consistencia se analizaron mediante la prueba estadística Q19. Se utilizó el parámetro I2 para determinar qué parte de la variabilidad observada en los resultados es debida a la heterogeneidad y no al azar20. Además, se realizó una evaluación gráfica de los resultados para determinar si la RAR y el intervalo de confianza (IC) del 95% obtenido tras la CIA estaban dentro del rango del valor Δ calculado. Para evaluar la posible equivalencia terapéutica también es preciso considerar la seguridad de los fármacos. Esto se hizo mediante un análisis de las diferencias entre los eventos adversos (EA) provocados por los distintos agentes anti-CGRP.
Resultados
Búsqueda en la literatura
La búsqueda permitió identificar 50 ensayos en total, de los que se excluyeron 20 por no ser ECA. Los restantes 30 ECA evaluaban el uso de agentes anti-CGRP en indicaciones de migraña: 12 eran relativos a erenumab, 7 a fremanezumab, 10 a galcanezumab y 1 a eptinezumab. Tras descartar los ECA que no cumplían con todos los criterios de inclusión, finalmente quedaron tres ensayos para llevar a cabo la CIA: uno sobre erenumab8, uno sobre fremanezumab9 y uno sobre eptinezumab13. El proceso de selección se presenta en la Figura 1.

Figura 1. Proceso seguido para seleccionar los ensayos utilizados para realizar una comparacion indirecta ajustada entre tratamientos.
El ensayo de erenumab escogido fue un estudio de fase II doble ciego y controlado con placebo en pacientes de edades comprendidas entre 18 y 65 años que presentaban MC (n = 667)8. Este estudio requería que los pacientes hubiesen respondido a tratamientos anteriores. Los pacientes fueron aleatorizados en proporción 3:2:2 a recibir placebo subcutáneo, erenumab 70 mg cada 4 semanas y erenumab 140 mg cada 4 semanas, respectivamente.
El ensayo de fremanezumab fue un estudio de fase III doble ciego y controlado con placebo9 (n = 1.130) en pacientes de edades comprendidas entre 18 y 70 años y diagnóstico de MC que habían respondido a tratamientos anteriores. Fueron aleatorizados en proporción 1:1:1 a recibir placebo subcutáneo, fremanezumab trimestral (625 mg al inicio de cada trimestre y placebo en las semanas 4 y 8) y fremanezumab mensual (625 mg al inicio y 225 mg en las semanas 4 y 8).
Por último, el ensayo de eptinezumab fue un estudio de fase IIb doble ciego y controlado con placebo13 en pacientes de edades comprendidas entre 18 y 55 años y diagnóstico de MC (n = 616). Fueron aleatorizados en proporción 1:1:1:1:1 a recibir una única infusión intravenosa de eptinezumab de 300 mg, 100 mg, 30 mg, 10 mg o placebo.
Los tres estudios se realizaron en pacientes de similares características, utilizando la misma definición de MC, es decir, cefalea de cualquier duración o severidad durante ≥ 15 días por mes, de los que 8 días son días de migraña. Un día de migraña se definió como un día en el que se produce una cefalea de más de 4 horas consecutivas de duración. El ensayo de eptinezumab considera como día de migraña también aquel en el que se produce una cefalea de 30 minutos a 4 horas de duración que, según el paciente, remitirá con la medicación. Todos los estudios utilizaban placebo como comparador común. En estos estudios se utilizó como variable para evaluar la eficacia del tratamiento la consecución de una reducción de al menos el 50% en el número de días de migraña al mes, medida desde el inicio hasta la semana 12.
Análisis de los datos
Los tres agentes anti-CGRP evaluados, con sus distintos esquemas de dosificación, demostraron ser superiores a placebo para la variable de eficacia evaluada en sus respectivos ECA8,9,13. A partir de estos datos, se calculó la RAR (IC: 95%) de cada brazo de tratamiento activo frente a placebo. Los resultados fueron estadísticamente significativos en todos los casos, a excepción de la RAR obtenida por eptinezumab 10 mg frente a placebo. La Tabla 1 muestra los resultados de eficacia de los distintos ECA y las RAR (IC: 95%) resultantes. La diferencia de riesgo combinado obtenida por el metaanálisis fue del 19% (IC 95%: 16-22), y el valor Δ correspondiente 9,5%. El valor de I2 fue de 0 y la p de la heterogeneidad fue 0,837. Posteriormente se realizó una CIA, de la que se excluyó el eptinezumab 10 mg, ya que el resultado obtenido para ese fármaco con esa dosis no había sido estadísticamente significativo. Se seleccionó fremanezumab de administración mensual como tratamiento de referencia, ya que en el ECA correspondiente obtuvo el mejor resultado frente a placebo. Los resultados
de la CIA se muestran en la Tabla 1.
Tabla 1. Eficacia demostrada por cada brazo de tratamiento en los ensayos clínicos aleatorizados seleccionados para la variable analizada, y resultados de la comparación indirecta ajustada de las distintas alternativas de tratamiento frente a fremanezumab mensual, en base al método de Bucher

ECA: ensayo clinico aleatorizado; IC: intervalo de confianza; N: numero de pacientes; RAR: reduccion absoluta del riesgo.
La Figura 2 muestra una representación gráfica del resultado de la CIA realizada. No se encontraron diferencias estadísticamente significativas ni clínicamente relevantes entre los distintos esquemas. Además, la mayor parte del IC (95%) está dentro del rango ± Δ. Según la Guía ATE15, la variable de eficacia analizada se consideraría reversible, ya que el fracaso terapéutico no supondría un daño grave ni irreversible para los pacientes. Para evaluar la seguridad, no fue posible el desarrollo de una CIA debido a la existencia de discrepancias en los datos recogidos en los ECA. El porcentaje de EA obtenido en el brazo placebo fue distinto para cada fármaco: 47% en el estudio de erenumab, 64% en el de fremanezumab y 56% en el de eptinezumab. Esto supone que la variable de evaluación de la seguridad podría haberse medido de forma diferente en los tres ECA. Por lo demás, puesto que los resultados del brazo placebo para EA severos y para EA asociados con la interrupción del tratamiento fueron similares, se analizaron las principales diferencias entre estos dos criterios de evaluación. La Tabla 2 muestra los resultados de los ECA en materia de seguridad. Todos los regímenes estudiados presentaron un número escaso de EA severos o asociados a la interrupción del tratamiento, sin observarse diferencias estadísticamente significativas frente a placebo. No se encontraron diferencias relevantes entre los tres fármacos en relación con estas variables de seguridad.

Figura 2. Resultados de la comparacion indirecta ajustada entre tratamientos: proporcion de pacientes que experimentaron una reduccion ≥ 50% en sus dias de migrana/mes. RAR (IC 95%) de las distintas alternativas frente a fremanezumab mensual.
Tabla 2. Seguridad demostrada por cada brazo de tratamiento en los ensayos clínicos aleatorizados seleccionados para las variables analizadas
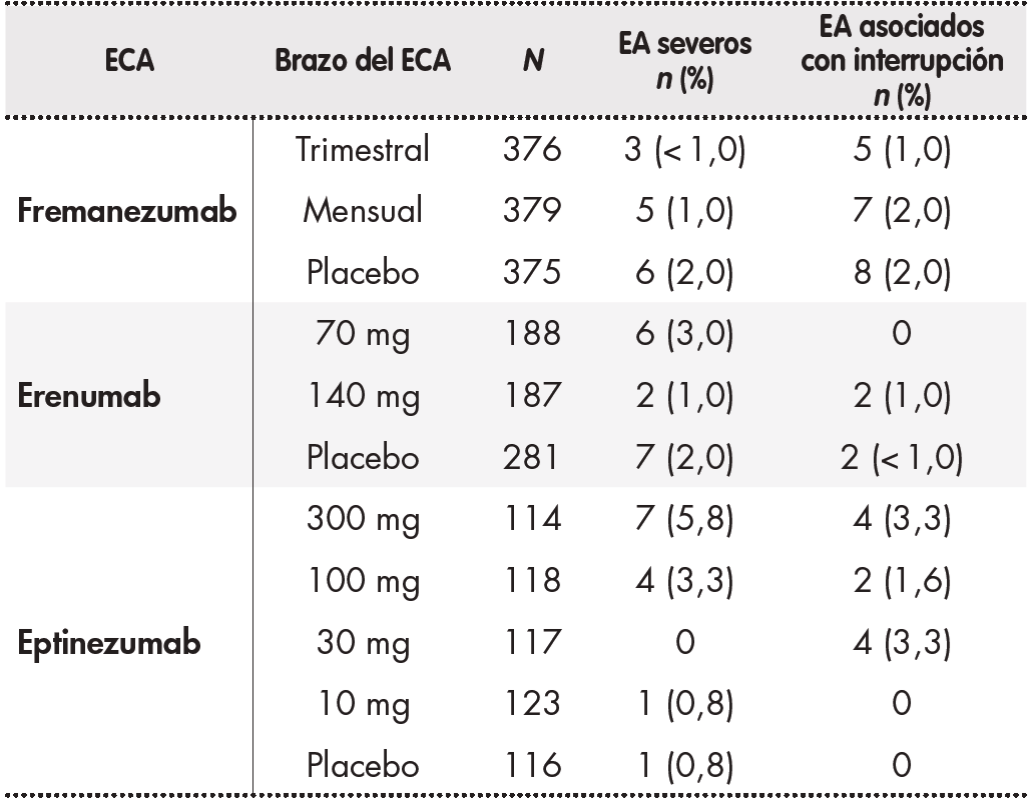
EA: evento adverso; ECA: ensayo clinico aleatorizado; N: numero de pacientes.
En los ECA analizados, los EA más habituales fueron infecciones de las vías aéreas superiores, náuseas y nasofaringitis, sin observarse diferencias significativas frente a placebo. El dolor en el lugar de inyección sólo se registró en pacientes que recibían erenumab y fremanezumab debido a la administración subcutánea de estos fármacos, aunque las diferencias frente a placebo no fueron estadísticamente significativas.
Tomando en consideración los resultados obtenidos en materia de eficacia y seguridad, los siguientes esquemas terapéuticos podrían considerarse como alternativas terapéuticas equivalentes en pacientes con MC: erenumab 70 mg, erenumab 140 mg, fremanezumab trimestral, fremanezumab mensual, eptinezumab 300 mg, eptinezumab 100 mg y eptinezumab 30 mg.
Discusión
Los nuevos anticuerpos dirigidos contra la vía del péptido CGRP podrían suponer una opción terapéutica adicional en el tratamiento de pacientes con MC. En ausencia de ECA que comparen los distintos fármacos anti-CGRP entre sí, las CIA y metaanálisis en red surgen como herramientas prometedoras para compensar la falta de evidencia científica y establecer un posicionamiento en cuanto a la eficacia de este grupo de fármacos. En nuestro estudio hemos comprobado que, probablemente, no existan diferencias de eficacia entre erenumab, fremanezumab y eptinezumab. Para ello, hemos aplicado los criterios establecidos por la Guía ATE15. Consideramos que es posible aceptar un valor Δ del 9,5% como criterio clínico de no inferioridad en ausencia de un consenso establecido en relación con la magnitud de dicho parámetro, tomando en consideración que las consecuencias de un fracaso terapéutico no son irreversibles. En el peor de los casos, un fármaco cuya RAR y cuyo IC 95% se mantengan dentro de este rango conservará al menos la mitad de su efecto terapéutico. Este posicionamiento terapéutico promueve la competencia de precios entre estos fármacos, optimizando la eficiencia gracias a un menor coste de adquisición21. La reducción de costes es una estrategia de gran importancia para la sostenibilidad de los sistemas sanitarios.
Nuestro trabajo es más conservador que otros estudios recientemente publicados22-24. Aunque los metaanálisis son herramientas de gran valor en lo relativo a la selección farmacológica, sus resultados sólo deberían tomarse en consideración cuando los estudios analizados incluyan poblaciones o patrones farmacológicos similares. La interpretación de los resultados arrojados por estudios en poblaciones heterogéneas22-24 conlleva un alto grado de incertidumbre, que podría tener repercusiones clínicas o farmacoeconómicas significativas. Un error que a menudo cometen los metaanálisis que se han publicado sobre la MC consiste en incluir ECA con distintas definiciones de “migraña” o poblaciones que no demostraron resistencia a tratamientos anteriores. Por otro lado, la selección de estudios con poblaciones con diagnóstico de ME10-12 o con criterios diferentes en lo relativo a la duración de un día de migraña, como es el caso del ensayo sobre galcanezumab en pacientes con MC14, entraña un sesgo considerable. Nuestro trabajo sólo incluye ECA comparables en cuanto a población estudiada, brazos de tratamiento y comparadores utilizados, y variable analizada. El principal inconveniente que presentan las comparaciones entre fármacos anti-CGRP es la falta de datos que permitan realizar comparaciones fiables entre los distintos anticuerpos que actúan sobre la MC. Una limitación de este estudio radica en que la CIA fue realizada entre tres estudios con diseños diferentes. Mientras que los ECA de erenumab y eptinezumab eran de fase II8,13, los datos de fremanezumab se extrajeron de un ECA de fase III9. Tomando en consideración las características generales de los ECA, los resultados de la fase II suelen ser preliminares y deben tomarse con cautela, en tanto que los ECA de fase III presentan datos más concluyentes. No obstante, la ausencia de estudios de similares características impide desarrollar comparaciones entre ECA de idéntico diseño. Además, el ensayo de eptinezumab estudió pacientes que experimentaron días de migraña tanto de más de 4 horas como de entre 30 minutos y 4 horas, lo que podría constituir un sesgo que afecte a los resultados, ya que parte de la población de ese ensayo podría estar integrada por sujetos con migrañas más leves que los de los otros dos estudios.
La reciente autorización para comercializar fármacos anti-CGRP en la indicación de MC y su posible impacto económico, así como las trascendentales repercusiones socioeconómicas de la patología, exigen la realización de estudios como éste para determinar el posicionamiento terapéutico de las distintas alternativas de tratamiento disponibles.
En definitiva, nuestra CIA no encontró diferencias entre erenumab, fremanezumab y eptinezumab, administrados en distintos esquemas farmacológicos, en cuanto a su potencial de reducir en al menos un 50% los días de migraña sufridos al mes. Tampoco se encontraron diferencias significativas en seguridad entre los tres fármacos. Por lo tanto, teniendo en cuenta la evidencia científica actualmente disponible, los tres fármacos pueden considerarse alternativas terapéuticas equivalentes en pacientes con MC.
Aportación a la literatura científica
Este estudio presenta la primera comparación indirecta ajustada entre fármacos anti-CGRP utilizados en migraña crónica que incluye ensayos comparables en cuanto a población, definición de la enfermedad y variables evaluadas.
Los resultados de este trabajo permitirán determinar si estos fármacos pueden considerarse como alternativas terapéuticas equivalentes para pacientes con esta patología.
Bibliography
Riesco N, Garcia-Cabo C, Pascual J. Migraine. Med Clin (Barc). 2016 Jan;146(1):35-9. DOI: 10.1016/j.medcli.2015.07.003 [ Links ]
Stovner LJ, Nichols E, Steiner TJ, Abd-Allah F, Abdelalim A, Al-Raddadi RM, et al. Global, regional, and national burden of migraine and tension-type headache, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol. 2018 Nov 1;17(11):954-76. DOI: 10.1016/S1474-4422(18)30322-3 [ Links ]
Ezpeleta D, Rosich PP, Romero JV, Gago Veiga A, Santos Lasaosa S. Guias diagnosticas y terapeuticas de la Sociedad Espanola de Neurologia 2015. 3. Guia oficial de practica clinica en cefaleas (Internet monograph). Edicion 3. Madrid: Luzan 5:SEN; 2015. Available at: http://cefaleas.sen.es/pdf/GUIA_NEURO_2015.pdf [ Links ]
Loder E, Burch R, Rizzoli P. The 2012 AHS/AAN Guidelines for Prevention of Episodic Migraine: A Summary and Comparison With Other Recent Clinical Practice Guidelines. Headache. 2012 Jun;52(6):930-45. DOI: 10.1111/j.1526-4610.2012.02185.x [ Links ]
Committee for Medicinal Products for Human Use (CHMP). Ajovy, INN-fremanezumab. European Medicines Agency. Assessment report (Internet). 2019. Available at: www.ema.europa.eu/contact [ Links ]
Committee for Medicinal Products for Human Use (CHMP). Emgality, INN-galcanezumab. European Medicines Agency. Assessment report (Internet). 2018. Available at: www.ema.europa.eu/contact [ Links ]
Committee for Medicinal Products for Human Use (CHMP). Aimovig, INN-erenumab. European Medicines Agency. Assessment report (Internet). 2018. Available at: www.ema.europa.eu/contact [ Links ]
Tepper S, Ashina M, Reuter U, Brandes JL, Doležil D, Silberstein S, et al. Safety and efficacy of erenumab for preventive treatment of chronic migraine: a randomised, double-blind, placebo-controlled phase 2 trial. Lancet Neurol. 2017 Jun 1;16(6):425-34. DOI: 10.1016/S1474-4422(17)30083-2 [ Links ]
Silberstein SD, Dodick DW, Bigal ME, Yeung PP, Goadsby PJ, Blankenbiller T, et al. Fremanezumab for the Preventive Treatment of Chronic Migraine. N Engl J Med. 2017 Nov 30;377(22):2113-22. DOI: 10.1056/NEJMoa1709038 [ Links ]
Reuter U, Goadsby PJ, Lanteri-Minet M, Wen S, Hours-Zesiger P, Ferrari MD, et al. Efficacy and tolerability of erenumab in patients with episodic migraine in whom two-to-four previous preventive treatments were unsuccessful: a randomised, double-blind, placebo-controlled, phase 3b study. Lancet. 2018 Nov 24;392(10161):2280-7. DOI: 10.1016/S0140-6736(18)32534-0 [ Links ]
Goadsby PJ, Reuter U, Hallstrom Y, Broessner G, Bonner JH, Zhang F, et al. A Controlled Trial of Erenumab for Episodic Migraine. N Engl J Med. 2017 Nov 30;377(22):2123-32. DOI: 10.1056/NEJMoa1705848. [ Links ]
Dodick DW, Silberstein SD, Bigal ME, Yeung PP, Goadsby PJ, Blankenbiller T, et al. Effect of Fremanezumab compared with placebo for prevention of episodic migraine a randomized clinical trial. JAMA. 2018 May 15;319(19):1999-2008. DOI: 10.1001/jama.2018.4853 [ Links ]
Dodick DW, Lipton RB, Silberstein S, Goadsby PJ, Biondi D, Hirman J, et al. Eptinezumab for prevention of chronic migraine: A randomized phase 2b clinical trial. Cephalalgia. 2019 Aug;39(9):1075-85. DOI: 10.1177/0333102419858355 [ Links ]
Detke HC, Goadsby PJ, Wang S, Friedman DI, Selzler KJ, Aurora SK. Galcanezumab in chronic migraine: The randomized, double-blind, placebo-controlled REGAIN study. Neurology. 2018;91(24):E2211-21. DOI: 10.1212/WNL.0000000000006640 [ Links ]
Alegre Del Rey EJ, Fenix Caballero S, Castano Lara R, Sierra Garcia F. Assessment and positioning of drugs as equivalent therapeutic alternatives. Med Clin (Barc). 2014 Jul 22;143(2):85-90. DOI: 10.1016/j.medcli.2013.11.033 [ Links ]
Bucher HC, Guyatt GH, Griffith LE, Walter SD. The results of direct and indirect treatment comparisons in meta-analysis of randomized controlled trials. J Clin Epidemiol. 1997;50(6):683-91. DOI: 10.1016/s0895-4356(97)00049-8 [ Links ]
Wells GA, Sultan SA, Chen L, Khan M CD. Indirect Evidence: Indirect Treatment Comparisons in Meta-Analysis (Internet monograph). Ottawa: Canadian Agency for Drugs and Technologies in Health; 2009. Available at: https://www.researchgate.net/profile/Shagufta_Sultan/publication/264119732_Canadian_Agency_for_Drugs_and_Tec hnologies_in_Health_Indirect_Evidence_Indirect_Treatment_Comparisons_in_Meta-Analysis_Publications_can_be_requested_from_Canadian_Agency_for_Drugs_and_Technologies_in_/links/53ce9c180cf25dc05cf8f944/Canadian-Agency-for-Drugs-and-Technologies-in-Health-Indirect-Evidence-Indirect-Treatment-Comparisons-in-Meta-Analysis-Publicationscan-be-requested-from-Canadian-Agency-for-Drugs-and-Technologies-in.pdf [ Links ]
Primo J. Calculadoras. CASPe (Internet). 2015. Available at: http://www.redcaspe.org/herramientas/calculadoras [ Links ]
Higgins JPT, Jackson D, Barrett JK, Lu G, Ades AE, White IR. Consistency and inconsistency in network meta-analysis: concepts and models for multi-arm studies. Res Synth Methods. 2012 Jun;3(2):98-110. DOI: 10.1002/jrsm.1044 [ Links ]
Higgins JPT, Thompson SG, Deeks JJ, Altman DG. Measuring inconsistency in meta-analyses. BMJ. 2003;327(7414):557-60. DOI: 10.1136/bmj.327.7414.557 [ Links ]
Garcia JG, Diaz MAR. Demostracion de equivalencia terapeutica previa al análisis de minimizacion de costes. PharmacoEconomics Spanish Res Artic. 2012 Nov;9(4):109-16. DOI: 10.1007/BF03320880 [ Links ]
Hou M, Xing H, Cai Y, Li B, Wang X, Li P, et al. The effect and safety of monoclonal antibodies to calcitonin gene-related peptide and its receptor on migraine: a systematic review and meta-analysis. J Headache Pain. 2017 Dec 1;18(1). DOI: 10.1186/s10194-017-0750-1 [ Links ]
Huang IH, Wu PC, Lin EY, Chen CY, Kang YN. Effects of anti-calcitonin generelated peptide for migraines: A systematic review with meta-analysis of randomized clinical trials. Int J m. MDPI AG; 2019;20(14):3527. DOI: 10.3390/ijms20143527 [ Links ]
Han L, Liu Y, Xiong H, Hong P. CGRP monoclonal antibody for preventive treatment of chronic migraine: An update of meta-analysis. Brain Behav. 2019 Feb 1;9(2). DOI: 10.1002/brb3.1215 [ Links ]
Recibido: 09 de Febrero de 2020; Aprobado: 08 de Mayo de 2020











 texto en
texto en 


