Introducción
La fibrilación auricular es la arritmia cardíaca mantenida en el tiempo más común en pacientes adultos y se estima que más de 40 millones de individuos la presentaban en 20161. Estas cifras se espera que aumenten en el futuro, proyectándose solamente en la Unión Europea un aumento de más del doble de casos en pacientes de 55 o más años2. La fibrilación auricular está asociada a una elevada morbimortalidad, condiciona una alta carga tanto personal como económica, es la causa más común de formación de émbolos de origen cardíaco y se asocia a un incremento de 4 a 5 veces el riesgo de ictus3,4. Las actuales guías basadas en la evidencia recomiendan tratamiento anticoagulante en pacientes con factores de riesgo adicionales; así, la guía CHEST recomienda iniciar tratamiento anticoagulante oral en pacientes con un CHA2DS2-VASc mayor o igual a 1 (sin tener en cuenta el sexo)5, mientras que la guía conjunta de la American Heart Association, American College of Cardiology y Heart Rythm Society recomienda el inicio del tratamiento para un CHA2DS2-VASc de 2 en hombres y 3 en mujeres6. El tratamiento anticoagulante oral se puede realizar mediante el empleo de antagonistas de la vitamina K (AVK) o mediante los denominados anticoagulantes de acción directa (ACOD)6.
Rivaroxabán es un ACOD que no presenta las interacciones propias de los AVK, como puede ser con alimentos, pero sí interacciona con algunos fármacos, entre los que se encuentran los inhibidores selectivos de la recaptación de la serotonina (ISRS)7.
El manejo del trastorno depresivo consiste en la aplicación de medidas no farmacológicas, como puede ser la terapia cognitivo-conductual, y medidas farmacológicas, entre las que se encuentran los ISRS como agentes de primera línea8. La depresión es una de las enfermedades mentales más comunes en pacientes mayores, con una prevalencia global del 10%9. La Asociación Americana de Psicología recomienda utilizar paroxetina en pacientes adultos de más de 60 años con trastorno depresivo persistente10, si bien hace referencia a la contraindicación de este fármaco en estos pacientes según los criterios de Beers de 2019 por su perfil anticolinérgico11 y a la preferencia de muchos psiquiatras geriátricos por escitalopram y sertralina.
Por tanto, en pacientes mayores puede darse la necesidad de emplear ambos tipos de fármacos. El uso conjunto de rivaroxabán e ISRS puede conllevar la aparición de dos tipos de interacciones, por un mecanismo farmacodinámico de grupo y otro farmacocinético. Por un lado, los ISRS impiden la recaptación de serotonina por las plaquetas e interfieren en su capacidad antiagregante, incrementando el riesgo de sangrado al administrarse concomitantemente con rivaroxabán. Por otro lado, algunos ISRS son inhibidores del CYP3A4 (paroxetina, fluoxetina y sertralina), citocromo involucrado en el metabolismo del rivaroxabán y cuya inhibición aumenta el riesgo de aparición de toxicidad por el ACOD12,13. Esta interacción condiciona que se aconseje precaución cuando se tengan que utilizar de forma concomitante rivaroxabán e ISRS14, pero no se conoce si algún ISRS puede tener un perfil más favorable en esta situación.
El objetivo del presente estudio fue evaluar con datos de vida real si el tipo de ISRS utilizado influye en la frecuencia y en la gravedad de sangrado en pacientes anticoagulados con rivaroxabán, con el fin de optimizar el manejo terapéutico de pacientes que requieran ser tratados con ISRS y rivaroxabán.
Métodos
Estudio observacional, longitudinal, retrospectivo, de cohortes, en el que se incluyó a pacientes que recibieron tratamiento concomitante con rivaroxabán e ISRS entre enero de 2016 y febrero de 2020, en un hospital general de clase 5. Se identificó a los pacientes que ingresaron con tratamiento concomitante y que recibían rivaroxabán y se realizó una búsqueda a través de la prescripción electrónica para determinar el momento en el que había comenzado la administración concomitante de ambos fármacos. Se incluyeron los pacientes ≥ 18 años que recibieron tratamiento con rivaroxabán para indicaciones autorizadas y financiadas en ficha técnica. Se excluyeron los pacientes oncológicos, con plaquetopenia previa al inicio de rivaroxabán o con coagulopatías.
Antes de iniciar el estudio y la recogida de datos se presentó la solicitud al Comité Ético de Investigación con Medicamentos (CEIM) del centro, obteniéndose un dictamen favorable (21/026).
Se realizó un seguimiento desde que los pacientes comenzaron con el tratamiento combinado de ISRS y rivaroxabán durante un máximo de 2 años o hasta la finalización de dicha combinación.
Se recogieron las siguientes variables: sexo, edad, ISRS prescrito, aparición de sangrado, gravedad del sangrado, número de eventos hemorrágicos, dosis de rivaroxabán y medicación concomitante que pudiese influir en el riesgo de sangrado [antiinflamatorios no esteroideos (AINE), inhibidores de la bomba de protones (IBP), antihistamínicos del receptor H2 (anti-H2) y antiagregantes].
La variable sangrado grave se definió como aquel sangrado que produjo: fallecimiento del paciente, lesión por ocupación de espacio, un descenso de hemoglobina mayor o igual a 2 g/dl de su valor basal, necesidad de transfusión de dos o más unidades de sangre o una discapacidad permanente en el paciente.
Los pacientes se dividieron en dos cohortes: una cohorte (grupo 1) formada por pacientes que recibieron ISRS inhibidores del CYP3A4 (sertralina, paroxetina y fluoxetina), y otra (grupo 2) integrada por pacientes que recibieron ISRS no inhibidores del CYP3A4 (citalopram y escitalopram).
Los datos se recogieron en un cuaderno de recogida de datos pseudoanonimizado. Se utilizó la información presente en la historia clínica de cada paciente, en los sistemas informáticos de prescripción del hospital y en el módulo único de prescripción utilizado para las prescripciones ambulatorias.
El análisis estadístico se realizó con el paquete SPSS Statistics versión 21.0. Se analizó la muestra poblacional para comprobar si se ajustaba a una distribución normal mediante la prueba de Kolmogorov-Smirnov. Las variables cuantitativas se analizaron mediante un análisis descriptivo utilizando medidas de tendencia central (media) y dispersión (desviación estándar); para las variables cualitativas se calculó la distribución de frecuencias. Para observar las diferencias entre ambas cohortes se utilizaron las pruebas de t de Student y chi cuadrado (en función del tipo de dato analizado: cuantitativo (versus cualitativo). Los valores de p para el análisis de chi-cuadrado cuando se analizó la variable sangrado fueron los valores p de una cola, por tratarse de una interacción que potencialmente sólo puede aumentar el riesgo de sangrado, nunca disminuirlo. Se estableció el nivel de significación estadística como un valor de p < 0,05.
Resultados
Un total de 146 pacientes que habían recibido rivaroxabán para la profilaxis del ictus o la embolia sistémica en pacientes con fibrilación auricular fueron incluidos en el estudio (Tabla 1). De estos pacientes, 89 conformaron la cohorte de ISRS inhibidores del CYP3A4 (grupo 1) y 57 la cohorte de ISRS no inhibidores del CYP3A4 (grupo 2). Ambos grupos mostraron homogeneidad en cuanto a edad y sexo. Se comprobó que la variable edad se ajustaba en ambos grupos a una distribución normal mediante la prueba de Kolmogorov-Smirnov (grupo 1: p = 0,364, y grupo 2: p = 0,292) y se calcularon la media y la desviación estándar, que fueron de 85,7 ± 8,2 años para el grupo 1 y de 83,6 ± 9,7 años para el grupo 2 (p = 0,155). La homogeneidad en cuanto a sexo arrojó un resultado no significativo (p = 0,3403).
Tabla 1. Características demográficas, eventos hemorrágicos y dosis de rivaroxabán en los dos grupos de pacientes establecidos en función del inhibidor selectivo de recaptación de la serotonina administrado
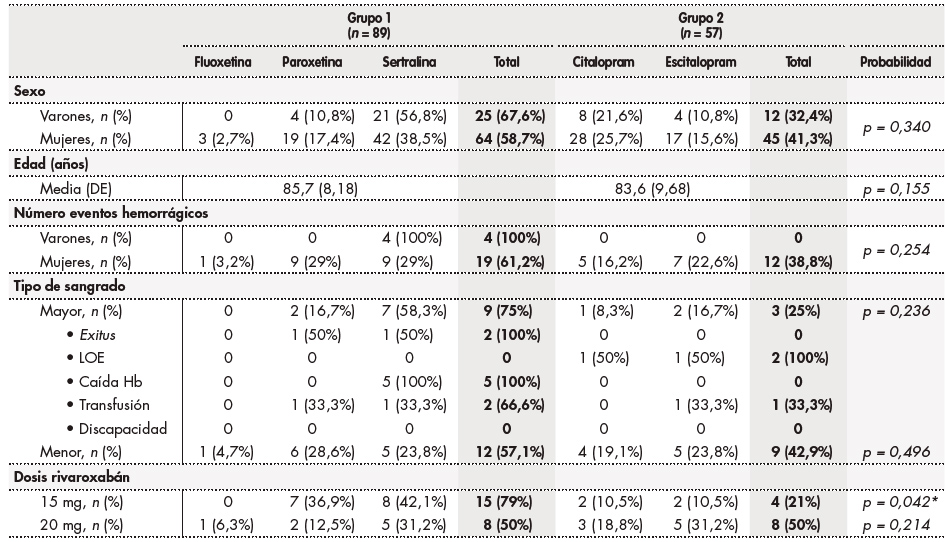
DE: desviación estándar; Hb: hemoglobina; LOE: lesión por ocupación de espacio. * p < 0,05.
Se identificaron un total de 35 eventos hemorrágicos (24% de los pacientes) (Figura 1). La frecuencia de sangrado fue mayor en el grupo 1 (25,8%; 23/89) que en el grupo 2 (21%; 12/57), no encontrándose diferencias estadísticamente significativas (p = 0,2542) Los sangrados menores (n = 23) supusieron el 65,7% del total de los eventos hemorrágicos. De estos, 14 ocurrieron en el grupo 1 (15,7%) y 9 en el grupo 2 (15,8%) (p = 0,4962). Por lo que se refiere a los sangrados mayores, 9 (10,1%) ocurrieron en el grupo 1 y 3 en el grupo 2 (5,3%) (p = 0,2359), siendo el motivo más frecuente de consideración como sangrado grave la disminución de los niveles de hemoglobina en más de 2 g/dl (siete eventos, que en algunos casos necesitaron el empleo de transfusiones), seguido de la lesión por ocupación de espacio (Tabla 1). Se observaron dos exitus como consecuencia del sangrado, ambos en el grupo 1 y en pacientes que recibían la dosis de 15 mg, un caso por inestabilidad hemodinámica posterior y otro por sobreinfección de hematoma que condicionó una sepsis.
Cuarenta y siete pacientes del grupo 1 y 32 pacientes del grupo 2 recibían una dosis diaria de 20 mg de rivaroxabán. La frecuencia de eventos con esta dosis fue del 9% (8/89) en el grupo 1 y del 14% (8/57) en el grupo 2, obteniéndose una p = 0,2137 mediante el test de chi cuadrado de una cola. La dosis de rivaroxabán de 15 mg la recibían 42 pacientes del grupo 1 y 25 pacientes del grupo 2. Con esta dosis la frecuencia de eventos hemorrágicos fue del 16,9% (15/89) en el grupo 1 y del 7% (4/57) en el grupo 2, obteniéndose en este caso una p = 0,04165, mediante el test de chi cuadrado de una cola (Tabla 1).
La información sobre la medicación concomitante que pudiese afectar a la aparición de sangrado (AINE, IBP/anti-H2 y antiagregantes) se recoge en la tabla 2. No se observaron diferencias significativas en la presencia de estos fármacos entre los grupos establecidos (AINE: p = 0,1060; IBP/ anti-H2: p = 0,7321; antiagregantes: p = 0,8477), si bien hubo una mayor proporción de pacientes con AINE en el grupo 2 que en el grupo 1 (16,8% (versus 28,1%). La mayoría de los pacientes tenía activa una prescripción de un IBP o un anti-H2 (121 pacientes, el 81,2% del total), seguidos de la prescripción de AINE (31 pacientes, el 21,2% del total) y de antiagregantes (17 pacientes, el 11,6% del total). En algunos casos, los pacientes tenían prescritos medicamentos de dos o más grupos: AINE + IBP/Anti-H2 (n = 23; 15,6%); antiagregante + IBP/anti-H2 (n = 10; 6,8%) y antiagregante + AINE (n = 1; 0,7%). Tres pacientes (2%) tenían prescrito AINE + IBP/anti-H2 + antiagregante.
Discusión
El presente estudio es uno de los primeros en intentar determinar la posible doble interacción que presentan los ISRS inhibidores del CYP3A4 con rivaroxabán en pacientes con fibrilación auricular no valvular. Estudios previos realizados sobre la combinación de ACOD con ISRS han arrojado datos contradictorios. Un reciente estudio en población coreana evaluó el riesgo de sangrado de pacientes con fibrilación auricular que recibieron concomitantemente ISRS o AINE y halló un mayor riesgo en pacientes que recibieron la combinación que en aquellos que no, llegando a aconsejar el uso de inhibidores de IBP para prevenir la hemorragia de vías digestivas altas15. No obstante, otros estudios no observaron un mayor riesgo de sangrado en pacientes que recibieron la combinación de ISRS con ACOD16,17.
Los estudios anteriores se centraron en la interacción de tipo farmacodinámico. Un reciente estudio sobre población inglesa evaluó el riesgo de sangrado mayor al combinar ACOD con diversos fármacos que presentan interacción farmacodinámica y farmacocinética (inhibidores del CYP3A4 y de la glicoproteína P), observando que la interacción farmacocinética con ACOD no confería un riesgo aumentado de sangrado mayor en comparación con las interacciones farmacodinámicas que sí lo hacían18.
En nuestro estudio no se observó una diferencia significativa en el riesgo de sangrado al usar concomitantemente ISRS inhibidores del CYP3A4 (interacción farmacodinámica + interacción farmacocinética) (versus ISRS no inhibidores del CYP3A4 (interacción farmacodinámica). Parece ser que el posible efecto sobre el citocromo p450 de los ISRS no sería clínicamente relevante en pacientes que reciben tratamiento con rivaroxabán. Estos resultados concuerdan con la información registrada en la ficha técnica de rivaroxabán, en la que se especifica que solamente inhibidores potentes del CYP3A4 podrían tener un efecto clínicamente significativo debido a la baja contribución de este citocromo al metabolismo del fármaco14. No obstante, al analizar el riesgo de sangrado estratificando los pacientes según la dosis de rivaroxabán recibida (15 mg (versus 20 mg) se observaron diferencias significativas y un mayor riesgo de sangrado en pacientes que recibieron la dosis de 15 mg e ISRS inhibidores del CYP3A4 frente a aquellos pacientes que recibieron la dosis de 15 mg e ISRS no inhibidores del CYP3A4. Aunque pueda parecer paradójico, la dosis de 15 mg es la que reciben los pacientes con fibrilación auricular que tienen una disminución de la función renal, y en estos pacientes, la interacción farmacocinética podría tener un mayor impacto clínico, al poder verse aumentada la vida media del rivaroxabán, aumentando el riesgo de sangrado.
En cuanto a la gravedad del sangrado, no se observaron diferencias significativas con ISRS inhibidores del CYP3A4 (versus ISRS no inhibidores del CYP3A4, si bien se detectó una mayor frecuencia de sangrados graves en pacientes que recibían inhibidores del CYP3A4 (10,1%) que en aquellos que recibían ISRS que no lo inhiben (5,2%). El evento adverso más frecuente fue la caída de hemoglobina en más de 2 g/dl sin necesidad de transfusión posterior.
La presencia de medicación concomitante que pudiese influir en el riesgo de sangrado fue elevada, si bien no hubo diferencias significativas en la presencia de esta medicación entre ambos grupos. El alto porcentaje de pacientes que recibían medicación, especialmente en el caso de IBP/ anti-H2, denota la importancia de realizar una prescripción correcta y de herramientas como la deprescripción para optimizar el uso racional de medicamentos y evitar posibles riesgos de uso prolongado de medicamentos19 y de interacciones entre medicamentos, más aún, en pacientes mayores, como los de nuestro estudio, los cuales suelen tener un mayor riesgo20.
La exposición al rivaroxabán, y a los ACOD en general, puede verse afectada por otra serie de factores, entre los que se encuentran la edad avanzada, el bajo peso corporal y la insuficiencia renal y hepática21. Una de las limitaciones de nuestro estudio es no haber registrado y analizado algunos de estos factores, particularmente la función renal, que debería tenerse en consideración en estudios futuros, teniendo en cuenta que los ACOD tienen una dependencia del aclaramiento renal que no presentan los AVK. Otras limitaciones son las intrínsecas a los estudios de naturaleza retrospectiva. Los sangrados leves en muchos casos no son registrados al no necesitar de atención sanitaria, así como tampoco la medicación que toma el paciente, la cual se ha obtenido de la prescripción electrónica, que no incluye la medicación de venta libre en farmacias, entre la que se encuentran ciertos analgésicos. La medicación inhibidora de la glicoproteína P tampoco se tuvo en cuenta. Por último, el limitado tamaño muestral impide la posibilidad de realizar análisis de subgrupos que permitieran dilucidar si hay otras variables que intervengan en el riesgo de sangrado.
La interacción entre rivaroxabán e ISRS continúa siendo controvertida. Los estudios publicados en la literatura son contradictorios y las recomendaciones actuales se basan en la realización de un análisis exhaustivo del balance beneficio-riesgo en cada paciente7. Dado que la terapia con rivaroxabán no presenta una técnica de monitorización establecida en la práctica clínica, a diferencia de los AVK, las posibles interacciones deben tenerse en cuenta previamente al inicio del tratamiento con rivaroxabán. En aquellos pacientes que requieran tratamiento combinado es importante seleccionar el ISRS más adecuado para las características y situación del paciente. Los ISRS no inhibidores del CYP3A4 podrían presentar un beneficio frente a aquellos que lo son en pacientes con insuficiencia renal, teniendo en cuenta otros factores como la prolongación del intervalo QT atribuible al uso de citalopram y escitalopram22, si bien es cierto que la prolongación es mínima y la relevancia clínica prácticamente nula23. Por ello, consideramos que es importante que se continúe realizando estudios al respecto, más teniendo en cuenta que la coadministración de ISRS y rivaroxabán es cada vez más prevalente en pacientes mayores24, pudiendo afectar negativamente a la seguridad del tratamiento, en algunos casos de forma muy grave.
En conclusión, en nuestra experiencia, la combinación de rivaroxabán e ISRS no muestra un mayor riesgo de aparición de eventos hemorrágicos en función del tipo de ISRS utilizado, independientemente de la gravedad de estos. Sí se observó un mayor riesgo de sangrado en los pacientes que recibieron la dosis de 15 mg junto con ISRS inhibidores del CYP3A4. Dada la prevalencia de la combinación y la importancia clínica del evento adverso sería necesaria la realización de estudios adicionales que complementen la evidencia aportada, con el fin de mejorar la seguridad de los pacientes.
Aportación a la literatura científica
El estudio realizado en nuestro centro proporciona información acerca de la incidencia y gravedad del sangrado que pueden sufrir los pacientes con tratamiento concomitante de rivaroxabán y distintos inhibidores selectivos de recaptación de la serotonina, centrándonos en una situación poco estudiada como es la posible doble interacción que presentan algunos de estos antidepresivos.
Esta información permitirá optimizar el manejo terapéutico de pacientes que requieran ser tratados con inhibidores selectivos de recaptación de la serotonina y rivaroxabán, con el fin de reducir el riesgo de eventos hemorrágicos.
















