Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista de la Sociedad Española del Dolor
versão impressa ISSN 1134-8046
Rev. Soc. Esp. Dolor vol.21 no.5 Madrid Set./Out. 2014
https://dx.doi.org/10.4321/S1134-80462014000500004
Manejo del dolor en la fibrodisplasia osificante progresiva
Treatment of pain crisis in fibrodysplasia ossificans progressiva
J. J. Arén Frontera, J. López Garrido, L. J. Martínez Álvarez, J. L. Cordero López y G. A. Ortiz Gómez
Clínica del Dolor. Servicio de Anestesiología y Reanimación. Hospital General Universitario de Granollers. Barcelona
Dirección para correspondencia
RESUMEN
La fibrodisplasia osificante progresiva es una enfermedad de escasa prevalencia, 1 caso cada 2 millones de habitantes, hereditaria, severamente incapacitante, caracterizada por un proceso de osificación en músculos esqueléticos, fascias, tendones y ligamentos, sin tratamiento eficaz y que evoluciona por empujes, que se acompañan de dolor intenso, dando lugar a posteriori, después de varios empujes, a la instalación de dolor basal permanente.
Analizamos las características más salientes de la enfermedad, su historia habitual, su forma de presentación, su evolución, el dolor acompañante y su tratamiento. Este se realiza para combatir el dolor, ya que no existe tratamiento en el momento actual, para la enfermedad de fondo, y será variable de acuerdo al momento evolutivo de la misma, comenzándose con paracetamol y AINE en etapas iniciales, para dar lugar luego al uso de opioides. En lo que se refiere a las crisis de dolor, secundarias a brotes de osificación heterotópicos, existe consenso actualmente en cuanto a la utilización de corticoides de alta potencia antiinflamatoria.
Siendo el dolor un hecho relevante en esta patología, no hemos encontrado ninguna publicación que lo aborde específicamente, por lo cual entendemos oportuna esta comunicación.
Presentamos el caso de persona de 27 años, sexo femenino, portadora de fibrodisplasia osificante progresiva, controlada desde hace años en nuestra Unidad por sus crisis dolorosas severas, así como también por dolor basal instalado en los últimos años. Se relata la presentación de la enfermedad, su evolución, su estado actual, los tratamientos que se han realizado, así como el manejo de su última, reciente y más severa crisis de dolor, en base a dexametasona en altas dosis, y al uso de pregabalina como coadyuvante.
Se concluye con recomendaciones para tratar los empujes dolorosos, basadas en el uso de corticoides, así como el manejo del dolor basal siempre presente en estos pacientes, fundamentado en el uso de opioides.
Palabras clave: Fibrodisplasia osificante progresiva. Crisis dolor. Tratamiento. Dexametasona. Pregabalina.
ABSTRACT
The fibrodysplasia ossificans progressiva is a disease of low prevalence, 1 case per 2 million inhabitants, hereditary, severely disabling, characterized by a process of ossification in skeletal muscles, fascia, tendons and ligaments, without effective treatment, evolving by thrusts which are accompanied by severe pain, resulting in a posteriori, after several thrusts, to installing permanent baseline pain.
We analyze the most salient features of the disease, common history, its presentation, its evolution, the accompanying pain and its treatment. This is done to combat the pain, since there is no treatment at present, for the underlying disease, and will vary according to the time course of the same, beginning itself with paracetamol and NSAIDs in early stages, giving rise then to the use of opioids. In regard to pain crises, buds secondary heterotopic ossification, currently there is consensus regarding the use of high potency anti-inflammatory corticosteroids.
With pain as a relevant in this disease, we found no publication that specifically addresses; therefore we consider this presentation timely.
We report the case of a person of 27 years, female gender, fibrodysplasia ossificans progressiva carrier controlled for years in our unit, for its severe painful crises and baseline pain also installed in recent years. We report the presentation of the disease, its evolution, its current status, as well as treatments that have been made, well as the handling of her latest, recent and more severe pain thrust, based on high-dose dexamethasone, and the use of pregabalin as an adjuvant.
It concludes with recommendations for treating painful crises, based on the use of corticosteroids, and baseline pain management always present in these patients, based on the use of opioids.
Key words: Fibrodysplasia ossificans progressiva. Pain crisis. Treatment. Dexamethasone. Pregabalin.
Introducción
La fibrodisplasia osificante progresiva (FOP) (1) es una enfermedad hereditaria grave e incapacitante, autosómica dominante, del tejido conectivo caracterizado por malformaciones congénitas del primer dedo de ambos pies y osificación heterotópica progresiva en sitios característicos extraesqueléticos: músculos esqueléticos, fascias, tendones y ligamentos (1,2). Es decir, algunos tejidos del organismo, como músculos o tendones, se osifican y se convierten en hueso.
La prevalencia mundial es de aproximadamente 1/2.000.000 (1,3). No hay variaciones étnicas, raciales, de género o predilección geográfica para FOP. Los niños con FOP parecen normales al nacer, excepto para las malformaciones congénitas del primer dedo de ambos pies.
Desde el siglo XIX ha habido referencias esporádicas en la literatura médica describiendo a pacientes que, aparentemente, "se volvieron como piedra" (1,4). Es posible que muchos de estos casos puedan haber sido atribuibles a la FOP.
Quizá el caso más conocido de FOP en tiempos modernos sea el de Harry Raymon Eastlack Jr., nacido en Filadelfia, EE. UU., en noviembre de 1933. Su enfermedad comenzó a manifestarse a la edad de diez años y para la época de su muerte por una neumonía en noviembre de 1973 (seis días antes de su cuadragésimo cumpleaños), su cuerpo se había osificado por completo y solo podía mover sus labios (1,5).
Lo que hace al caso de Eastlack particularmente notable es que antes de su muerte hizo conocer su intención de donar su cuerpo a la ciencia, con la esperanza de que su muerte pueda ayudar a encontrar una cura a esta poco entendida enfermedad. Como era su deseo, su esqueleto preservado ahora reside en el museo Mütter, en el Colegio de Medicina de Filadelfia y fue una invalorable fuente de información para el estudio de esta enfermedad.
Munchmeyer describe la enfermedad en 1969, aunque la primera mención del cuadro patológico fue hecha por el francés Guy Patin en 1672.
Patología
Estas formaciones óseas se producen por brotes desde la infancia. Tras la inflamación de los tejidos blandos en cuestión (músculos, tendones o ligamentos), estos se convierten en hueso, lo que poco a poco supone la pérdida de movilidad (6). Los primeros signos de la enfermedad se suelen dar en las zonas cercanas a la columna vertebral y posteriormente se van propagando hacia otras articulaciones y grupos musculares como los codos o las rodillas. El avance de la patología es progresivo, según se desarrolla aparecen deformidades, discapacidades funcionales y perturbaciones diversas. Por otro lado, tanto los músculos faciales como los músculos indispensables para las funciones vitales del organismo como la respiración, el diafragma, o el corazón para la circulación sanguínea, están característicamente fuera de peligro. Es una enfermedad genética, originada en un gen defectuoso que es transmitido por uno o ambos padres, siendo suficiente que uno de ellos lo haga.
La fibrodisplasia es progresiva, ocasionando deformidades en la medida que avanza, hasta provocar incapacidad severa. La pérdida de la movilidad es grave y puede inmovilizar completamente al paciente.
Los síntomas comienzan a desencadenarse generalmente entre los tres y cinco años y la evolución de la enfermedad es impredecible, presentando periodos de latencia y de agravación (6,7). Durante la primera década de la vida, los episodios esporádicos de inflamaciones dolorosas de tejidos blandos (brotes) se producen a menudo precipitados por traumatismos de los tejidos blandos, las inyecciones intramusculares, intervenciones quirúrgicas, infección viral, estiramiento muscular, caídas o fatiga. Estos brotes llevan a la transformación de los músculos esqueléticos, los tendones, los ligamentos, fascias y aponeurosis, en hueso heterotópico, lo que hace imposible el movimiento.
La cuarta parte de los pacientes desarrolla sordera y calvicie (8). Su diagnóstico se realiza por evidencia clínica y radiológica, pues no se presentan indicios en los análisis de laboratorio (9).
Según estudios de la Universidad de Pensilvania la causa se halla en la activación de un gen (el ACVR1) mutado (10-13), que provoca la formación de tejido cartilaginoso o tejido óseo en las zonas en las que se encuentra. No hay tratamiento ni medicación que sea 100 % eficaz contra esta condición.
Caso Clínico
Mujer de 27 años de edad, que es controlada en nuestra Unidad desde febrero de 2004, en que acudió a la edad de 18 años enviada por su traumatólogo.
Antecedentes
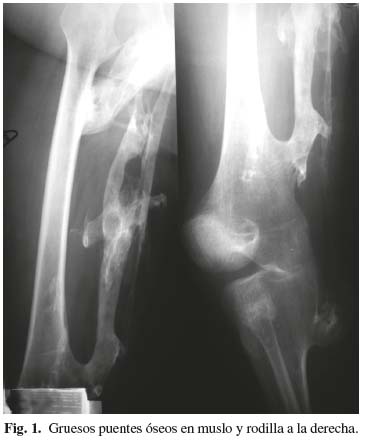
- Fibrodisplasia osificante progresiva. Diagnóstico a los 6 años de edad. Fusión a nivel de cuerpos vertebrales de columna cervical, osificaciones múltiples a nivel de musculatura paravertebral cervical, dorsal, lumbar, cintura escapular bilateral, articulaciones coxofemorales, muslos, rodillas y abdomen (Figs. 1 y 2), que condicionan intenso dolor e incapacidad para la deambulación, requiriendo silla de ruedas para los desplazamientos.
- Intervención quirúrgica de exostosis a nivel de rodilla derecha, y en la primera articulación metatarsofalángica bilateralmente.
- Otosclerosis bilateral intervenida a los 6 años de edad. Portadora de prótesis auditiva.
- Anemia ferropénica probablemente secundaria a sangrado crónico gástrico por tratamiento con AINE y corticoides. En tratamiento con hierro oral.
- Obesidad, aspecto cushingoide.
- Intolerancia al metamizol.
- Síndrome ansioso-depresivo reactivo.
- Episodios de insuficiencia respiratoria hipercápnica secundaria a trastorno ventilatorio restrictivo debido a su enfermedad de base, que han merecido ocasionalmente tratamiento con VMNI domiciliaria desde el año 2004.
Las últimas exploraciones complementarias realizadas han sido:
- TC torácico (febrero de 2010): calcificaciones groseras en tejidos de partes blandas de cavidad torácica en relación a patología de base de la paciente. Cardiomegalia.
- TC abdominal (abril de 2010): se visualizan múltiples calcificaciones musculares en territorio pectoral, periescapular, dorsal, paravertebral y fundamentalmente en territorio glúteo izquierdo, sugestivas de corresponder a su enfermedad de base.
- PFR (marzo de 2011) FVC 1.57 (40 %); FEV1 1.36 (42 %); FEV1 86 %, GSA: (marzo de 2011) P02 70, PC02 55.
Situación sociofuncional: vive con sus padres. Estudiante de administración de empresas. Se moviliza en silla de ruedas.
En su primera visita acudió con pauta de morfina oral de liberación lenta, más pauta permanente de prednisona. Previamente se habían establecido pautas variadas de AINE y paracetamol que fueron progresivamente inefectivas, alternando después distintos tipos de opioides y distintas formas de presentación. Desde febrero de 2004 es controlada periódicamente, tanto por su dolor basal provocado por las múltiples osificaciones heterotópicas que presenta, como también y fundamentalmente, por sus empujes dolorosos secundarios a cuadros inflamatorios en partes blandas que dan lugar a nuevas formaciones óseas, empujes ocasionados por traumatismos leves, posturas anómalas, cuadros virales, etc.
Progresivamente le fuimos retirando los corticoides, dejándolos confinados sólo a los episodios dolorosos por neo-osificación, mejorando en gran parte los elementos cushingoides que presentaba. Control basal con fentanilo transdérmico más fentanilo sublingual para dolor irruptivo. Últimamente, con fentanilo transdérmico 100 mcg/h cada 3 días, el dolor estaba controlado.
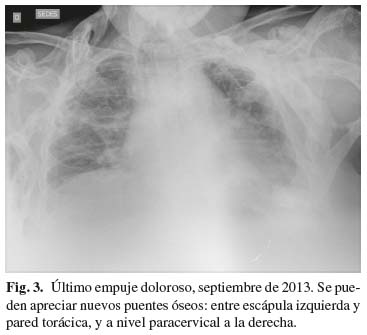
Hace pocas semanas presenta su empuje de dolor más severo desde que la asistimos: por cambio de domicilio, 2odía de vacaciones de la familia, y sin otra causa aparente, inicia dolor severo a nivel de escápula izquierda, sin fiebre y sin ninguna sintomatología respiratoria paralela. Acude al hospital más cercano donde la estudian, no constatando ningún componente respiratorio ni infeccioso difuso, atribuyendo el cuadro a su enfermedad de fondo. La medican con AINE, pirazolonas y morfina, todo por vía IV. Al cabo de 24 horas, como no perciben mejoría, la remiten a nuestro Centro. Al llegar, EVA de 100 mm. La Rx (Fig. 3) muestra neoformación ósea en forma de puente entre escápula izquierda y parrilla costal, así como acentuación de neoformación ósea paracervical derecha. Iniciamos pauta de dexametasona IV 4 mg c/6 horas + morfina IV 5 mg c/6 horas + desketoprofeno 50 mg IV c/8 horas + diazepam oral 10 mg hora 22. Cobertura con omeprazol, 40 mg/día. A las 24 horas persiste prácticamente igual, por lo cual subimos dosificación de dexametasona a 12 mg c/6 horas. Tras 24 horas se produce mejoría, EVA de 40 mm, subimos la dosificación de dexametasona por la mañana a 20 mg, dejando las otras 3 administraciones a 12 mg. Además, como relata algunas disestesias y parestesias a la movilización de la región dolorida, añadimos pregabalina oral: 75mg-5mg-150 mg. Mejoría progresiva. Al cabo de 3 días de esta última pauta, EVA 0 mm. Comenzamos descenso en la dosificación de dexametasona, pasándola a vía oral, y de la morfina. Cinco días después alta a domicilio, con pauta oral de paracetamol 1 gramo c/8 horas + naproxeno 500 mg 1-0-0 + pregabalina 75 1-0-2 + diazepam 10 mg 0-0-1 + montelukast 5 mg 0-0-1. A los 6 días del inicio de los corticoides la analítica es normal.
Desde el alta realizamos seguimiento telefónico, mostrando buena evolución. Sin dolor. Ha reanudado sus estudios universitarios a distancia.
Discusión
Este caso en general, y el manejo y evolución de este último empuje doloroso, en particular, son típicos en la evolución de esta severa patología.
En esta última crisis dolorosa se han seguido los criterios recomendados (1,15), primero descartar, por clínica y paraclínica, otro origen posible, y a continuación tratar el cuadro de dolor, buscando paralelamente de detectar radiológicamente, el foco o focos de neo-osificación, hallándose este a nivel periescapular izquierdo.
El tratamiento inicial, basado en AINE, mostró una vez más en esta patología su escasa o nula eficacia ante el severo cuadro inflamatorio que se pone en marcha y que desemboca rápidamente en neo-osificación.
En cuanto al uso de los corticoides, las recomendaciones de la International Fibrodysplasia Ossificans Progressiva Association (IFOPA) (1,14,15) hablan de tratar las crisis de dolor con prednisona 2 mg/kg durante un máximo de 4-5 días. En este caso empleamos dexametasona por su mayor poder antiinflamatorio (6 veces más potente que la prednisona, 25 veces más potente que la hidrocortisona) (16-18), y su casi nula acción mineralocorticoidea (16-18). Además, es necesario enfatizar que fue necesario utilizar dosis francamente superiores a las recomendadas para poder yugular el empuje doloroso. Tratando de seguir el principio en terapia corticoidea de emplear la mínima dosis necesaria durante el menor tiempo posible, una vez superado el empuje doloroso, comenzamos progresivamente el descenso en la dosificación del fármaco. Importa señalar que la analítica practicada a los 6 días del inicio de la dexametasona fue normal, incluyendo glucemia normal.
Tal como es preceptivo en estos casos, apenas recibimos la paciente se comenzó el tratamiento corticoideo, y también como se recomienda, se empleó la vía endovenosa, pasando luego a la vía oral.
Además del uso de la dexametasona, otro elemento novedoso en este caso, fue la utilización de pregabalina, justificada por la presencia de componentes de dolor neuropático añadidos al dolor nociceptivo de fondo, lo cual contribuyó rápidamente a la mejoría de la sintomatología. Las múltiples distorsiones anatómicas que se originan con los procesos de neo-osificación, elongando y/o comprimiendo estructuras nerviosas, dan lugar a tales componentes de dolor neuropático.
En el alta hospitalaria dejamos pautado un AINE generalmente bien tolerado, como es el naproxeno, e iniciamos pauta oral de montelukast, en mínima dosificación de 5 mg, antagonista de los leucotrienos (15,19) que tienen que ver con la puesta en marcha del proceso inflamatorio que a su vez puede desembocar en una neo-osificación (1,14,15).
Por último, dado lo infrecuente de esta patología, en aquellos casos ya diagnosticados, es recomendable entregar al paciente un esquema básico del abordaje de los empujes de dolor, para ser presentado en los servicios de urgencia hospitalaria, cuando sea necesario hacerlo en circunstancias de viajes, vacaciones, etc., pues, al ser esta entidad tan poco conocida, pueden originarse actitudes terapéuticas erróneas e incluso contraproducentes como pueden ser analgésicos por vía intramuscular, punciones, etc., lo cual daría lugar a nuevos focos de inflamación-osificación.
Bibliografía
1. Pignolo RJ, Shore EM, Kaplan FS. Fibrodysplasia ossificans progressiva: Clinical and genetic aspects. Orphanet J Rare Dis 2011;6:80. [ Links ]
2. Kaplan FS, Xu M, Seemann P, Connor M, Glaser DL, Carroll L, Delai P, et al. Classic and atypical fibrodysplasia ossificans progressiva (FOP) phenotypes are caused by mutations in the bone morphogenetic protein (BMP) type I receptor ACVR1. Hum Mutat 2009;30:379-90. [ Links ]
3. Kaplan FS, Xu M, Glaser DL, Collins F, Connor M, Kitterman J, et al. Early diagnosis of fibrodysplasia ossificans progressiva. Pediatrics 2008;121:295-300. [ Links ]
4. Cohen RB, Hahn GV, Tabas JA, Peeper J, Levitz CL, Sando A, et al. The natural history of heterotopic ossification in patients who have fibrodysplasia ossificans progressiva. A study of forty-four patients. J Bone Joint Surg Am 1993;75:215-9. [ Links ]
5. Kaplan FS, Glaser DL. Thoracic insufficiency syndrome in patients with fibrodysplasia ossificans progressiva. Clin Rev Bone Miner Metab 2005;3:213-6. [ Links ]
6. Kaplan FS, Xu M, Glaser DL, Collins F, Connor M, Kitterman J, et al. Early diagnosis of fibrodysplasia ossificans progressiva. Pediatrics 2008;121:295-300. [ Links ]
7. Pignolo RJ, Suda RK, Kaplan FS. The fibrodysplasia ossificans progressiva lesion. Clin Rev Bone Miner Metabol 2005;3:195-200. [ Links ]
8. Levy CE, Lash AT, Janoff HB, Kaplan FS. Conductive hearing loss in individuals with fibrodysplasia ossificans progressiva. Am J Audiol 1999;8:29-33. [ Links ]
9. Kaplan FS, Strear CM, Zasloff MA. Radiographic and scintigraphic features of modeling and remodeling in the heterotopic skeleton of patients who have fibrodysplasia ossificans progressiva. Clin Orthop Relat Res 1994;238-47. [ Links ]
10. Shore EM, Xu M, Feldman GJ, Fenstermacher DA, Cho T-J, Choi IH, et al. A recurrent mutation in the BMP type I receptor ACVR1 causes inherited and sporadic fibrodysplasia ossificans progressiva. Nature Genetics 2006;38:525-7. [ Links ]
11. Shen Q, Little SC, Xu M, Haupt J, Ast C, Katagiri T, et al. The fibrodysplasia ossificans progressiva R20H ACVR1 mutation activates BMP independent chondrogenesis and zebrafish embargo ventralization. J Clin Invest 2009;119:3462-72. [ Links ]
12. Kaplan FS, Groppe J, Pignolo RJ, Shore EM. Morphogen receptor genes and metamorphogenes: Skeleton keys to metamorphosis. Ann N Y Acad Sci 2007;1116:113-33. [ Links ]
13. Kaplan FS, Chakkalakal SA, Shore EM. Fibrodysplasia ossificans progressiva: Mechanisms and models of skeletal metamorphosis. Dis Model Mech 2012;5(6):756-62. [ Links ]
14. Kaplan FS, Shore EM, Pignolo RJ. The medical management of fibrodysplasia ossificans progressiva: Current treatment considerations. Clin Proc Intl Clin Consort FOP 2011;4:1-100. [ Links ]
15. International Fibrodysplasia Ossificans Progressiva Association. Available at: http://www.ifopa.org/en/living-with-fop-menu/treatment-guidelines.html. [ Links ]
16. Kravitz J, Dominici P, Ufberg J, Fisher J, Giraldo P. Two days of dexamethasone versus 5 days of prednisone in the treatment of acute asthma: A randomized controlled trial. Ann Emerg Med 2011;58(2):200-4. [ Links ]
17. Galofré JC. Manejo de los corticoides en la práctica clínica. Rev Med Univ Navarra 2009;53:9-18. [ Links ]
18. Spies CM, Strehl C, van der Goes MC, Bijlsma JW, Buttgereit F. Glucocorticoids. Best Pract Res Clin Rheumatol 2011;25(6):891-900. [ Links ]
19. Knorr B, Franchi LM, Bisgaard H, Vermeulen JH, LeSouef P, Santanello N, et al. Montelukast, a leukotriene receptor antagonist, for the treatment of persistent asthma in children aged 2 to 5 years. Pediatrics 2001;108(3):E48. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Juan José Arén Frontera
Clínica del Dolor
Servicio de Anestesiología y Reanimación
Hospital General Universitario de Granollers
Avda. F. Ribas, s/n
08402 Granollers-Barcelona
e-mail: jjaren@telefonica.net
Recibido: 10-09-13.
Aceptado: 20-12-13.