INTRODUCCIÓN
El dolor crónico es una de las principales causas de incapacidad e impotencia funcional. La demanda de las infiltraciones en las unidades de dolor crónico aumenta cada día. Por otro lado, las enfermedades cardiovasculares y cerebrovasculares son las que generan más morbimortalidad en nuestro medio. Por ello, uno de los problemas que nos encontramos, previo a la realización de las infiltraciones, es el aumento del número de pacientes que están bajo tratamiento antiagregante plaquetario (AAP) y/o anticoagulante.
Para la realización de bloqueos periféricos, infiltraciones intrarticulares o miofasciales superficiales 1 no es necesaria la suspensión de antiagregantes plaquetarios (AAP) ni anticoagulantes (ACO). Un estudio realizado entre los años 2009 y 2013 2, en el cual se revisaron 901 procedimientos de rodilla y de hombro, registró tan solo 2 sangrados clínicamente significativos, por lo que se concluye de dicho estudio que la anticoagulación oral no debe considerarse un factor de riesgo para el desarrollo de complicaciones por sangrado tras punciones articulares y, por lo tanto, no deben diferir su realización cuando están indicadas.
La toma de antiagregantes plaquetarios o anticoagulantes suscitan una gran preocupación de cara a ofrecer al paciente una infiltración que afecte al neuroeje, infiltraciones miofasciales profundas o bloqueos profundos, ya que estos procedimientos presentan un riesgo hemorrágico elevado. Respecto a los antiagregantes plaquetarios, es habitual que se recomiende su retirada entre una semana y 10 días antes de la infiltración para minimizar el riesgo de hematomas. Sin embargo, esta práctica no está exenta de riesgos, pues un paciente sin la necesaria cobertura antiagregante durante un determinado periodo de tiempo puede tener mayores posibilidades de desarrollar complicaciones cardiacas, cerebrales o vasculares periféricas; por lo tanto, la recomendación de retirada del fármaco durante un determinado tiempo de forma sistemática debe ser cuestionada. La recomendación actual es la cuidadosa valoración del riesgo trombótico de manera individualizada para minimizar el tiempo en que el paciente está sin la debida protección antiagregante.
El problema que plantean los anticoagulantes es cómo realizar la "terapia puente" de los pacientes anticoagulados con antivitamina K o con los nuevos anticoagulantes orales, problema que habitualmente solucionamos consultando al hematólogo o derivando al MAP. En estos casos no se debe realizar una terapia puente de manera rutinaria, sino que se debe aplicar una estrategia adaptada a cada paciente, teniendo en cuenta el riesgo trombótico de cada paciente y el riesgo hemorrágico de cada infiltración.
Por ese motivo hemos constituimos un equipo multidisciplinar formado por médicos de los servicios de Hematología/Hemostasia, Cardiología, Anestesia/Unidad de Dolor y Rehabilitación, para generar una Guía consensuada.
El objeto de esta guía es mejorar la calidad y seguridad en la atención de los pacientes antiagregados y anticoagulados de cara a recibir una infiltración en la Unidad de Dolor, así como evitar derivaciones innecesarias a otros especialistas.
INDICACIONES DE LOS ANTIAGREGANTES
Prevención primaria
Paciente de alto riesgo coronario: DM, HTA, DLP, fumador.
En mayores de 50 años asintomáticos sin factores de riesgo (FR) valorar riesgo-beneficio.
Fibrilación auricular sin factores de riesgo (con FR: de elección anticoagulación; en caso de recurrencia añadir antiagregantes).
Prevención secundaria
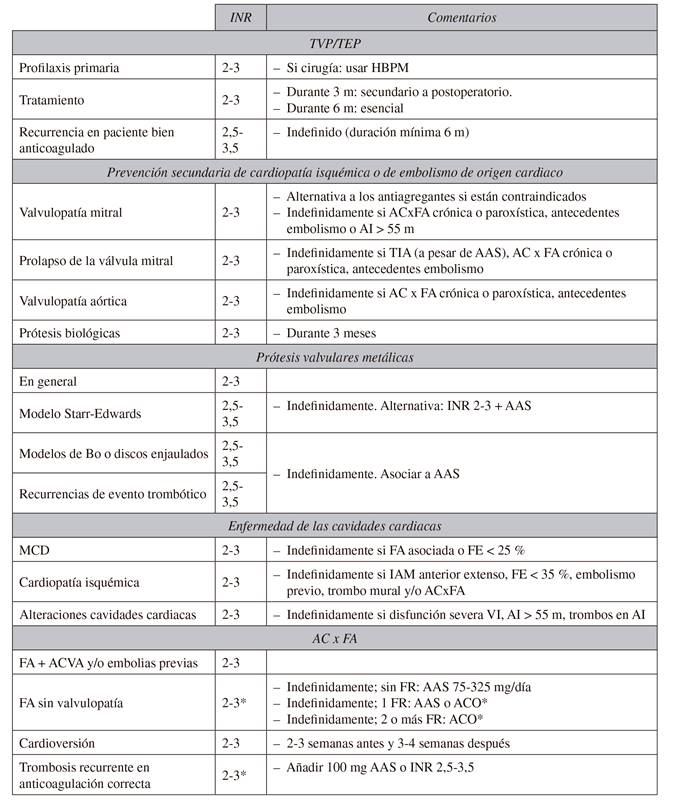
En la Tabla I se muestran las patologías que precisan mantener la antiagregación con AAS como prevención secundaria.
Es importante señalar que en algunas de estas indicaciones, en función del tiempo de evolución y del riesgo trombótico asociado, estaría recomendada la administración de un fármaco anticoagulante y no de un fármaco AAP.
Doble terapia: ¿cuándo se puede pasar a monoterapia con un antiagregante (AAS)?
4 semanas: STENT intracraneal.
4-6 semanas: STENT convencional coronario.
4 meses: STENT carotídeo.
STENT coronario: duración variable en función de tipo de stent. Los stent de nueva generación permiten suspender la doble antiagregación en 3, 6 o 12 meses (se recomienda consultar con cardiología intervencionista el tipo de stent que se ha colocado). Por norma general se suspende la doble antiagregación pasados 12 meses.
INDICACIONES DE ACO
Las indicaciones del tratamiento anticoagulante oral están en continua revisión. En la Tabla II se muestran las principales indicaciones de la terapia con ACO 3) (4.
RIESGO TROMBOEMBÓLICO
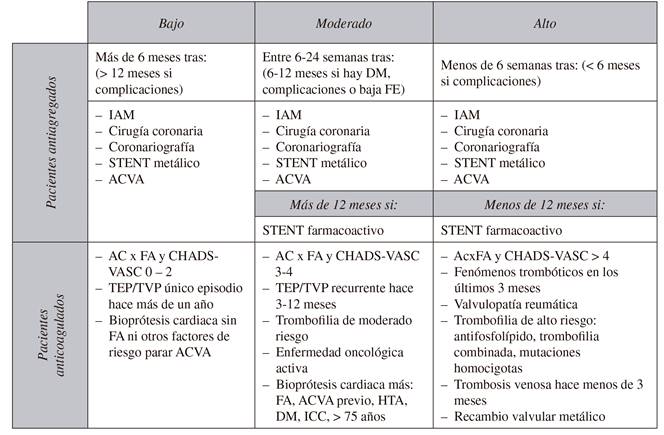
La Tabla III muestra un modelo de estratificación del riesgo trombótico 4) (5 de los pacientes antiagregados y/o anticoagulados.
Basándonos en la estratificación del riesgo trombótico, se puede establecer que las intervenciones consideradas como de alto riesgo hemorrágico (como puede ser el caso de las infiltraciones del neuroeje, rizólisis de ganglio estrellado o del trigémino, etc.) presentarán un mayor beneficio en la suspensión preoperatoria de los AAP y de terapia puente si se está tomando ACO, siempre y cuando se realicen cuando el riesgo trombótico sea lo menor posible (es preferible respetar los tiempos tras eventos cardio/neurovasculares).
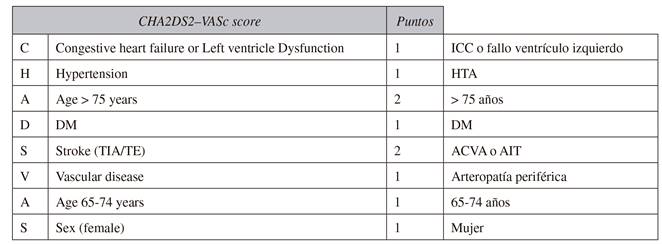
La escala CHA2DS2-VASc estratifica el riesgo trombótico en la fibrilación auricular: a mayor puntuación mayor riesgo trombótico (Tabla IV).
RIESGO DE SANGRADO
Según el procedimiento ( 1 ) ( 6 ) ( 7 ) (Tabla V)
Factores relativos al paciente ( 6 ) ( 8 )
Tabla V ESTRATIFICACIÓN DEL RIESGO HEMORRÁGICO SEGÚN EL TIPO DE PROCEDIMIENTO

C: cervica.; L: lumbar. T: torácico. Pasarán a considerarse pacientes de alto riesgo hemorrágico aquellos pacientes de: edad avanzada, historial previo de dificultades en la coagulación, uso de otros anticoagulantes/antiagregantes, cirrosis hepática o insuficiencia hepática o renal avanzada. Nuestras recomendaciones sobre antiagregación: En rojo: técnicas en las que se han de suspender los antiagregantes plaquetarios. En negro: se puede realizar con AAS 100 mg/24 h. En azul: cualquier antiagregante en monoterapia
Green y Machin describieron factores de riesgo asociados al hematoma epidural: edad avanzada, sexo femenino, coagulopatía (fallo hepático o renal, neoplasia, síndrome de HELLP, coagulación intravascular diseminada, etc.), trombocitopenia, alteraciones anatómicas espinales (espina bífida, estenosis de canal, neoplasias espinales, espondilitis anquilosante y osteoporosis.
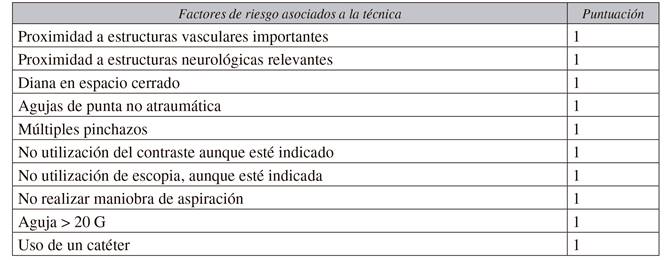
Factores relativos a la técnica ( 6 ) ( 9 ) (Tabla VI)
Uso escopia y contraste radiológico: minimiza la necesidad de punciones innecesarias, disminuye la dificultad del procedimiento, permite localizar la posición exacta de la aguja y reconocer precozmente la punción de un vaso sanguíneo.
Aspiración: si al realizar la aspiración se observa refluir sangre, significa que se ha puncionado un vaso sanguíneo; sin embargo, si la maniobra de aspiración es negativa (no refluye sangre) no excluye que no hayamos puncionado un vaso.
Calibre de las agujas: las agujas de menor calibre disminuyen el riesgo de hemorragia.
Número de punciones: el riesgo de hemorragia aumenta proporcionalmente al número de punciones realizadas.
SUSPENSIÓN/SUSTITUCIÓN ACOS Y AAP PREVIO A INFILTRACIÓN (Anexo I-II-III-IV-V-VI-VII)
La realización de técnicas en la Unidad de Dolor bajo los efectos de los AAP/ACO ha sido durante mucho tiempo una cuestión polémica. En el caso de una infiltración electiva de alto riesgo hemorrágico se recomienda posponer la infiltración en las situaciones de alto riesgo trombótico hasta que este disminuya. Las recomendaciones existentes para la sustitución del tratamiento antiagregante y anticoagulante se basan en los resultados de estudios observacionales y en la descripción de casos clínicos.
Límites de seguridad ( 1 ) ( 7 ) ( 10 ) ( 11 )
En la Tabla VII se resumen los intervalos mínimos de seguridad recomendados para la suspensión de los fármacos que alteran la hemostasia antes de una infiltración en la Unidad de Dolor y para su posterior reintroducción después de la misma. Son recomendaciones generales extraídas de las guías de anestesia regional 12) (13) (14) (15) (16, y hay que señalar que las infiltraciones de bajo riesgo hemorrágico no requieren la suspensión de los anticoagulantes ni antiagregantes plaquetarios, por lo que los valores inferiores de los intervalos de reintroducción de estos fármacos no serán utilizados en este escenario terapéutico.
Tabla VII INTERVALOS DE SEGURIDAD PARA LA SUSPENSIÓN Y REINTRODUCCIÓN DE FÁRMACOS QUE ALTERAN LA HEMOSTASIA

1. Si riesgo trombótico elevado y bajo riesgo hemorrágico. Punción traumática y el resto de los casos 24 horas. 2. Sustituir por AAS 100 mg/24 h. 3. La suspensión puede ser de 3 días si el INR está en rango terapéutico (INR 2-3), si está por encima de 3,5 deberá suspenderse al menos 5 días antes. 4. Ver apartado de IR. 5. A las 12 horas se puede administrar la primera dosis si el riesgo trombótico es elevado y el de sangrado bajo, aunque es preferible reintroducir a las 24 h post-punción.
Recomendaciones de las diferentes sociedades de anestesiología
Respecto a las técnicas invasivas realizadas en la Unidad de Dolor en pacientes en terapia antiagregante y/o anticoagulante se recogen en una serie de revisiones de las distintas sociedades Europeas y Norte Americanas (ASRA) 7) (8) (9) (17) (18, resumidas en la Tabla VIII.
La implantación de neuroestimuladores requiere una consideración especial: se deberá reducir al máximo el intervalo entre el 1º y 2º tiempo para no aumentar innecesariamente el periodo en el que el paciente esté sin antiagregación/anticoagulación.
Tabla VIII RECOMENDACIONES DE LAS DIFERENTES SOCIEDADES DE ANESTESIOLOGÍA PARA INFILTRACIONES/TÉCNICAS INTERVENCIONISTAS EN PACIENTES EN TERAPIA CON AAP, ACO Y OTROS FÁRMACOS QUE ALTERAN LA HEMOSTASIA

*En la práctica diaria no se suspenden para procedimientos con elevado riesgo de sangrado como son: transforaminales lumbares, caudales.
Recomendaciones del equipo multidisciplinar del HUMV para técnicas invasivas realizadas en la Unidad de Dolor en pacientes en terapia antiagregante y/o anticoagulante
Terapia puente para los antiagregantes plaquetarios
Un solo fármaco antiagregante:
AAS 100 mg/ 24 h (Anexo I): se ha de suspender en pacientes de alto y en determinados casos de técnicas de moderado riesgo hemorrágico (consultar Tabla V): en prevención primaria con menos de 3 factores de riesgo cardiovascular se podría suspender el AAS sin problemas. En el resto de situaciones se debería suspender entre 3 y 4 días antes de la técnica.
Clopidogrel, ticagrelor, prasugrel, ticlopidina (Anexo II): en pacientes con bajo riesgo hemorrágico no sería necesaria su suspensión. En el resto de pacientes se deberían sustituir por AAS 100 mg/24 h los 5-10 días previos (según el fármaco, Tabla VII) a la técnica y suspender el AAS 3-4 días en todas las técnicas de elevado riesgo de sangrado y en aquellas de moderado riesgo de sangrado que lo precisen (Tabla V).
Doble terapia antiagregante: pacientes de elevado riesgo trombótico (Anexo III):
Bajo riesgo hemorrágico: se pasará a monoterapia con AAS 100 mg/24 los 5-7 días previos a la técnica (depende del fármaco usado para la doble antiagregación, generalmente es el clopidogrel que se suspenderá los 7 días previos a la infiltración; para el resto consultar la Tabla VII). Hay infiltraciones de moderado riesgo hemorrágico en las que se puede mantener el AAS en monoterapia (Tabla V).
Moderado o alto riesgo hemorrágico: se debe de suspender la doble antiagregación. Por lo tanto, insistimos en tomar una decisión conjunta con los equipos de cardiología y hemostasia.
Es recomendable aplazar las infiltraciones en pacientes de elevado riesgo trombótico con doble antiagregación hasta que pasen a estar con un solo antiagregante.
En caso de que la infiltración sea mandatoria por un dolor incoercible con importante disminución de la calidad de vida del paciente, se tomará una decisión multidisciplinar consensuada (Cardiólogos, Neurólogos, Hematólogos, U. Dolor).
Todas las recomendaciones sobre la suspensión de antiagregantes persiguen el objetivo de llegar a la prueba con los niveles de fármaco lo suficientemente bajos para no producir un sangrado con riesgo vital y que permita alcanzar los niveles terapéuticos de cada fármaco lo más rápido posible tras la reintroducción.
La sustitución de los AAP por HBPM a dosis terapéuticas es una posibilidad no completamente validada.
Nuestra recomendación acerca de cuándo se ha de suspender el AAS en pacientes de elevado moderado-alto riesgo trombótico que se van a someter a técnicas con moderado-elevado riesgo hemorrágico de sangrado sería mantener únicamente 100 mg AAS hasta 3 días previos a la infiltración. Si nos encontramos antes un caso de una paciente en tratamiento con inhibidores de la P2Y12 (por ejemplo alergia a AAS) se suspenderán los 5 días previos a la realización de la técnica.
Esta recomendación está basada en el hecho de que a los 3 días de la suspensión del AAS y a los 5 días de la suspensión de los inhibidores p2y12 existe ya un número suficiente de plaquetas normofuncionantes para asegurar la hemostasia 1.
Reintroducción de los antiagregantes: a las 24 horas de la realización de la técnica.
Bridging (terapia puente) para los anticoagulantes con HBPM ( 10 ) ( 11 ) ( 19 ) (Tabla IX)
De antivitamina K a HBPM (Anexo IV):
Riesgo hemorrágico bajo: no es preciso suspender el tratamiento.
Riesgo hemorrágico moderado o alto:
Suspender el antivitamina K: 3-5 días antes de la infiltración; acenocumarol 4 días (la suspensión puede ser de 3 días si el INR está entre 2-3, si está por encima de 3,5 deberá suspenderse al menos 5 días antes) y warfarina 5 días.
Iniciar la administración de HBPM a las 24 horas de la última dosis de antivitamina K: 1. A dosis profiláctica (Tabla IX) si el riesgo trombótico es bajo-moderado, administrándose la última dosis 12 horas antes de la infiltración. 2. A dosis terapéuticas (Tabla IX) si el riesgo de tromboembolismo es elevado, administrándose la última dosis 24 h antes de la infiltración.
Intervenir si el INR ≤ 1,5.
Reintroducción de su pauta habitual (Tabla X): 1. HBPM: se reiniciará a las 24 h, se administrará hasta que el INR esté en rango terapéutico según el control de coagulación (se remitirá al paciente a su centro de salud para realizarse dicho control a los 5 días de la infiltración). 2. El ACO se reintroducirá a las 24 horas de a la infiltración.
Tabla X PERIODOS DE SEGURIDAD PARA LA REINTRODUCCIÓN DE LOS ANTIVITAMINA K TRAS LA TÉCNICA

*La última dosis de HBPM se administrará cuando se alcancen niveles de INR en rango terapéutico según los controles de coagulación.
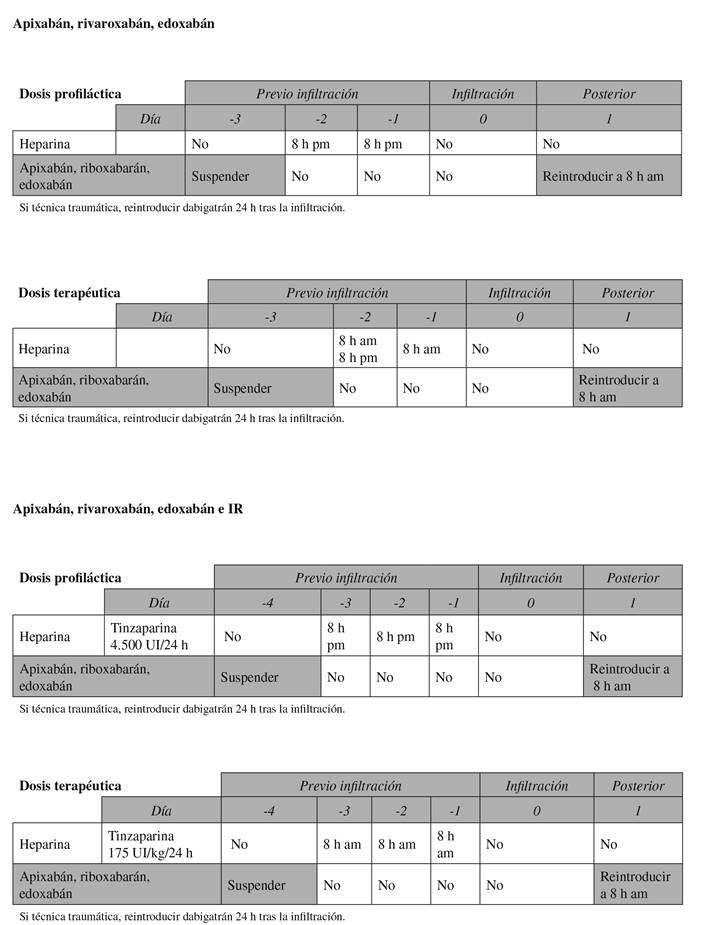
DE DACOS A HBPM (Anexo V):
Riesgo hemorrágico bajo: no es preciso suspender el tratamiento.
Riesgo hemorrágico moderado o alto:
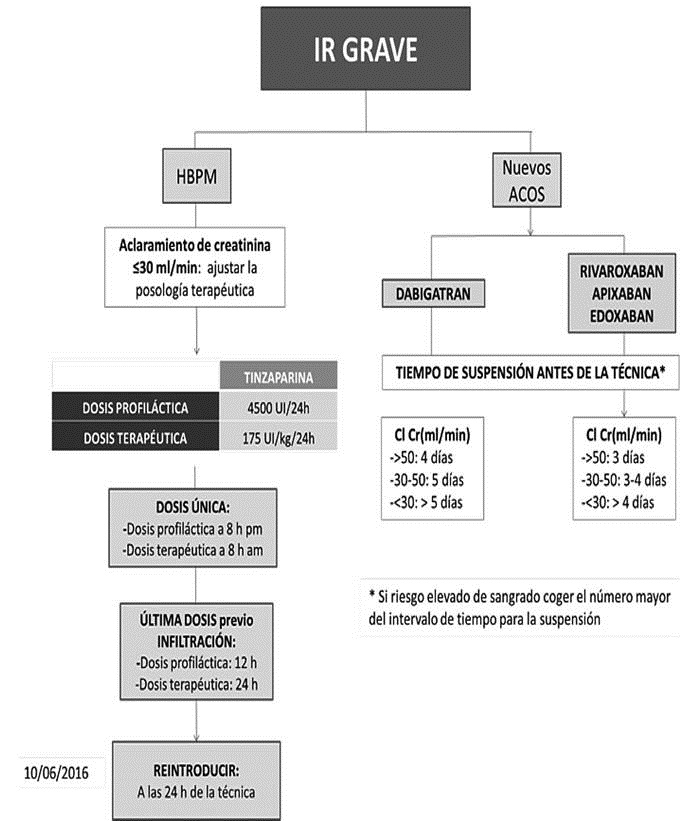
Suspender el DACO de 3-6 días antes de la infiltración y atendiendo a la función renal (Tabla IX).
Se ha de iniciar una terapia puente con HBPM a las 24 horas de la última toma del DACO con HBPM: 1. En riesgo bajo e intermedio de tromboembolismo la pauta de HBPM será de dosis profiláctica (Tabla IX) y se administrará última dosis 12 h antes de la infiltración. 2. Si el riesgo de tromboembolismo es elevado se iniciará la administración de HBPM a dosis terapéuticas (Tabla IX) y se administrará última dosis 24 h antes de la infiltración.
Para la reintroducción de los DACOS: estos se reiniciarán a las 24 horas de la técnica.
Pacientes antiagregados y anticoagulados: triple terapia antitrombótica. Dado que todos los procedimientos llevados a cabo en la Unidad de Dolor son electivos, se han de demorar las técnicas hasta que el paciente pase a estar con doble terapia por disminución de su riesgo trombótico.
En caso de que la técnica a realizar fuese mandatoria, el paciente deberá ser informado del elevadísimo riesgo trombótico que padece y de las consecuencias de la suspensión de la triple terapia. Asimismo, el paciente deberá ser evaluado de manera conjunta por el equipo de Cardiología y Hematología/Hemostasia previamente a la toma de cualquier decisión.
Otras recomendaciones: insuficiencia renal ( 10 ) ( 18 ) (Anexo VI)
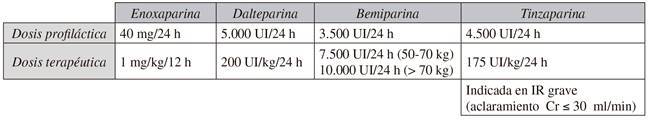
Ajuste de dosis de HBPM: en relación a las HBPM, si el aclaramiento de creatinina es menor o igual a 30 ml/min tiene indicación clara como HBPM de uso ambulatorio la tinzaparina administrada una sola vez al día. La posología de esta heparina se muestra en la Tabla XI.
Aumento del tiempo de suspensión de los DACOS: en el caso de los nuevos anticoagulantes también aumentará el intervalo mínimo de seguridad a la infiltración (Tabla XII).
Tabla XI PAUTA DE TINZIPARINA INDICADA EN PACIENTE AMBULATORIO CON INSUFICIENCIA RENAL (ACLARAMIENTO CR ≤ 30 ML/MIN)

CONDICIONES DE SEGURIDAD
Recomendamos solicitar un estudio de coagulación completa (AP, TTPA, fibrinógeno) a todos los pacientes que vayan a ser sometidos a infiltraciones de moderado o elevado riesgo hemorrágico. Los valores de los parámetros de la coagulación que nos permitirán realizar las infiltraciones con el menor riesgo de sangrado serán:
Plaquetas normofuncionantes y recuento ≥ 75.000.
INR < 1,5.
Fibrinógeno ≥ 150.
TTPA ratio < 1,4.
Acenocumarol y warfarina: actividad de protrombina ≥ 70 %.
Dabigatran: TTPA ratio < 1,4.
Rivaroxaban , apixaban, edoxaban: TP ratio < 1,3 y AP ≥ 70 %.
En caso de pacientes en tratamiento anticoagulante sería recomendable realizar la analítica la mañana de la infiltración para comprobar que los valores están dentro de los rangos de seguridad tras la realización de las terapias puente.