INTRODUCCIÓN
La C5-carnitina (C5) es uno de los marcadores primarios utilizados en los programas de cribado neonatal para la detección precoz de diversos errores congénitos del metabolismo (ECM). Este marcador permite la detección precoz de la acidemia isovalérica (OMIM 243500) (IVA) gracias a la concentración elevada de isovalerilcarnitina que presentan los recién nacidos afectos en la sangre después de nacer1. La C5 también puede estar alterada en otros ECM (deficiencia de 2-metilbutiril-CoA deshidrogenasa, OMIM 610006; encefalopatía etilmalónica, OMIM 602473; acidemia glutárica de tipo 2, OMIM 231680) por elevación de 2-metilbutirilcarnitina o de isovalerilcarnitina, ambos isómeros estructurales para los que se obtiene un pico común (isobárico) en espectrometría de masas en tándem (MS/MS) cuando el procedimiento analítico se lleva a cabo sin derivatización previa. La IVA es una enfermedad autosómica recesiva para la que se han descrito dos fenotipos: uno de presentación neonatal grave con manifestaciones en los primeros días de vida, y otro crónico intermitente caracterizado por retraso en el desarrollo físico y mental2. En ambas formas y a lo largo de la vida se pueden producir descompensaciones en situaciones de estrés metabólico (enfermedades intercurrentes, ayuno prolongado) que pueden causar la muerte del individuo o bien dejar secuelas a nivel de sistema nervioso. Su prevalencia en poblaciones occidentales se ha estimado en 1:5260003, aunque la detección de formas leves mediante programas de cribado neonatal apunta a que podría ser mayor4.
El ácido piválico, también denominado ácido neo-pentanoico o ácido trimetilacético, es un isómero estructural de C5 al igual que la isovalerilcarnitina. La administración de medicamentos que incluyen en su composición profármacos o excipientes en forma de ésteres de este compuesto puede dar lugar a elevaciones de C5 en la sangre de los recién nacidos. En este sentido se han descrito falsos positivos de cribado neonatal por una elevación de C5 debida a la ingesta por parte del bebé de cremas empleadas por las madres para el cuidado del pezón cuya composición incluía isodecilneopentanoato5,6, y al tratamiento de la madre con pivoxilsulbactam antes del parto7. La frecuencia de falsos positivos debidos a estas causas ha llevado a que algunos laboratorios desarrollen e implementen pruebas de segundo nivel para aumentar la especificidad del cribado de IVA8,9.
Desde hace algunos años se utilizan en España medicamentos cuyo principio activo es el cefditoreno, una cefalosporina oral de tercera generación de amplio espectro indicada en el tratamiento de faringoamigdalitis aguda, sinusitis maxilar aguda, exacerbación aguda de bronquitis crónica, neumonía adquirida en la comunidad, e infecciones no complicadas de la piel y tejidos blandos10,11. Este antibiótico se administra en forma de cefditoreno pivoxilo (CFP), profármaco del cual se libera el principio activo por acción de las esterasas intestinales10,11,12. La acción de estas enzimas libera también el pivalato esterificado, que se absorbe y se conjuga con carnitina para ser eliminado a través de la orina13.
El objetivo de este trabajo fue hacer un análisis descriptivo de los falsos positivos asociados al tratamiento preparto de la madre con CFP, en la detección precoz de IVA dentro el Programa de Cribado Neonatal de Enfermedades Endocrino-Metabólicas de la Comunidad de Madrid.
SUJETOS Y MÉTODOS
Los casos presentados proceden del Laboratorio de Cribado Neonatal de la Comunidad de Madrid, que incluye la detección precoz de 17 enfermedades de las cuales 13 son ECM (entre ellos la IVA) cuyos marcadores bioquímicos (aminoácidos, carnitina y acilcarnitinas) se cuantifican por MS/MS, y fueron recopilados desde octubre de 2011 hasta octubre de 2017.
La concentración de C5 y del resto de analitos se cuantificó utilizando el kit Neobase™ Non-Derivatized MSMS (Perkin Elmer®) en un equipo Acquity™ TDQ UPLC/MS (Waters®) en muestras de sangre seca impregnada en papel (Perkin Elmer® 226) y extraídas a las 48 horas de vida. Las muestras posteriores para seguimiento de los casos con resultados altos de C5 se extrajeron y procesaron en las mismas condiciones.
Como punto de corte se tomó el percentil 99.5 (P99.5); este punto de corte se revisa anualmente, variando entre 0.49 y 0.58 µmol/L en el periodo abarcado por este estudio. El perfil de acilcarnitinas obtenido mediante MS/MS de los niños con concentración elevada de C5 se comparó con el perfil de los casos de IVA diagnosticados e incluidos en el proyecto Region 4 Stork (www.clir-r4s.org). La aplicación informática desarrollada por este proyecto calcula la probabilidad de que un caso sospechoso padezca realmente la enfermedad, basándose en los valores de concentración de acilcarnitinas de casos con diagnóstico establecido de IVA14,15.
Coincidiendo con la realización de este trabajo, una paciente no gestante a la que se había prescrito un tratamiento con CFP se ofreció a participar en este estudio con objeto de analizar los niveles de C5 y estudiar la evolución de dichos niveles. Previa obtención de consentimiento informado, se le tomaron muestras en distintos días del tratamiento, así como antes y después de este. Para obtener las muestras de sangre capilar se emplearon las mismas lancetas y tarjetas de toma de muestra que las utilizadas en el programa de cribado neonatal. La concentración de C5 se midió con el mismo equipo que se utiliza para las muestras de cribado neonatal.
RESULTADOS
Durante los 6 años y 1 mes que abarcó este estudio se analizaron un total de 418.863 recién nacidos. En este periodo no se encontró ningún caso afecto de IVA. Sin embargo se detectaron 18 casos de elevación de C5 relacionados con madres gestantes tratadas con CFP. La concentración de C5 en sangre de estos neonatos varió entre 0.67 y 3.65 µmol/L (mediana 1.69 µmol/L), y un intervalo de concentraciones de C5 entre los percentiles 1 y 99 claramente mayor que el de la población de referencia del laboratorio (figura 1). Por el contrario se observó un gran solapamiento al compararla con la distribución en los casos diagnosticados incluidos en la base de datos del proyecto Region 4 Stork. Seis de los casos se enviaron a la unidad clínica de seguimiento para su evaluación, desde la cual se solicitaron pruebas que confirmaron el carácter de falso positivo por pivaloílcarnitina. En los doce casos restantes, al conocerse el tratamiento de la madre con CFP antes del parto, se hizo el seguimiento desde el propio laboratorio de cribado neonatal solicitando nuevas muestras en las que se confirmó la normalización del resultado una vez cesada la exposición del neonato al medicamento (figura 2). El tiempo requerido para que la concentración de C5 se normalizase en todos los casos, excepto en uno (C5 = 0.77 µmol/L a los 19 días de vida), fue de aproximadamente tres semanas.
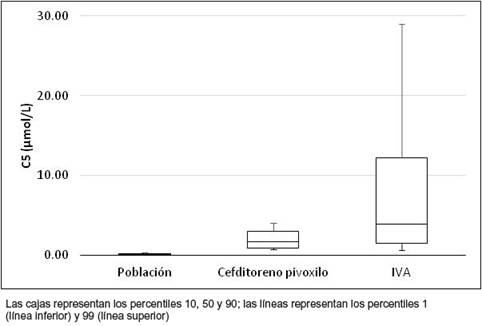
Figura 1 Distribución de concentraciones de C5 a las 48 horas de vida en población general de neonatos, hijos de madres tratadas con CFP al final de la gestación, y casos diagnosticados de IVA

Figura 2 Resultados de concentración de C5 en sangre seca en papel de neonatos cuyas madres fueron tratadas con CFP al final de la gestación
Respecto al efecto del pivalato sobre los depósitos de carnitina del organismo, solo en tres casos se obtuvo una concentración baja de carnitina a las 48 horas de vida, tomando como punto de corte el percentil 1 del laboratorio (6.03 µmol/L). La figura 3 muestra la comparación del intervalo de concentraciones de C0 entre los percentiles 1 y 99 de nuestra serie en comparación con la población de referencia y la de casos diagnosticados del Proyecto Region 4 Stork.
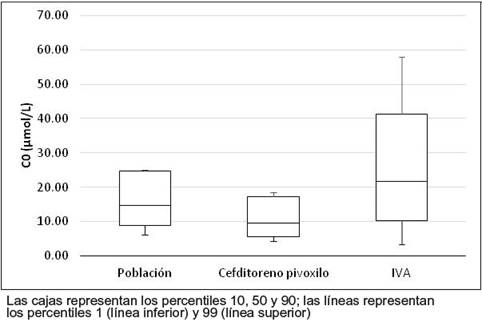
Figura 3 Distribución de concentraciones de C0 a las 48 horas de vida en población general de neonatos, hijos de madres tratadas con CFP al final de la gestación, y casos diagnosticados de IVA
Al comparar el perfil de acilcarnitinas de nuestros casos con los casos diagnosticados de IVA del proyecto Region 4 Stork (n = 309) se obtuvo un grado de sospecha de IVA muy probable (“most likely IVA”) en 9 casos; de IVA probable (“likely IVA”) en 5 casos; y de posible IVA o deficiencia de 2-metilbutiril-CoA deshidrogenasa (“likely either IVA or 2MBG”) en 4 casos.
La figura 4 muestra la evolución de la concentración de C5 en sangre a lo largo del tratamiento con CFP de la paciente no gestante a la que fue prescrito el antibiótico. A partir del nivel basal, cuya muestra se tomó momentos antes de iniciar el tratamiento, se aprecia una elevación del analito en sangre, alcanzando un valor máximo de 4.33 µmol/L. La administración de CFP finalizó el día 10, tras el cual se tomaron dos últimas muestras a los días 13 y 17 del comienzo del tratamiento observándose una normalización de los niveles de C5.
DISCUSIÓN
Los casos presentados, correspondientes a neonatos cuyas madres habían sido tratadas con CFP al final de la gestación, muestran una concentración de C5 en sangre superior al punto de corte para el cribado neonatal de IVA. La magnitud de esta elevación es variable, lo que se podría explicar por diferencias individuales en la eliminación del metabolito, porque a unas gestantes se les prescribiera una dosis menor que a otras (posología de 400 mg frente a 200 mg cada 12 horas), o por la finalización del tratamiento varios días antes del parto (dando más tiempo al organismo del neonato para eliminar el pivalato). Una vez cesada la exposición al CFP, se puede considerar que la concentración de C5 se normaliza aproximadamente a las tres semanas de vida. Esto es lo que hemos observado en todos los casos a los que se hizo un seguimiento desde nuestro laboratorio excepto en uno de ellos, que presentó una concentración aún elevada a los 19 días de vida. No obstante, aunque no disponemos de valores de referencia a dicha edad para la concentración de C5, el valor obtenido en este caso se debería considerar como una elevación leve (P99.5 = 0.60 µmol/L a la semana de vida, algo superior al P99.5 a las 48 horas de vida).
El resultado de la comparación con los casos diagnosticados de IVA incluidos en la base de datos del proyecto Region 4 Stork muestra una probabilidad variable (alta en la mitad de los casos) pero siempre informativa de padecer IVA en todos los casos presentados, lo que se confirma por el solapamiento entre la distribución de valores de concentración de C5 de nuestra serie y la de los casos diagnosticados. Los casos incluidos en esta base de datos proceden de programas de cribado neonatal de todo el mundo y constituyen una población heterogénea en cuanto a edad, procedimiento analítico, punto de corte de cribado y criterios diagnósticos; no obstante, dada la baja prevalencia de la enfermedad3, esta fuente es actualmente la más completa para comparar casos.
En humanos, la eliminación del ácido piválico se produce mediante su excreción en orina tras conjugación con carnitina13. Se ha descrito en varias ocasiones una reducción de la concentración sanguínea de carnitina asociada a tratamiento con profármacos formados por ésteres de ácido piválico16,17,18,19,20,21. Algunos autores han relacionado además esta deficiencia secundaria de carnitina con manifestaciones clínicas, principalmente encefalopatía asociada a hipoglucemia22,23, si bien no se han observado manifestaciones en todos los casos de hipocarnitinemia24. En nuestra serie, la concentración de carnitina en la muestra extraída a las 48 horas de vida solo fue baja en 3 de los 18 casos, siendo la distribución de este analito similar a la de la población general de neonatos, por lo que no parece que este analito sea un buen marcador de elevación de C5 por acumulación de pivalato.
Los tres casos con concentración baja de carnitina presentaron valores intermedios de C5 dentro de la serie, por lo que parece no haber una correlación entre la concentración de C5 y la deficiencia de carnitina secundaria al tratamiento. Aunque no disponemos de información sobre la duración de la exposición de los niños al medicamento, no parece probable que estas diferencias en la concentracion de carnitina se puedan explicar porque la exposición fuera más o menos prolongada. En este sentido, Kobayashi y cols., no encontraron una correlación entre la duración de la exposición y la concentración de carnitina, si bien su serie de casos es muy heterogénea, y la información de que disponían incompleta24. La carnitina es un producto que se sintetiza por el organismo, aunque durante la infancia podría haber una dependencia mayor de su ingesta con la dieta probablemente debido a una inmadurez en su ruta sintética25. Teniendo esto en cuenta, la diferencia observada en las concentraciones de carnitina se podría explicar por una distinta disponibilidad dietética y, en menor medida, por factores individuales relacionados con la biosíntesis de carnitina.
Los resultados de la paciente no gestante tratada con CFP muestran una elevación de la concentración de C5. Este efecto ya se había descrito previamente para este profármaco por otros autores24. A pesar de haber sido tratada con dosis bajas (200 mg cada 12 horas), las concentraciones alcanzadas pocos días después de empezar el tratamiento son similares a las más altas obtenidas en los casos de nuestra serie. Estos altos niveles de C5, obtenidos a pesar de las bajas dosis administradas (200 mg/12 horas), se podrían deber a que el pivalato o el profármaco tengan unas propiedades farmacocinéticas diferentes en el caso de las gestantes, o, más probablemente, a que el cese de aporte de pivalato a los neonatos por parte de la madre tras el parto haga que disminuya la concentración de C5.
Los resultados obtenidos en este estudio no permiten sacar conclusiones sobre si el tratamiento afecta de forma similar a la concentración de C5 de todos los neonatos con madres tratadas con CFP, ni sobre sus posibles implicaciones clínicas. Es posible que neonatos cuyas madres fueron tratadas al final de la gestación no den valores altos de C5. No obstante, esta serie de casos muestra que el CFP se prescribe a mujeres gestantes, y que su administración al final de la gestación a dosis terapéuticas puede provocar una elevación de la concentración de C5 en muestras de sangre seca impregnada en papel para el cribado neonatal de ECM. Estos datos se deben tener en cuenta en el ámbito clínico, especialmente por obstetras y médicos de Atención Primaria, a la hora de escoger entre distintas alternativas terapéuticas para el tratamiento de infecciones en gestantes, y en los laboratorios de cribado neonatal al interpretar resultados con elevacion de C5. Dada la gravedad que puede representar esta enfermedad, un resultado positivo en el cribado sin infomación sobre la historia clínica de la madre, obligaría a movilizar inmediatamente a la familia y a la unidad clínica de referencia para hacer el seguimiento del caso. Debido a la angustia que puede generar un caso positivo de cribado neonatal en las familias tras un reciente alumbramiento26,27,28, es importante que el prescriptor del tratamiento con CFP informe a las gestantes de que se pueden obtener resultados positivos o dudosos en el cribado neonatal de ECM de su hijo, y que se alerte al laboratorio de una posible interferencia en los resultados del cribado.















