Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Anales del Sistema Sanitario de Navarra
versão impressa ISSN 1137-6627
Anales Sis San Navarra vol.38 no.2 Pamplona Mai./Ago. 2015
https://dx.doi.org/10.4321/S1137-66272015000200003
ARTÍCULOS ORIGINALES
Calidad de vida de pacientes con cáncer de próstata en tratamiento con bloqueo androgénico continuo vs intermitente. Estudio prospectivo mediante la aplicación del cuestionario CAVIPRES
Quality of life in patients diagnosed of prostate cancer treated with continuous androgen deprivation therapy vs. intermittent therapy. Prospective study through the application of the CAVIPRES questionnaire
C.R. Sierra Labarta, D. Sánchez Zalabardo y Á. de Pablo Cárdenas
Hospital Reina Sofía. Tudela. Navarra
Dirección para correspondencia
RESUMEN
Fundamento: El tratamiento con bloqueo androgénico intermitente (BAI) pretende mejorar la calidad de vida de los pacientes con cáncer de próstata con los mismos resultados oncológicos que el bloqueo androgénico continuo (BAC). El presente trabajo compara la calidad de vida mediante la aplicación del cuestionario CAVIPRES entre dos grupos de pacientes, uno tratado con BAC y otro con BAI.
Material y métodos: Se realizó un estudio longitudinal de 24 meses de duración que incluyó 114 pacientes. Tras 6 meses se aleatorizaron a ambos grupos de tratamiento (49 pacientes a BAC y 51 a BAI), controlándose posteriormente a los 6, 12 y 18 meses de aleatorizarlos. Se comparó la puntuación de los bloques de ítems y la puntuación global del cuestionario CAVIPRES entre ambos grupos de tratamiento y se estudió su variación a lo largo del tiempo.
Resultados: Los pacientes con BAI presentaron mejor calidad de vida global que los pacientes con BAC (p=0,002). De los 5 bloques en los que se divide el cuestionario, el grupo BAI presentó mejor puntuación que el BAC en "Aspectos psicológicos" (p=0,009) y "Apoyo social y pareja" (p=0,008). El BAI mejoró la calidad de vida global de los pacientes a los 18 meses respecto al momento de la aleatorización (p=0,000), y la puntuación de "Vida Sexual" (p=0,000) y "Apoyo social y pareja" (p=0,002). El BAC no mejoró ni la calidad de vida global ni la puntuación de los diferentes bloques a largo del estudio (p>0,05).
Conclusión: El BAI mejora la calidad de vida global de los pacientes a los 18 meses de la suspensión del tratamiento.
Palabras clave: Calidad de vida. Cáncer de próstata. Bloqueo androgénico intermitente.
ABSTRACT
Background: Treatment with intermittent androgen deprivation (IAD) seeks to improve the quality of life of patients with prostate cancer, with the same oncologic results as continuous androgen deprivation (CAD). The aim of this paper is to compare, using the CAVIPRES questionnaire, the quality of life between two groups of patients, one treated with CAD and the other with IAD.
Materials and methods: A longitudinal study was performed for 24 months involving 114 patients. After 6 months, patients were randomized to two treatment groups (49 patients in CAD and 51 patients in IAD), controlled at 6, 12 and 18 months from randomisation. The score of the items and the overall score of the CAVIPRES questionnaire between the two groups was compared and their variation over time was studied.
Results: Patients with IAD had a better overall score than patients with CAD (p=0.002). Of the 5 blocks of items into which the questionnaire was divided, the IAD group had a better score than CAD in "Psychological aspects" (p=0.009) and "Social and partner support" (p=0.008). At 18 months, IAD improved the overall quality of life of patients relative to the time of randomization (p=0.000), as well as the score for "Sexual Life" (p=0.000) and "Social and partner support" (p=0.002). CAD did not improve overall quality of life or the score for the different blocks throughout the study (p>0.05).
Conclusions: IAD improves overall quality of life of patients at 18 months of stopping treatment.
Keywords: Quality of life. Prostate cancer. Intermittent androgen deprivation.
Introducción
La Organización Mundial de Salud (OMS) en 1948 definió el concepto de salud como un estado de completo bienestar físico, psíquico y social y no meramente la ausencia de enfermedad1. Posteriormente, en 1994, definió la calidad de vida como la percepción individual de la posición en la vida en el contexto de la cultura y sistema de valores en el cual se vive y su relación con las metas, expectativas, estándares e intereses. El concepto de calidad de vida es muy relativo, siendo influenciado por lo histórico, cultural y la clase social a la que se pertenece y aunque remite en última instancia al plano individual, a cómo el individuo se siente y se ve a sí mismo, su percepción varía por dichas influencias2.
El cáncer de próstata y su tratamiento afecta de forma general a la calidad de vida relacionada con la salud, así como a la salud urinaria, sexual y digestiva de los pacientes, quienes además se enfrentarán a cambios de perspectiva relacionados con su esperanza de vida, integridad corporal y relaciones personales3,4.
El bloqueo androgénico intermitente (BAI) se basa en periodos alternantes de tratamiento con otros de cese del mismo. Estos periodos de ausencia de tratamiento permitirían disminuir los efectos secundarios no deseados y retrasar la progresión a la etapa final de la historia natural del cáncer de próstata, la resistencia a la castración. Su objetivo final es mejorar la calidad de vida con, al menos, los mismos resultados oncológicos que el bloqueo androgénico continuo (BAC) sin resultados adversos sobre la supervivencia5,6, beneficiando al paciente principalmente en 3 aspectos: 1) Posibilidad de recuperar la función sexual durante el periodo libre de tratamiento al restaurarse los niveles de testosterona y al disminuir la morbilidad de origen cardiovascular y osteoporótica, que contribuiría a una recuperación de los síntomas; 2) Disminuir gastos; 3) Seguir el mismo control oncológico que el BAC7.
En este contexto, creemos necesario estudiar si en nuestro medio el BAI aporta uno de los tres beneficios por los que se comenzó a utilizar, como es la mejoría de la calidad de vida.
En la actualidad disponemos de instrumentos de medición de la calidad de vida relacionada con la salud, los cuales deben combinar una serie de características que les den solidez conceptual, confiabilidad y validez, siendo fundamental que sean relevantes culturalmente8.
El Cuestionario Español de Calidad de Vida en Pacientes con Cáncer de Próstata (CAVIPRES), desarrollado y validado por el "Grupo de Trabajo en Calidad de Vida en Cáncer de Próstata" en más de 1.200 pacientes españoles y en lenguaje español, constituye en la actualidad una herramienta manejable, fiable, sensible y específica para evaluar la calidad de vida de los pacientes con cáncer de próstata en España, basado en la percepción del propio paciente9.
El cuestionario CAVIPRES analiza 5 dominios distintos: aspectos psicológicos (ítems del 1 al 8), esperanza y futuro (ítems del 9 al 12), vida sexual (ítems del 13 al 18), apoyo social y pareja (ítems del 19 al 24) e información y comunicación (ítems del 25 al 30).
Cada pregunta o ítem tiene opciones de respuesta en escala tipo Likert de 5 puntos (1 = siempre; 5= nunca). A mayor puntuación, mejor calidad de vida relacionada con la salud referida por el paciente con cáncer de próstata, siendo la mayor puntuación 150 puntos.
Los valores de referencia del cuestionario CAVIPRES para la calidad de vida relacionada con la salud respecto a la puntuación global del cuestionario CAVIPRES se estratifican en los siguientes grupos: muy mala (30-54 puntos), mala (55-78 puntos), regular (79-102 puntos), buena (103-126 puntos) y muy buena (127-150 puntos)10.
El presente trabajo compara la calidad de vida y estudia la variación de la misma a lo largo del tiempo mediante la aplicación del cuestionario CAVIPRES en dos grupos de pacientes: uno tratado con bloqueo androgénico continuo (BAC) y otro con bloqueo androgénico intermitente (BAI).
Material y métodos
Se realizó un estudio experimental aleatorizado, longitudinal y prospectivo de 24 meses de duración en el Hospital Reina Sofía de Tudela (Navarra) en el que se comparó la calidad de vida en ambos grupos de pacientes.
Al diagnóstico de cáncer de próstata, todos los pacientes recibieron tratamiento con un antiandrógeno 15 días más un análogo de LHRH semestral y posteriormente se revisó a todos los pacientes a los 6 meses, momento en el que se aleatorizaban a uno de los dos grupos de tratamiento. Las siguientes revisiones se programaron a los 6, 12 y 18 meses de la aleatorización. En cada uno de estos momentos de control, los pacientes cumplimentaban de forma individual el cuestionario español de calidad de vida en pacientes con cáncer de próstata CAVIPRES (Fig. 1).
Criterios de inclusión: pacientes diagnosticados clínica o histológicamente de cáncer de próstata que recibieron bloqueo androgénico como único tratamiento. En el caso de inclusión en el grupo BAI, se incluyeron en este grupo a aquellos pacientes que presentaban un descenso de PSA por debajo de 4 ng/ml en el momento de la aleatorización (posteriormente, si en el seguimiento el PSA ascendía por encima de 20 ng/ml, se reintroducía el tratamiento para volverlo a suspender si bajaba de 4 ng/ml. Ningún paciente requirió la reintroducción del tratamiento).
Criterios de exclusión: se excluyeron a los pacientes que no reunían los criterios de inclusión, a los mayores de 85 años, a los sometidos a otros tratamientos de cáncer de próstata (prostatectomía radical, radioterapia...) y a los pacientes que presentaron progresión de la enfermedad y precisaron tratamientos para la resistencia a la castración a lo largo del estudio.
Se incluyeron en el estudio 114 pacientes diagnosticados de cáncer de próstata que iniciaron bloqueo androgénico. A todos ellos se les informó del estudio y firmaron un consentimiento informado, previa autorización del comité ético de nuestro hospital.
En el momento de la aleatorización la distribución de los pacientes fue de 49 en el grupo BAC y 51 en el BAI. A los 6 meses de la misma había 47 pacientes en BAC y 49 en BAI. A los 12 meses, el número de pacientes era de 47 en BAC y 48 en BAI. A los 18 meses de la aleatorización, el recuento era de 91 pacientes, estando 44 en el grupo BAC y 47 en BAI. La pérdida de pacientes a lo largo del estudio se debió a diversos motivos como el no complimiento de la revisión pautada, la progresión de la enfermedad, la realización de cirugía desobstructiva prostática o al fallecimiento (Fig. 2).
Respecto a las características de la población estudiada al inicio del estudio, la edad media de los pacientes fue de 77,9 años, y el IMC de 28,54 kg/m2. La media de PSA de 168,1 ng/ml (mediana 22,58 ng/ml). El Gleason Score mayoritario fue Gleason <6 (43,9%), seguido del Gleason 7 (31,7%) y Gleason >8 (24,4%). En cuanto a la clasificación TNM, predominó el T2 (35,1%) seguido de T3 (31,3%), T1 (26,3%) y T4 (7%), el N0 (87,7%) y el M0 (84,2%). Los valores medios de los parámetros analíticos de hemograma y bioquímica se encontraba dentro de rangos de normalidad.
El tamaño de la muestra se realizó con el programa de Análisis Epidemiológico de Datos EPIDAT 4.0, siendo el valor mínimo de pacientes 92 (46 por grupo de tratamiento) para obtener un nivel de confianza del 95% (p=0,05). Se siguió un método de aleatorización estratificada para la distribución de los pacientes, siguiendo un criterio de edad (mayor o menor de 79 años) e índice de masa corporal (mayor o menor de 29), tras el cual, en cada grupo de estratificación, se realizó una estratificación simple mediante un programa informático en función del número final de la historia clínica. Para el análisis estadístico se utilizó el programa SPSS Statistics, versión 22, utilizando la prueba t de Student para muestras apareadas y para muestras independientes en el estudio de variables cuantitativas y cálculo de comparación de medias. Para el estudio de variables cualitativas se utilizó la prueba del Chi-cuadrado.
Resultados
En el momento de la aleatorización, cuando todos los pacientes habían recibido el tratamiento con análogo LHRH semestral, nos encontramos dos grupos de pacientes sin diferencias estadísticamente significativas en sus parámetros antropométricos ni analíticos, ni en el resultado global del cuestionario CAVIPRES. Sólo se apreciaban diferencias significativas en el bloque de ítems "Vida sexual", siendo la mayor puntuación para el grupo que recibiría BAC (11,37 puntos) respecto al que recibiría BAI (8,57 puntos), p=0,006 (Tabla 1).
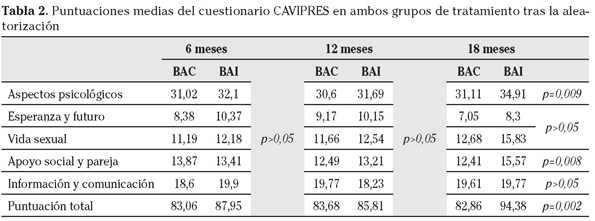
La puntuación global del cuestionario CAVIPRES, así como la puntuación media de cada uno de los bloques por grupo de tratamiento a lo largo del estudio, se recoge en la tabla 2.
A los 18 meses de la aleatorización el resultado global del cuestionario CAVIPRES es mayor en el grupo de tratamiento BAI (82,86 puntos BAC y 94,38 puntos BAI), y en los bloques "Aspectos psicológicos" (31,11 y 34,91 puntos para BAC y BAI respectivamente) y "Apoyo social y pareja" (12,41 puntos BAC y 15,57 puntos BAI), siendo estas diferencias estadísticamente significativas (p=0,002, p=0,009 y p=0,008 respectivamente).
En el resto de los dominios del cuestionario CAVIPRES no se observaron diferencias estadísticamente significativas.
Al analizar la evolución temporal del cuestionario CAVIPRES desde la aleatorización al final del estudio (Tabla 3) se observa que en el grupo que recibió BAC, no hay diferencias estadísticamente significativas en la puntuación global del cuestionario ni en ninguno de los bloques de ítems a lo largo del tiempo. En el grupo que recibió BAI, la puntuación global en el momento de la aleatorización fue de 80,29 puntos y al final del estudio se incrementó a 94,38 puntos (p=0,000). A los 18 meses en el bloque "Vida sexual" hay un incremento de la puntuación de 8,57 puntos a 15,83 desde la aleatorización, siendo esta diferencia estadísticamente significativa (p=0,000). Así mismo, el bloque "Apoyo social y pareja" presenta un aumento de puntuación media de 11,67 en la aleatorización a 15,57 puntos a los 18 meses (p=0,002).
No se encontraron diferencias estadísticamente significativas en el resto de los bloques estudiados.
Discusión
La prevalencia de cáncer de próstata unido al aumento de la edad media de la población y la mejora en los tratamientos, permiten a estos pacientes una supervivencia relativamente alta y obligan a plantearse la calidad de vida que van a presentar en el periodo que convivan con su enfermedad, ya que ésta se va a ver afectada tanto por la carga emocional como por los efectos de los tratamientos y las alteraciones funcionales secundarias a los mismos y a la propia enfermedad11. A ello se le une la tendencia actual de incorporar la opinión y la percepción de la enfermedad del paciente en la toma de decisiones clínicas12.
Para evaluar la calidad de vida en pacientes diagnosticados de cáncer de próstata se dispone de cuestionarios específicos elaborados en EEUU, Canadá e Inglaterra, como PROSQOLI, FACT-P, EORTC-QLQ-PR25, QOLM-P14, UCLA-PCI, EPIC entre otros, siendo tan solo el CAVIPRES desarrollado y validado en España13-20.
Dada la variabilidad de instrumentos que miden la calidad de vida en pacientes con cáncer de próstata, es importante la creación de instrumentos de medición lo más homogéneos posible21. Así mismo, no se dispone de un método común para interpretar resultados, por lo que la mayor parte de la veces esa interpretación se deja a la significación estadística, no siempre bien correlacionada con la significación clínica22.
Se escogió para el análisis de los pacientes el cuestionario de vida CAVIPRES por ser un cuestionario desarrollado y validado en nuestro país, disponible en la Asociación Española de Urología, y con las mismas garantías de manejabilidad, fiabilidad, sensibilidad y especificidad para evaluar la calidad de vida referida por los pacientes que otros cuestionarios9,23.
Aspectos como si el paciente tenía o no pareja estable, si tomaba tratamientos sintomáticos o presentaba comorbilidades limitantes de la vida diaria no fueron analizados, así como tampoco se diferenció entre aquellos pacientes que eran metastásicos o no, centrándose el estudio en la comparación de la calidad de vida solo influenciada por el tipo de tratamiento recibido.
En lo referente a la duración de los ciclos de intermitencia en el BAI, ninguno de los pacientes de nuestro estudio requirió reintroducción de tratamiento en los 18 meses posteriores a la aleatorización, debido a que no fue superado el valor umbral de PSA de 20 ng/ml. El valor de PSA tras un periodo inicial de 6 meses de tratamiento con bloqueo androgénico es un factor pronóstico significativo en relación a la supervivencia independientemente del tipo de bloqueo empleado, continuo o intermitente. Así valores menores de 0,2, y menores y mayores de 4 ng/ml se han relacionado con una supervivencia global de 74, 44 y 13 meses respectivamente24,25. Existe una gran heterogeneidad en las publicaciones entre el tiempo del periodo de on/off del bloqueo androgénico intermitente, siendo la fase libre de tratamiento más larga en aquellas provenientes de Estados Unidos y más corta en las europeas26. Así en el estudio metodológico más importante realizado (que utiliza criterios similares de valor de PSA de suspensión y reintroducción de tratamiento que el nuestro), el estudio SEUG de Calais da Silva y col describe periodos de 70 semanas de ausencia de tratamiento en el periodo "off" del bloqueo androgénico intermitente (para valores límite de 10 ng/ml en pacientes sintomáticos o 20 ng/ml en los no sintomáticos)27.
Numerosos estudios apoyan la mejora de la calidad de vida referida por el paciente en el periodo de intermitencia del bloqueo androgénico28-30, coincidiendo con nuestros resultados. Entre ellos, el de Spry y col28, que escogió para medir la calidad de vida en 250 pacientes divididos en un grupo de bloqueo androgénico intermitente y otro grupo de bloqueo continuo, el cuestionario EORTC-C30, cuestionario de calidad de vida global para pacientes oncológicos que explora mediante 30 preguntas, aspectos relacionados con el funcionamiento físico, actividades cotidianas, funcionamiento emocional, funcionamiento cognitivo y funcionamiento social ampliado con el módulo específico de cáncer de próstata EORTC-QLQ-PR25, aplicado por un periodo de 3 años y observando que, hay una mejora progresiva de la calidad de vida en relación con la recuperación de la testosterona, recuperación más lenta que el deterioro de la calidad de vida que se experimenta al introducir el tratamiento.
El estudio de Calais da Silva y col27, que utiliza los mismos cuestionarios de valoración de la calidad de vida que el anterior en 626 pacientes divididos en los dos grupos de tratamiento durante 3 años aunque con un periodo de inducción de tratamiento de 3 meses, no encontró diferencias significativas entre ambos grupos en lo referente a la calidad de vida, pero concluyó que el bloqueo androgénico intermitente no está relacionado con un deterioro clínicamente significativo de la calidad de vida, mejorando efectos secundarios tales como los sofocos y la ginecomastia, y hallando diferencias estadísticamente significativas relacionadas con la calidad de la vida sexual.
Abrahamsson29 realizó una revisión extensa y sistemática de publicaciones en la que hace referencia a los beneficios en la calidad de vida de los pacientes en tratamiento con bloqueo androgénico intermitente, especialmente en lo referente a la recuperación de la potencia sexual.
Buchan y Goldenberg30 realizaron otra revisión en la que también se aprecian mejoras significativas de la calidad de vida y sobre todo de la calidad sexual, en los periodos sin tratamiento del bloqueo androgénico intermitente.
En nuestro estudio, el resultado en cuanto a grupo de tratamiento de la calidad de vida objetivada por el cuestionario CAVIPRES al final del tratamiento, nos indica que "Aspectos psicológicos", "Apoyo social y pareja" y "Puntuación global" del cuestionario tienen una puntuación significativamente más elevada en el grupo de bloqueo androgénico intermitente que en el grupo de bloqueo continuo.
Así mismo, a lo largo de la evolución de los pacientes en bloqueo androgénico continuo (desde el momento de la aleatorización hasta el final del estudio a los 18 meses), no se observan diferencias significativas en cuanto a los resultados del cuestionario CAVIPRES. Sin embargo, en el grupo intermitente se observa al final del estudio aumentos significativos en la puntuación de los bloques "Vida sexual", "Apoyo social y pareja" y sobre todo en "Puntuación global" con respecto al momento de la aleatorización.
El tratamiento del cáncer de próstata mediante BAI mejora la calidad de vida global percibida por los pacientes y medida con el cuestionario de calidad de vida CAVIPRES con respecto a los pacientes tratados con BAC a los 18 meses de la suspensión del tratamiento. Así mismo, en los pacientes tratados con BAI existe una mejoría evolutiva de la calidad de vida global percibida por los pacientes desde el momento de la aleatorización hasta los 18 meses de la suspensión del tratamiento.
Bibliografía
1. Constitution of the World Health Organization. Am J Public Health Nations Health 1946; 36: 1315-1323. [ Links ]
2. Minayo MC, Hartz ZM, Buss P. Quality of life and Health: a necessary debate. Ciencia & Saúde Coletiva ABRASCO 2000; 1: 7-18. [ Links ]
3. Ptacek JT, Fries EA, Eberhardt TL, Ptacek JJ. Breaking bad news to patients: physicians' perceptions of the process. Support Care Cancer 1999; 7: 113-120. [ Links ]
4. Barceló Obrador A, Ramos M, De La Iglesia M, Zaforteza M. Tratamiento del cáncer de próstata en función de la esperanza de vida, la comorbilidad y las guías de práctica clínica. An Sis Sanit Navar 2014; 37: 339-348. [ Links ]
5. Oliver RT, Williams G, Paris AM, Blandy JP. Intermittent androgen deprivation after PSA-complete response as a strategy to reduce induction of hormone-resistant prostate cancer. Urology 1997; 49: 79-82. [ Links ]
6. Bhandari MS, Crook J, Hussain M. Should intermittent androgen deprivation be used in routine clinical practice? J Clin Oncol 2005; 23: 8212-8218. [ Links ]
7. López JD, López-Fontana G, López-Fontana R. Evidencia actual acerca de bloqueo hormonal intermitente en cáncer de próstata. Actas Urol Esp 2012; 36: 608-612. [ Links ]
8. Schwartzmann L. Calidad de vida relacionada con la salud: aspectos conceptuales. Cienc enferm (online). 2003; 9: 9-21. [ Links ]
9. Gómez-Veiga F, Cozar-Olmo JM, Günthner S, Puyol-Pallas M, Silmi-Moyano A, Baró-Ramos E, et al. Desarrollo y validación del primer cuestionario español de calidad de vida en pacientes con cáncer de próstata, basado en la percepción del paciente. Actas Urol Esp 2009; 33: 623-634. [ Links ]
10. Gómez-Veiga F, Silmi-Moyano A, Günthner S, Puyol-Pallas M, Cozar-Olmo JM. Valores de referencia para el cuestionario CAVIPRES-30, un cuestionario global sobre la calidad de vida relacionada con la salud de pacientes con cáncer de próstata. Actas Urol Esp 2014; 38: 304-312. [ Links ]
11. Gomella LG, Johannes J, Trabulsi EJ. Current prostate cancer treatments: effect on quality of life. Urology 2009; 73 (5 Suppl): S28-35. [ Links ]
12. Husson O, Mols F, Van De Poll-Franse LV. The relation between information provision and health-related quality of life, anxiety and depression among cancer survivors: A systematic review. Ann Oncol 2011; 22: 761-772. [ Links ]
13. Esper P, Mo F, Chodak G, Sinner M, Cella D, Pienta KJ. Measuring quality of life in men with prostate cancer using the functional assessment of cancer therapy-prostate instrument. Urology 1997; 50: 920-928. [ Links ]
14. Van Andel G, Bottomley A, Fossa SD, Efficace F, Coens C, Guerif S, et al. An international field study of the EORTC QLQ-PR25: a questionnaire for assessing the health-related quality of life of patients with prostate cancer. Eur J Cancer 2008; 44: 2418-2424. [ Links ]
15. Litwin MS. Measuring health related quality of life in men with prostate cancer. J Urol 1994; 152 (5 Pt 2): 1882-1887. [ Links ]
16. Hays RD, Sherbourne CD, Mazel RM. The RAND 36-Item Health Survey 1.0. Health Econ 1993; 2: 217-227. [ Links ]
17. Wei JT, Dunn RL, Litwin MS, Sandler HM, Sanda MG. Development and validation of the expanded prostate cancer index composite (EPIC) for comprehensive assessment of health-related quality of life in men with prostate cancer. Urology 2000; 56: 899-905. [ Links ]
18. Tannock IF, Osoba D, Stockler MR, Ernst DS, Neville AJ, Moore MJ, et al. Chemotherapy with mitoxantrone plus prednisone or prednisone alone for symptomatic hormone-resistant prostate cancer: a Canadian randomized trial with palliative end points. J Clin Oncol 1996; 14: 1756-1764. [ Links ]
19. Osoba D, Tannock IF, Ernst DS, Neville AJ. Health-related quality of life in men with metastatic prostate cancer treated with prednisone alone or mitoxantrone and prednisone. J Clin Oncol 1999; 17: 1654-1663. [ Links ]
20. Ferrer M, Garín O, Pera J, Prats JM, Mendivil J, Alonso J, et al. Evaluación de la calidad de vida de los pacientes con cáncer de próstata localizado: validación de la versión española del cuestionario EPIC. Med Clin (Barc) 2009; 132: 128-135. [ Links ]
21. Parker WR, Montgomery JS, Wood DP, Jr. Quality of life outcomes following treatment for localized prostate cancer: is there a clear winner? Curr Opin Urol 2009; 19: 303-308. [ Links ]
22. Cocks K, King MT, Velikova G, Fayers PM, Brown JM. Quality, interpretation and presentation of European Organisation for Research and Treatment of Cancer quality of life questionnaire core 30 data in randomised controlled trials. Eur J Cancer 2008; 44: 1793-1798. [ Links ]
23. Gómez-Veiga F, Cozar JM, Günthner S, Puyol-Pallas M, Silmi-Moyano A, Rebollo FJ. Cuestionario Español de Calidad de Vida en Pacientes con Cáncer de Próstata como medida de la calidad de vida de los pacientes con cáncer de próstata en España: aplicación a la actividad diaria. Actas Urol Esp 2010; 34: 686-693. [ Links ]
24. Hussain M, Tangen CM, Higano C, Schelhammer PF, Faulkner J, Crawford ED, et al. Absolute prostate-specific antigen value after androgen deprivation is a strong independent predictor of survival in new metastatic prostate cancer: data from Southwest Oncology Group Trial 9346 (INT-0162). J Clin Oncol 2006; 24: 3984-3990. [ Links ]
25. Moul JW, Wu H, Sun L, Mcleod DG, Amling C, Donahue T, et al. Early versus delayed hormonal therapy for prostate specific antigen only recurrence of prostate cancer after radical prostatectomy. J Urol 2008; 179 (5 Suppl): S53-59. [ Links ]
26. Prapotnich D, Sanchez-Salas R, Cathelineau X, Stakhovskyi O, Rocha JE, Jr, Vallancien G. Bloqueo androgénico intermitente (BAI) en cáncer de próstata avanzado. ¿Por qué no el tratamiento estándar? Arch Esp Urol 2009; 62: 689-694. [ Links ]
27. Calais Da Silva FE, Bono AV, Whelan P, Brausi M, Marques Queimadelos A, Martin JA, et al. Intermittent androgen deprivation for locally advanced and metastatic prostate cancer: results from a randomised phase 3 study of the South European Uroncological Group. Eur Urol 2009; 55: 1269-1277. [ Links ]
28. Spry NA, Kristjanson L, Hooton B, Hayden L, Neerhut G, Gurney H, et al. Adverse effects to quality of life arising from treatment can recover with intermittent androgen suppression in men with prostate cancer. Eur J Cancer 2006; 42: 1083-1092. [ Links ]
29. Abrahamsson PA. Potential benefits of intermittent androgen suppression therapy in the treatment of prostate cancer: a systematic review of the literature. Eur Urol 2010; 57: 49-59. [ Links ]
30. Buchan NC, Goldenberg SL. Intermittent versus continuous androgen suppression therapy: do we have consensus yet? Curr Oncol 2010; 17 Suppl 2: S45-48. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Carmen Rocío Sierra Labarta
Hospital Reina Sofía
Carretera de Tarazona km 3
31500 Tudela (Navarra)
E-mail: roc.sierra@gmail.com
Recepción: 26 de diciembre de 2014
Aceptación provisional: 2 de marzo de 2015
Aceptación definitiva: 17 de marzo de 2015