INTRODUCCIÓN
La tuberculosis (TBC) es una enfermedad infectocontagiosa causada por micobacterias del complejo Mycobacterium tuberculosis, frecuentemente M. tuberculosis, M. africanum, M. microti, M. bovis y el bacilo de Calmette - Guérin o BCG. Aunque la TBC se transmite habitualmente por vía aérea, también puede hacerlo por vía cutánea-mucosa1; esta inoculación de micobacterias vía dérmica es forma poco frecuente, pero ocurre en ocasiones en profesionales sanitarios en contacto con pacientes con TBC o sus muestras biológicas contaminadas, tras punción accidental con aguja hueca.
Se presenta el caso de una mujer, técnico especialista de laboratorio, que sufrió un accidente de trabajo con riesgo biológico tras pinchazo accidental en el segundo dedo de la mano derecha con aguja hueca utilizada en la muestra de hemocultivo de un paciente con TBC. Veinticinco años antes la trabajadora había completado seis meses de tratamiento de infección latente tuberculosa (TILT) tras un primer accidente, y actualmente estaba en tratamiento con corticoesteroides por polimialgia reumática. Este caso ilustra la necesidad de documentar el accidente, la fuente de exposición y el estado inmunitario del trabajador, indicando el tipo de profilaxis y el seguimiento adecuado del accidente, teniendo en cuenta la duración prolongada de la profilaxis de TBC y los posibles efectos secundarios de los fármacos empleados.
CASO CLÍNICO
Mujer de 57 años, Técnico Especialista de Laboratorio en el Servicio de Microbiología con antecedentes personales de polimialgia reumática en tratamiento crónico con corticoesteroides, En el año 1996 mostró un Mantoux de 20 mm tras pinchazo accidental con muestra de paciente TBC y completó seis meses de TILT. En los controles realizados en 2017 y 2020 con QuantiFERON® TB Gold in-tube (QFT-GIT) dio resultado negativo. A mediados de marzo de 2021 volvió a sufrir accidente de trabajo con riesgo biológico tras pinchazo accidental en el segundo dedo de la mano derecha con aguja hueca (Fig. 1A) utilizada para puncionar el frasco de hemocultivo de un paciente con TBC.
Tras la exposición vía sanguínea, se aplicaron las medidas inmediatas sobre la herida establecidas en el protocolo de actuación frente a riesgo biológico. Posteriormente la trabajadora contactó con el Servicio de Prevención de Riesgos Laborales (SPRL) donde se realizó valoración inicial del riesgo de infección. La paciente inició profiláctico con emtricitabina, tenofovir y raltegravir (prevención post exposición a VIH), cuya duración fue de cinco días hasta que se localizó al paciente fuente del que se obtuvo muestra sanguínea para análisis serológicos de virus de la inmunodeficiencia humana (VIH), virus de la hepatitis B (VHB) y virus de la hepatitis C (VHC), cuyos resultados fueron negativos.
El accidente con riesgo biológico fue notificado a través del formulario on-line (Anexo B) según lo establecido en el procedimiento de notificación e investigación de sucesos del SPRL en el cumplimiento de la Ley de Prevencion de Riesgos Laborales 31/1995, de 8 de noviembre.
Se le realizó seguimiento con determinación del QFT-GIT a finales de abril de 2021 con resultado positivo. Presentó zona eritematosa con pequeña erosión en la punta del dedo índice de la mano derecha (Fig. 1B) y dudosa pequeña adenopatía superior en epitróclea del brazo derecho.

Figura 1. A. Objeto punzante causante del accidente. B. Lesión cutánea en el segundo dedo de la mano derecha tras pinchazo accidental.
Se le derivó al Servicio de Dermatología donde se le realizaron biopsia tipo punch, biopsia por aspiración con aguja gruesa (BAAG), y tru-cut de piel lesionada que fueron enviadas al servicio de Anatomía Patológica para estudio de posible inoculación de bacilos tuberculosos. Se diagnosticó como inflamación granulomatosa necrotizante-caseificante compatible con TBC cutánea. La PCR de TBC efectuada a petición del dermatólogo dio resultado positivo. Se extrajo ADN del tejido parafinado de la biopsia mediante el kit QIAamp DNA FFPE tissue kit (Qiagen, Alemania), para realizar la detección molecular cualitativa del complejo de M. tuberculosis (MTB), con técnica de High-Resolution Melting mediante el kit FluoroType® MTB (Hain Lifescience, Nehren, Alemania) en el equipo FluoroCycler® 12 (Hain Lifescience). La sensibilidad y especificidad de detección del kit en tejido parafinado es 60,0% y 71,4% 2, respectivamente, y dependen de la cantidad de bacilos presentes en la muestra. Se envió un fragmento de biopsia al servicio de Microbiología para el aislamiento del agente del cuadro clínico mediante los cultivos correspondientes y la realización de pruebas de sensibilidad antimicrobiana. Se detectó crecimiento de M. tuberculosis y no se observaron resistencias antimicrobianas.
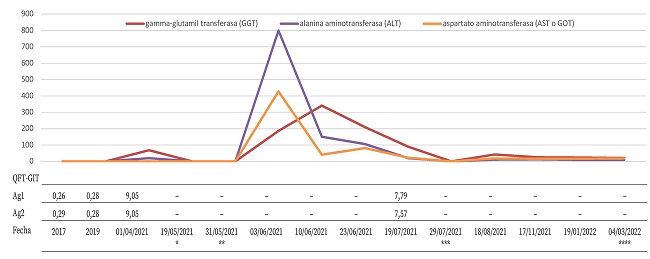
A mediados de mayo de 2021 se inició tratamiento con rifampicina (R), isoniazida (I), pirazinamida (P) y etambutol hidrocloruro (E), manifestando mejoría cutánea. El último día del mismo mes se suspendió el tratamiento por intolerancia con astenia generalizada, náuseas y vómitos, mal estado general con artralgias generalizadas, lesiones cutáneas inespecíficas, sin sensación distérmica ni alteración analítica del perfil hepático (Fig. 2).
A finales de julio la paciente fue valorada en Medicina Interna, observándose la normalización del perfil hepático y la desaparición de la clínica referida. La determinación de QFT-GIT seguía positiva, aunque cuantitativamente mejor que la anterior. En este mismo momento se inició tratamiento con R/H y levofloxacino (Lfx) con buena tolerancia. En agosto, la paciente refirió un cuadro de astenia que se relacionó con su antecedente de polimialgia reumática, y se le pautó prednisona en pauta descendente. Continuó con la triple terapia de TBC hasta mediados de marzo de 2022. Se concluyó la segunda pauta de tratamiento al cabo de siete meses, con recuperación completa desde el punto de vista clínico respecto a la lesión dermatológica (Fig. 2).
DISCUSIÓN
La vía de transmisión habitual de la TBC es por inhalación de gotitas de Pflügge aerosolizadas (emitidas por el enfermo al toser y expectorar), con bacilos en su interior, capaces de transportarse por aire hasta alcanzar los alvéolos, desde donde pueden diseminarse por vía hematógena o linfo-hemática, afectando cualquier otro sistema u órgano1. Otras vías de trasmisión son la digestiva y, menos frecuente, la cutánea-mucosa, presentando varias formas clínicas de acuerdo con el tipo de diseminación1 (Tabla 1).
Tabla 1. Clasificación de la tuberculosis cutánea.
| Tipo | Vía de inoculación | Aspecto clínico | Cambios patológicos |
|---|---|---|---|
| Inoculación exógena | |||
| Chancro tuberculoso | Inoculación directa | Papulonoduliar indoloro, ulceraciones, adenopatías | Inflamación aguda con granuloma |
| TBC verrugosa | Inoculación directa | Pápula, placa verrugosa con centro blando | Granuloma tuberculoide |
| Lupus vulgar | Inoculación directa | Placa gelatinosa, nódulo hipertrófico blando, ulceración necrótica | Granuloma tuberculoide |
| Vacunación BCG | |||
| Origen endógeno | |||
| Lupus vulgar | Hematógeno, linfático, contiguo | Placa gelatinosa, nódulo hipertrófico blando, ulceración necrótica | Granuloma tuberculoide |
| Escrofuloderma | Contiguo | Nódulo ulcerado sobre la glándula afectada | Necrosis absceso |
| TBC miliar | Hematógeno | Pápulas puntiformes discretas diseminadas | Microabscesos |
| TBC de orificios | Autoinoculación | Nódulos, úlceras dolorosas | Granuloma tuberculoide |
| Absceso tuberculoso | Hematógeno | Nódulos subcutáneos | Necrosis absceso |
| Tuberculoide papilonecrótico | Hematógeno | Pequeñas pápulas, costras ulceradas | Área de necrosis en forma de cuña |
TBC: Tuberculosis.
La TBC cutánea tras accidente de trabajo se manifiesta con lesiones que se localizan en la zona accidentada, frecuentemente afectando a dedos (como en el caso presentado), dorso de las manos, y menos frecuente, en la cara. Se inicia con la formación de una pápula eritematosa que puede evolucionar a una placa de aspecto verrucoso que recibe el nombre de chancro tuberculoso, sin ser exclusiva de la infección por accidente de trabajo. Con variaciones, la TBC cutánea tiene un periodo de incubación de aproximadamente 30 días3; en el caso presentado trascurrieron aproximadamente 40 días desde el accidente hasta la aparición de la lesión eritomatosa, la cual no evolucionó a chancro tuberculoso. Se diagnostican mediante el aislamiento de Mycobacterium complejo tuberculosis tras biopsiar la lesión. A pesar de la alta probabilidad de afecciones de la piel, generalmente las lesiones son transitorias, de buen pronóstico y escasa repercusión sobre la actividad laboral. No obstante, y de forma menos frecuente, existen variables relacionadas con la TBC cutánea, otros antecedentes personales o los efectos secundarios de los tratamientos que pueden tener repercusiones sobre el estado general de la persona trabajadora. El riesgo aumenta significativamente en personas inmunodeprimidas por enfermedades (VIH, trasplante, neoplasia, tratamiento con quimioterapia, insuficiencia renal crónica, hemodiálisis, silicosis, etc.) o por tratamientos inmunodepresores. El antecedente personal de la trabajadora de polimialgia reumática en tratamiento crónico con corticoesteroides en el momento del accidente, la convierte en una persona especialmente sensible.
Actualmente no está indicado tratamiento específico post exposición frente a la TBC según el protocolo ministerial de vigilancia sanitaria específica de agentes biológicos4. Seleccionar herramientas de trabajo que se acerquen a la máxima seguridad para evitar futuras exposiciones en el lugar de trabajo es uno de los pilares fundamentales en la prevención.
Se aplican técnicas moleculares de diagnóstico rápido en las muestras clínicas basadas en la amplificación de fragmentos de ADN de M. tuberculosis mediante una reacción en cadena de la polimerasa (PCR) que puede aumentar la sensibilidad del diagnóstico hasta un 90%5. Entre otras técnicas para diagnosticar infección activa o latente, se encuentran las conocidas como pruebas IGRA (Interferon-Gamma Release Assay)6, que miden el grado de reacción del sistema inmunitario de una persona ante las bacterias de la TBC. Las más usadas en la práctica clínica son la técnica ELISpot, acrónimo de enzymelinked immunospot assay, (T-SPOT®.TB) y el QFT-GIT, método de cuantificación de la respuesta inmune mediada por células que consiste en detectar in vitro la liberación de interferón gamma secretado por leucocitos T del paciente sensibilizado en presencia de antígenos específicos de M. tuberculosis7.
El diagnóstico de la TBC con afectación dermatológica se basa en los criterios absolutos (cultivo microbiológico) y relativos (historia clínica, examen físico, reacción tuberculina, tuberculosis activa en otros órganos, bacteriología, histología de las muestras obtenidas y respuesta al tratamiento) de Robert J. Wilkinson8.
Las personas afectadas no suelen requerir de incapacidad temporal, aunque podrían necesitarla en función de la zona afectada, la extensión y de variables dependientes del puesto de trabajo hasta la resolución el cuadro. Rara vez llegarán a ser causa de incapacidad permanente. La TBC cutánea no precisa aislamiento, ni es necesario realizar estudio de contactos, por riesgo de propagación.
Existen diferentes grupos de fármacos para el tratamiento de la TBC (Tabla 2)9. En cuanto a la duración, la pauta de elección es seis meses con los fármacos R/H/Z/E, si no lo contraindica el antibiograma mostrando resistencias. La fase inicial, de dos meses de duración, consiste en una combinación de tres o cuatro fármacos (R/H/Z con o sin E)3; en la fase de continuación, de cuatro meses de duración hasta completar los seis meses, se combinan R y H. El manejo de la TBC cutánea se hace siguiendo las mismas guías de la TBC de otros órganos, ajustando tiempo y dosis, vigilando la aparición de efectos adversos10,11. En el caso presentado, el tratamiento con R/H/Z/E fue suspendido al cabo de un mes por mala tolerancia. Se continuó con pauta de R/H y Lfx hasta completar siete meses de tratamiento.
Tabla 2. Fármacos para el tratamiento de la tuberculosis9.
| Grupo | Fármacos | Abreviatura |
|---|---|---|
| Grupo 1 | Isoniazida | H |
| Rifampicina | R | |
| Pirazinamida | Z | |
| Etambutol hidrocloruro | E | |
| Grupo 2 | Fluoroquinolonas | Lfx |
| Levofloxacino | Mfx | |
| Moxifloxacino | ||
| Grupo 3 | Estreptomicina | S |
| Fármacos de segunda línea | Kanamicina | Km |
| Amikacina | Am | |
| Capreomicina | Cm | |
| Grupo 4 | Protionamida | Pto |
| Otros fármacos de segunda línea, menos eficaces y con más efectos secundarios | Cicloserina | Cs |
| Grupo 5 | Linezolid | Lzd |
| Otros fármacos con menor experiencia clínica | Bedaquilina | Bdq |
| Delamanid | Dlm | |
| Clofazimina | Cfz | |
| Meropenem | Mpm | |
| Amoxicilina-clavulánico | Aml-cl |
La importancia de la indicación de TILT en personal sanitario infectado radica en que, si este colectivo desarrolla TBC activa, constituyen un riesgo social y epidemiológico3. Es ineludible descartar enfermedad tuberculosa antes de pautar TILT, basándose principalmente en el uso de H y R, por separado o conjuntamente. La H en las pautas de 6-9 meses sigue siendo el medicamento de referencia. Sin embargo, la duración y su toxicidad, especialmente hepatotoxicidad, plantean un serio obstáculo para su uso, por lo que se están introduciendo nuevas pautas de tratamiento más cortas, de 3-4 meses, utilizando asociaciones de diversos medicamentos antituberculosos, como R en monoterapia o asociada con H. Las personas infectadas deben ser monitorizadas para detectar posibles efectos secundarios. La pauta de tratamiento debería seleccionarse teniendo en cuenta la coexistencia de alguna enfermedad de base, las posibles interacciones farmacológicas y el hecho de que la pauta más adecuada debe acordarse con el propio paciente a fin de asegurar el cumplimiento. Previo al TILT, y al cabo de un mes de haberlo iniciado, puede estar indicada la determinación de enzimas hepáticas3; valores de AST (aspartato-aminotransferasa) y ALT (alanina-aminotransferasa) de hasta 3-5 veces su valor normal no contraindican la profilaxis, pero obligan a realizar una monitorización analítica estrecha. El TILT se debe retirar si se produce una elevación mayor de 5 veces el valor normal de AST o ALT, o si existe evidencia clínica de hepatitis.
Este caso remarca la importancia de fomentar las actuaciones preventivas tras accidentes con riesgo de exposición a agentes biológicos, adoptando las medidas de control inmediatas. Es necesario documentar debidamente no solo cómo ocurrió la lesión, la fuente de exposición y el estado inmunitario del trabajador, sino también el tipo de profilaxis. Hay que realizar un seguimiento adecuado del accidente, teniendo en cuenta la duración prolongada de la profilaxis de TBC y los posibles efectos secundarios de los fármacos empleados.
La realización de anamnesis clínico-laboral, la recogida de las inmunizaciones recibidas y la exploración detallada, siguen siendo fundamentales en la investigación de las infecciones tras accidente de trabajo con agentes biológicos, incluyendo otros distintos al VIH y hepatitis. Es necesario reforzar las medidas preventivas, seleccionando herramientas de trabajo que se acerquen a la máxima seguridad y colaborando con los proveedores en el diseño de nuevos materiales mejorado los sistemas de seguridad.