Señor Director:
El Real Decreto Legislativo 1/2015, entre los elementos de soporte para el uso racional de medicamentos en los hospitales, contempla que los servicios de farmacia (SF) realizarán actividades de farmacocinética (PK) clínica1. En este sentido, en las líneas estratégicas de los objetivos para el 2020 de la SEFH se recoge que, para contribuir al uso racional de los medicamentos, en el 80% de los hospitales el SF realizará informes de monitorización terapéutica (PK/ farmacogenética) en aquellos pacientes y para aquellos medicamentos que lo precisen2. A su vez, el Plan Nacional de Resistencias a los Antibióticos aprobado en España en 2014, que adopta los requerimientos de la Comisión Europea, indica que para la promoción de buenas prácticas de uso de antibióticos en los hospitales se deberían incluir actividades de monitorización. Cabe destacar que una encuesta previa a la aprobación del plan, mostró que sólo el 40% de los centros españoles lo estaban realizando, reflejando la existencia de una oportunidad de optimización terapéutica para el farmacéutico en nuestro entorno.
Actualmente, la determinación de concentraciones de fármacos es habitual en la práctica asistencial. Sin embargo, su utilidad está comprometida en ausencia de una historia de dosificación precisa, información sobre el muestreo y un soporte informático de PK clínica que permita una adecuada interpretación por los profesionales capacitados para ello3.
Con el objetivo de atender al cumplimiento de estos requerimientos, así como a la demanda clínica, el SF del hospital coordinó un proyecto de diseño de un circuito de monitorización PK e integración en la historia clínica electrónica (HCE). Se contempla como un sistema de soporte a la toma de decisiones clínicas (CDSS) en la monitorización del tratamiento, ayudando al clínico a la predicción de la respuesta individualizada, que mejora la calidad, el coste-eficacia y la seguridad en el cuidado de los pacientes4. Para alcanzar el éxito en su implantación, se dio cumplimiento a las premisas citadas por el grupo TECNO de la SEFH en la II-Edición del Curso “Elementos de soporte a la prescripción y monitorización del tratamiento farmacológico”: liderazgo de la dirección del hospital, elección del escenario adecuado y consenso de los usuarios.
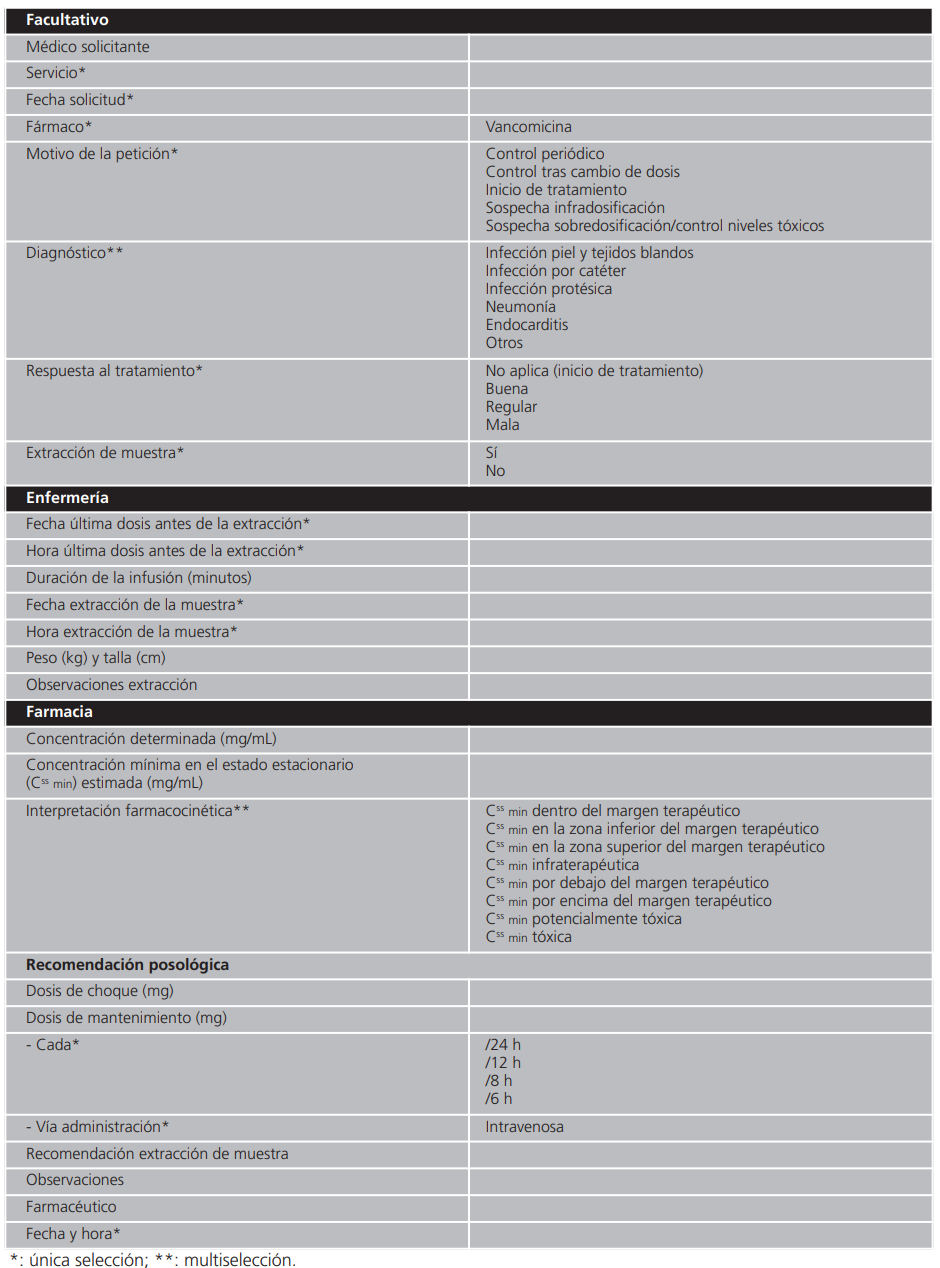
En la etapa inicial, se definieron el circuito de monitorización en el hospital, los flujos de trabajo y los profesionales implicados. Posteriormente, se desarrollaron las herramientas informáticas que permiten el registro de información y la comunicación entre el equipo interprofesional en el programa de HCE. El orden de intervención en dicho circuito es el siguiente (Tabla 1):
1º) Facultativo médico: inicia su solicitud cumplimentando la Petición “Monitorización farmacocinética”, que una vez confirmada se vuelca a un buzón de enfermería.
2º) Enfermería: desde un buzón habilitado al efecto, accede a un Formulario asociado a la Petición para el registro de información sobre el muestreo, que una vez cumplimentado pasa al buzón del farmacéutico.
3º) Farmacéutico: desde otro buzón habilitado al efecto, completa en el Formulario la información farmacocinética y la recomendación posológica. En este punto, se genera un Informe Farmacocinético que recoge la información cumplimentada por los tres perfiles profesionales quedando registrado en la HCE del paciente.
Se redactó un procedimiento integrado en el Sistema de Calidad del hospital, disponible en la intranet, y posteriormente se impartieron sesiones formativas por unidades clínicas para enfermería y médicos. La implantación se inició con un proyecto piloto para un fármaco, vancomicina, en una planta de hospitalización y posteriormente, se fue ampliando al resto del hospital así como también se fue extendiendo la prestación a otros fármacos.
Hasta el momento, el funcionamiento y aceptación del CDSS está siendo muy favorable, según lo esperado en línea con la bibliografía y las recomendaciones del grupo TECNO4,5. El diseño del CDSS permite el registro de manera sencilla de la información necesaria para una adecuada interpretación PK y a su vez, el Informe Farmacocinético con la recomendación posológica está accesible en la HCE para todos los profesionales sanitarios responsables del paciente. De este modo, se contempla como una oportunidad de optimización en la gestión de los recursos disponibles en el hospital (determinación de concentraciones plasmáticas de fármacos, software de PK clínica y resultados analíticos) y un aprovechamiento en la gestión de los conocimientos del farmacéutico clínico a través de la aplicación de criterios PK que contribuye a su integración en los equipos y decisiones clínicas. Por otra parte, el diseño del CDSS posibilita una explotación de toda la información recogida para futuras investigaciones sobre PK poblacional.