INTRODUCCIÓN
La proteína CD30 forma parte de la superfamilia de receptores de factor de necrosis tumoral (TNF) y es expresada por los linfocitos B de los pacientes con linfoma de Hodgkin clásico y en algunas formas de linfoma no Hodgkin (LH), como el linfoma anaplásico de células grandes (LACG). Por tanto, la proteína CD30 se ha convertido en una diana terapéutica para el tratamiento de estos linfomas1.
El linfoma de Hodgkin supone un 10% de todos los casos de neoplasias linfoides. Se presenta bajo dos formas principales: LH clásico, que representa el 95% de todos los casos, y el LH con predominio linfocítico nodular2. quimioterapia de primera línea conduce a una alta tasa de remisiones completas, sin embargo más de un 20% de los pacientes son refractarios o recaen tras la terapia de primera línea3. El tratamiento estándar de los pacientes con LH refractario o en recaída es la quimioterapia de rescate seguida de trasplante autólogo de progenitores hematopoyéticos (TAPH). En primera recaída podemos encontrar dificultades por toxicidades acumuladas, enfermedad quimiorefractaria, edad avanzada o comorbilidades no siendo, por tanto, candidatos al trasplante4-5.
Además, no se ha establecido un régimen estándar de tratamiento para los pacientes que recaen después del TAPH, siendo las opciones disponibles quimioterapia paliativa, alotrasplante o participación en un ensayo clínico. Aunque el trasplante alogénico sigue siendo una opción para lograr una remisión a largo plazo, la mayoría de los estudios concluyen que se produce recaída de la enfermedad en más del 50% de los pacientes6.
Aunque LH afecta predominantemente a los jóvenes, los pacientes ancianos representan un subgrupo de pacientes que son más difíciles de tratar existiendo pocas opciones cuando se requieren líneas posteriores de tratamiento. Por lo tanto, es necesaria la incorporación de agentes con nuevos mecanismos de acción2.
El LACG es un tipo de linfoma periférico no Hodgkin de células T. Supone un 2-3% de todos los casos de neoplasias linfoides2. La expresión de ALK se observa en un 85% de los pacientes y presentan mejor pronóstico que los ALK-negativos.
Aproximadamente entre un 40 y un 65% de los pacientes recaen tras la terapia de primera línea. No hay un tratamiento estándar y las opciones son limitadas7. Quimioterapia a altas dosis y TAPH pueden lograr remisión en un 30-40% de los pacientes.
La supervivencia global a 5 años para pacientes con ALK positivo es del 70% al 80% con quimioterapia convencional, pero es solo del 50% para pacientes con ALK negativo. Hay pocos tratamientos efectivos disponibles para pacientes con recaída o refractarios ALK negativos, por tanto, se necesitan nuevas opciones terapéuticas para mejorar el pronóstico en este subtipo de linfoma poco frecuente2.
Brentuximab vedotina es un anticuerpo monoclonal conjugado con un agente citotóxico (vedotina) que es capaz de provocar la apoptosis específicamente de células que presenten la proteína CD30 en su superficie. El anticuerpo se une selectivamente a la parte extracelular del CD30 presente en la superficie de la membrana, formando un complejo que es internalizado mediante endocitosis. Una vez en el interior celular, el fármaco accede al interior de los lisosomas donde sufre un proceso de escisión proteolítica liberando la vedotina (monometil auristatina E). La vedotina es un potente agente citotóxico que actúa interfiriendo con la polimerización de la tubulina; por ello, impide la formación del huso mitótico durante la división celular bloqueando el ciclo celular en fase G2/M, lo que provoca la activación de los mecanismos de apoptosis (muerte celular programada) y, en definitiva, la muerte celular de las células CD30+.
Brentuximab vedotina ha sido autorizado para el tratamiento de pacientes adultos con LH CD30+ en recaída o refractario después de trasplante autólogo de células madre o después de, al menos, dos tratamientos previos cuando el trasplante autólogo de células madre o la poliquimioterapia no es una opción terapéutica y, en pacientes con mayor riesgo de recaída o progresión después de un trasplante autólogo de células madre. También está indicado para el tratamiento de pacientes adultos con LACG sistémico en recaída o refractario y para el tratamiento de pacientes adultos con linfoma cutáneo de células T CD30+ tras, al menos, un tratamiento sistémico8,9.
El objetivo de este trabajo es describir la experiencia de uso de brentuximab vedotina (BV) en monoterapia o en combinación con quimioterapia convencional, en términos de efectividad y seguridad, en el tratamiento de LH en recaída o refractario y del LACG en varios centros hospitalarios.
MATERIAL Y MÉTODOS
Se realizó un estudio descriptivo, observacional, retrospectivo y multicéntrico de todos los pacientes con LH o LACG en recaída o refractarios, tratados con brentuximab vedotina en monoterapia o en combinación hasta febrero de 2019. Las variables recogidas fueron sexo, edad, diagnóstico, estadio de la enfermedad, afectación ósea, índice pronóstico internacional (IPI), líneas quimioterápicas previas, trasplante previo, ciclos recibidos y posología. La efectividad se midió en términos de supervivencia libre de progresión (SLP) y tasa de respuesta objetiva (TRO) definida como la suma de remisiones completas (RC) y de respuestas parciales (RP) y los efectos adversos (EA) según Common Terminology Criteria for Adverse Events v4.0 (CTCAE).
Los datos se obtuvieron del programa de validación y preparación de fármacos citostáticos (Farmis-Oncofarm®) y de la historia clínica electrónica (Selene®).
RESULTADOS
Se incluyeron 16 pacientes. 10 recibieron brentuximab en monoterapia (grupo 1) y 6 pacientes lo recibieron en combinación con bendamustina (grupo 2).
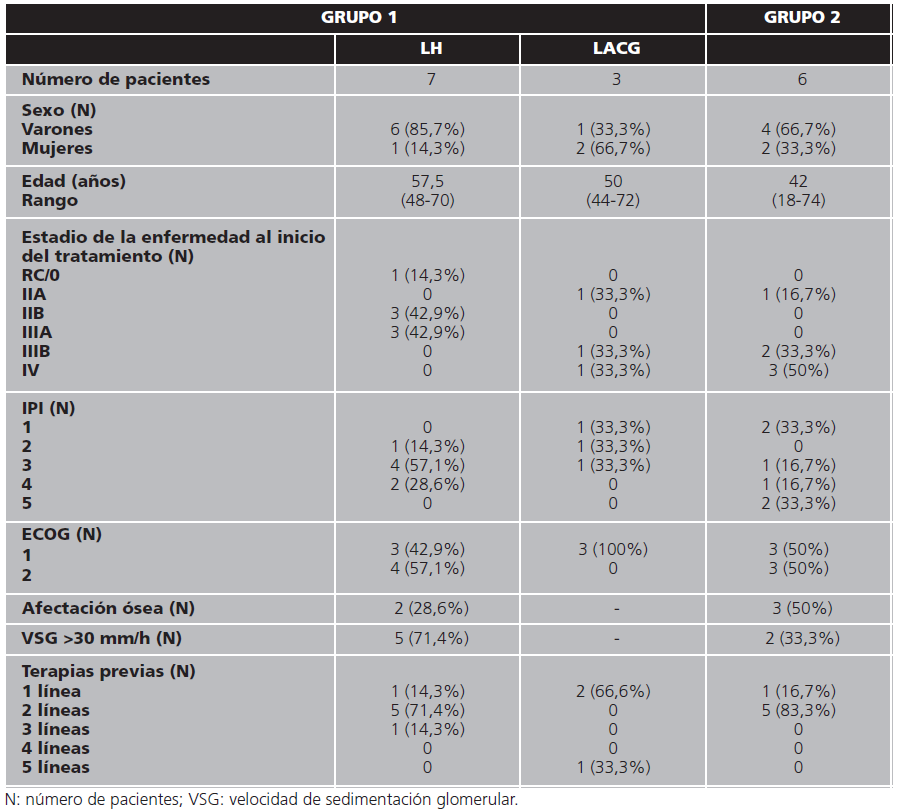
Las características de los pacientes del grupo 1 fueron: 7 pacientes presentaban LH y 3 LACG refractario o en recaída.
6 de los pacientes con LH eran hombres, la mediana de edad fue 57,5 años (rango: 48-70). Al inicio del tratamiento presentaban estadio IIB (n=3), IIIA (n=3) y RC/0 (n=1); con IPI 2 (n=1), 3 (n=4) y 4 (n=2); y ECOG 1 (n=3) y 2 (n=4). Dos presentaban afectación ósea y 5 presentaban VSG elevada.
1 paciente recibió brentuximab en 2ª línea, 5 en 3ª línea y 1 en 4ª línea. Todos los pacientes recibieron ABVD (1ª línea), 6 pacientes recibieron ESHAP (2ª línea). 1 paciente fue sometido a TAPH (3ª línea).
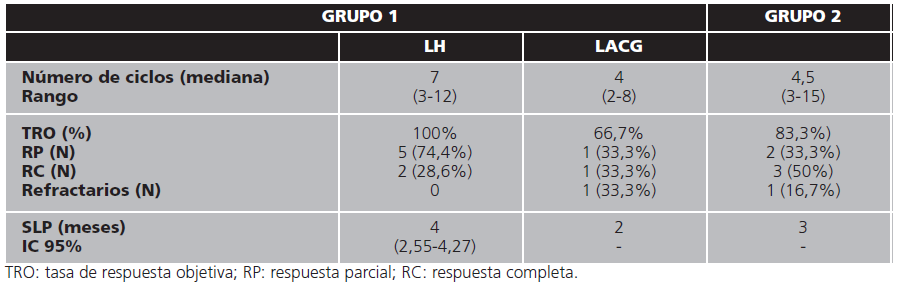
Todos los pacientes fueron tratados con brentuximab 1,8 mg/kg cada 3 semanas, excepto 2 que iniciaron con dosis reducidas por toxicidades previas. La mediana de ciclos recibidos fue 7 (rango 3-12).
En cuanto a la efectividad tras 4 ciclos de tratamiento, se obtuvieron 5 respuestas parciales (RP) y 2 respuestas completas (RC). La TRO fue 100%. 4 de los pacientes con RP progresaron siendo la SLP 4 meses (IC 95% 2,55-4,27). Uno de los pacientes en RC fue sometido a trasplante y recibió 6 ciclos de brentuximab como mantenimiento.
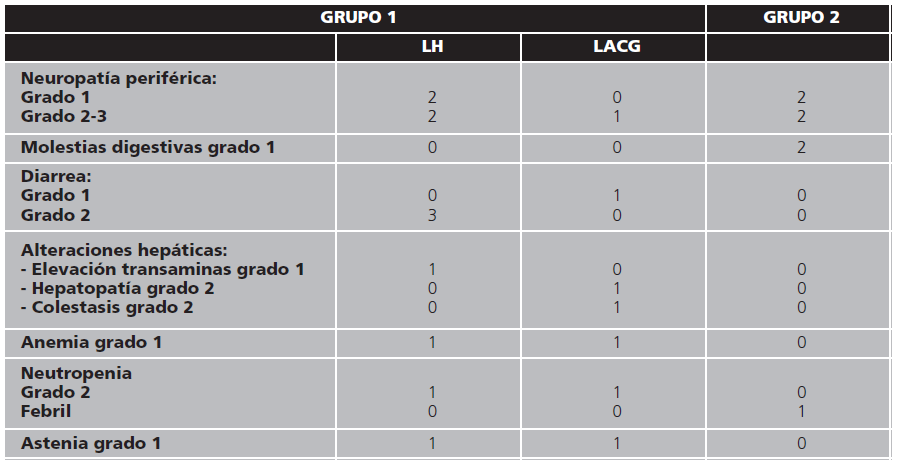
6 pacientes presentaron EA. Estos fueron neuropatía periférica grado 1 (n=2) y grado 2-3 (n=2); diarrea grado 2 (n=3); anemia grado 1 (n=1); elevación de transaminasas grado 1 (n=2); neutropenia grado 2 (n=1); astenia grado 1 (n=1). En un paciente fue necesario reducción de dosis y otro suspendió el tratamiento durante el mantenimiento, ambos por neurotoxicidad.
La mediana de edad de los pacientes con LACG fue 50 años (rango 44-72), siendo uno de ellos hombre. Presentaban estadio IIA, IIIB y IV con IPI 1, 3 y 2, respectivamente. ECOG 1 en todos los pacientes. 2 pacientes recibieron brentuximab en 2ª línea y 1 en 6ª línea. Todos los pacientes recibieron CHOP en 1ª línea.
Todos los pacientes fueron tratados con brentuximab 1,8 mg/kg cada 3 semanas. La mediana de ciclos recibidos fue 4 (rango 2-8).
En cuanto a la efectividad tras 4 ciclos de tratamiento, se obtuvieron 1 RP, 1 RC y un paciente fue refractario. La TRO fue 66,7%. El paciente con RP progresó siendo la SLP 2 meses.
Los EA descritos fueron neuropatía periférica grado 2 (n=1); diarrea grado 1 (n=1); hepatopatía grado 2 (n=1); colestasis grado 2 (n=1); neutropenia grado 2 (n=1); astenia grado 1 (n=1). Fue necesaria reducción de dosis en un paciente por neurotoxicidad.
Las características de los pacientes del grupo 2 fueron: todos los pacientes presentaban LH. 4 eran hombres, mediana de edad 42 años (rango: 18-74). Al inicio del tratamiento presentaban estadio IIA (n=1), IIIB (n=2) y IV (n=3); con IPI 1 (n=2), 3 (n=1), 4 (n=1) y 5 (n=2); ECOG 1 (n=3) y 2 (n=3). 3 pacientes presentaban afectación ósea y 2 presentaban VSG elevada.
1 paciente recibió brentuximab en 2ª línea, 5 en 3ª línea. Todos los pacientes recibieron ABVD (1ª línea) y ESHAP (n=3) o IGEV (n=2) (2ª línea).
Fueron tratados con brentuximab 1,8 mg/kg cada 3 semanas. La mediana de ciclos recibidos fue 4,5 (rango 3-15). Tras 4 ciclos de tratamiento se obtuvieron 2 RP y 3 RC y 1 paciente fue refractario al tratamiento. La TRO fue 83,33%. 1 paciente en RP progresó siendo la SLP 3 meses. Los pacientes que consiguieron RC pudieron beneficiarse de TAPH. En estos pacientes se continuó con brentuximab en mantenimiento hasta completar 18 dosis totales (pre y postrasplante).
Los EA descritos fueron neuropatía periférica grado 1 (n=2), grado 2-3 (n=2); molestias digestivas (n=2); y neutropenia febril (n=1). No fue necesario reducción de dosis pero sí retraso en un ciclo.
DISCUSIÓN
La eficacia del brentuximab en monoterapia en LH está basada en un ensayo fase II controlado, prospectivo, multicéntrico, de una sola rama (SG035-0003)10. Las características de nuestra población diferían de las de los pacientes del ensayo pivotal en algunos aspectos: mediana de edad 31 años vs. 57,5 y TAPH previo (100% vs. 14,3%). En cuanto a TRO fue del 100%, siendo 28,6% RC, mientras que en el ensayo pivotal la TRO fue 75% y la tasa de RC 34%. La SLP de nuestra muestra fue 4 meses y la estimada en el ensayo pivotal fue 5,6 meses. La mediana de SLP en los pacientes que alcanzaron RC tras brentuximab vedotina fue de 21,7 meses mientras que ninguno de nuestros pacientes en RC presentó progresión de la enfermedad. Un 14,3% de los pacientes pudieron ser sometidos a TAPH tras el tratamiento con brentuximab vedotina, un porcentaje superior al objetivado en el ensayo pivotal (6,9%). Cabe destacar que un 57% de nuestros pacientes presentaron ECOG 2 y todos los pacientes del ensayo pivotal presentaron ECOG 0-1. Esta puede ser una de las causas de las discrepancias observadas en cuanto a efectividad11.
En cuanto al LACG la eficacia de bretuximab en monoterapia está basada en el ensayo SG035-000412, estudio fase II controlado, prospectivo, multicéntrico, de una sola rama.
Las características demográficas de nuestra población fueron similares a las del estudio pivotal. La TRO fue del 66,67% vs. 86% del ensayo pivotal y la RC 33,33% vs. 57%10. Los resultados son inferiores a los del estudio pero debido al pequeño tamaño muestral de este subgrupo de pacientes no resulta adecuado realizar comparaciones.
Los efectos adversos descritos fueron similares a los reportados en los estudios. Un paciente presentó neuropatía periférica grado 3, todos los demás efectos adversos fueron grado 1 y 2. Es importante tener en cuenta que 2 pacientes iniciaron brentuximab con dosis reducidas debido a las toxicidades producidas por líneas de tratamientos previas. La presencia de toxicidades previas puede sesgar el análisis de datos realizado.
Debido a los buenos resultados publicados sobre la combinación con bendamustina se decidió utilizar esta combinación en nuestro centro. Los resultados obtenidos son prometedores. A pesar de que se obtuvieron TRO inferiores versus brentuximab en monoterapia (100% vs. 83,33%), mayor número de pacientes obtuvieron RC lo que permitió que fuesen sometidos a trasplante.
En el estudio publicado por LaCasce y colaboradores13 se investigó la combinación en pacientes con LH en recaída o refractario como tratamiento puente al TAPH. Se diseñó en dos fases, la fase 1 fue diseñada para determinar la dosis de bendamustina y evaluar seguridad y tolerabilidad. Los pacientes recibieron 1,8 mg/kg de brentuximab el día 1 de cada ciclo+ 90 mg/m2 los días 1 y 2. La fase 2 se diseñó para evaluar la actividad de la combinación.
En cuanto a las características basales de los pacientes incluidos, cabe comentar que, un 1,8% presentó ECOG 2, y en nuestra muestra este valor asciende al 50%. Además, un 52,8% presentó enfermedad en estadio III-IV al diagnóstico, mientras que en nuestro estudio lo presentaba el 83% de los pacientes. La TRO fue 92% y se obtuvieron un 74% de RC, mientras que en nuestro estudio la TRO fue 83,33% y la RC un 50% (tras 4 ciclos). Los peores resultados obtenidos pueden ser debidos a que nuestra muestra de pacientes se encontraba en peor situación basal y con enfermedad más avanzada.
Los efectos adversos descritos fueron inferiores a los descritos en los estudios publicados13,14. No se obtuvo ninguna reacción infusional mientras que en los estudios publicados las presentaron un porcentaje elevado de los pacientes (56,4% en estudio de LaCasce et al. y 60% en O'Connor et al.). Se reportaron efectos adversos grado 3-4 en un 56,4% (LaCasce et al.), un 18% (O'Connor et al.) y en nuestra muestra un 16% (neuropatía periférica descrita por un paciente). Se reportó que un 36,4% (LaCasce et al.) de los pacientes discontinuaron el tratamiento por EA. En ninguno de los pacientes se suspendió el tratamiento por toxicidad.
Entre las limitaciones del estudio cabe destacar el reducido número de pacientes tratados, que dificulta obtener conclusiones contundentes. También las limitaciones propias del diseño retrospectivo, ocasionando la pérdida de datos no recogidos.
CONCLUSIONES
Brentuximab vedotina es un fármaco eficaz en las neoplasias CD30+. Su introducción al tratamiento de LH y LACG ha permitido expandir el arsenal terapéutico y mejorar el pronóstico de estos pacientes.
Presenta una buena actividad como agente en monoterapia, logrando TRO elevadas. Además, la combinación con regímenes de quimioterapia convencionales como bendamustina ha permitido aumentar la eficacia logrando respuestas más duraderas.
Aumentando la superviviencia y potenciando el efecto de la poliquimioterapia brentuximab vedotina nos ha permitido ofertar TAPH a pacientes no candidatos previamente por falta de respuesta.
Del mismo modo, los datos sugieren que el inicio del mantenimiento con brentuximab tras TAPH parece ser una opción razonable en pacientes que tienen un alto riesgo de progresión después del trasplante.
Se han reportado efectos adversos en muchos de los pacientes tratados pero estos se han manejado con reducción de dosis, y no han supuesto discontinuaciones de tratamiento en la mayoría de los pacientes. El mantenimiento post-trasplante con brentuximab vedotina es muy bien tolerado. Los principales efectos adversos observados fueron neurotoxicidad y diarrea.
Los resultados podrían ser utilizados como criterio de decisión en el algoritmo terapéutico del LH y LACG pero son necesarios estudios con mayor número de pacientes.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.