INTRODUCCIÓN
La prevalencia de la infección por virus de hepatitis C (VHC) presenta importantes variaciones de unas áreas geográficas a otras, llegando a oscilar entre el 5 y el 43%1. Se han observado notables diferencias incluso entre diferentes regiones dentro del mismo país2. Asimismo, estos datos presentan importantes incertidumbres inherentes, ya que en muchas ocasiones se cuantifica la población VHC seropositiva, y no se diferencia de aquella con infección de VHC activa -que precisa de determinaciones positivas para ARN de VHC-3,4. Dentro de la población general, existen subpoblaciones de alto riesgo como los pacientes institucionalizados, en las que se ha estimado que la prevalencia puede ser hasta 9,5 veces superior a la población general5,6. Esto se debe a los factores de riesgo asociados como la realización de tatuajes y piercings en condiciones inadecuadas de salud, bajo nivel económico y sociocultural, transmisión por uso de drogas inyectadas y determinadas conductas sexuales7,8.
La infección por VHC se asocia con una considerable morbimortalidad, entre la que destaca el carcinoma hepatocelular o la fibrosis hepática9. Por ello, la Organización Mundial de la Salud se ha marcado como objetivo prioritario la eliminación de VHC en 203010. Aun así, y a pesar de que existen numerosas guías y leyes que apoyan una cobertura sanitaria equivalente entre la población general y la población de las prisiones11,12, se observan importantes diferencias de acceso a la asistencia sanitaria.
La incorporación de los nuevos antirretroviales de acción directa (AAD) en el tratamiento de VHC ha supuesto un importante avance13. No sólo se ha demostrado una importante mejoría en la eficacia del tratamiento en comparación con los esquemas basados en interferón -con respuestas virales sostenidas (RVS) mayores del 90%-, sino que apenas se han observado reacciones adversas, a diferencia de los tratamientos predecesores. Por otra parte, la reducción del tiempo de tratamiento con los nuevos AAD supone otra mejoría. Esta ventaja es un elemento facilitador para la eliminación del VHC en la población institucionalizada, ya que en algunos estudios se han incluido sólo aquellos pacientes con sentencias lo suficientemente largas como para completar el tratamiento y poder confirmar el estado de la enfermedad1. Esta restricción se debe a que se ha observado una mayor pérdida de seguimiento en aquellos pacientes liberados o trasladados. El seguimiento de los pacientes es esencial no sólo para detectar la presencia de infección, sino a la hora de reforzar la educación del paciente curado de VHC, pues se ha detectado un mayor riesgo de re-infección en presos liberados14,15.
Hasta ahora, se han realizado algunos estudios en Europa, Canadá y Australia sobre el tratamiento de VHC en prisiones15,16,17,18. En ellos, se observa que los métodos basados en un equipo multidisciplinar o con enfermeras de referencia han obtenido buenos resultados. En otros estudios se ha usado la telemedicina para evitar los elevados costes y escasa operabilidad de las visitas de los presos al médico especialista en el hospital7. Sin embargo, la incorporación de la telemedicina también supone limitaciones, ya que en muchas prisiones no se dispone de los recursos necesarios para implantarla. Por tanto, esto afectaría a la reproducibilidad de programas basados en la telemedicina, sin contar con las dificultades de comunicación que se pudieran producir con los presos.
El objetivo de nuestro estudio es el desarrollo de un programa multidisciplinar para el diagnóstico y tratamiento de la infección por VHC en los presos de nuestra área.
MATERIAL Y MÉTODOS
Se realizó un estudio retrospectivo de la implantación de un programa multidisciplinar de detección y tratamiento de infección por VHC en prisiones, desarrollado desde el 01/06/2016 a 30/09/2019.
Centros penitenciarios
Los centros penitenciarios en los que se llevó a cabo fueron 3 instituciones mixtas de 522 celdas (Centro Penitenciario Puerto I, Cádiz), 394 (Centro Penitenciario Puerto II, Cádiz) y 1.008 (Centro Penitenciario Puerto III, Cádiz). La asistencia sanitaria de estos centros depende del Hospital Universitario de Puerto Real.
Protocolo de detección y tratamiento de pacientes
Se estableció un protocolo de cribado poblacional del VHC en centros penitenciarios basado en guías de detección precoz de la infección y el Plan estratégico para el abordaje de la hepatitis C en el Sistema Nacional de Salud19,20. Para realizar el diagnóstico, se determinó la serología de todos los presidiarios que ingresaron en el centro mediante Abbott Architect Anti-HCV® y de los antígenos Core con Abbott Diagnostics Architect HCV core Ag assay®. Aquellos pacientes con resultados de infección positiva fueron sometidos a una determinación de la carga viral (CV) con Roche Cobas HCV Test en cobas 6800® y genotipado con Abbott Realtime HCV Genotype II®. Se determinó el grado de fibrosis de los pacientes virémicos (CV por encima de 19 copias/ml). Por otra parte, el protocolo también incluyó el cribado de los pacientes con virus de inmunodeficiencia humana (VIH). El diagnóstico de los pacientes se realizó en acto único.
Posteriormente, se gestionó el tratamiento de los presos diagnosticados de infección por VHC junto con el Servicio de Farmacia Hospitalaria. Al inicio, se priorizaron los tratamientos de los pacientes con mayor grado de fibrosis (F4 y F3) siguiendo los criterios del Plan estratégico para el abordaje de la hepatitis C en el Sistema Nacional de Salud20. Posteriormente, se trataron todos los pacientes diagnosticados de infección por VHC, independientemente de su grado de fibrosis. Se usaron aquellos fármacos o combinaciones de los mismos adaptados a las guías clínicas en cada momento y contexto clínico. No hubo financiación de la medicación por parte de ningún sponsor. Se excluyeron aquellos pacientes que abandonarían la prisión en los siguientes 6 meses al momento del diagnóstico y decisión de tratamiento, así como los presos que tuvieran previsto un traslado de prisión. Este criterio ha sido comentado anteriormente en otros estudios para evitar la pérdida del seguimiento de los pacientes1. Los pacientes que fueron excarcelados fueron remitidos al hospital de referencia. Los tratamientos fueron prescritos por el facultativo especialista en enfermedades infecciosas del hospital de referencia, tras la valoración de cada caso individual por el personal de referencia de las prisiones y del farmacéutico del hospital. Se estableció un circuito de dispensación y traslado de la medicación desde la farmacia del hospital de referencia a las prisiones, con dispensaciones mensuales por paciente.
El seguimiento de los pacientes fue llevado a cabo por el médico especialista en enfermedades infecciosas de forma presencial en los centros penitenciarios. La periodicidad de las visitas del facultativo hospitalario fue mensual durante los meses de tratamiento, y posteriormente de forma bimensual hasta el alta. Los médicos y enfermeras de referencia de cada prisión proporcionaron apoyo al facultativo del hospital, informándose de cualquier incidencia de forma bidireccional. La medicación se dispensaba a los pacientes diariamente con presencia física del personal de prisiones junto con el tratamiento opiáceo (metadona), para garantizar la adherencia al tratamiento. Toda la asistencia proporcionada a los pacientes fue presencial, desde el diagnóstico hasta el alta.
Antes de iniciar los tratamientos se llevó a cabo un proceso de educación del personal sanitario y de los pacientes con sesiones formativas sobre medidas de prevención, la transmisión del virus de VHC, tratamiento y reinfección. Tales sesiones se adecuaron a las costumbres de cada institución penitenciaria. Asimismo, en cada acto de seguimiento de los pacientes se reforzaron tales conceptos.
Equipo multidisciplinar
Se seleccionó un referente de enfermería y médico general en cada uno de los centros penitenciarios, que colaboraba con el médico especialista en enfermedades infecciosas del hospital de referencia. El enfermero referente de cada centro penitenciario lideró el proceso de cribado y reclutamiento de los pacientes. También fue el profesional sanitario encargado de extraer las muestras de sangre para las determinaciones analíticas.
El equipo multidisciplinar estaba compuesto por: 1 médico especialista en enfermedades infecciosas del centro de referencia, 3 médicos generales de los centros penitenciarios, 3 enfermeras de referencia de las prisiones, 1 microbiólogo y 2 farmacéuticos especialistas en farmacia hospitalaria.
Datos, variables del estudio y tratamiento estadístico
Se recogieron los siguientes datos de los pacientes y tratamientos: género, edad, grado de fibrosis, genotipo del virus VHC, uso de terapia sustitutiva (opioides), tratamiento previo, esquema de tratamiento usado para infección por VHC y seguimiento realizado. Asimismo, fueron registrados los siguientes parámetros analíticos: creatinina, colesterol, enzimas transaminasas, linfocitos, bilirrubina, international normalized ratio (INR), albúmina, alfa-fetoporteína, hemoglobina y plaquetas. Se valoró la respuesta al final del tratamiento (RFT) y respuesta viral sostenida a las 12 semanas de tratamiento (RVS12). RFT fue definida como la ausencia de ARN del virus de VHC detectable (>19 copias de virus VHC/ml) al final del tratamiento. RVS12 fue definido como la ausencia de ARN del virus de VHC detectable a las 12 semanas de terminar el tratamiento. Las recidivas, definidas como la determinación de CV detectable a los 6 meses después de alcanzar RVS12, y reinfecciones fueron registradas. Por otra parte, también se recogieron los efectos secundarios irreversibles asociados al tratamiento y los abandonos. Finalmente, se comparó la prevalencia de infección por VHC activa antes de la implantación del programa con los datos al final del presente estudio, considerando RVS12 como curación de la infección por VHC. Los pacientes sin datos de RVS12, ya sea por pérdida de seguimiento o por no haber completado el tratamiento fueron considerados como portadores de infección activa de VHC.
Las bases de datos utilizadas para la extracción de información fueron la historia médica digital y el módulo de pacientes externos de la aplicación Farmatools®.
RESULTADOS
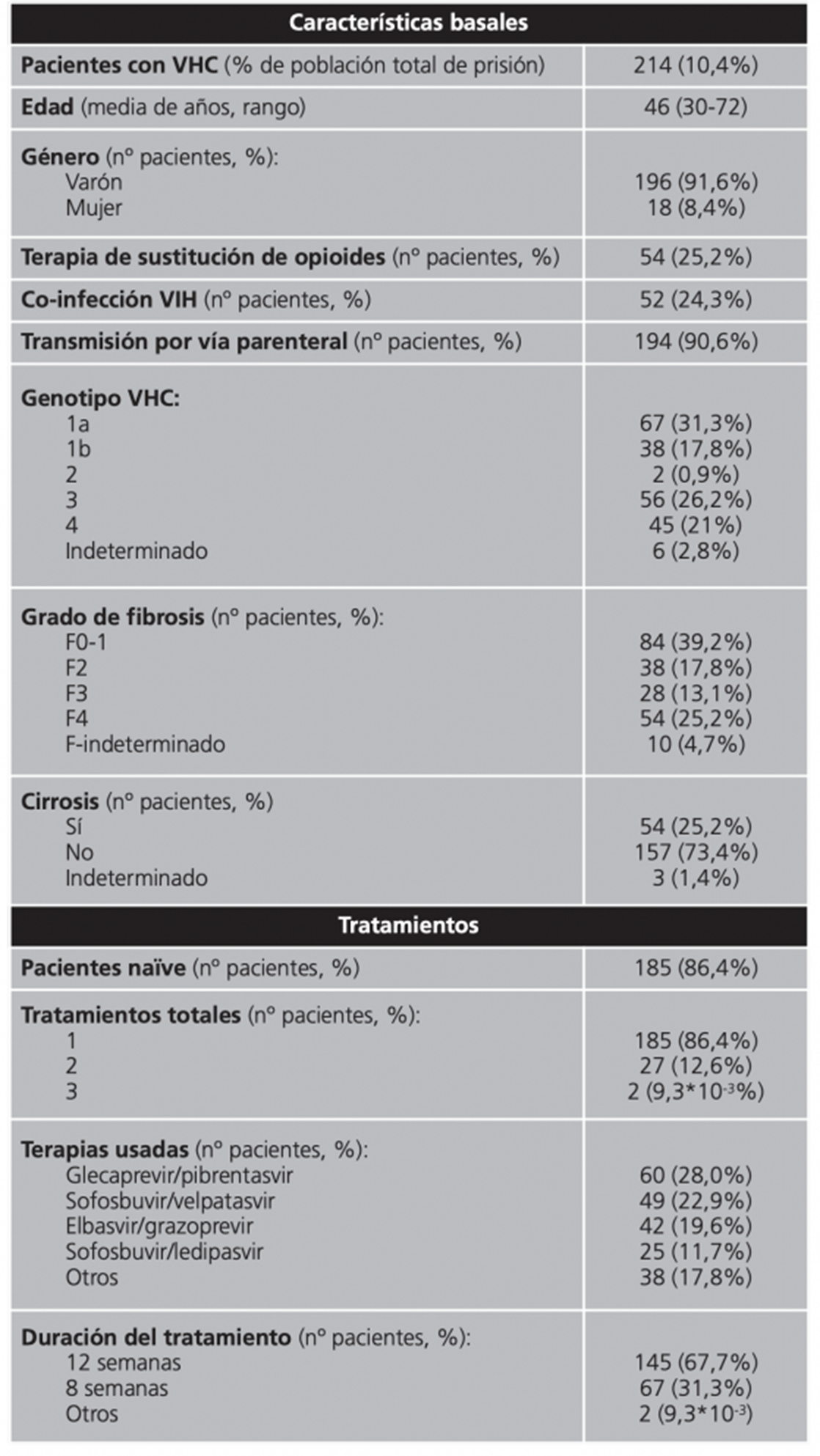
La población global de los centros penitenciarios incluidos en el estudio es de 2.065 presos. El número de presos con serología positiva frente al VHC con CV detectable fue 214 (Tabla 1).
Características de los pacientes y tratamiento usado
Aunque se trataron pacientes de ambos géneros, la mayoría de los pacientes fueron varones (91,6%). Una cuarta parte (25,2%) de estos presidiarios estaban incluidos en programas de terapia de sustitución de opioides. Los genotipos de VHC más frecuentes fueron el genotipo 1a (31,3%) y genotipo 3 (26,2%). Los pacientes fueron en su mayoría no cirróticos (73,4%). Más del 85% de los convictos no habían recibido un tratamiento previo para VHC. Los tratamientos más frecuentemente empleados fueron glecaprevir/pibrentasvir (28,0%) y sofosbuvir/velpatasvir (22,9%). Más de dos tercios de los tratamientos prescritos tuvieron un esquema de 12 semanas (67,7%). Estos datos pueden ser consultados en la Tabla 1.
Parámetros analíticos
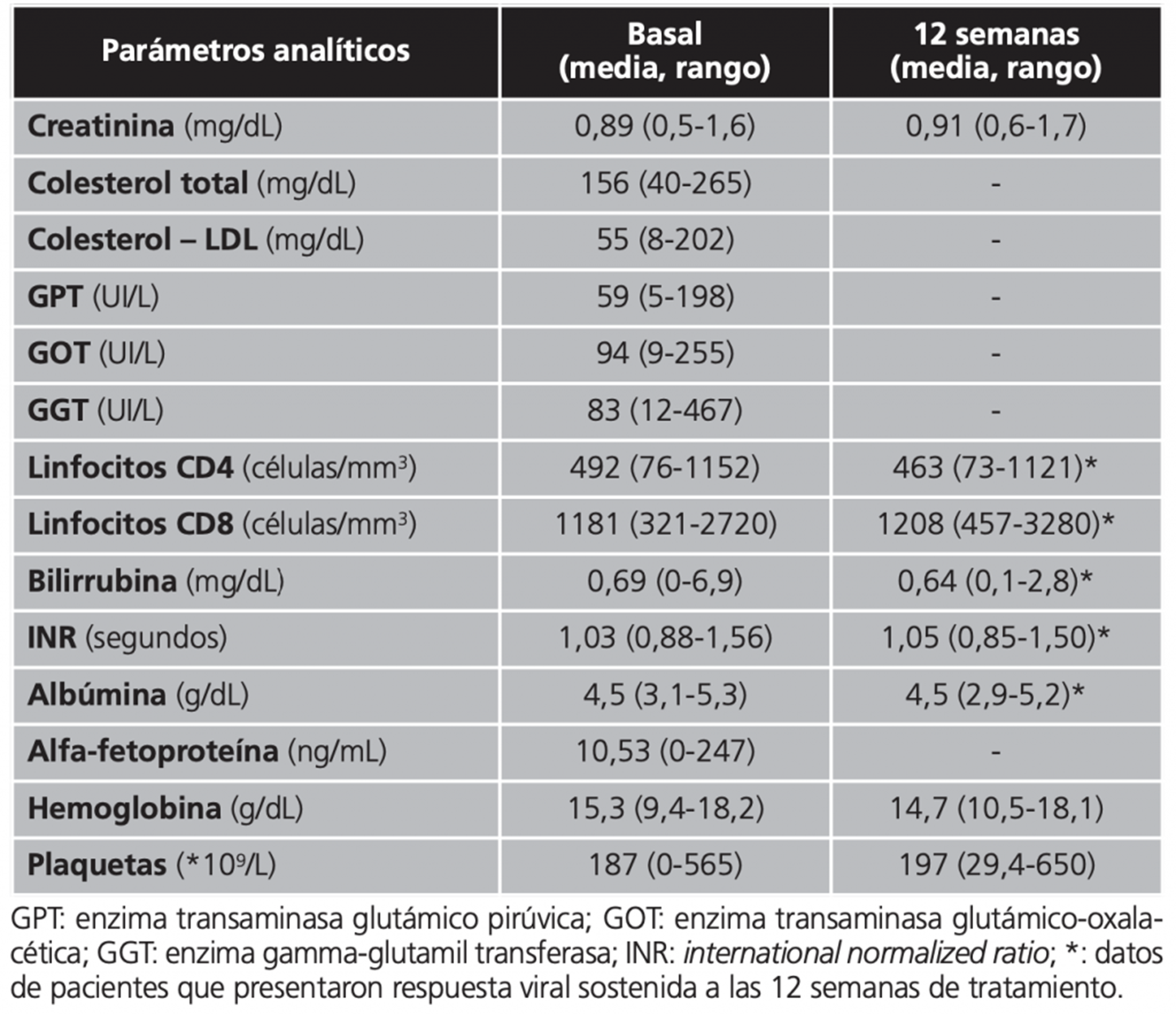
Las concentraciones séricas de los parámetros recogidos se mantuvieron estables desde el inicio del tratamiento para VHC hasta las 12 semanas posteriores. Algunos datos presentados, como los linfocitos CD4 y CD8, pertenecen sólo a los pacientes con RVS12. La Tabla 2 resume la información disponible respecto a los parámetros analíticos.
Resultados en salud: efectividad y seguridad
En el momento de finalización del presente estudio, 194 reclusos habían completado el tratamiento. De estos presos, 193 (99,5%) habían alcanzado RFT. La RVS12 pudo ser analizada en 191 convictos, de los cuales 178 (93,2%) presentaron RVS12. Los 13 pacientes restantes tuvieron un traslado a otro centro penitenciario o pérdida de seguimiento, por lo que su RVS12 no pudo confirmarse por no ser valorable. Se detectaron 5 (2,8%) recidivas en los pacientes que alcanzaron RVS12. No se registró ningún caso de reinfección por VHC. Durante el desarrollo del programa, se notificaron 7 (3,3%) abandonos de tratamiento. Los efectos adversos irreversibles asociados al tratamiento fueron observados en 2 pacientes. El primero de ellos fue una descompensación hepática que desembocó en el fallecimiento del convicto. El segundo fue una hemorragia bilateral cerebral, que no fue mortal. Finalmente, la prevalencia registrada al inicio del programa fue del 10,4%, mientras que al final del estudio fue del 1,7%.
DISCUSIÓN
Las prisiones constituyen un micro-ambiente ideal para el tratamiento del VHC por las características que presentan: alta prevalencia y riesgo de transmisión de enfermedad6,7. Aquellos presos liberados que hayan sido curados de VHC no podrán transmitir el virus a la población fuera de las prisiones, evitando así la propagación de la infección.
Sin embargo, la escasez de bibliografía acerca del tratamiento de VHC en reclusos hace que este tipo de estudios tengan una notable relevancia. Teniendo en cuenta el volumen de presidiarios tratados y duración del estudio de anteriores publicaciones18,21,22,23, podemos afirmar que nuestro programa de detección y tratamiento de VHC en prisiones ha sido uno de los mayores desarrollados hasta la fecha en Europa. También se mejora el diagnóstico de infección de VHC de otros estudios3,4, en los cuales no se distingue entre población VHC seropositiva y con infección activa. También se estableció la determinación de la CV y genotipado en un solo paso desde el comienzo del estudio, presentándose como estrategia pionera hasta ese momento. Frente al diseño de ensayo clínico de la principal investigación de cribado y tratamiento de VHC realizada en prisiones de España18, nuestro estudio describe datos de práctica clínica habitual en un ambiente real. Otra diferencia con respecto a este citado ensayo clínico, es que nuestro estudio no usó un único esquema como tratamiento, sino varios de ellos, ya que no recibió ningún tipo de apoyo por parte de empresas farmacéuticas. Debido a esta circunstancia, nuestro trabajo podría presentar más similitudes con la práctica clínica habitual, proporcionando una valiosa información que puede complementar a los datos descritos con anterioridad en nuestro país.
Nuestro trabajo ha alcanzado unos valores de RVS12 de más del 90%, ausencia de nuevos casos de reinfección y una disminución importante de la prevalencia de VHC en los reclusos. Aunque es cierto que la RVS12 es algo menor que la descrita en los ensayos clínicos de los AAD de última generación24,25,26, no hay que olvidar la influencia de la pérdida de datos por traslado a otros centros penitenciarios, los factores de riesgo y las barreras de la población de prisiones. Es muy posible que algunos de los pacientes cuyo seguimiento se perdió por traslado a otros centros hayan obtenido RVS12. Asimismo, es importante reseñar que los resultados descritos no son del todo definitivos, pues no se ha completado el tratamiento de 20 pacientes ni se ha podido valorar la RVS12 de más de 30 convictos. Si a todo ello añadimos nuestro análisis conservador de los datos, considerando infección activa en todos los pacientes con pérdida de seguimiento, podemos afirmar que nuestro programa de diagnóstico y tratamiento de VHC en prisiones ha conseguido unos resultados de efectividad considerables.
Asimismo, hemos podido confirmar que los programas de educación tanto de los pacientes como de los profesionales sanitarios genera un importante impacto en la población tratada, tal y como se ha comprobado en otros estudios16. Por otra parte, los efectos adversos irreversibles han sido escasos, aunque se haya registrado un evento mortal en un paciente.
Las diferencias del acceso a la asistencia sanitaria de la población reclusa con respecto a la población general vulneran los derechos humanos. Se han detectado numerosas barreras que favorecen la inequidad sanitaria: estigmatización de la población institucionalizada, dificultades para el transporte de la medicación, costes elevados de los tratamientos, ausencia de facultativos especialistas en prisiones, miedo de las reacciones asociadas al tratamiento o procesos de diagnóstico, etc.27,28. Por otra parte, también se han localizado elementos facilitadores en la eliminación del VHC: trabajo de equipos multidisciplinares, circuitos de diagnóstico y cribado de la población diana, formación del staff de las prisiones, educación de los presos, programas de intercambio de jeringas y terapia de sustitución de opioides21,28.
Con el programa desarrollado se ha podido salvar algunas barreras y potenciar muchos de estos elementos facilitadores. El principal ha sido la presencia física de facultativos especialistas en colaboración con otros profesionales sanitarios, que ha hecho posible el acercamiento entre dos contextos que, con frecuencia, se encuentran muy alejados: los centros penitenciarios y los hospitales. Este fenómeno podría contribuir a mejorar procesos de humanización en la asistencia sanitaria prestada a los reclusos. Asimismo, este trabajo puede ser ejemplo del procedimiento a seguir en centros que carecen de recursos para instalar sistemas de avanzada tecnología, como la telemedicina.
La principal limitación de nuestro estudio es la falta de madurez de los datos de RVS12, que se traduce en una efectividad ligeramente inferior a los descritos en algunas investigaciones de similar índole16,18. Sin embargo, no hay que olvidar el carácter conservador del análisis de los resultados.
A la hora de evaluar el tratamiento de la población institucionalizada, no sólo hay que tener en cuenta el beneficio obtenido por el individuo o la población en las prisiones, sino las ventajas que ello supone para la población general27. Se han desarrollado modelos que estiman que el tratamiento del VHC en prisiones podría evitar hasta 12.500 nuevas infecciones en los próximos 30 años9, así como los problemas de salud asociados. A pesar del elevado coste de los AAD, no son pocos los estudios que concluyen que las estrategias de tratamiento de VHC en prisiones son coste-efectivas29,30.
CONCLUSIONES
Podemos concluir que en nuestro estudio se ha desarrollado un programa multidisciplinar de diagnóstico y tratamiento de VHC en prisiones que ha alcanzado importantes resultados de curación de la enfermedad, evitando la aparición de reinfecciones y con pocos efectos adversos irreversibles.
Todos los autores han contribuido intelectualmente, han tenido en cuenta las responsabilidades éticas, reúnen las condiciones de autoría y han aprobado la versión final del mismo.
Responsabilidades éticas: Para desarrollar este estudio los autores cumplieron con todos los criterios éticos y legales. Este manuscrito ha sido elaborado respetando las recomendaciones internacionales sobre investigación clínica (Declaración de Helsinki de la Asociación Médica Mundial).
Confidencialidad de los datos: Todos los autores declaran que se han seguido los protocolos establecidos por sus respectivos centros sanitarios para acceder a los datos de las historias clínicas.
Conflictos de intereses: Gil-Sierra MD participó en un advisory board de Janssen Pharmaceutica. El resto de los autores no posee conflictos de interés.