Introducción
La fenilcetonuria (PKU) es un trastorno hereditario que produce concentraciones elevadas de fenilalanina y concentraciones bajas de tirosina en la sangre. Es el trastorno hereditario más frecuente del metabolismo de los aminoácidos, con una prevalencia de 1:12.0001.
Se caracteriza por un patrón de herencia autosómica recesiva con más de 200 variantes patogénicas identificadas en el gen de la enzima fenilalanina-hidroxilasa (PAH), o de su cofactor la tetrahidrobiopterina1.
Los niveles elevados de fenilalanina en sangre son tóxicos para el cerebro y, si no se tratan, pueden afectar al desarrollo del cerebro y causar retraso mental, alteraciones del estado de ánimo y problemas de comportamiento. Los signos y síntomas de la fenilcetonuria no tratada pueden ser leves o graves, e incluyen problemas neurológicos que pueden incluir: convulsiones, hiperactividad, discapacidad intelectual, retraso en el desarrollo, problemas de comportamiento, emocionales y sociales, trastornos de salud mental, erupciones cutáneas, microcefalia, piel, cabello y ojos más claros que los de otros miembros de la familia (la fenilalanina no puede transformarse en melanina) y olor similar al de la humedad en el aliento, la piel o la orina provocados por el exceso de fenilalanina en el cuerpo, entre otros2.
La detección precoz mediante screening neonatal ha permitido a los pacientes fenilcetonúricos alcanzar un desarrollo cognitivo “aparentemente” dentro de la normalidad. Sin embargo, a pesar de la intervención dietética temprana y continuada, las personas con fenilcetonuria experimentan secuelas neurocognitivas significativas con una mayor incidencia de trastornos del ánimo, dificultades en la atención e interacción social, entre otros. Por ello, la guía Europea de PKU recomienda evaluaciones neurocognitivas periódicas durante la infancia y adolescencia y al menos una evaluación llegada la edad adulta o ante cambios drásticos en la vida del paciente3.
La mayoría de los tratamientos de la PKU pretenden mantener niveles aceptables de fenilalanina en sangre mediante la restricción de alimentos ricos en proteínas (carne, pescado, huevos, productos lácteos, frutos secos y semillas), muchos alimentos ricos en almidón, incluidos los que contienen harina (pan, pasta), así como alimentos y bebidas que contienen aspartamo. El tratamiento dietético con dietas restringidas en fenilalanina es el más habitual y eficaz1.
El Aspartamo, éster metílico de un dipéptido compuesto por L-ácido aspártico y L-fenilalanina, es un edulcorante no calórico ampliamente utilizado como endulzante de mesa y en una amplia variedad de bebidas y alimentos ya que su poder edulcorante es 200 veces mayor al de sacarosa4.
Su uso como aditivo alimentario se presenta bajo la denominación E-951. Descubierto en 1965 fue catalogado como edulcorante potente y patentado por la empresa Searlecon el nombre de Nutrasweet®. Se estima que 25 mg de aspartamo equivalen a 14 mg de fenilalanina. El aspartamo se usa como aditivo alimentario en bebidas refrescantes, zumos, helados, chicles, bollería industrial, yogures, alimentación de control de peso, entre otros. Los consumidores pueden identificar los productos alimenticios que contienen aspartamo mediante la lista de ingredientes en el etiquetado. El aspartamo al igual que todos los aditivos alimentarios, aparece bajo la etiqueta E9515, y está contraindicado en pacientes fenilcetonúricos, ya que el 56 % del mismo se convierte en fenilalanina libre.
A pesar de que existe una gran controversia sobre las deficiencias de los estudios de evaluación de su seguridad, este edulcorante está aprobado por el Join FAO/WHO Expert Committee and Food Aditives (JECFA) y por la Food and Drug Administration (FDA), entre otras4,6.
Tras su ingesta, el aspartamo se digiere por acción enzimática (esterasas y peptidasas) en sus tres componentes principales: metanol (10 % en peso de aspartamo), ácido aspártico (40 %) y fenilalanina (50%)5.
El aspartamo no penetra en el torrente sanguíneo ni se acumula en el organismo y solo los tres productos de digestión llegan al torrente sanguíneo y se encuentran en la misma forma que cuando se absorben a partir de fuentes de alimentos7.
Los excipientes de las especialidades farmacéuticas tienen la importante función de garantizar la dosificación, estabilidad y biodisponibilidad del principio activo, por lo que son sustancias esenciales para la fabricación de medicamentos. Permiten mantener la forma física, la calidad, la estabilidad, la conservación y la biodisponibilidad, así como la aceptabilidad del paciente. Los excipientes deben presentar las características requeridas para su función tecnológica pero, también, deben responder a requisitos de seguridad8.
El artículo 34 del Real Decreto 1345/2007 establece que, en la declaración de la composición del medicamento en el etiquetado, deben incluirse los excipientes de declaración obligatoria cuyo conocimiento resulta necesario para una correcta administración y uso del medicamento. La AEMPS categoriza al aspartamo como excipiente de declaración obligatoria y se debe contemplar en las advertencias del prospecto y ficha técnica la siguiente nota: “El aspartamo contiene una fuente de fenilalanina que puede ser perjudicial en caso de padecer fenilcetonuria, una enfermedad genética rara en la que el organismo no es capaz de eliminarla correctamente”9.
La omisión y la inexactitud de la información de la etiqueta del medicamento sobre los excipientes farmacéuticos pueden exponer a las personas susceptibles a inseguridad y riesgos10. Los riesgos del consumo de aspartamo en fenilcetonúricos han sido bien descritos. Un estudio realizado en pacientes con fenilcetonuria, destaca que a un 23% de estos pacientes se les había prescrito medicamentos conteniendo aspartamo en su composición y que, en el 75% de ellos, los prescriptores no consultaron la composición de los medicamentos en el momento de la prescripción11.
Los farmacéuticos facilitan la obtención de resultados terapéuticos adecuados y evitan o resuelven, en muchos casos, la aparición de Problemas Relacionados con los Medicamentos (PRM) y Resultados Negativos asociados a la Medicación (RNM)(12).
El Servicio de Indicación Farmacéutica (SIF) se define como “el SPFA prestado ante la consulta de un problema de salud (PS) concreto, para un paciente o cuidador que llega a la farmacia solicitando el remedio más adecuado para el mismo”13. Con esta definición la petición por parte del paciente o cuidador se expresa como “¿Qué me da para..?”. Pero también pueden solicitar un medicamento específico para un síntoma menor…”Deme esto para”, y en este contexto también se transforma la petición en un SIF.
Un síntoma menor se define como “…problemas de salud de carácter no grave, auto-limitados, de corta duración, que no tienen relación alguna con las manifestaciones clínicas de los otros problemas de salud que sufra el paciente, ni con los efectos, deseados o no, de los medicamentos que toma, que no precisa por tanto diagnóstico médico y que responde o se alivia con un tratamiento sintomático”14). El tratamiento farmacológico indicado para estos PS no graves es un MSR. En la Tabla 1podemos ver la clasificación de síntomas menores.
Tabla 1. Clasificación de síntomas menores15.
| Grupo | Síntoma menor |
|---|---|
| Respiratorios | Congestión nasal Síndrome gripal y catarral Tos |
| Dolor moderado | Cefalea Dolor articular y de espalda Dolor dentario Dolor de garganta Dolor menstrual o dismenorrea primaria |
| Digestivos | Acidez o pirosis Aerofagia, flatulencia y meteorismo Diarrea aguda Estreñimiento Vómitos |
| Dermatológicos | Acné Aftas Dermatitis Heridas cutáneas Herpes labial Hiperhidrosis Picaduras Pie de atleta Quemaduras cutáneas Urticaria |
| Otros | Estrés Fiebre Hemorroides Ojo rojo Ojo seco Vaginitis Varices en miembros inferiores |
Se debe fomentar la seguridad en el uso de los MSR en pacientes con fenilcetonuria, debido a la posible aparición de RNM causados por este grupo de medicamentos con aspartamo.
Objetivo
El objetivo principal es la revisión de los medicamentos sin receta comercializados en España hasta marzo de 2023 y que contienen aspartamo en su composición.
Los objetivos secundarios son:
Métodos
Estudio descriptivo observacional de la presencia del excipiente aspartamo en MSR.
En el buscador de la base de datos BOT plus se obtuvieron todos los medicamentos comercializados en España que contenían aspartamo hasta 31 de marzo de 2023. Se seleccionaron solo los MSR.
Se consultaron las fichas técnicas utilizando el Centro de información online de medicamentos de la AEMPS (CIMA) y el apartado de composición de BOT plus, y los datos obtenidos se registraron en una tabla con las siguientes variables: denominación del MSR, cantidad de aspartamo en miligramos por forma farmacéutica o por 1 mililitro, grupo de síntoma menor al que pertenece, edad a partir de la cual está indicado y, por último, alternativa MSR sin aspartamo.
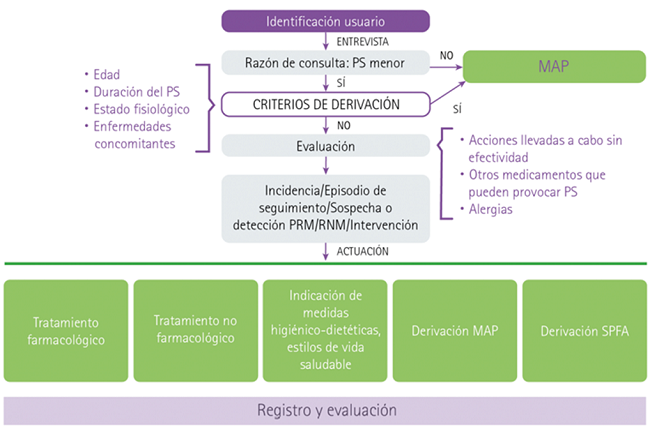
En el desarrollo del método utilizado, se tuvo en cuenta que el farmacéutico va utilizar los MSR en una parte del SIF según la definición de Foro de Atención Farmacéutica en Farmacia Comunitaria (FORO AF-FC)13como se indica en la Figura 1.
El procedimiento del SIF se divide en cuatro pasos:
Resultados
De los 570 medicamentos comercializados en España hasta marzo de 2023 con aspartamo en su composición, se revisaron la totalidad de las fichas técnicas para verificar la existencia de este excipiente y registrar las variables que a continuación iremos describiendo. De estos 570 están clasificados como MSR 58, es decir, un 10 % de los medicamentos con aspartamo.
Las dosis del edulcorante existentes en los MSR revisados se encuentran entre 0,75 y 70 mg por forma farmacéutica o por dosis media en casos de los jarabes. Teniendo en cuenta que la IDA (ingesta diaria admisible) de Aspartamo ha sido establecida en 40 mg/kg2,16, las cantidades utilizadas en los MSR es mínima por lo que con lo ingerido con la posología habitual nunca se llegaría a sobrepasar la ingesta diaria recomendada (IDA) de aspartamo, representando el mayor peligro de posible aparición de PRM que deriven en RNM la población fenilcetonúrica. Para los pacientes que padecen esta condición médica, la IDA no es aplicable. Aun siendo usado como excipiente, el umbral para estos pacientes fenilcetonúricos será cero.
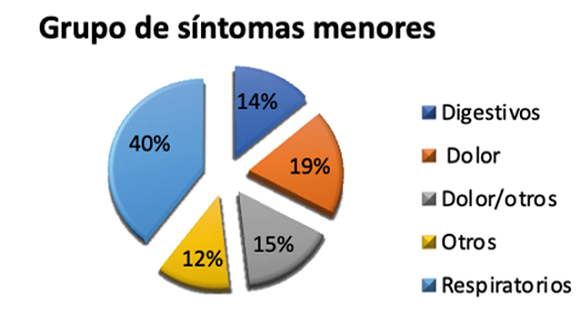
Atendiendo a la clasificación por Grupo de Síntomas Menores, el grupo mayoritario es el que corresponde a medicamentos para síntomas respiratorios, seguido por los que corresponde a dolor o dolor/otros, digestivos y, por último, los clasificados para otros síntomas menores15. Ver Figura 2.
Respiratorios: 23 medicamentos sin receta
Dolor: 11 medicamentos sin receta
Dolor/otros: 9 medicamentos sin receta
Digestivos: 8 medicamentos sin receta
Otros: 7 medicamentos sin receta
Analizando la variable de la edad a partir de la cual se puede administrar los MSR estudiados, se obtiene el dato de que el 83% de estos MSR están indicados en menores de 18 años. Se debe incidir en la importancia del cuidador de pacientes con fenilcetonuria menores de 18 años, no solo por el porcentaje mayoritario de MSR con aspartamo, sino por las secuelas que puede acarrear a esa edad. Interviniendo en la educación sanitaria de estos cuidadores también evitaremos PRM desde el SIF.
En la Figura 3se desglosan los resultados por edades.
Tras revisar los grupos terapéuticos de los distintos niveles de la clasificación ATC, se comprobó la existencia de MSR alternativos que no contienen aspartamo como excipiente. Todos los MSR poseen un equivalente sin aspartamo ya sea con igual forma farmacéutica y distinto fabricante, con el mismo principio activo y diferente forma farmacéutica o un principio activo diferente con la misma acción terapéutica.
Podemos ver dentro del resultado del trabajo, que el farmacéutico comunitario puede disponer de un amplio arsenal terapéutico, el cual se plasma en la Tabla 2para realizar el SIF en pacientes con fenilcetonuria.
Tabla 2. Tabla de MSR con aspartamo para uso por el SIF en la Atención Farmacéutica a pacientes fenilcetonúricos. Periodo hasta marzo-2023.
| NOMBRE REGISTRADO | CONTENIDO EN ASPARTAMO | GRUPO DE SÍNTOMA MENOR | EDAD | ALTERNATIVA SIN ASPARTAMO |
|---|---|---|---|---|
| ALKA-SELTZER® 2,1 g 20 COMPRIMIDOS EFERVESCENTES | 10 mg/comp | Digestivos | Niños 12-15 años | Bicarbonato MN® 1g sobres |
| ANTIDOL® 500 mg 20 SOBRES GRANULADO ORAL | 23,62 mg/sobre | Dolor/otros | Niños 12-15 años | Antidol® 500 mg comp recub® |
| ANTIDOL® NIÑOS 325 mg 20 SOBRES GRANULADO ORAL | 15,35 mg/sobre | Dolor/otros | Niños<12 | Antidol® 650 mg comp. Ajustar dosis |
| APIRETAL® 325 mg 24 COMPRIMIDOS BUCODISPERSABLES | 15,6 mg/comp | Dolor/otros | Niños<12 | Apiretal® 100mg/ml sol oral. Ajustar dosis |
| APIRETAL® 500 mg 12 COMPRIMIDOS BUCODISPERSABLES | 24 mg/comp | Dolor/otros | Niños 12-15 años | Apiretal® 100mg/ml sol oral.Ajustar dosis |
| APIRETAL® 500 mg 24 COMPRIMIDOS BUCODISPERSABLES | 24 mg/comp | Dolor/otros | Niños 12-15 años | Apiretal® 100mg/ml sol oral. Ajustar dosis |
| ARITOS® 2 mg/ml SOLUCIÓN ORAL 1 FRASCO 200 ml | 2 mg/ml | Respiratorios | Niños 6-12 años | Bisolvon antitusivo®, Cinfatos® |
| ASPIRINA® 500 mg 10 SOBRES GRANULADO ORAL | 5 mg/sobre | Dolor/otros | >16 años | Aspirina® Comp 500 mg |
| ASPIRINA® 500 mg 20 SOBRES GRANULADO ORAL | 5 mg/sobre | Dolor/otros | >16 años | Aspirina® Comp 500 mg |
| BACTIL FLAS® 10 mg 10 LIOFILIZADOS ORALES | 1 mg/liofilizado | Respiratorios | >12 años | Bactil flas® Comp recubiertos 10 mg |
| BACTIL FORTE FLAS® 20 mg 10 LIOFILIZADOS ORALES | 2 mg/liofilizado | Respiratorios | <12 años | Bactil forte flas® Comp recubiertos 20 mg |
| BIODRAMINA® 20 mg 6 CHICLES MEDICAMENTOSOS | 3 mg/chicle | Otros | >6 años | Biodramina® comp 50 mg/ Ajustar dosis |
| BIODRAMINA® 20 mg 12 CHICLES MEDICAMENTOSOS | 3 mg/chicle | Otros | >6 años | Biodramina® comp 50 mg/ Ajustar dosis |
| BRONCHOGRIP® 10 SOBRES POLVO PARA SOLUCIÓN ORAL | 12 mg/sobre | Respiratorios | >15 años | Antigripal: Bisolgrip®, pharmagrip forte® / Ajustar dosis / Principios activos no exactamente iguales |
| BUCOMETASANA® 20 COMPRIMIDOS PARA CHUPAR | 6 mg/comp | Dolor | >18 años | Deratin complex®: los principios activos varian |
| BUCOMETASANA® 30 COMPRIMIDOS PARA CHUPAR | 6 mg/comp | Dolor | >18 años | Deratin complex®: los principios activos varian |
| CINFAMUCOL ACETILCISTEINA® 200 mg 20 SOBRES POLVO PARA SOLUCIÓN ORAL | 6,67 mg/sobre | Respiratorios | >12 años | Acetilcisteina® Sandoz Care EFG 200 mg sobres |
| CINFAMUCOL ACETILCISTEINA FORTE® 600 mg 10 SOBRES POLVO PARA SOLUCIÓN ORAL | 20 mg/sobre | Respiratorios | >18 años | Cinfamucol Acetilcisteina forte® 600 mg comp eferv |
| CINFATOS COMPLEX® SUSPENSION ORAL 1 FRASCO 125 ml | 5 mg/5ml | Respiratorios | >12 años | Pharmatusgrip® sobres/ Ajustar dosis |
| COULDINA CON IBUPROFENO® 400 mg/2 mg/7,5 mg 20 COMPRIMIDOS EFERVESCENTES | 25 mg/comp | Respiratorios | >12 años | Grippostad® con ibuprofeno/Ajustar dosis/ Ajustar principios activos |
| COULDINA INSTANT CON ACIDO ACETILSALICILICO® 10 SOBRES GRANULADO EFERVESCENTE | 20 mg/sobre | Respiratorios | >16 años | Couldina con AAS® comp efervescentes |
| COULDINA INSTANT CON ACIDO ACETILSALICILICO® 20 SOBRES GRANULADO EFERVESCENTE | 20 mg/sobre | Respiratorios | >16 años | Couldina con AAS® comp efervescentes |
| EFFERALDOL FLAS® 500 mg 16 COMPRIMIDOS BUCODISPERSABLES | 4,8 mg/comp | Respiratorio | >18 años | Efferalgan® 500 mg comp efervescentes o caps |
| ESPIDIDOL® 400 mg 20 SOBRES GRANULADO PARA SOLUCIÓN ORAL (SABOR MENTA) | 25 mg/sobre | Dolor | >18 años | Espididol® Comp recubiertos 400 mg |
| FLUIMUCIL® 200 mg 30 SOBRES GRANULADO PARA SOLUCIÓN ORAL | 25 mg/sobre | Otros | >12 años | Acetilcisteina® Sandoz Care EFG 200 mg sobres |
| FLUIMUCIL COMPLEX® 500 mg/200 mg 12 COMPRIMIDOS EFERVESCENTES | 60 mg/comp | Otros | >12 años | Acetilcisteina® Sandoz Care EFG 200 mg sobres + paracetamol comp 500 mg |
| FLUIMUCIL FORTE® 600 mg 20 COMPRIMIDOS EFERVESCENTES | 20 mg/comp | Respiratorios | >18 años | Acetilcisteina® Sandoz Care EFG 600 mg comp eferv |
| FODONAL® 3 mg 24 PASTILLAS PARA CHUPAR (SABOR LIMÓN) | 3,409 mg/comp | Dolor | >6 años | Tantum verde® 3 mg pastillas para chupar sabor eucalipto o naranja/miel |
| FODONAL® 3 mg 24 PASTILLAS PARA CHUPAR (SABOR MIEL Y NARANJA) | 3,409 mg/comp | Dolor | >6 años | Tantum verde® 3 mg pastillas para chupar sabor eucalipto o naranja/miel |
| FORTASEC FLAS® 2 mg 12 LIOFILIZADOS ORALES | 0,75 mg/liof | Digestivos | >12 años | Fortasec® Caps 2 mg |
| GAVISCON® 24 COMPRIMIDOS MASTICABLES (SABOR FRESA) | 8,8 mg/comp | Digestivos | >12 años | Gaviscon® Sobres sabor menta |
| GAVISCON® 24 COMPRIMIDOS MASTICABLES (SABOR MENTA) | 8,8 mg/comp | Digestivos | >12 años | Gaviscon® Sobres sabor menta |
| GAVISCON® 48 COMPRIMIDOS MASTICABLES (SABOR MENTA) | 8,8 mg/comp | Digestivos | >12 años | Gaviscon® Sobres sabor menta |
| GAVISCON FORTE® 24 COMPRIMIDOS MASTICABLES | 5,863 mg | Digestivos | >12 años | Gaviscon® Sobres sabor menta |
| GAVISCON FORTE® 48 COMPRIMIDOS MASTICABLES | 5,863 mg | Digestivos | >12 años | Gaviscon® Sobres sabor menta |
| GELOCATIL® 325 mg 12 SOBRES GRANULADO ORAL | 15,35 mg/sobre | Dolor/otros | >8 años | Gelocatil® 650 mg comp. Ajustar dosis |
| GELOCATIL® 500 mg 12 SOBRES GRANULADO ORAL | 23,62 mg/sobre | Dolor/otros | >12 años | Gelocatil® Comp 1g. Ajustar dosis |
| GRIPALNORM® 10 SOBRES GRANULADO PARA SOLUCIÓN ORAL | 30 mg/sobre | Respiratorios | >18 años | Gripalcold® sobres polvo para sol oral |
| IBUDOL RAPID® 400 mg 20 SOBRES GRANULADO PARA SOLUCIÓN ORAL | 30 mg/sobre | Dolor | >12 años | Ibudol® 400 mg sobres susp oral |
| ILVIGRIP EXPECTORANTE® 10 SOBRES POLVO PARA SOLUCIÓN ORAL | 6 mg/sobre | Respiratorios | >15 años | Antigripal: Bisolgrip®, pharmagrip forte® / Ajustar dosis / Principios activos no exactamente iguales |
| MUCIBRON FORTE® 6 mg/ml SOLUCIÓN ORAL 1 FRASCO 250 ml | 5 mg/1 ml | Respiratorios | >2 años | Ambroxol Stada® 6mg/ml o Mucosan® 6mg/ml |
| NICOTINELL® MINT 1 mg 36 COMPRIMIDOS PARA CHUPAR | 9,40 mg/comp | Otros | >18 años | Niquitin® comp 1,5 mg ajustar dosis |
| NICOTINELL® MINT 2 mg 36 COMPRIMIDOS PARA CHUPAR | 9,40 mg/comp | Otros | >18 años | Niquitin® comp 1 mg o Nicorette® 2 mg |
| NICOTINELL® MINT 2 mg 96 COMPRIMIDOS PARA CHUPAR | 9,40 mg/comp | Otros | >18 años | Niquitin® comp 1 mg o Nicorette® 2 mg |
| NORMODOL EFG® 400 mg 12 SOBRES GRANULADO PARA SOLUCIÓN ORAL | 20 mg/sobre | Dolor | >12 años | Espididol® 400 mg comp recub |
| NORMODOL EFG® 400 mg 20 SOBRES GRANULADO PARA SOLUCIÓN ORAL | 20 mg/sobre | Dolor | >12 años | Espididol® 400 mg comp recub |
| NORMOFLUDIL® 600 mg 20 COMPRIMIDOS DISPERSABLES | 35 mg/comp | Respiratorio | >2 años | Acetilcisteina® Sandoz Care EFG 600 mg comp eferv |
| NORMOFLUDIL EFG® 200 mg 30 SOBRES GRANULADO PARA SOLUCIÓN ORAL | 10 mg/sobre | Respiratorio | >2 años | Acetilcisteina® Sandoz Care EFG 200 mg sobres |
| NORMOGRIP® 10 SOBRES GRANULADO PARA SOLUCIÓN ORAL | 30 mg/sobre | Respiratorio | >14 años | Normogrip® Caps |
| NOTUS ANTITUSIVO Y EXPECTORANTE® 2 mg/ml + 20 mg/ml SOLUCIÓN ORAL 1 FRASCO 200 m | 7 mg/1 ml | Respiratorio | >6 años | Cinfatos expectorante® jbe |
| NOTUS MUCUS® 600 mg 10 COMPRIMIDOS EFERVESCENTES (SABOR LIMON) | 20 mg/comp | Respiratorio | >7 años | Acetilcisteina® Sandoz Care EFG 600 mg comp eferv |
| NOTUS MUCUS® 600 mg 20 COMPRIMIDOS EFERVESCENTES (SABOR LIMON) | 20 mg/comp | Respiratorio | >7 años | Acetilcisteina® Sandoz Care EFG 600 mg comp eferv |
| OKALTUS® 10 mg/100 mg 20 SOBRES SOLUCION ORAL 5 ml | 35 mg/sobre | Respiratorio | >6 años | Cinfatos expectorante® sobres |
| PROPALGAR® 3 mg 24 PASTILLAS PARA CHUPAR | 3,40 mg/comp | Dolor | >6 años | Tantum verde® 3 mg pastillas para chupar sabor eucalipto o naranja/miel |
| SALVACOLINA FLAS® 2 mg 12 COMPRIMIDOS BUCODISPERSABLES | 9 mg/comp | Digestivo | >12 años | Salvacolina® Comp 2 mg |
| TANTUM VERDE® 3 mg 20 PASTILLAS PARA CHUPAR (SABOR LIMÓN) | 3,26 mg/comp | Dolor | >6 años | Tantum verde® 3 mg pastillas para chupar sabor eucalipto o naranja/miel |
| TANTUM VERDE® 3 mg 20 PASTILLAS PARA CHUPAR (SABOR MENTA) | 3,50 mg/comp | Dolor | >6 años | Tantum verde® 3 mg pastillas para chupar sabor eucalipto o naranja/miel |
| TERMALGIN RESFRIADO® 10 SOBRES POLVO PARA SOLUCIÓN ORAL | 38 mg/sobre | Respiratorio | >15 años | Vincigrip forte® sobres. Contiene tb clorfeniramina. Ajustar dosis |
Discusión
Atendiendo a los resultados obtenidos y conociendo que el autocuidado y la automedicación son habitualmente los tratamientos de elección en el manejo de los síntomas menores, desde el SIF, en pacientes con fenilcetonuria, intervendremos:
Actuando directamente dispensando MSR sin aspartamo ante la petición de “¿Qué me da para..?”
Intercambiando MSR demandados por el paciente o cuidador (“deme esto para”), por otro MSR sin aspartamo como excipiente. Existe siempre una alternativa terapéutica para alcanzar la seguridad del paciente con fenilcetonuria.
En cualquiera de las dos situaciones se evitarían PRM que nos llevarían a RNM en pacientes fenilcetonúricos, con lo que la prestación de SPFA puede no solo lograr una mejora en el proceso y resultados derivados del uso del medicamento, sino que también podría lograr una reducción de los gastos derivados del uso de otros recursos sanitarios (disminución del número de medicamentos, ingresos hospitalarios, visitas al médico y/o los servicios de urgencias)17. Para alcanzar la implantación de un SPFA y que éste sea sostenible, la mejor práctica es desarrollar intervenciones de manera sistemática18.
Tras el análisis de la edad a partir de la que se pueden usar los MSR con aspartamo estudiados, se propone educación sanitaria a los cuidadores sobre la composición de los medicamentos que puede incluir el aspartamo como excipiente en su elaboración. Sin olvidarnos de los médicos pues, según Newbould et al11, a un 23% de pacientes fenilcetonúricos se les había prescrito medicamentos conteniendo aspartamo en su composición y que, en el 75% de ellos, los prescriptores no consultaron la composición de los medicamentos en el momento de la prescripción. La educación sanitaria dada por los farmacéuticos ha de hacerse extensiva a los centros de salud reuniendo a prescriptores y pacientes, siendo a su vez una herramienta para dar visibilidad desde la Farmacia Comunitaria a las enfermedades raras.
Por último, señalar que aunque en este estudio se incide en evitar la inseguridad del paciente fenilcetonúrico en el autocuidado y automedicación mediante el uso correcto de los medicamentos, faltaría una evaluación del impacto económico del SIF en estos pacientes para la optimización del uso de los recursos del sistema sanitario19.
Los profesionales sanitarios, entre ellos los farmacéuticos, en su continua formación y actualización de conocimientos, afrontan el reto del manejo de novedosos MSR cuyas indicaciones y principios activos condicionan su uso y potenciales efectos adversos e interacciones, entre otros aspectos, al tiempo que algunos excipientes como el aspartamo pueden generar, excepcionalmente, inseguridad durante su uso20.
Aun siendo los MSR formulados con aspartamo como excipiente una minoría respecto al total de las referencias autorizadas en España, la prevención de los riesgos derivados de este excipiente exige evitar su uso, prescripción, dispensación e indicación a pacientes con fenilcetonuria.
Conclusiones
La actuación del farmacéutico comunitario para aplicar el SIF es de gran importancia en pacientes con fenilcetonuria.
Todos los MSR poseen un equivalente sin aspartamo ya sea con igual forma farmacéutica y distinto fabricante, con el mismo principio activo y diferente forma farmacéutica o un principio activo diferente con la misma acción terapéutica.
Esta revisión bibliográfica facilita a los Farmacéuticos Comunitarios una herramienta de gran utilidad que agiliza la labor asistencial en pacientes con fenilcetonuria durante el Servicio de Indicación Farmacéutica.