Ciprofloxacino oral discontinuo en resección transuretral de próstata. resultados iniciales.
Discontinuos oral ciprofloxacin for transurethral resection of the prostate
Juan Pablo Valdevenito, Raúl Valdevenito, Álvaro Gómez y Moisés Russo1.
Servicio de Urología Hospital Clínico Universidad de Chile. Santiago.
1Interno de Medicina, Universidad de Chile. Santiago. Chile.
Dirección para Correspondencia
]]>
RESUMEN
Objetivos: Describir las complicaciones infecciosas con el uso de ciprofloxacino oral discontinuo en resección transuretral de próstata (RTU-P). Ponderar la influencia de los antecedentes clínicos, hallazgos y complicaciones intraoperatorias y evolución postoperatoria en el desarrollo de dichas complicaciones. Comparar los resultados con estudio previo de igual metodología en que se usó esquema antibiótico continuo hasta el retiro de la sonda uretrovesical.
Método: Estudio prospectivo abierto de 53 pacientes consecutivos con orina estéril no usuarios de sonda uretrovesical, sometidos a RTU-P. Los pacientes recibieron ciprofloxacino 500 mg. oral (4 dosis) antes de su traslado a pabellón, la noche de la operación, la mañana siguiente de ésta y antes de retirar la sonda uretrovesical. Se excluyeron 3 pacientes después de su incorporación (5,6%) y no hubo pérdidas en el seguimiento.
Resultados: Se analizan 50 pacientes. Se presentó fiebre en 8 pacientes (16%). Se presentó infección clínica sistémica en 3 pacientes (6%). No se presentó bacteriuria postoperatoria aislada. El antecedente de ITU previa presentó asociación estadística con el desarrollo de infección clínica sistémica (p= 0,007) y con el hallazgo de prostatitis crónica activa en la biopsia operatoria (p= 0,002).
conclusión: Probablemente el antecedente de ITU previa hace menos aconsejable el uso de esquema antibiótico discontinuo en RTU-P, aunque se requiere de un mayor número de pacientes para confirmar este planteamiento. Al comparar estos resultados con aquellos obtenidos usando un esquema antibiótico continuo, se observa una significativa mayor frecuencia de fiebre durante la evolución (p= 0,022).
Palabras clave: Antibióticos. Resección transuretral de próstata.
SUMMARY
Objetives: To describe the rate of infectious complications using a discontinuous scheme of oral ciprofloxacin in transurethral resection of the prostate (TUR-P). To try to weigh the influence of clinical background, operative complications and postoperative outcome on the development of such complications. To compare the results to those obtained with equal methodology using antibiotics in a continual scheme until the catheter removal. ]]>
Method: a prospective open study was designed including 53 consecutive patients with sterile urine and without indwelling catheter subjected to TUR-P. Patients received oral ciprofloxacin 500 mg (4 doses) before going to the surgical room, the night of surgery, next morning of surgery and before catheter removal. Three patients were excluded after incorporation (5,6%) and all the remainders completed follow up.
Results: fifty patients are analyzed. Fever was present in 8 patients (16%). Systemic clinical infection was present in 3 patients (6%). No isolated-germ postoperative bacteriuria was present. Previous urinary infection (UTI) was statistically associated to systemic clinical infection (p= 0,007) and to active chronic prostatitis on operative biopsy (p= 0,002).
Conclusion: probably previous UTI antecedent made less advisable the discontinuous scheme use in TUR-P, although a greater number of patients is needed to confirm these statement. When these results are compared to those using antibiotics in a continual scheme until catheter removal, a significant higher frequency of fever is seen (p= 0,022).
Keywords: Antibiotics. Prostatic transurethral resection.
Introducción
La septicemia sigue siendo una de las principales causas de muerte en la resección transuretral de próstata (RTU-P): Murphy y cols. reportan la muerte de 6 pacientes en 1.604 intervenciones (0,34%), 4 de las cuales fueron por sepsis (67%); Mebust y cols. reportan 9 defunciones en 3.885 cirugías (0,23%), 5 de las cuales fueron por sepsis (56%) (1, 2).
Los principales factores de riesgo de complicaciones infecciosas de la RTU-P son la bacteriuria preoperatoria, el uso preoperatorio de sonda uretrovesical y los estados inmunodepresores. Se sabe que existen 2 momentos críticos para el desarrollo de complicaciones infecciosas graves después de una RTU-P: el periodo operatorio y postoperatorio inmediato y el día del retiro de la sonda uretrovesical (3).
En pacientes sin bacteriuria preoperatoria el uso de antibióticos ha reducido la bacteriuria postoperatoria en promedio de un 26% a un 9,1% y la septicemia de un 4,4% a un 0,7% (4). Sin embargo hay que tener en cuenta que las definiciones de bacteriuria significativa y septicemia no son homogéneas en los diferentes estudios y en muchos de éstos no es posible saber el efecto del uso de sonda uretrovesical antes de la cirugía en los resultados obtenidos.
La profilaxis antimicrobiana debe ser administrada antes de la cirugía y permitir un adecuado nivel tisular al momento de ésta, sin sobrepasar las 24 a 48 hrs. de uso (5). Sin embargo existe evidencia que hace razonable plantear el uso de antimicrobianos en RTU-P después de este período: un 2 a 10% de riesgo de desarrollar bacteriuria por cada día de uso de la sonda uretrovesical (6, 7) y el riesgo de bacteremia al retirarla (1, 8). La utilidad del uso de antibióticos más allá del retiro de la sonda Foley uretrovesical no estaría claramente demostrada (3).
]]> En un estudio comparativo, prospectivo y aleatorio previo hemos demostrado una significativa menor frecuencia de infección urinaria postoperatoria (representada por una menor bacteriuria postoperatoria) con el uso de un esquema de Cefazolina 1 gr. intravenoso preoperatorio y cada 8 hrs. durante el primer día (3 dosis) seguido de Ciprofloxacino 250 mg. oral cada 12 hrs. hasta el retiro de la sonda uretrovesical, al comparar con el uso de un esquema de Cefazolina 1 gr. intravenoso preoperatorio y a las 8 hrs. postoperatorio (2 dosis) seguido de Nitrofurantoína 100 mg oral en la noche hasta el retiro de la sonda (9). Sin embargo resulta claramente más sensato el uso de una droga única, la cual podría administrarse sólo en los momentos críticos de desarrollo de complicaciones infecciosas graves, en un afán se reducir el uso de antibióticos en pacientes con bajo riesgo de complicaciones infecciosas sometidos a RTU-P. Es por esto que planteamos un nuevo estudio en pacientes con orina estéril, no usuarios de sonda uretrovesical utilizando 4 dosis de Ciprofloxacino oral en forma discontinua, intentando a la vez ponderar la influencia de los antecedentes clínicos, hallazgos y complicaciones intraoperatorios y evolución postoperatoria en el desarrollo de dichas complicaciones. Estos resultados serán comparados con el primero de los esquemas antes descritos.
Material y Método
El estudio fue discutido y aprobado en reunión clínica del Servicio de Urología del Hospital Clínico de la Universidad de Chile y se obtuvo consentimiento informado de todos los pacientes enrolados. Se incluyeron pacientes con orina estéril, no usuarios de sonda Foley uretrovesical antes de la cirugía. Los criterios de exclusión fueron: a) historia de hipersensibilidad a ciprofloxacino; b) uso de antimicrobianos 7 días antes de la cirugía; c) Diabetes Mellitus insulino requirente; d) uso crónico de corticoides o inmunosupresores; e) usuarios de prótesis cardiacas y vasculares; f) insuficiencia renal crónica (creatinina sérica mayor de 2,0 mg/dl).
Corresponde a un estudio abierto prospectivo que incluyó pacientes consecutivos sometidos a RTU-P entre Marzo y Diciembre de 2004, los cuales recibieron 4 dosis de Ciprofloxacino 500 mg. oral (Grifociprox-®, Laboratorio Chile SA): antes de su traslado a pabellón, la noche de la operación, la mañana siguiente de ésta y 1 hora antes del retiro de la sonda uretrovesical. En el caso de necesidad de reoperación se administró Ciprofloxacino 500 mg. oral antes del traslado del paciente a pabellón y a las 12 hrs. de haber sido reintervenido.
Se consignó en un protocolo estandarizado la edad, patologías asociadas, clasificación de la Sociedad Americana de Anestesia (ASA) (10) y los antecedentes de infección urinaria y biopsia prostática previas. La cirugía se realizó bajo anestesia espinal o peridural; se aseptizó la piel con povidona yodada al 10%, se utilizó Steri-Drape-® (3M) para aislar escroto, periné y ano, y se usó como lubricante vaselina líquida estéril. La RTU-P se efectuó con resectoscopio Storz 24F sin flujo continuo utilizando solución de glicina al 1,5% (Baxter-®). Al término de la cirugía se instaló sonda Foley uretrovesical de latex siliconado semirrígida 20 o 22F (Porges-®) la que se conectó a recolector urinario cerrado. Se registró el tiempo quirúrgico y cirugías transuretrales anexas, e interrogó al cirujano a la salida de pabellón sobre perforación de la cápsula prostática y presencia de secreción purulenta al corte del tejido prostático.
En el postoperatorio se realizó irrigación vesical con solución salina al 0,9% generalmente hasta el día previo al retiro de la sonda y en caso de obstrucción de ésta por coágulos se lavó con jeringa urológica usando igual solución. Diariamente se consignó el número de lavados vesicales, necesidad de recambio de sonda Foley uretrovesical, necesidad de reoperación (revisión endoscópica) y otras complicaciones hospitalarias, así como también la necesidad de transfusión sanguínea. Para la evaluación de las complicaciones infecciosas se registró cualquier alza térmica mayor de 37,°C axilar. En caso de temperatura axilar igual o superior a los 38°C (fiebre alta) se solicitó proteína C reactiva (PCR) asociada a urocultivo con recuento de colonias si el paciente se encontraba sin irrigación vesical (toma de muestra por punción de la sonda, con aplicación previa de antiséptico). La persistencia de fiebre alta (segundo día) o una PCR superior a 40 mg/L motivó toma de muestras para hemocultivos y el cambio de esquema antibiótico, considerándose este hecho como complicación infecciosa. A todos los pacientes se les tomó urocultivo de muestra de orina de 2° chorro entre las 2 y 3 semanas después del retiro de la sonda Foley uretrovesical. Se registró además los días de uso de sonda Foley y de hospitalización, así como el informe anatomopatológico que consignaba los gramos de tejido resecado y la presencia o ausencia de prostatitis crónica con o sin componente activo (presencia de leucocitos polimorfonucleares).
Análisis estadístico: Para el análisis de los resultados se consideraron como sucesos clínicos relevantes: 1) Fiebre (temperatura axilar igual o superior a 37,5°C); 2) Bacteriuria postoperatoria, evaluada en forma independiente y a ciegas por el laboratorio de microbiología (se consideró significativa 100.000 UFC por ml de orina) y 3) Infección clínica sistémica (persistencia de temperatura axilar superior a 38°C y/o PCR mayor de 40 mg/L) con o sin confirmación microbiológica. Los datos obtenidos fueron ingresados en el programa Stata 6.0 y analizados estadísticamente con la Prueba de chi-cuadrado para la comparación de proporciones y t de Student para la comparación de promedios. La significación estadística se definió como un p<0.05.
Resultados
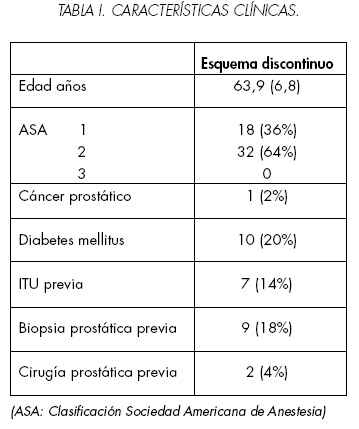
]]> Se ingresaron 53 pacientes, debiendo excluirse tres después de su incorporación (5,6%): uno por no contar con urocultivo reciente, uno por decidirse finalmente cirugía abierta y otro por ser portador de válvula cardiaca. Se analizan 50 pacientes, No hubo pérdidas en el seguimiento. Se demostraron 5 violaciones de protocolo. Tres paciente recibieron una dosis extra de antibiótico en la inducción anestésica: dos pacientes recibieron Cefazolina 1 gr y uno Ciprofloxacino 200 mg intravenosos (6%). Dos pacientes no recibieron la segunda dosis de Ciprofloxacino oral (4%).Las características clínicas de los pacientes se muestran en la Tabla I. Diez pacientes eran diabéticos (20%) y siete pacientes tenían antecedente de ITU (14%). La Tabla II resume los parámetros quirúrgicos de los pacientes estudiados. Se reporta perforación de la cápsula prostática en nueve pacientes (18%) y secreción purulenta al corte del tejido prostático en siete (14%). Los parámetros postoperatorios y complicaciones se muestran en la Tabla III. Seis pacientes requirieron de lavado de la sonda Foley uretrovesical por obstrucción por coágulos (12%); un paciente (2%) fue sometido a revisión endoscópica por hemovejiga, requiriendo además transfusión de 2 unidades de glóbulos rojos. No hubo mortalidad en la serie. Los resultados de la histopatología se muestran en la Tabla IV. El peso promedio de tejido resecado fue 17,1 gramos; 48 pacientes (96%) presentaron algún grado de prostatitis crónica en su biopsia y 17 presentaron componente activo (34%).
La Tabla V muestra los sucesos clínicos relevantes. Ocho pacientes presentaron fiebre en algún momento de la evolución (16%), la que se presentó después del primer día postoperatorio, periodo en que no existía cobertura antibiótica. Tres pacientes no diabéticos presentaron infección clínica sistémica (6%): un paciente evolucionó con obstrucción de la sonda uretrovesical por coágulos requiriendo seis lavados vesicales, recambio de ésta y finalmente revisión endoscópica por hemovejiga al 7° día postoperatorio; presentó fiebre alta durante un total de cuatro días y PCR seriada de 89 y 190 mg/L; su urocultivo demostró un Enterobacter cloacae sólo sensible a amikacina e imipenem, siendo tratado satisfactoriamente con el primero de los antibióticos ya nombrados. Un segundo paciente, con antecedente de ITU previa 6 meses antes, presentó fiebre alta al 2° y 3° día postoperatorio con PCR de 69 mg/L y urocultivo negativo, siendo tratado con Ciprofloxacino oral con buena respuesta. Un tercer paciente, también con antecedente de ITU previa tres semanas antes, presentó fiebre alta al 3° y 4° día postoperatorio con PCR de 106 mg/L y urocultivo negativo, siendo tratado satisfactoriamente con Ciprofloxacino oral. Los tres pacientes antes citados tuvieron hemocultivos negativos. No se presentó bacteriuria postoperatoria tardía en el resto de los pacientes ni se objetivó episodios de epididimitis aguda o uretritis.
Se ponderó la influencia de los antecedentes clínicos, hallazgos y complicaciones intraoperatorios y la evolución postoperatoria en el desarrollo de las complicaciones infecciosas. El antecedente de ITU previa presentó asociación estadística con el desarrollo de infección clínica sistémica (p= 0,007) y con el hallazgo de prostatitis crónica activa en la biopsia operatoria (p= 0,002). La asociación entre ITU previa y fiebre durante la evolución no alcanzó significación estadística (0,071).
]]> Discusión
Este es un estudio prospectivo de pacientes consecutivos con bajo riesgo de complicaciones infecciosas sometidos a RTU-P, en el cual se utiliza un esquema de Ciprofloxacino oral con dosis sólo en los momentos críticos de desarrollo de complicaciones infecciosas graves (discontinuo), en un afán de reducir al máximo el uso de antibióticos en dicha cirugía. Tiene la limitante de ser un estudio abierto por lo cual está expuesto a una mayor cantidad de sesgos. Tiene a su favor que un porcentaje bajo de pacientes fue excluido después de la incorporación al estudio (5,6%) y que todos los pacientes fueron evaluados al término de éste.
Algunos estudios no han encontrado diferencias en la incidencia de fiebre en pacientes sometidos a RTU-P con o sin uso de antibióticos, atribuyéndose la fiebre a factores como la liberación de proteínas tisulares durante la operación, endotoxinas que contaminan la sonda uretrovesical o substancias exógenas (3, 11-15). Sin embargo otros estudios sí han encontrado una menor frecuencia de algún registro de fiebre en la evolución y una menor temperatura máxima promedio en aquellos pacientes que han recibido tratamiento antibiótico al compararlos con los que no lo recibieron (16-18).
El presente estudio que usa antibióticos en forma discontinua, muestra que un 16% de los pacientes presentó fiebre, especialmente en el periodo en que no existía cobertura antibiótica. Esto resulta ser significativamente mayor (p= 0,022) que el 2% que se encontró en un estudio nuestro anterior de igual metodología con un grupo similar de 45 pacientes en que se usó antibióticos en forma continua hasta el retiro de la sonda uretrovesical (9), y puede explicarse por la reducción de los episodios de bacteremia con el uso de antibióticos (Tabla VI).
Los microorganismos que determinan complicaciones infecciosas después de RTU-P pueden ubicarse en la próstata o uretra e incluso en instrumental contaminado o líquidos de irrigación (3, 5, 19, 20). La etiología bacteriana de la prostatitis crónica se ha atribuido fundamentalmente a enterobacterias Gram negativas aunque también a Streptococcus faecalis (21). Por otro lado la flora microbiana uretral está compuesta fundamentalmente por bacterias Gram positivas, sin embargo también presenta enterobacterias a nivel distal en entre un 5 y un 11% de los hombres (5, 22). Estos mismos microorganismos son responsables de las infecciones después de RTU-P (19) y se han aislado en cultivos de tejido prostático resecado de un 13,5% de pacientes sin bacteriuria preoperatoria y no portadores de sonda Foley uretrovesical antes de la cirugía (23). Nuestro estudio presenta 3 pacientes con complicaciones infecciosas sistémicas. En uno de ellos se aisló un gérmen multiresistente intrahospitalario producto de la pérdida del circuito cerrado del drenaje urinario al lavarse la sonda uretrovesical obstruida por coágulos. En los otros dos casos, que presentaron fiebre alta y PCR elevada en los cuales no se aisló germen, la ausencia de lavados vesicales en su evolución y la buena respuesta clínica a Ciprofloxacino oral permiten plantear que su cuadro clínico se debió a microorganismos endógenos; ambos tenían el antecedente de ITU previa.
Nuestro estudio presenta un 6% de infección clínica sistémica el cual resulta ser muy alto en comparación con el 0,7% promedio de septicemia descrito en pacientes sin bacteriuria preoperatoria sometidos a RTU-P con uso de antibióticos (4). Esta frecuencia es claramente mayor, aunque sin significación estadística (p= 0,095), que aquella descrita en un estudio nuestro anterior de igual metodología con un grupo similar de 45 pacientes en que se usó antibióticos en forma continua hasta el retiro de la sonda uretrovesical (9) (Tabla VI). Por otra parte la infección clínica sistémica se asoció estadísticamente con el antecedente de ITU previa y con el hallazgo de prostatitis crónica activa en la biopsia operatoria. Una posible causa es que aquellos pacientes con historia de ITU previa efectivamente tuvieran microrganismos en el tejido prostático en una mayor proporción y/o concentración, los cuales serían liberados al torrente sanguíneo durante la cirugía. Otra posibilidad es que dichos pacientes hayan estado con infección urinaria al momento de la cirugía, desarrollada después de la toma del último urocultivo: entre 1 y 6,5% de los pacientes que llegan a la intervención quirúrgica sin sonda uretrovesical supuestamente sin infección tienen urocultivo tomado en pabellón positivo (16, 24-28).
Finalmente se puede plantear que probablemente el antecedente de infección urinaria previa hace menos aconsejable el uso de antibióticos en dosis discontinua en RTU-P, sin embargo se requiere un mayor número de pacientes con esta característica para confirmar este planteamiento. Estos pacientes se podrían manejar con el mismo esquema bajo un seguimiento mas estricto o con un esquema de dosis continua. Por otro lado, agregar el antecedente de ITU previa como criterio de exclusión en próximos estudios, permitiría explorar esquemas antibióticos aun más reducidos en RTU-P de pacientes con bajo riesgo de complicaciones infecciosas.
Bibliografía y lecturas recomendadas (*lectura de interés y ** lectura fundamental).
]]>1. MURPHY, D.M.; FALKINER, F.R.; CARR, M. y cols.: Septicemia after transurethral prostatectomy. Urology, 22: 133, 1983. [ Links ]
2. MEBUST, W.K.; HOLTGREWE, H.L.; COCKETT, A.T.K. y cols.: Transurethral prostatectomy: immediate and postoperative complications. A cooperative study of 13 participating institutions evaluating 3,885 patients. J. Urol., 141: 243, 1989. [ Links ]
**3. GRABE, M.: Antimicrobial agents in transurethral prostatic resection. J. Urol., 138: 245, 1987. [ Links ]
**4. BERRY, A.; BARRATT, A.: Prophylatic antibiotic use in transurethral prostatic resection: a meta-analysis. J. Urol., 167: 571, 2002. [ Links ]
**5. CHILDS, S.J.: Appropriate surgical prophylaxis in transurethral genitourinary surgery and potential reduction in nosocomial infections. Urology, 27: 415, 1986. [ Links ]
6. KUNIN, C.M.; McCORMACK, R.C.: Prevention of catheter-induced urinary-tract infections by sterile closed drainage. New Eng. J. Med., 274: 1155, 1966. [ Links ]
7. GARIBALDI, R.A.; BURKE, J.P.; BRITT, M.R. y cols.: Meatal colonization and catheter-associated bacteriuria. New Eng. J. Med., 303: 316, 1980. [ Links ]
*8. DUCLOS, J.M.; LARROUTOROU, P.; SARKIS, P.: "Timing of antibiotic prophylaxis with cefotaxime for prostatic resection: better in the operative period or at urethral catheter removal?" .Am. J. Surg., 164: 21, 1992. [ Links ]
9. VALDEVENITO, J.P.: "Antibioticos en reseccion transuretral de prostata de pacientes con bajo riesgo de complicaciones infecciosas: estudio comparativo prospectivo aleatorio". Arch. Esp. Urol., 57: 48, 2004. [ Links ]
10. DRIPPS, R.D.; LAMONT, A.; ECKENHOFF, J.E.: "The role of anesthesia in surgical mortality". JAMA, 178: 261, 1961. [ Links ]
11. STRICKER, P.D.; GRANT, B.F.: "Relative value of antibiotics and catheter care in the prevention of urinary tract infection after transurethral prostatic resection". Br. J. Urol., 61: 494, 1988. [ Links ]
12. MORRIS, M.J.; GOLOVSKY, D.; GUINNESS, M.D.G. y cols.: "The value of prophylactic antibiotics in transurethral prostatic resection: a controlled trial, with observations on the origin of postoperative infection". Br. J. Urol., 48: 479, 1976. [ Links ]
13. NIELSEN, O.S.; MAIGAARD, S.; FRIMODT-M¢LLER, N. y cols.: "Prophylactic antibiotics in transurethral prostatectomy". J. Urol., 126: 60, 1981. [ Links ]
14. HOLL, W.H.; ROUS, S.N.: Is antibiotic prophylaxis worthwhile in patients with transurethral resection of prostate?. Urology, 19: 43, 1982. [ Links ]
15. GRABE, M.; FORSGREN, A.; HELLSTEN, S.: The effect of a short antibiotic course in transurethral prostatic resection. Scand J. Urol. Nephrol.,18: 37, 1984. [ Links ]
16. SLAVIS, S.A.; MILLER, J.B.; GOLJI, H. y cols.: Comparison of single-dose antibiotic prophylaxis in uncomplicated transurethral resection of the prostate. J. Urol., 147: 1303, 1992. [ Links ]
17. HARGREAVE, T.B.; HINDMARSH, J.R.; ELTON, R. y cols.: Short-term prophylaxis with cefotaxime for prostatic surgery. Brit. Med. J., 284: 1008, 1982. [ Links ]
18. PROKOCIMER, P.; QUAZZA, M.; GIBERT, C. y cols.: Short-term prophylactic antibiotics in patients undergoing prostatectomy: report of a double-blind randomized trial with 2 intravenous doses of cefotaxime. J. Urol., 135: 60, 1986. [ Links ]
19. MADSEN, P.O.; LARSEN, E.H.; DÄRFLINGER, T.: The role of antibacterial prophylaxis in urologic surgery. Urology, 26: 38, 1985. [ Links ]
20. LAST, P.M.; HARBISON, P.A.; MARSH, J.A.: Bacteraemia after urological instrumentation. Lancet, 1: 74, 1966. [ Links ]
21. MEARES, Jr. E.M.: Prostatitis and related disorders. Walsh PC, Retik AB, Stamey TA, Vaughan Jr ED, ed. Campbells Urology. 6th ed. 807-22. W.B. Saunders Company, Philadelphia, 1992. [ Links ]
22. HELMHOLZ, H.F.: Determination of the bacterial content of the urethra: a new method, with results of a study of 82 men. J. Urol., 64: 158, 1950. [ Links ]
*23. GORELICK, J.I.; SENTERFIT, L.B.; VAUGHAN, Jr. E.D.: Quantitative bacterial tissue cultures from 209 prostatectomy specimens: findings and implications. J.Urol., 139: 57, 1988. [ Links ]
24. FERRIE, B.G.; SCOTT, R.: Prophylactic cefuroxime in transurethral resection. Urol. Res., 12: 279, 1984. [ Links ]
25. MURDOCH, D.A.; BADENOCH, D.F.; GATCHALIAN, E.R.: Oral ciprofloxacin as prophylaxis in transurethral resection of the prostate. Br. J. Urol., 60: 153, 1987. [ Links ]
26. DESAI, K.M.; ABRAMS, P.H. WHITE, L.O.: A double-blind comparative trial of short-term orally administered enoxacin in the prevention of urinary infection after elective transurethral prostatectomy: a clinical and pharmacokinetic study. J. Urol., 139: 1232, 1988. [ Links ]
*27. HARGREAVE, T.B.; BOTTO, H.; RIKKEN, G.H.J.M. y cols.: European collaborative study of antibiotic prophylaxis for transurethral resection of the prostate. Eur. Urol., 23: 437, 1993. [ Links ]
*28. VIITANEN, J.; TALJA, M.; JUSSILA, E. y cols.: Randomized controlled study of hemoprophylaxis in transurethral prostatectomy. J. Urol, 150:1715, 1993. [ Links ]
]]>
Trabajo recibido: 20 de abril 2005.
]]>